一支箭黄酮类化学成分研究*
2022-04-11曾碧涛
曾碧涛
(宜宾职业技术学院,四川 宜宾 644003)
一支箭为瓶尔小草科(Ophioglossaceae)瓶尔小草属蕨类植物[1],在四川、贵州、云南、西藏等西南各省均有分布[2-3]。现在药材市场上流通的三个种为瓶尔小草(Ophioglossum vulgatum Linn.)、狭叶瓶尔小草(Ophioglossum thermale Kom.)和尖头瓶尔小草(Ophioglossum pedunculosum Desv.)。一支箭是重要的民间中草药,具有多种药用价值,主要治疗毒蛇咬伤、跌打损伤、烧伤烫伤、瘀血疼痛、肝炎等[4-7]。由于近年来过度采挖、农药使用和环境变化等因素,使其分布范围日益缩减,数量越来越稀少[8]。
黄酮类化合物作为一支箭的主要物质基础,具有重要的药理活性[9-11],为了进一步开发该药材资源提供依据,我们对一支箭(Ophioglossum vulgatum Linn.)的黄酮类成分进行系统研究,共分离得到了5个化合物,化合物1~4首次从该植物中分离得到。其结构见图1。
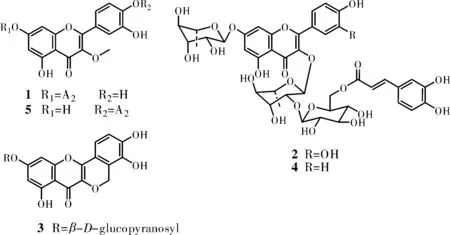
图1 化合物1~5的结构图
1 仪器与材料
Thermo Scientific LTQ Orbitrap XL型高分辨质谱仪;Agilent 400 MHz 核磁共振仪(TMS为内标);FS-9200T中压制备色谱仪,天津博纳艾杰尔科技有限公司;半制备型高效液相色谱仪,Waters公司;薄层色谱硅胶、柱色谱硅胶,青岛海洋化工厂;乙腈、甲醇(色谱纯),其余试剂为国产分析纯。
实验所用药材一支箭2020年5月采自四川宜宾市,经西南民族大学民族药物研究所张志锋教授鉴定为一支箭Ophioglossum vulgatum Linn.,样品保存于宜宾职业技术学院(标本号:CN20201032)。
2 提取与分离
将一支箭药材1.5 kg粗粉,加10倍体积的95%乙醇。加热回流提取3次,第一次2 h,第二次2 h,第三次1.5 h,合并三次提取液,减压回收溶剂,加入2倍体积的水混匀。过滤,滤渣用50%乙醇洗涤2次,合并滤液。将滤液上经过处理活化的聚酰胺,控制流速为0.2 L·min-1,完成后水洗至流出液无色,用20%、70%和95%乙醇梯度洗脱,收集洗脱液,减压回收溶剂,得各粗提取物,称重分别得到3 g、11 g和2 g。TLC检测发现用70%乙醇洗脱得到的粗提取物斑点最多。将70%乙醇洗脱部分(10 g)甲醇溶解后用硅胶拌样(60~80目),硅胶湿法装柱(200~300目)进行分离。洗脱剂用二氯甲烷-甲醇 (20∶1→2∶1),约500 mL收集一份,共收集33份。以5%三氯化铝-乙醇溶液为显色剂进行TLC检测,对相同部分进行合并后得到Fr. A~F。将Fr. B(0.3 g)进行再次硅胶柱层析,洗脱剂为二氯甲烷-甲醇(8∶1),TLC监控,收集主要斑点部分用半制备反相色谱再次分离,以乙腈-0.1%磷酸水(35∶65)为流动相,检测波长为254 nm,得到化合物5(17 mg);对具有明显斑点的Fr. C(0.7 g)进行再次硅胶柱色谱分离,洗脱剂为二氯甲烷-甲醇(6∶1),用TLC过程监控,收集相对单一部分Fr. C1,用半制备反相色谱分离,流动相为乙腈-0.1%磷酸水(32∶68),得化合物4(15 mg),将Fr. D(1.0 g)用常压反相硅胶柱色谱再次粗分,甲醇-水(50∶50→90∶10)梯度洗脱,TLC监控,得Fr. D3、Fr. D4,Fr. D6三个相对单一样品,再用半制备高效液相对样品进行精制,乙腈-0.1%磷酸水为流动相,检测波长254 nm,得化合物1(13 mg)、化合物3(16 mg),Fr. F(0.4 g)再次进行硅胶柱色谱分离,洗脱剂为二氯甲烷-甲醇(5∶1),TLC监控,得相对单一的组分Fr. F1,将其用半制备反相色谱分离,以乙腈-0.1%磷酸水(25∶75)为流动相,检测波长254 nm,收集主要目标物,减压抽干,甲醇溶解后过滤,滤液用凝胶色谱精分,用纯甲醇为洗脱剂,得到化合物2(12 mg)。
3 结构鉴定
化合物1:淡黄色粉末。1H-NMR(400 MHz,DMSO-d6):δ7.56 (1H,d,J=2.4 Hz,H-2′),7.52 (1H,dd,J=8.4,2.5 Hz,H-6′),7.26 (1H,d,J=8.4 Hz,H-5′),6.80 (1H,d,J=2.4 Hz,H-8),6.43 (1H,d,J=2.0 Hz,H-6),5.07 (1H,d,J=7.2 Hz,H-1‴),4.84 (1H,d,J=7.6 Hz,H-1″),3.79 (1H,s,-OCH3);13C-NMR (100 MHz,DMSO-d6)δ:148.2 (C-2),138.9 (C-3),178.6 (C-4),161.3 (C-5),99.7 (C-6),163.4 (C-7),95.0 (C-8),156.5 (C-9),101.6 (C-10),124.2 (C-1′),116.1(C-2′),146.9 (C-3′),156.0 (C-4′),116.2 (C-5′),120.7 (C-6′),100.1 (C-1″),73.5 (C-2″),76.8(C-3″),69.9(C-4″),77.5(C-5″),61.0(C-6″),106.3 (C-1),73.6 (C-2),76.3 (C-3),70.2 (C-4),77.7 (C-5),61.1 (C-6),60.2(-OCH3)。与文献[12]报道基本一致,故鉴定为 3-O-甲基槲皮素7-O-β-D-葡萄糖基-4′-O-β-D-葡萄糖苷。
化合物2:淡黄色粉末。1H-NMR(400 MHz,DMSO-d6):δ7.40 (1H,d,J=2.0 Hz,H-2′),7.35 (1H,d,J=15.6 Hz,H-7″″′),7.27 (1H,dd,J=8.4,2.0 Hz,H-6′),6.93 (1H,d,J=2.0 Hz,H-2″″′),6.88 (1H,d,J=8.4 Hz,H-5′),6.85 (1H,dd,J=8.0,1.6 Hz,H-6″″′),6.67 (1H,d,J=2.0 Hz,H-8),6.66 (1H,d,J=8.4 Hz,H-5″″′),6.39 (1H,d,J=2.0 Hz,H-6),6. 13 (1H,d,J=16.0 Hz,H-8″″′),5. 50 (1H,br s,H-1‴),5.48 (1H,br s,H-1″″),4.26 (1H,d,J=7.8 Hz,H-1),1.10 (3H,d,J=6.0 Hz, H-6″″),0. 91 (3H,d,J=6.0 Hz,H-6″);13C-NMR(100 MHz,DMSO-d6)δ:157.6 (C-2),135.0 (C-3),178.4 (C-4),161.3 (C-5),99.8 (C-6),162.1 (C-7),94.8 (C-8),156.4 (C-9),106.0 (C-10),120.8 (C-1′),116.0 (C-2′),145.6 (C-3′),149.2 (C-4′),116.0 (C-5′),121.5 (C-6′),101.1 (C-1″),82.1(C-2″),70.6 (C-3″),72.1 (C-4″),70.8 (C-5″),18.3 (C-6″),106.6 (C-1),74.1 (C-2),76.3 (C-3),69.6 (C-4),74.0 (C-5),63.1 (C-6),98.8 (C-1″″),70.2 (C-2″″),70. 6 (C-3″″),72.0 (C-4″″),70.5 (C-5″″),17.8 (C-6″″),125.9 (C-1″″′),115.8 (C-2″″′),145.5 (C-3″″′),148.6 (C-4″″′),116.0 (C-5″″′),121.5 (C-6″″′),145.6 (C-7″″′),114.2 (C-8″″′),166.7 (C-9″″′)。与文献[13]报道基本一致,故鉴定为槲皮素3-O-(6-O-咖啡酰基)-β-D-葡萄糖基-(1→2)-α-L-鼠李糖-7-O-α-L-鼠李糖苷。
化合物3:淡黄色粉末。1H-NMR(400 MHz,DMSO-d6):12.7 (1H,br s,H-5-OH),7.19 (1H,d,J=8.4 Hz,H-4′),6.90 (1H,d,J=8.4 Hz,H-3′),6.73 (1H,d,J=2.4 Hz,H-8),6.40 (1H,d,J=2.0 Hz,H-6),5.20 (2H,s,H-7′),5.03 (1H,d,J=7.2 Hz,H-1″);13C-NMR (100 MHz,DMSO-d6)δ:149.8 (C-2),133.1 (C-3),174.1 (C-4),161.1 (C-5),99.2 (C-6),162.5 (C-7),94.6 (C-8),155.4 (C-9),106.1 (C-10),119.9 (C-1′),114.2 (C-2′),114.6 (C-3′),149. 9 (C-4′),140.5 (C-5′),115.2 (C-6′),63.1 (C-7′),100.1 (C-1″),77.2 (C-2″),69.5 (C-3″),72.9 (C-4″),76.4 (C-5″),60.6 (C-6″)。文献[14]报道基本一致,故鉴定为瓶尔小草素-7-O-β-D-葡萄糖苷。
化合物4:淡黄色粉末。1H-NMR(400 MHz,DMSO-d6):7.75 (1H,d,J=8.4 Hz,H-2′,6′),7.34 (1H,d,J=15.6 Hz,H-7″″′),6.91(1H,d,J=2.0 Hz,H-2″″′),6.88 (1H,d,J=8.4 Hz,H-3′,5′),6.83 (1H,dd,J=8.4,2.0 Hz, H-6″″′),6.67 (1H,d,J=2.0 Hz,H-8),6.65(1H,d,J=8.4 Hz,H-5″″′),6.40 (1H,d,J=2.0 Hz,H-6),6.10 (1H,d,J=16.0 Hz,H-8″″′),5.58 (1H,br s,H-1″),5.50 (1H,br s,H-1″″),4.28 (1H,d,J=7.8 Hz,H-1),4.13 (1H,m,H-6),4.12 (1H,br s,H-2″),3.84 (1H,br s,H-2″″),3.63 (1H,dd,J=9.2,3.2 Hz,H-3″″),3.55 (1H,dd,J=9.6,3.2 Hz,H-3″),3.43 (1H,m,H-5″″),3.37 (1H,m,H-5″),3.28 (1H,m,H-4″″,5″″),3.20(1H,m,H-3),3.19 (1H,m,H-4),3.12 (1H,t,J= 9.6 Hz,H-4″),3.06 (1H,t,J=8.0 Hz,H-2),1. 10 (3H,d,J=6.0 Hz,H-6″″),0.88 (3H,d,J=6.0 Hz,H-6″);13C-NMR (100 MHz,DMSO-d6)δ:157.6 (C-2),135.0 (C-3),178.3 (C-4),161.4 (C-5),99.9 (C-6),162.1 (C-7),94.9 (C-8),156.4 (C-9),106.5 (C-10),120.6 (C-1′),131.0 (C-2′),115.8 (C-3′),160.6(C-4′),116.0 (C-5′),131.0 (C-6′),101.0 (C-1″),81.9 (C-2″),70.6 (C-3″),72.0 (C-4″),70.9 (C-5″),18.3 (C-6″),106.1 (C-1),74.1 (C-2),76.4 (C-3),70.2 (C-4),74.1 (C-5),63.3 (C-6),98.9 (C-1″″),70.3 (C-2″″),70.6 (C-3″″),72.1 (C-4″″),70.5 (C-5″″),18.2 (C-6″″),125.8 (C-1″″′),115.3 (C-2″″′),145.9 (C-3″″′),148.6 (C-4″″′),115.8(C-5″″′),121.4 (C-6″″′),145.5 (C-7″″′),114.1 (C-8″″′),166.7 (C-9″″′)。与文献[15]报道基本一致,故鉴为山柰酚3-O-(6-O-咖啡酰基)-β-D-葡萄糖基-(1→2)-α-L-鼠李糖-7-O-α-L-鼠李糖苷。
化合物5:淡黄色粉末。1H-NMR(400 MHz,DMSO-d6):7.56 (1H,d,J=2.4 Hz,H-2′),7.43 (1H,dd,J=8. 4,2.4 Hz,H-6′),6.90 (1H,d,J=8.4 Hz,H-5′),6.74 (1H,d,J=2.0 Hz,H-8),6.42 (1H,d,J=2.0 Hz,H-6),5.06 (1H,d,J=7.2 Hz,H-1″),3.78 (3H,s,-OCH3),3.67 (1H,br d,J=10.4 Hz,H-5″),3.45 (1H,dd,J=6.0,12.0 Hz,H-6″),3.37 (1H,m,H-5″),3.30(1H,t,J=7.2 Hz,H-6″),3.20 (1H,dd,J=7.2,8.8 Hz,H-2″),3.17(1H,t,J=9.0 Hz,H-4″);13C-NMR (100 MHz,DMSO-d6)δ:155.9 (C-2),137.9 (C-3),178.1 (C-4),160.9 (C-5),99.2 (C-6),162.9 (C-7),94.4 (C-8),156.2(C-9),105.8 (C-10),120.7 (C-1′),115.6 (C-2′),145.2 (C-3′),148.9 (C-4′),115.7(C-5′),120.7(C-6′),99.8 (C-1″),73.1(C-2″),76.4(C-3″),69.5(C-4″),77.1 (C-5″),60.6 (C-6″),59.7 (-OCH3)。与文献[16]报道基本一致,故鉴定为 3-O-甲基槲皮素 7-O-β-D-葡萄糖苷。
4 结 论
本文通过硅胶柱色谱、凝胶色谱及高压制备色谱等方法对一支箭(OphioglossumvulgatumLinn.) 的黄酮类成分进行分离纯化,通过测定分离得到化合物的理化性质和波谱数据进行结构表征。共分离得到5个黄酮类化合物,前4个化合物为首次从该植物中分离得到。为了进一步开发该药材资源提供了依据。
