经英夫利西单抗治疗后转化为阿达木单抗治疗克罗恩病1例
2022-04-11庄逸瀚罗梦馨王和礼林伊婷黄泽羽周思思
庄逸瀚,罗梦馨,王和礼,林伊婷,黄泽羽,周思思,俞 晶
(1.汕头大学医学院第一附属医院消化内科,广东 汕头 515041;2.汕头大学医学院第一附属医院病理科,广东 汕头 515041)
1 病例资料
患者女性,32岁,因“反复腹痛腹泻2年,伴肛周肿痛流脓1个月”于2017年3月21日初次入院。患者自2015年始间断性出现腹泻、排黏液便,未排血便,曾至外院就诊,肠镜提示回肠末段慢性炎症,升结肠、横结肠黏膜可见裂隙状溃疡;送检病理结果符合克罗恩病(Crohn's disease,CD)。外院予柳氮磺吡啶联用糖皮质激素治疗,症状好转后出院。出院后予“硫唑嘌呤25 mg/d”维持治疗,症状时有反复。
入院查体:全腹轻压痛,无反跳痛,余未见阳性体征;既往史、家族史、个人史无特殊。实验室检查结果(2017年3月22日):粪隐血(+),粪便白细胞3~4个/HP,C反应蛋白13.90 mg/L,乙肝表面抗原阳性,乙肝病毒DNA<100 IU/mL,余实验室检查结果未见异常。胃镜(2017年3月24日):慢性浅表性胃窦炎。肠镜(2017年3月24日):回肠末端、降结肠及乙状结肠可见散在斑片状充血水肿及糜烂,局部可见息肉样增生;回盲部、盲肠、升结肠和右半横结肠黏膜粗糙,呈“铺路石”样改变,可见纵行溃疡(图1)。病理(2017年3月25日):回肠末端、回盲瓣、升结肠及乙状结肠黏膜充血、水肿、伴大量急慢性炎症细胞浸润,可见上皮样肉芽肿(图2),符合克罗恩病。计算机断层扫描肠造影(computerized tomographic enterography,CTE)(2017年 3月 23日):回肠末端-回盲部-升结肠-横结肠肠壁不规则增厚(图3)。磁共振肠造影(magnetic resonance imaging enterography,MRE)(2017年3月25日):肛管见2条管状影,向上经括约肌间隙走行,分别达肛管腔截石位2点钟、5点钟处,其外口均开于左侧臀缝区皮肤截石位约2点钟、5点钟处,考虑肛瘘(括约肌间型)(图4)。
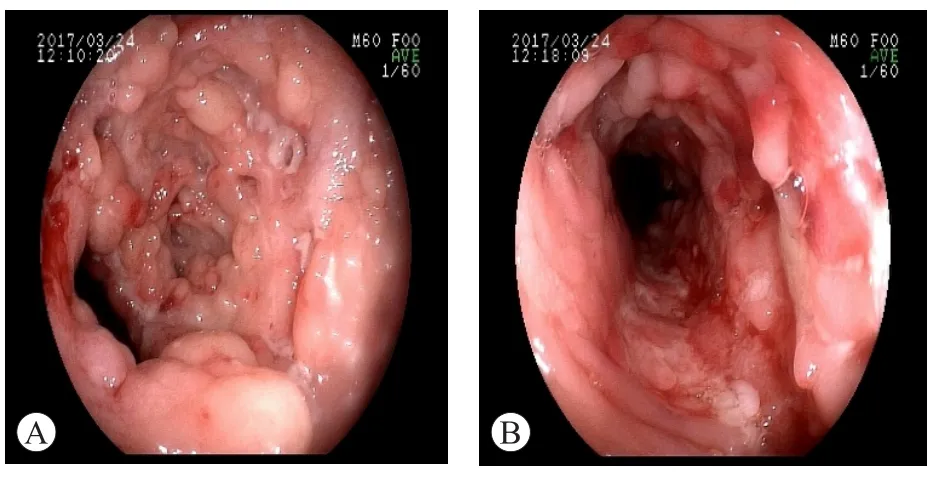
图1 患者肠镜检查图(2017年3月24日)
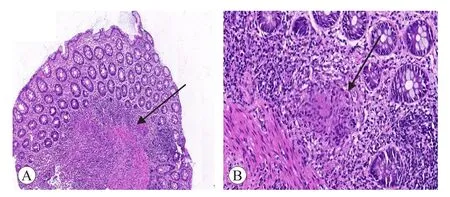
图2 患者病理结果图
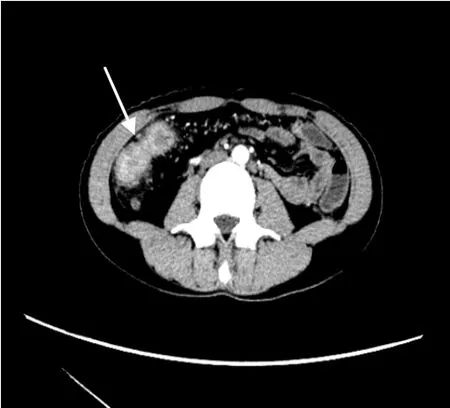
图3 患者CTE结果图
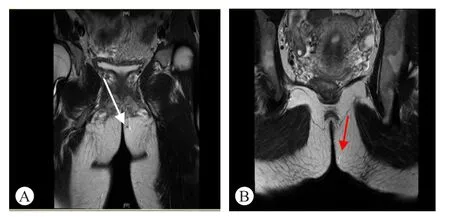
图4 患者肛周MRE图
诊断与治疗:患者主诉为腹痛腹泻,合并肛瘘,在排除肠结核、白塞病等其他疾病后,结合内镜、病理及影像学资料,诊断为:(1)克罗恩病(A2,L3,B1p,轻度活动期),克罗恩病活动指数为170.9分;(2)乙肝病毒携带者。患者于2017年4月8日、2017年4月20日、2017年5月18日、2017年7月22日、2017年9月21日、2017年11月28日分别接受英夫利西单抗300 mg治疗。2017年7月19日复查CTE:回肠末端-回盲部-升结肠-横结肠肠壁不规则增厚较前减轻。2017年7月20日复查MRE:原截石位2点钟处瘘管下部分管腔较前变小,上部分管腔仍可见,管腔内积液较前吸收减少;原截石位5点钟处瘘管现已闭合,管腔内积液及周围渗出基本吸收。2017年7月21日复查肠镜:回盲瓣、盲肠、升结肠、横结肠及降结肠黏膜可见多发息肉增生样改变,局部可见白色瘢痕及斑片状充血,未见糜烂及溃疡。患者经过6次英夫利西单抗的治疗,达到了内镜下黏膜愈合的良好疗效,影像学亦提示肠壁水肿增厚较前减轻,肛瘘情况好转。患者因个人经济原因终止了英夫利西单抗的治疗,仅以不完全肠内营养及硫唑嘌呤25 mg/d维持治疗。
2018年6月13日患者因“排水样便1个月”入院。实验室检查艰难梭菌谷氨酸脱氢酶阳性,艰难梭菌毒素A+B(实时荧光PCR)阴性,患者住院期间(2018年6月19日至6月21日)予万古霉素(0.125 g,1次/6 h)口服治疗,经治疗,患者排水样便症状迅速缓解。出院后继续予口服万古霉素至疗程足够(14 d)。此次出院后,患者又接受了5次英夫利西单抗治疗,后再次因经济因素中断了生物制剂的治疗。
2021年5月21日患者因“反复腹泻6年余,腹痛6 d”入院。肠镜(2021年5月21日):回肠末端可见散在小溃疡;盲肠、升结肠、降结肠黏膜可见多发息肉样增生改变,另可见多发溃疡形成,病变以升结肠最重,横结肠未见溃疡及糜烂。病理(2021年5月22日):回肠、升结肠黏膜上皮缺失伴炎性肉芽组织增生;局灶隐窝延长扩张,黏膜大量急、慢性炎症性细胞浸润,隐窝炎形成;可见小灶上皮样肉芽肿。此次入院患者克罗恩病病情反复并加重,就患者后续的诊治方案,我们再次与患者商讨,综合经济情况及使用便捷性,最终为患者选用了阿达木单抗。患者于2021年5月25日(160 mg)、2021年6月8日(80 mg)、2021年6月22日(40 mg)、2021年7月6日(40 mg)、2021年7月20日(40 mg)、2021年8月3日(40 mg)分别接受了6次阿达木单抗的治疗。
患者在使用了6次阿达木单抗后,复查肠镜提示黏膜基本愈合,仅遗留部分肠段的息肉增生样病变(图5);影像学所示肠壁水肿及肛瘘亦有缓解。现患者继续于家中每2周皮下注射阿达木单抗40 mg。
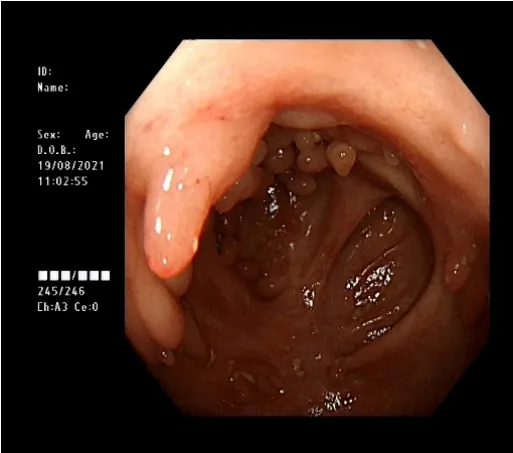
图5 患者肠镜检查图(2021年8月19日)
2 讨论
CD是一种慢性非特异性肠道疾病,病因尚未明确,可能与遗传、免疫、环境以及精神心理因素等相关[1]。CD的治疗应根据疾病活动严重程度及对治疗的反应做出选择:轻度活动期CD治疗原则是控制症状;中重度活动期CD最常用的治疗药物是糖皮质激素,激素无效或依赖时加用免疫抑制剂;抗TNF-α单克隆抗体用于激素和上述免疫抑制剂治疗无效者或激素依赖者或不能耐受上述药物治疗者。
英夫利西单抗(infliximab,IFX)是纯化的重组DNA衍生的嵌合人-小鼠IgG单克隆抗TNF-α抗体,其分子含75%人序列和25%鼠序列,是首个应用于克罗恩病治疗的生物制剂。IFX通过特异性结合可溶性和跨膜的TNF,阻断其与受体结合,阻止促炎细胞因子释放,最终发挥抗炎作用[2]。目前推荐第0、2、6周以IFX 5 mg/kg静脉输注诱导缓解,以后每隔8周以相同剂量维持缓解,根据疗效和药物浓度监测调整使用间期和剂量[3]。多个大型临床试验已证实英夫利西单抗对CD的缓解率可达36%~88%[4]。
阿达木单抗(adalimumab,ADA)是一种重组全人源化抗TNF-α单克隆IgG抗体,作用机制与IFX相似,但因ADA是完全人源性抗IgG抗体,免疫原性较低,即使是对于IFX抵抗或不耐受的患者,亦显示出良好的疗效和安全性。目前推荐方法为首次皮下注射负荷量160 mg,第2周予80 mg进行诱导治疗,后每2周予40 mg维持治疗,首次内镜复查不建议早于首次给药后第12周[3]。多个大型临床试验均证实了ADA在CD诱导及维持缓解治疗中的良好疗效[5-7]。ADA总体安全性良好,常见不良反应是感染、注射部位反应、头痛和骨骼肌肉疼痛[3]。ADA有效稳态谷浓度为4~8 mg/L,本病例患者共进行4次药物浓度检测,均在有效范围内,监测最低浓度14.4 mg/L,最高浓度>35 mg/L。
本例CD患者先前使用过IFX,未出现失应答,但因价格因素中断了治疗。后结合经济因素及使用便捷性考虑,为患者改用了ADA,监测血药浓度全程处于有效范围,并取得了临床症状缓解、内镜黏膜下愈合的良好疗效,为我们使用ADA治疗CD树立了信心。另国内外已有不少研究表明,对IFX治疗失败的CD患者,仍能从ADA的治疗中获益[8-9]。ADA单抗全程为皮下注射治疗,使用方便,在新冠疫情的世界背景下,能有效降低住院率,减少交叉感染的风险,应用前景广阔。
关于ADA是否联用免疫抑制剂,中华医学会消化病学分会炎症性肠病学组建议:目前尚无充分证据支持ADA与嘌呤类药物联合治疗可以提高疗效,但对于重度活动、病变广泛、既往使用过TNF单克隆抗体者,仍建议联合免疫抑制剂治疗[3]。本病例中患者既往使用过IFX,且病变累及回肠末端及全结肠,故改用ADA后继续联用免疫抑制剂。
使用生物制剂前需行活动性感染筛查,需特别注意结核及乙肝病毒感染。ECCO指南建议:炎症性肠病合并乙型肝炎表面抗原阳性患者,无论接受传统或生物制剂治疗,均需接受抗乙肝病毒治疗[10]。本例患者为乙肝病毒携带者,在针对原发病治疗同时,我们全程予恩替卡韦抗乙肝病毒治疗,患者全程乙肝病毒DNA<100 IU/mL,无病毒激活。
该患者病程中出现疑似艰难梭菌感染的症状,艰难梭菌毒素检测为阴性,但考虑到毒素检测灵敏度较低,易漏诊。结合症状,我们临床诊断患者合并艰难梭菌感染,按照艰难梭菌感染的标准予以治疗,患者排水样便的症状在使用万古霉素后得到明显缓解。CD合并艰难梭菌感染,病情重,预后差,多项临床研究结果提示炎症性肠病是艰难梭菌感染的独立危险因素之一[11-12]。对于临床上疑似艰难梭菌感染的CD病例,应灵活积极处理,以免耽误患者病情。
