利拉鲁肽、度拉糖肽、贝那鲁肽治疗初发肥胖2型糖尿病患者TIR的对比研究
2022-03-30吴嘉鸣马亚楠吴巧娟唐宏霞
吴嘉鸣,马亚楠,吴巧娟,唐宏霞,彭 一
(1.河北省张家口市第一医院东院区内分泌科,河北 张家口 075000; 2.河北省张家口市桥西区医院检验科,河北 张家口 075000)
随着生活水平的提高,2型糖尿病的发病率逐年升高,据统计,中国成年人总糖尿病患病率为12.8%[1]。众所周知,胰岛功能衰退及胰岛素抵抗的加重是2型糖尿病发病和进展的重要因素,作为降糖新靶点的胰高血糖素样肽1(glucagon-like peptide-1,GLP-1)具有改善胰岛素分泌、减少胰高糖素分泌、抑制胰岛β细胞凋亡等多种机制。目前临床中广受关注的GLP-1受体激动剂有利拉鲁肽、艾塞那肽、利司那肽、度拉糖肽、贝那鲁肽、洛塞那肽、司美格鲁肽等,如此众多的GLP-1受体激动剂在药物吸收、临床疗效、不良反应等方面各有不同特点,本研究旨在应用动态血糖监测系统,探讨3种不同半衰期的GLP-1受体激动剂代表药物利拉鲁肽、度拉糖肽、贝那鲁肽治疗初发肥胖2型糖尿病患者前后目标葡萄糖范围内时间(time in range ,TIR)等持续血糖监测指标的变化特点及其临床意义。
1 资 料 与 方 法
1.1一般资料 选择2019年10月—2021年1月河北省张家口市第一医院内分泌科就诊的肥胖2型糖尿病患者90例,按照随机对照研究设计方案分为利拉鲁肽组、度拉糖肽组、贝那鲁肽组各30例。利拉鲁肽组男性16例,女性14例,年龄35~62岁,平均(50.81±4.39)岁,病程0.50(0.75)年;度拉糖肽组男性15例,女性15例,年龄34~60岁,平均(48.87±5.14)岁,病程0.48(0.72)年。贝那鲁肽组男性13例,女性17例,年龄36~59岁,平均(49.90±4.74)岁,病程0.52(0.70)年。3组性别、年龄、病程差异无统计学意义(P>0.05),具有可比性。
纳入标准:①年龄>18岁;②符合2型糖尿病诊断标准;③糖化血红蛋白(glucated haemoglobin A1c,HbA1c)6.5%~11%;④体重指数(body mass index,BMI)≥24。入选前给予饮食指导、运动调整基础上,可联合二甲双胍治疗,使用剂量调整充分。
排除标准:①糖尿病酮症酸中毒、糖尿病高血糖高渗综合征、低血糖等糖尿病急性并发症;②1型糖尿病;③各种急性感染性疾病,妊娠、哺乳,严重心脑肾等全身重要脏器疾病,电解质紊乱,胰腺炎,其他可能导致胃排空异常的胃肠道疾病,胃肠手术病史等;④甲状腺髓样癌等恶性肿瘤;⑤其他影响按疗程用药及随访的患者。
本研究经医院医学伦理委员会批准通过,所有患者均知情同意并签署知情同意书。
1.2给药方法 利拉鲁肽组患者皮下注射利拉鲁肽,1次/d,起始剂量0.6 mg/d,耐受后根据血糖情况调整剂量至1.2 mg/d,最高1.8 mg/d;度拉糖肽组患者皮下注射度拉糖肽,1.5 mg,每周1次;贝那鲁肽组患者皮下注射贝那鲁肽,0.1 mg/次,3次/d,餐前5 min皮下注射,逐渐增加至治疗剂量0.2 mg,3次/d。3组均根据血糖调整用药剂量,观察12周。
1.3观察指标 治疗前及治疗12周后观察BMI、空腹血糖(fasting plasma glucose,FPG)、餐后2 h血糖(2 h plasma glucose,2 hPG)、HbA1c、空腹胰岛素(fasting insulin,FINS)、空腹C肽(fasting connecting peptide,FC-P)、尿白蛋白/肌酐(urinary albumin creatinine ratio, UACR)等指标,记录低血糖发生例数及严重程度、皮疹、恶心、呕吐等胃肠道反应、急性胰腺炎等不良反应发生情况。根据FC-P计算胰岛β细胞功能指数(homeostasis model assessment-β,HOMA-β)=20×FC-P/(FPG-3.5)及胰岛素抵抗指数(homeostasis model assessment for insulin resistance,HOMA-IR)=1.5+FPG×FC-P/2.8。3组患者入组后及研究终止前均采用美敦力CGM(722泵)动态血糖监测系统(continuous glucose monitoring system,CGMS)(722泵)监测动态血糖,连续记录 3 d 葡萄糖水平,每天记录 288 个连续感应值,并采用指尖电脑血糖仪每日4次末梢血糖校准。根据所得数据计算干预治疗前后血糖波动指标、TIR,即CGMS监测期间24 h内血糖值在3.9~10.0 mmol/L的范围所占的时间百分比,计算平均血糖波动幅度(mean amplitude of glycemic excursions,MAGE)。分析TIR与UACR的相关性。
1.4统计学方法 应用SPSS 19.0统计软件分析数据。HOMA-β、HOMA-IR及UACR呈非正态分布,进行对数转换后比较,计量资料组间比较采用单因素方差分析和SNK-q检验,组内比较采用配对t检验。计数资料比较采用χ2检验。相关性采用Pearson相关分析。P<0.05为差异有统计学意义。
2 结 果
2.13组治疗前后观察指标比较 治疗前,3组BMI、FPG、2 hPG、HbA1c、UACR、FINS、FC-P、HOMA-β、HOMA-IR、MAGE、TIR差异均无统计学意义(P>0.05)。治疗后,3组BMI、FPG、2 hPG、HbA1c、UACR、HOMA-IR、MAGE均低于治疗前,FINS、FC-P、HOMA-β、TIR高于治疗前,差异有统计学意义(P<0.05)。治疗后,贝那鲁肽组BMI、2 hPG低于利拉鲁肽组和度拉糖肽组;度拉糖肽组UACR、MAGE低于利拉鲁肽组和贝那鲁肽组,TIR高于利拉鲁肽组和贝那鲁肽组,差异有统计学意义(P<0.05)。3组FPG、HbA1c、FINS、FC-P、HOMA-β、HOMA-IR差异无统计学意义(P>0.05)。见表1。
2.23组不良反应发生率比较 随访过程中3组患者均有恶心、呕吐、食欲减退等胃肠道症状和心悸、饥饿感等轻度低血糖反应,个别患者出现皮疹,瘙痒不适,可自行消退。贝那鲁肽组胃肠道症状发生率高于利拉鲁肽组和度拉糖肽组,差异有统计学意义(P<0.05);3组患者低血糖、皮疹发生率差异无统计学意义(P>0.05)。3组患者均无急性胰腺炎等其他严重不良反应发生。见表2。
2.3相关性分析 TIR与UACR呈负相关(r=-0.73,P<0.05)。见图1。
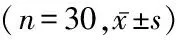
表1 三组治疗前后临床指标比较
表2 3组不良反应发生率比较 (n=30,例数,%)
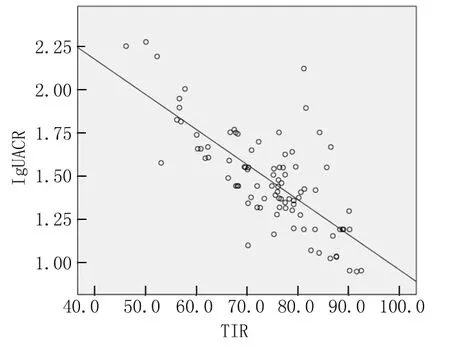
图1 TIR与UACR相关性分析
3 讨 论
糖尿病的治疗药物研发和相关循证医学研究迅猛发展,目前临床中常见的有磺脲类、双胍类、噻唑烷二酮类、α-糖苷酶抑制剂、二肽基肽酶4 抑制剂、钠-葡萄糖协同转运蛋白2抑制剂、胰岛素等多种降糖药物。GLP-1是一类由肠道L细胞分泌的葡萄糖依赖性的多肽类物质,其降糖机制非常广泛,促进胰岛β细胞分泌胰岛素、抑制胰高血糖素的分泌、延缓胃排空、抑制肝糖输出、改善外周组织利用葡萄糖、抑制大脑进食中枢等,能有效降低FPG及2 hPG,减轻体重,改善胰岛β细胞功能,调节血压、血脂,减少尿蛋白,改善糖尿病血管并发症[2]。随着大量循证医学证据的出现,GLP-1受体激动剂类药物在糖尿病治疗中的地位不断提升, 《中国2型糖尿病防治指南(2020版)》也将其列入降糖治疗的重要选择之一[3]。本研究通过动态血糖监测系统观察应用利拉鲁肽、度拉糖肽、贝那鲁肽3种GLP-1受体激动剂的血糖波动特征,探讨不同GLP-1受体激动剂对糖尿病患者胰岛功能及血管并发症的影响。
天然GLP-1是具有30个氨基酸的肽类激素,其末端第2个氨基酸为丙氨酸,可被二肽基肽酶4降解,所以半衰期仅1~2 min,利拉鲁肽是较早上市的利用基因重组技术合成的GLP-1类似物,与内源性GLP-1具有97%同源性,通过独特的自联作用使其在皮下吸收入血减慢,同时因在血浆中与白蛋白结合稳定,减缓被二肽基肽酶4及中性内肽酶降解,故其清除半衰期大约为13 h,1次/d,即可达到稳定血药浓度[4]。度拉糖肽为新型长效GLP-1受体激动剂,包含2个相同且各含有一个经过修饰的人GLP-1类似物的二硫键连接链,通过连接肽共价连接于修饰后的免疫球蛋白重链片段(Fc)上,尽管仍与人GLP-1具有90%同源性,但因其相对分子质量较大,能够延缓皮下吸收和肾脏滤过清除,故半衰期约为 30 h,可以实现每周一次皮下注射的长效作用[5]。贝那鲁肽是国内原研的重组人GLP-1(7-36),为全人源氨基酸序列,皮下注射后迅速吸收入血,在排泄系统分布较高,可快速清除和降解,无明显蓄积,故半衰期为11 min左右,作用时间较利拉鲁肽短,需要每日3次餐前皮下注射,理论上可用于更好控制2 hPG[6]。
本研究结果显示,3种GLP-1受体激动剂均能够很好的控制2型糖尿病患者的HbA1c、FPG及2 hPG,贝那鲁肽组2 hPG水平低于利拉鲁肽组和度拉糖肽组(P<0.05),证实贝那鲁肽确有更佳地控制餐后血糖效果,考虑与贝那鲁肽餐前注射,促进胰岛素早期时相分泌有关。但贝那鲁肽在获得更佳餐后血糖效果的同时,增加进餐时恶心、呕吐等胃肠道症状的发生。有研究证实,GLP-1受体激动剂类药物能抑制胃排空同时抑制十二指肠、小肠排空,增加饱腹感[7]。本研究结果显示,贝那鲁肽组较利拉鲁肽组和度拉糖肽组患者出现更多恶心、呕吐、食欲减退现象(P<0.05),且贝那鲁肽组患者普遍较利拉鲁肽组症状严重,个别患者需应用胃复安等促胃动力药物,但总体来说,3组胃肠道反应均发生在治疗开始后1周以内,经过药物及心理疏导等干预措施,后期均可逐渐耐受。另外,本研究观察到治疗12周后3组BMI均低于治疗前(P<0.05),且贝那鲁肽组BMI低于利拉鲁肽组和度拉糖肽组(P<0.05),推测贝那鲁肽更强地抑制食欲、减少胃排空作用,可能是造成体重降低的重要因素。已有的相关研究证实[8-10],GLP-1受体激动剂在引起更多胃肠道不适的同时,减少更多热量摄入,从而导致体重减少。事实上,利拉鲁肽已被批准肥胖症治疗的适应证。
临床研究发现,和格列美脲相比,度拉糖肽能够显著改善胰岛β细胞功能[11]。动物试验报道,经过12周利拉鲁肽干预,糖尿病小鼠的病态胰岛形态部分恢复,胰岛β细胞凋亡得到抑制[12]。也有相关动物试验报道,利拉鲁肽通过上调胰岛素信号转导和胰岛素整合受体表达,改善胰岛素抵抗指数[13]。本研究经过临床干预12周后,3组患者HOMA-β高于治疗前(P<0.05),且反映胰岛素抵抗的指标HOMA-IR均减低(P<0.05),提示GLP-1受体激动剂类药物可能具有保护胰岛功能、改善胰岛素抵抗作用的类效应。
糖尿病患者胰岛素抵抗产生多种炎性因子,加重内质网氧化应激,而抑制应激生成可通过减少血管内皮细胞凋亡延缓糖尿病肾病进展[14]。研究表明,利拉鲁肽可以抑制细胞凋亡,改善肾脏内皮功能,减少糖尿病患者尿蛋白排泄率[15-16]。一般认为,UACR反映了早期糖尿病肾病内皮细胞受损、微血管病变的严重程度。本研究结果显示,治疗12周后,3组UACR水平均低于治疗前(P<0.05),推测GLP-1受体激动剂通过改善胰岛素抵抗,减少氧化应激导致内皮受损,从而减少尿蛋白,保护肾脏功能。另外研究发现,血糖波动与尿蛋白增加密切相关[17],而GLP-1受体激动剂度拉糖肽的血药浓度稳定可以发挥更平稳的降糖作用。
TIR是葡萄糖浓度在不同指定范围内的时间,与HbA1c具有一定相关性,且更能反映血糖控制的多维视角,近年来,以TIR为参数了解血糖波动对糖尿病并发症风险评估重要价值的相关研究日益增多。本研究通过动态血糖监测系统监测3组患者24 h血糖波动曲线,计算血糖在3.9~10.0 mmol/L目标范围内的TIR及MAGE。结果显示,治疗12周后3组TIR均高于治疗前(P<0.05),MAGE均低于治疗前(P<0.05),证实GLP-1受体激动剂能够在有效降糖的同时减少血糖波动,其中度拉糖肽组较其他2组血糖TIR更高,MAGE波动更低,TIR与UACR呈负相关,说明血糖稳定是度拉糖肽减少早期糖尿病肾病微量蛋白尿的有利因素。
综上所述,利拉鲁肽、度拉糖肽及贝那鲁肽均可有效降糖,升高TIR,保护胰岛功能,减少尿微量白蛋白;度拉糖肽治疗后TIR改善最明显,提示具有更好地平稳降糖效果,减少血糖波动,从而延缓早期糖尿病肾病的发生发展;贝那鲁肽有更强地控制餐后血糖、减轻体重,但胃肠道反应发生率高。
