MnCu-SSZ-13@CeO2分子筛核壳结构催化剂的合成及其NH3-SCR性能
2022-03-18王志恒何丹丹刘立成
王志恒,何丹丹,刘立成*
(1 中国科学院 青岛生物能源与过程研究所,山东 青岛 266100; 2 中国科学院大学,北京 100049)
氮氧化物(NOx)的大量排放会造成严重的环境污染,深刻影响人类的生存环境[1-3]。近年来,以氨气为还原剂的选择性催化还原反应(NH3-SCR)成为降低NOx排放的有效方法,而催化剂的性能是影响上述反应活性的重要因素[4]。具有微孔结构的Cu-SSZ-13和Cu-SAPO-34催化剂在SCR反应中展示出较宽的催化反应区间和良好的水热稳定性,尤其是Cu-SSZ-13分子筛催化剂被认为是最有潜力的下一代脱硝催化剂[5]。大量实验研究表明,Cu-SSZ-13催化剂在200~500 ℃温度区间内能够实现NOx的有效催化转化,但是当温度低于200 ℃时反应效果并不理想;另外,抗硫性能差也是该催化剂的一个重要缺陷[6]。因此,改善Cu-SSZ-13分子筛催化剂的低温活性并提升其抗硫性能是推广应用Cu-SSZ-13需要突破的瓶颈问题。
对以SSZ-13分子筛为载体的催化剂而言,金属活性中心的种类和分布在催化反应中起着关键作用,尤其是不同种类的活性金属可以在不同温度区间内发挥各自的催化性能和抗硫性能。目前,通过引入不同活性金属成分(Fe、Mn、Ce、Ti、Zr等)来改善 Cu-SSZ-13催化剂反应性能的策略已经得到广泛关注[7-9]。在应用于脱硝反应的多种金属类催化剂中,锰氧化物(MnOx)催化剂由于具有丰富的活性位点和较强的氧化还原性,展现出良好的低温NH3-SCR催化活性。据报道,锰改性的Cu-SSZ-13催化剂可以在150~200 ℃温度区间内实现较高的低温催化活性,但其高温催化活性和水热稳定性较差[10]。
核壳结构催化剂由于结构独特,可以充分发挥多组分功能以改善催化活性,还可以保护催化剂的活性内核组分,抑制高温下的金属聚集,提高催化剂的水热稳定性。此外,核壳结构催化剂的外部壳层可以阻止SO2进入核中生成硫酸盐或亚硫酸盐物种,进而抵抗SO2中毒。鉴于上述优势,核壳结构催化剂已经成为当前的研究热点之一[11]。
由于SSZ-13分子筛的晶粒较大、孔径较小,包覆在其表面的金属氧化物极易进入孔道造成孔堵塞,试图通过控制壳层自组装合成核壳催化剂的策略仍然存在诸多挑战[12-14]。近年来,已有部分研究采用自组装技术合成了一系列以分子筛或金属为核、以金属氧化物为壳的核壳催化剂。例如,Zhang等采用化学沉积法制备了具有核壳结构的CeO2-MnOx催化剂,并将其应用于NH3-SCR反应[15];Chi等制备了结构中空、以Fe-ZSM-5为核、以CeO2为壳的Fe-ZSM-5@CeO2催化剂,该催化剂表现出优于CeO2和Fe-ZSM-5催化剂的抗H2O和抗SO2中毒性能[16]。虽然已有研究报道了分子筛@金属氧化物类核壳结构催化剂,且其在脱硝反应中表现出优异的催化性能,但是能够用于催化NH3-SCR反应并以SSZ-13为核的催化剂还很少见。
本文以Cu-SSZ-13为研究对象,首先通过负载过渡金属Mn来提高其低温NH3-SCR反应性能,继而通过自组装方法以CeO2为壳制备核壳结构催化剂MnCu-SSZ-13@CeO2。将所制备的催化剂应用于NH3-SCR反应并评价其催化活性和抗硫性能,通过NH3程序升温脱附(NH3-TPD)和H2程序升温还原(H2-TPR)技术探究催化剂的氧化还原能力及表面酸性位点分布情况,同时采用X射线衍射(XRD)、扫描电镜(SEM)和透射电镜(TEM)等技术对核壳催化剂的物化性质进行表征。
1 材料与方法
1.1 实验试剂
实验所用试剂及规格如下:铝酸钠(化学纯)、硅溶胶(纯度30%)、去离子水、氢氧化钠(化学纯)、金刚烷胺(TMAdaOH,质量分数25%)、氯化铵(化学纯)、二水合氯化铜(化学纯)、四水合氯化锰(化学纯)、六水合硝酸铈(化学纯)。
1.2 催化剂的合成
采用三步制备MnCu-SSZ-13@CeO2催化剂,合成过程如图1所示。步骤一:采用水热法合成Na-SSZ-13(Si/Al=15)分子筛。先将NaOH溶于去离子水中,搅拌至完全溶解,再加入NaAlO2搅拌均匀;滴加适量TMAdaOH至前述溶液中,搅拌溶解1 h后逐滴加入硅溶胶,持续搅拌老化24 h,形成前驱溶液;将上述前驱溶液转移至聚四氟乙烯内衬,装入不锈钢反应釜,放入均相反应器中,以60 r/min的速度在100 ℃条件下晶化12 h,160 ℃反应3 d;将反应釜中得到的产物离心,洗涤3次,60 ℃烘箱内干燥过夜,600 ℃条件下焙烧8 h,得到Na-SSZ-13粉末。步骤二:采用共同离子交换制备MnCu-SSZ-13。将Na-SSZ-13加入1.0 mol/L的NH4Cl溶液中,水浴加热至80 ℃,搅拌12 h,离心洗涤3次,60 ℃烘箱干燥过夜,得到H-SSZ-13;将H-SSZ-13加入CuCl2和MnCl2的混合水溶液中,水浴加热至80 ℃,搅拌8 h,离心洗涤3次,60 ℃烘箱干燥过夜;样品放入马弗炉中焙烧,以5 ℃/min的速率升温至500 ℃,保持6 h,得到MnCu-SSZ-13。步骤三:将MnCu-SSZ-13分子筛在无水乙醇和去离子水的混合溶液中均匀分散,将聚乙烯吡咯烷酮加入上述溶液中,搅拌均匀;加入不同量的六亚甲基四胺(0.15、0.3、0.6 g)搅拌2 h;加入不同量的Ce(NO3)3(0.2、0.4、0.8 g)后60 ℃水浴2 h;将上述溶液离心洗涤,60 ℃真空干燥过夜,马弗炉中以5 ℃/min的速率升温至500 ℃,焙烧3 h,得到MnCu-SSZ-13@CeO2催化剂。将制备的Ce(NO3)3添加量为0.2 g、0.4 g和0.8 g的催化剂分别命名为MnCu-SSZ-13@CeO2-1、MnCu-SSZ-13@CeO2-2和MnCu-SSZ-13@CeO2-3。

图1 MnCu-SSZ-13@CeO2催化剂合成过程示意图Fig.1 Schematic diagram of the fabrication process for MnCu-SSZ-13@CeO2 catalyst
1.3 催化剂的表征
通过X射线衍射(XRD)对样品进行物相检测,使用Cu靶Kα (λ=0.154 06 nm)作为辐射源,扫描速度为6(°)/min,扫描范围为5°~80°。通过透射电子显微镜(TEM)观察MnCu-SSZ-13@CeO2核壳催化剂的颗粒尺寸和表面形貌,结合高分辨透射电子显微镜(HRTEM)观察催化剂的结晶情况。通过TEM配套的能谱仪器(EDX)对MnCu-SSZ-13@CeO2催化剂进行面扫以分析各组分的分布情况,并进行线扫以分析壳层元素的分布情况。为了阐明样品表面Mn、Cu物种的化学状态,在Thermo Fisher-ESCALAB 250Xi系统上对催化剂进行X射线光电子能谱(XPS)分析。
使用化学吸附分析仪(AutoChem Ⅱ 2920)进行NH3程序升温脱附(NH3-TPD)和H2程序升温还原(H2-TPR)。NH3-TPD测试过程如下:样品在500 ℃氩气气氛中预处理1 h,然后冷却至50 ℃;将气流切换成体积分数为5%的NH3/Ar气氛(100 mL/min),并在100 ℃条件下吸收1 h;将气流改为纯Ar 30 min,直到基线稳定,并在相同Ar气流中以10 ℃/min的加热速率从50 ℃程序升温热至600 ℃。H2-TPR测试过程如下:100 mg样品(40~60目)在350 °C氩气气氛(30 mL/min)中预处理1 h,然后冷却至50 ℃;将样品置于体积分数为10%的H2/Ar气氛中,并以10 °C/min的加热速率从50 ℃程序升温至850 ℃。
1.4 催化剂的NH3-SCR活性及耐硫性测试
将所制备的粉末状催化剂压片后造粒至40~60目,取少量装入反应管中,并将反应管置于可以加热的反应炉内部。反应气体的体积分数为:0.05% NO,0.05% NH3,10% O2;平衡气为N2,气体总流量为200 mL/min,控制反应空速(GHSV)为150 000 h-1。
催化反应过程中,尾气采用装配2 m光程气体池的傅里叶红外光谱仪(Nicolet iS50)进行在线分析检测,反应温度为100~600 ℃。耐硫反应的测试温度为300 ℃,在反应气体中加入体积分数为0.01%的SO2后,标准NH3-SCR条件下测试催化剂的耐硫性能。
2 结果与讨论
2.1 催化剂结构特征分析
2.1.1 催化剂的XRD结果
图2为不同催化剂的XRD谱图,在2θ为9.5°、14.0°、16.1°、17.8°、20.7°、25.1°、26.2°、30.7°时,所有催化剂均出现了明显的归属于SSZ-13晶体的特征衍射峰,代表了典型的CHA晶型结构。与MnCu-SSZ-13相比,MnCu-SSZ-13@CeO2系列催化剂的XRD谱图中SSZ-13晶体的特征衍射峰得以保留,只有28.5°和48°附近的特征峰对应于CeO2特征峰[17]。随着催化剂中CeO2含量(壳层厚度)的增加,CeO2特征峰的强度增加,结晶度增强。

图2 MnCu-SSZ-13@CeO2催化剂的XRD图谱Fig.2 XRD patterns of MnCu-SSZ-13@CeO2 catalysts
2.1.2 催化剂的TEM和HRTEM结果
图3展示了MnCu-SSZ-13@CeO2系列催化剂的TEM和HRTEM 结果。如图3a所示,MnCu-SSZ-13表现出与SSZ-13类似的立方体形貌。图3b、3c和3d展示了不同含量CeO2包覆MnCu-SSZ-13的TEM图像,从中可以清楚地观察到MnCu-SSZ-13立方体外表面具有被CeO2纳米颗粒包覆的粗糙表面层。TEM元素分布图见图3e,Si元素、Mn元素和Cu元素均匀地分布在SSZ-13晶体表面,且Ce元素在边缘分布较为集中,中间分布均匀,进一步证明了MnCu-SSZ-13的核壳结构。根据线扫结果图3f可知,Ce元素主要集中在壳层,其他元素在分子筛中均匀分布, CeO2壳层厚度约为10 nm。由图3g可以看出,宽度为0.31 nm的有序晶格条纹对应于CeO2(JCPDS PDF#34-0394)的(111)晶面。综上,CeO2成功包覆在MnCu-SSZ-13表面。

a、b、c、d分别为MnCu-SSZ-13、MnCu-SSZ-13@CeO2-1、MnCu-SSZ-13@CeO2-2、MnCu-SSZ-13@CeO2-3的TEM图像;e为MnCu-SSZ-13@CeO2-1的高分辨TEM图像及对应的元素分布图;f为MnCu-SSZ-13@CeO2-1的线扫元素分布图;g为MnCu-SSZ-13@CeO2-1的高分辨TEM图像。
2.1.3 催化剂的XPS结果
图4是MnCu-SSZ-13@CeO2系列催化剂的XPS谱图及其分析结果,可以看出4种催化剂均含有Cu、Ce、O元素。未包覆CeO2的MnCu-SSZ-13催化剂能明显看到不同位置的Cu2+和Cu+,而MnCu-SSZ-13@CeO2催化剂由于CeO2的包裹,表面Cu物种减少。对于MnCu-SSZ-13@CeO2测试中Cu 2p的XPS结果(图4a),可能是由表面 Cu 单质或其氧化态物质形成的,由于CeO2的包覆,强度略有降低。
Ce3+和Ce4+共存于CeO2包覆后的MnCu-SSZ-13表面。对Ce 3d的XPS图谱(图4b)进行分峰处理,可以得到10个峰:u(881.5 eV)、u′(886.2 eV)、 u″(900.8 eV)、u‴(905.7 eV)、v(883.4 eV)、v′(889.0 eV)、v″(898.1 eV)、v‴(903.2 eV)、v″″(907.6 eV)和v″″′(916.4 eV),分别对应于5对自旋双轨道。其中,u、u′、v、v′、v″和u″、u‴、v‴、v″″、v″″′分别为Ce 3d5/2和Ce 3d3/2的多重轨道。图4b中Ce3+的峰被标注为u,被标注为v的峰被认为是Ce4+的峰。由于Ce4+在壳层CeO2中,大量NO在通过氧化层时能够被预氧化为NO2,从而加速SCR反应[18]。MnCu-SSZ-13@CeO2-1、MnCu-SSZ-13@CeO2-2和MnCu-SSZ-13@CeO2-3的Ce4+/Ce3+比值分别为1.49、1.28和1.30。

Ⅰ代表MnCu-SSZ-13;Ⅱ代表MnCu-SSZ-13@CeO2-1;Ⅲ代表MnCu-SSZ-13@CeO2-2; Ⅳ代表MnCu-SSZ-13@CeO2-3。
图4 MnCu-SSZ-13@CeO2系列催化剂的XPS谱图
Fig.4 The XPS spectra for the series of MnCu-SSZ-13@CeO2catalysts
据文献报道,图4c中结合能为532.3 eV(Oα)的峰为吸附H2O中的O,结合能为529.7 eV(Oβ)的峰为晶体晶格氧[19]。在CeO2包覆MnCu-SSZ-13后,晶格氧的对应峰出现,证明了CeO2的存在;并且随着CeO2含量的增加,晶格氧所占比例也增加。
4种催化剂中元素的相对含量和绝对含量统计结果分别如图4d和表1所示。可以看出,包覆的铈质量分数随着其添加量的增加而升高,从3.16%增加到8.11 %。Si、Cu和Mn的含量随着铈包覆量的增加逐渐降低,但晶格氧(Oα)的含量却逐渐增加。对于MnCu-SSZ-13@CeO2-1、MnCu-SSZ-13@CeO2-2和MnCu-SSZ-13@CeO2-3催化剂,CeO2中的氧主要以晶格氧的形式存在,Oα/Oβ分别为0.17、0.37和0.46。

表1 通过XPS分析和ICP测试得到的催化剂中各元素含量Tab.1 Element contents in the catalysts provided by XPS and ICP
2.1.4 催化剂的NH3-TPD和H2-TPR结果
在NH3-SCR反应中,催化剂的表面酸性对催化性能具有显著影响。图5a给出了MnCu-SSZ-13、MnCu-SSZ-13@CeO2-1、MnCu-SSZ-13@CeO2-2和MnCu-SSZ-13@CeO2-3催化剂的NH3-TPD结果,用于分析催化剂的表面酸浓度和酸强度。位于180 ℃左右的脱附峰归属为NH3的物理吸附和在弱Lewis酸性位点的吸附,位于300 ℃的脱附峰归属为NH3在强Lewis酸性位点的吸附,位于480 ℃的峰被定义为NH3在强Brφnsted酸性位点的吸附。低于250 ℃时,所有催化剂都有强脱附峰,说明催化剂与NH3形成的键较弱,NH3容易脱附[20]。而NH3在越高温度下脱附,催化剂高温吸附NH3的稳定性越强。相较于MnCu-SSZ-13,MnCu-SSZ-13@CeO2-1催化剂的脱附峰位置整体右移,说明适量引入CeO2壳层增强了MnCu-SSZ-13的酸强度,改善了催化剂的活性;但CeO2包覆量高的MnCu-SSZ-13@CeO2-3并没有表现出优于MnCu-SSZ-13的酸性。
通过测试MnCu-SSZ-13、MnCu-SSZ-13@CeO2-1、MnCu-SSZ-13@CeO2-2和MnCu-SSZ-13@CeO2-3的H2-TPR,考察催化剂的氧化还原性,结果如图5b所示。MnCu-SSZ-13主要表现出4个还原峰,低于650 ℃的还原峰为Cu2+还原为Cu+,高于650 ℃的还原峰为Cu+还原为Cu0。其中,在210 ℃出现的还原峰归属为八元环中的Cu2+还原为Cu+,在360 ℃出现的还原峰归属为CHA笼中的Cu2+还原为Cu+,在580 ℃出现的还原峰归属为六元环中的Cu2+还原为Cu+,而在800 ℃出现的还原峰归属为Cu+还原为Cu0。相比于MnCu-SSZ-13,MnCu-SSZ-13@CeO2催化剂的所有低温峰强度都有所增加并向右移动,认为是包裹的CeO2改变了催化剂的氧化还原性能,提高了Cu2+的低温还原能力,进而改善了催化剂的SCR反应性能;而MnCu-SSZ-13@CeO2的580 ℃还原峰向低温移动,说明出现的Ce4+还原使得峰值左移。
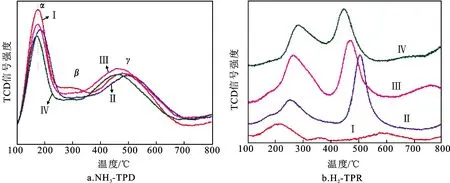
Ⅰ代表MnCu-SSZ-13;Ⅱ代表MnCu-SSZ-13@CeO2-1;Ⅲ代表MnCu-SSZ-13@CeO2-2; Ⅳ代表MnCu-SSZ-13@CeO2-3。
2.2 催化剂性能分析
以MnCu-SSZ-13为核、CeO2为壳合成了一系列核壳结构催化剂,其中CeO2质量分数是指壳层中Ce的质量占MnCu-SSZ-13@CeO2总质量的百分比。不同CeO2质量分数的MnCu-SSZ-13@CeO2催化剂的NH3-SCR反应活性如图6a所示。可以看出,CeO2质量分数对催化剂的催化性能有显著影响,MnCu-SSZ-13@CeO2-1的NOx转化率略高于其他催化剂。随着CeO2质量分数的增加,催化剂的低温催化活性明显下降,当增大到6.43%时,NOx转化率开始低于未负载CeO2的MnCu-SSZ-13催化剂。当MnCu-SSZ-13@CeO2中CeO2质量分数为8.11%时,MnCu-SSZ-13@CeO2-3催化剂具有较好的高温催化活性,说明CeO2可以显著提高催化剂的高温活性。而当CeO2质量分数为3.16%时,催化剂不仅具有最高的低温催化活性,同时也表现出较高的高温催化性能,说明CeO2和MnCu-SSZ-13的协同作用可以明显改善MnCu-SSZ-13的催化活性。
结合催化剂的活性和结构分析可知,新型MnCu-SSZ-13@CeO2-1催化剂通过MnCu-SSZ-13和CeO2的协同作用,构建了层次化的核壳结构。与单独MnCu-SSZ-13催化剂相比,CeO2壳层可以提供更高活性的SCR环境,促进NO氧化和NH3-SCR反应进行,这是MnCu-SSZ-13@CeO2催化剂低温活性提升的重要原因。但当CeO2含量过高时,在构建核壳结构的过程中可能会造成MnCu-SSZ-13催化剂的CeO2壳层变厚或孔道堵塞,进而抑制反应气体向分子筛笼内的快速扩散和NOx与活性位点之间的接触,降低反应活性。研究表明适量的CeO2壳层结构不仅能够促进NH3在Brφnsted或Lewis酸性位点上的吸附,还可以促进活性硝酸盐物种的形成。MnCu-SSZ-13@CeO2表面的Ce4+和活性氧可以有效促进NO的吸附和活化,并进一步与气态NH3反应生成N2和H2O[12],这导致其催化活性明显优于MnCu-SSZ-13催化剂。
在温度为300 ℃、进气中SO2体积分数为0.01%的条件下对催化剂进行耐硫性能测试,结果如图6b所示。可以看出,在SO2存在的条件下, MnCu-SSZ-13@CeO2催化剂具有相对较高的NOx转化率, 说明核壳结构催化剂比MnCu-SSZ-13具有更高的抗SO2中毒能力。这是因为CeO2壳层一方面可以有效抑制硫酸盐的形成,另一方面可以抑制形成的硫酸盐堵塞活性位点,从而提升了催化剂的抗硫性[21]。但是随着催化剂中CeO2包覆量的增加,MnCu-SSZ-13@CeO2-2和MnCu-SSZ-13@CeO2-3的抗硫性变差。
Ⅰ代表MnCu-SSZ-13;Ⅱ代表MnCu-SSZ-13@CeO2-1;Ⅲ代表MnCu-SSZ-13@CeO2-2; Ⅳ代表MnCu-SSZ-13@CeO2-3。
图6 催化剂的NOx转化率(a)和耐硫中毒性能测试(b)
Fig.6 NOxconversion (a) and SO2resistance (b) tests of different catalysts
3 结语
通过水热合成、双金属离子交换和自组装方法制备了一系列MnCu-SSZ-13@CeO2核壳结构催化剂,并成功实现了其较高的NH3-SCR反应活性。TEM、HRTEM、XRD和XPS分析结果表明成功合成了核壳结构的MnCu-SSZ-13@CeO2催化剂,通过XRD可以看出明显的CeO2特征峰,XPS中Cu含量的降低及晶格氧的出现进一步证明了核壳结构的存在。NH3-TPD和H2-TPR结果表明核壳结构的MnCu-SSZ-13@CeO2可以提高催化剂的酸性和氧化还原能力,进而改善NH3-SCR的反应性能。CeO2含量决定了壳层厚度,其中MnCu-SSZ-13@CeO2-1具有最适CeO2含量和较高的NOx转化率,且其抗硫性能也明显优于其他催化剂。
