继发于干燥综合征的帕金森综合征1例报告
2022-03-18胡必琴詹剑
胡必琴,詹剑
帕金森综合征是指有运动迟缓、静止性震颤和(或)肌肉僵直症状,并能找到明确的病因,包括药物使用、感染、中毒、脑血管疾病及免疫异常等的一种疾病[1]。原发性干燥综合征(sjögren's syndrome,SS)是一种常见的全身性自身免疫性疾病,组织学特征是腺泡内的局灶性淋巴细胞浸润,女性与男性的发病率比为9∶1,约< 5%的患者有中枢神经系统受累[2],有研究显示SS是发生帕金森综合征的独立危险因素[3]。至今,国内外有关继发于干燥综合征的帕金森综合征个案报道共22例,作为少见病,目前尚未形成统一的诊断标准[4]。此类患者初诊时多被误诊为帕金森病,其治疗效果差,甚至病情被延误。本文旨在通过1例个案报告并结合相关文献复习,为临床诊疗提供一定依据。
1 病例报告
患者,女,39岁,因“左侧肢体僵硬1+年,加重20+d”于2020年8月2日收入本院神经内科诊治。1+年前无明显诱因出现左侧肢体僵硬、运动迟缓,活动时见左侧肢体震颤,静止时好转,症状晨轻暮重,曾于外院诊断“帕金森病”,服用“多巴丝肼”治疗3 d后出现恶心、呕吐,遂自行停药,改口服中药(具体不详),上述症状无明显好转;多次就诊于外院查头颅MRI、颈椎MRI、头颈部CTA、胸椎、腰椎DR片均未见异常;20+d前左侧肢体僵硬、运动迟缓加重,无明显眼干、口干症状,于本院门诊就诊,以“肢体僵硬”原因收入院。既往体健,无服用抗精神病等药物史,无相关家族遗传病史。查体生命体征平稳,心、肺、腹查体未见异常,神经系统查体:左侧肢体肌张力增高(齿轮样强直),运动迟缓,行走拖曳,活动时可见左侧肢体轻微震颤,静止时消失,余神经系统查体阴性。辅助检查:抗SSA抗体+++,抗SSB抗体++,抗RO-52抗体+++,余阴性;抗核抗体(1∶100)为阳性,抗核抗体(1∶320)为弱阳性,抗核抗体(1∶1 000)为阴性;抗GBM抗体为弱阳性;血类风湿因子、抗环瓜氨酸肽抗体、cANCA、pANCA、抗PR3抗体、抗MPO抗体、免疫球蛋白、铜蓝蛋白、肝功能、血常规、血沉、C-反应蛋白、乙肝5项、HIV、梅毒均未见异常。新斯的明实验为阴性。视觉诱发电位及四肢感觉传导速度未见异常;四肢静脉、右上肢动脉彩超均未见异常。唇腺病理活检提示组织慢性炎性改变,Chishiolm分级3级:1个灶淋巴细胞浸润(图1)。
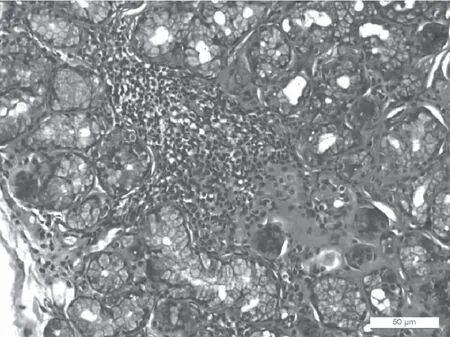
图1 本文患者的唇腺活检结果
2 治疗经过
患者有运动迟缓、肌张力增高,诊断帕金森综合征。相关检查回报后请眼科会诊:未见K-F环,考虑干眼症;肾病风湿科会诊:考虑“干燥综合征”,建议查唇腺活检、加羟氯喹治疗。结合唇腺病理活检结果,符合SS诊断标准,考虑帕金森综合征继发于SS。予替扎尼定2 mg口服,3次/d治疗2 d后上述症状缓解不明显;加用多巴丝肼片0.125 g口服,3次/d、硫酸羟氯喹片0.2g口服,3次/d治疗3 d后症状稍改善,因服用多巴丝肼患者恶心、呕吐症状明显,遂停用;治疗方案调整为替扎尼定4 mg口服,3次/d、硫酸羟氯喹片0.4 g口服,2次/d,治疗3 d后患者运动迟缓及肢体震颤缓解,肌张力较前稍降低,出院后规律服用上述药。2021年1月21日电话随访患者诉肢体僵硬、运动迟缓及震颤等症状基本消失。
3 讨论
与帕金森病的静止性震颤不同,本例患者表现为运动性震颤,这与Barba等的发现相符,Barba等[5]分析既往报道的17例继发于SS的帕金森综合征患者,发现约88.23%的患者表现为肌肉僵硬、82.3%表现为运动迟缓、58.8%表现为短步步态、47%表现为静止和(或)运动性震颤,故认为本例患者的运动性震颤症状符合继发于SS的帕金森综合征的临床表现。
继发于SS的帕金森综合征需与原发性、其他继发性帕金森综合征及其他运动障碍性疾病相鉴别。原发性帕金森病常见于65岁以上中老年人群、对左旋多巴制剂敏感;早发型帕金森病虽发病年龄≤50岁、有帕金森病症状、可表现为晨轻暮重,但具有早期对小剂量左旋多巴制剂治疗非常敏感、与遗传因素密切相关的特点[6]。常见的运动障碍性疾病包括:肝豆状核变性及多巴反应性肌张力障碍等,肝豆状核变性患者体内铜代谢异常引起血清铜蓝蛋白高、肝功能异常、角膜有K-F环;多巴反应性肌张力障碍患者左旋多巴制剂治疗效果好。以上疾病均与本例患者临床特征不符。结合本例患者病史及检查,可除外药源性、血管性帕金森综合征、多系统萎缩、重症肌无力及精神疾病等所致运动障碍。
该病可能的发病机制有:(1)SS患者体内高浓度的炎症因子通过引起神经炎症,诱导多巴胺能细胞死亡,而引起SS全身炎症反应的IL6和TNF-α可能是关键炎性因子[7-8];(2)Hassin-Baer等[9]认为SS患者体内抗β2-GPI 抗体升高引起基底神经节血管炎,导致帕金森综合征症状出现。本例患者血常规、血沉、C-反应蛋白等炎症指标均正常,未能查TNF-α和IL-6,但Chen等[7]发现,抗SSA或抗SSB抗体阳性的患者体内的TNF-α和IL-6细胞因子水平明显升高,且无眼干、口干症状,与本例患者临床特征相符,由此可合理推断:该患者体内的TNF-α和IL-6细胞因子可能较高,诱导多巴胺能细胞死亡,引起神经炎症,导致帕金森综合征症状出现。本例患者血清免疫球蛋白水平正常,头颅MRI提示基底节区域无炎性改变征象,故基底神经节血管炎导致帕金森综合征症状的可能性不大。
既往报道的个案中,约52.5%的患者头颅MRI显示白质、纹状体或苍白球的T2和FLAIR呈高信号[5],本病例的头颅MRI未见上述异常,可能与患者病程较短、神经系统损害不重有关,这也与本例患者临床症状不严重相一致。
既往的文献报道中,继发于SS的帕金森综合征的治疗包括免疫抑制疗法和对症治疗,欧洲抗风湿病联盟建议:合并系统性疾病的SS患者,若在一个临床领域表现出中度疾病活动或总体中度疾病活动(评分>5分),可遵循糖皮质激素、免疫抑制剂和生物制剂的顺序(或联合)使用,糖皮质激素为首选,在病情严重患者中可以考虑使用利妥昔单抗[10]。此类帕金森综合征患者多数使用激素治疗后能迅速、有效地改善临床症状[5,11-12],但也有报道发现,激素并不能改善神经症状,甚至会增加焦虑、抑郁情绪[13];左旋多巴制剂的治疗很少能减轻此类帕金森综合征的症状[5],部分患者虽然在使用初期症状能得到改善,但疗效会逐渐消失[14],不过,虽然左旋多巴的治疗效果差,但能延缓疾病进展[15],因此,可酌情加用,但不主张单独使用。在本病例的的治疗中患者拒绝激素等免疫抑制剂治疗,故服用羟氯喹治疗;羟氯喹是治疗SS的有效药物,通过减少炎症介质的产生来影响免疫反应;既往没有使用羟氯喹治疗继发于SS的帕金森综合征的报道,本例患者服用羟氯喹治疗后,帕金森综合征症状明显好转,因此,羟氯喹也是治疗此类帕金森综合征可考虑的药物。近年来中医也在不断探索SS的治疗方案,中药治疗可以使SS并发神经系统疾病的患者病情逐渐稳定、免疫指标恢复正常[16],且极少发生不良反应[17]。标准、规范的中药治疗也是可考虑的治疗方法。
本病例以神经系统受累为首发症状就诊,无明显口干、眼干症状,既往也有SS累及肾脏以重度低钾为首发症状就诊的病例报道[18],由此可见,SS累及全身其他系统时,腺体外症状可先于眼干、口干症状出现,极易造成漏诊,甚至误诊。总之,临床遇到以帕金森综合征症状来就诊的年轻患者,要尽量寻找病因,尤其是左旋多巴制剂治疗后症状无明显改善者,SS也是需要考虑的可能病因。
