LiCoO2-SiO/石墨锂离子电池循环衰减机理研究
2022-03-03孟繁慧甄会娟
周 江,孟繁慧,朱 莎,甄会娟,黄 铃
(天津力神电池股份有限公司,天津 300384)
锂离子电池在消费类电子产品、电动汽车和储能等领域[1]均已经得到广泛应用,轻量化、高比能量、长使用寿命一直是锂离子电池产品追求的目标。
硅基负极材料具有较高的理论比容量,作为高能量密度锂离子电池负极的技术方案倍受关注[2-3]。硅基负极材料目前主要包括硅负极材料和氧化亚硅负极材料。硅负极嵌锂后,最高锂硅比为4.4∶1,硅负极理论比容量高达4 200 mAh/g,但是,硅负极嵌锂后的体积膨胀较大,其体积膨胀可达300%。氧化亚硅负极材料结构中的氧原子可以缓冲硅基材料嵌锂后的体积膨胀,综合性能较好,得到了广泛的应用研究[4-5]。
目前,硅基负极仍然存在很多问题,阻碍了其大规模应用,如硅基负极材料在完全嵌锂状态下的体积膨胀不仅会导致SiO 负极颗粒破碎,还会对极片结构造成不可逆损伤。此外,硅负极的充放电电压平台较高,所以与石墨材料复合使用时,会对电池电化学性能造成影响。而随着循环的进行,上述不利因素均会加速电池性能衰减[6-7],所以,有必要对SiO负极电池体系循环衰减机理进行持续深入的研究。
1 实验
1.1 电池与材料
实验电池为软包锂离子电池,该电池正极活性物质为LiCoO2,负极活性物质为SiO 负极与人造石墨的复合负极。选择负极活性物质中SiO 质量分数为12%、20%和40%的SiO 与人造石墨复合负极制作软包锂离子电池,正负极的可逆容量比为1∶1.05。电解液配比为1 mol/L LiPF6/(EC+PC+DEC+EMC)(体积比20∶10∶30∶40),添加剂氟代碳酸乙烯酯(FEC)、1,3-丙磺酸内酯(PS)和己二腈(ADN)的质量分数分别为5%、3%、3%,注液量为1.9 g/Ah。隔膜采用16 μm 聚乙烯(PE)隔膜。扣式电池(CR2430)采用锂金属片为负极。
1.2 仪器与测试
使用多功能电池测试设备进行扣式电池(CR2430)和软包电池的充放电测试,使用电化学工作站进行电化学阻抗谱(EIS)测试。使用电池充放电设备进行扣式电池和软包电池的充放电曲线测试。使用离子束抛光设备对LiCoO2正极片进行表面抛光,使用扫描电子显微镜(SEM)进行正负极形貌表征及元素扫描。
2 结果与讨论
2.1 SiO 材料及LiCoO2-SiO/扣式电池表征
对负极活性物质中SiO 进行XRD 表征,如图1(a)所示,SiO 材料XRD 曲线有Si 的信号,说明所用SiO 材料中含有Si单质。图1(b)为不同SiO 含量负极扣式电池充放电曲线,随着SiO 材料含量的增加,扣式电池充放电平台逐渐上升,扣式电池的首次效率逐渐减小,SiO 含量为12%、20%和40%的扣式电池首次效率分别为84.4%、81.7%和80.1%。
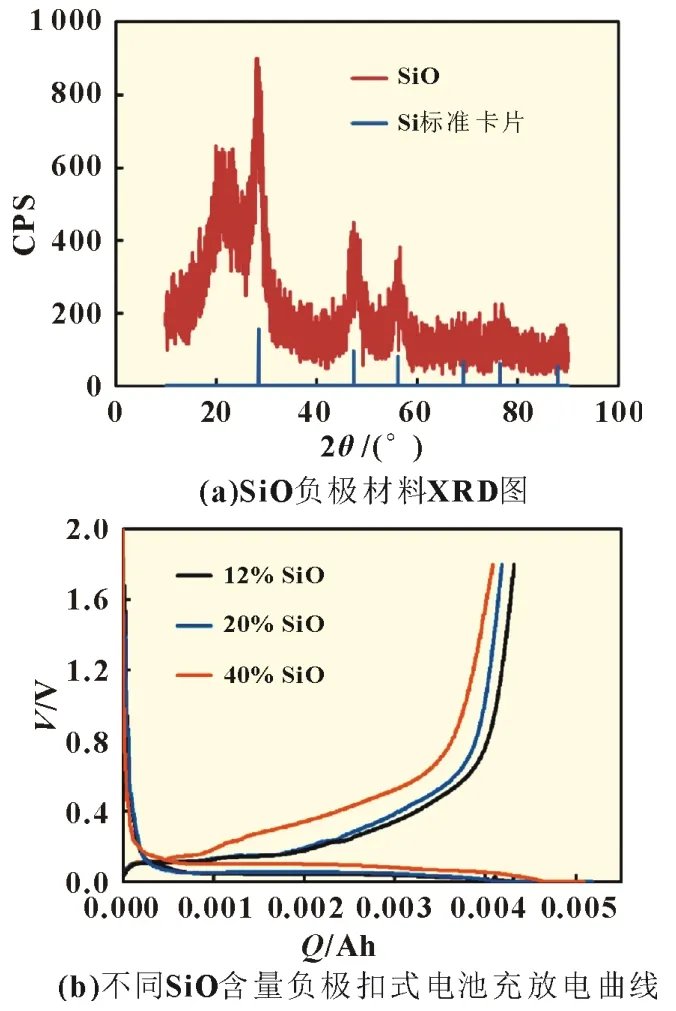
图1 SiO负极材料XRD及不同SiO含量负极扣式电池充放电曲线
2.2 LiCoO2-SiO/石墨软包电池性能表征
2.2.1 充放电性能表征
对负极活性物质中含量为12%、20%和40%的SiO 与人造石墨复合负极软包锂离子电池(简称12% SiO、20% SiO、40% SiO 锂离子电池)进行充放电测试及循环性能测试,并采用增量容量分析表征其电化学过程[8]。图2 为不同SiO 含量负极电池充放电曲线及dQ/dV-V曲线。充放电曲线测试结果表明,随着SiO 含量的增加,LiCoO2-SiO/石墨电池的充放电容量逐渐减小。不同SiO 含量负极电池的dQ/dV-V充电曲线在3.6~4.2 V 有3 个特征峰,说明电池在充电过程中有3 个电压平台,但是,随着SiO 含量的增加,较低电压特征峰高度逐渐减小,较高电压特征峰逐渐消失,表明SiO 含量的增加加剧了电池充电过程中的极化现象。12% SiO 负极电池的dQ/dV-V放电曲线在3.2~4.4 V 有5 个特征峰,说明电池在放电过程中有5 个电压平台,但是,随着SiO 含量的增加,电压特征峰数量逐渐减少,表明SiO 含量的增加加剧了电池放电过程中的极化现象。此外,dQ/dV-V放电曲线中,40% SiO 电池特征峰向低电压方向移动,说明40% SiO 电池放电电压平台较12%SiO 和20% SiO 电池低。分析结果表明,SiO 含量的增加会造成锂离子电池充放电容量的衰减及电池化学体系充放电过程中电化学极化现象的加剧。

图2 不同SiO含量负极电池充放电曲线及dQ/dV-V曲线
2.2.2 循环性能测试
图3(a)为不同SiO 含量负极软包电池常温循环曲线,结果表明,12% SiO、20% SiO、40% SiO 电池分别循环至200、175 和150 次时,循环劣化趋势明显变快,循环趋势上看,12% SiO 电池优于20% SiO 电池,而20% SiO 电池优于40%SiO 电池。图3(b)~(d)分别为12% SiO、20% SiO、40% SiO 锂离子电池EIS 曲线,结果表明,100 次循环后,电池内阻变化不大,且12% SiO、20% SiO、40% SiO 电池差异不明显;150次循环后,12% SiO、20% SiO、40% SiO 电池内阻明显增加,Rs分别为3.2、3.5 和4 mΩ,Rct分别为11、13 和16 mΩ;200 次循环后变化更加明显,12% SiO、20% SiO 电池Rs分别为5 和10 mΩ,Rct分别约为25 和30 mΩ。
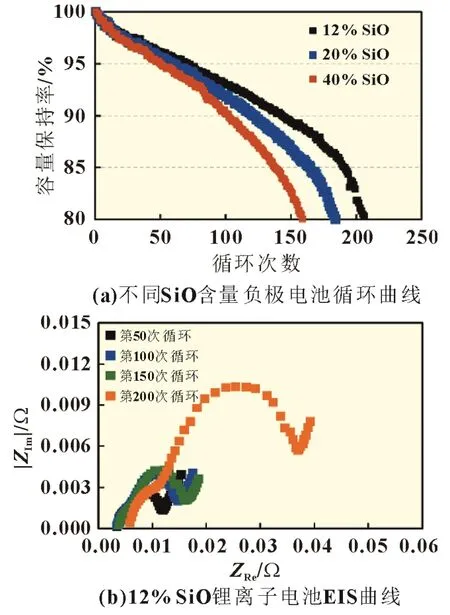
循环测试结果说明,SiO 含量影响电池循环性能,SiO 含量的增加会加速LiCoO2-SiO/石墨电池循环容量保持率的劣化,同时,加速电池内阻增长。
2.3 循环衰减机理分析
2.3.1 循环衰减电化学过程分析
采用增量容量分析法表征电池循环的电化学过程,图4为不同SiO 含量负极电池充放电循环过程的dQ/dV-V曲线。dQ/dV-V曲线的积分面积表示充放电容量,随着SiO 含量的增加,相同循环次数下,曲线的积分面积逐渐减小,说明随着SiO 含量的增加,LiCoO2-SiO/石墨电池的充放电容量逐渐减小。图4(a)中,循环开始前,12% SiO 负极电池的dQ/dV-V充电曲线在3.6~4.2 V 有3 个特征峰,说明电池在充电过程中有3 个电压平台;循环50 次时,在3.6~4.2 V 出现了4 个特征峰,循环前的3.75 V 的特征峰在50 次循环后转化为3.7 V 处较宽的峰和3.8 V 处较窄的峰。图4(b)~(c)中,20% SiO 和40% SiO 电池循环中观察到了同样的现象,这是由LiCoO2-SiO/石墨电池在循环前期的电化学活化造成的。对于12%SiO、20% SiO、40% SiO 电池,第50 次循环后,随着循环次数的增加,充电曲线的特征峰位置逐渐向高电压转移,并且曲线形状趋于平滑。结合图3 中电化学阻抗的测试结果,说明随着循环次数的增加,电池体系极化加剧,同时造成电池容量损失及电池电化学阻抗增加。而随着SiO 含量的增加,上述现象愈加明显,说明SiO 含量的增加加剧了循环过程中电池体系的极化现象。类似地,对于12% SiO、20% SiO、40%SiO 电池,随着循环次数的增加,放电曲线的特征峰位置逐渐向低电压转移,并且曲线形状趋于平滑。同时,随着循环次数的增加,放电曲线在3.2~4.4 V 电压特征峰数量逐渐减少,表明电池充放电循环加剧了电池放电过程中的极化现象。LiCoO2-SiO/石墨电池的充放电循环曲线分析结果说明,SiO含量的增加会加剧电池化学体系充放电过程中电化学极化现象,而在电池的全寿命周期内,随着充放电循环的进行,会加速电池极化的程度。
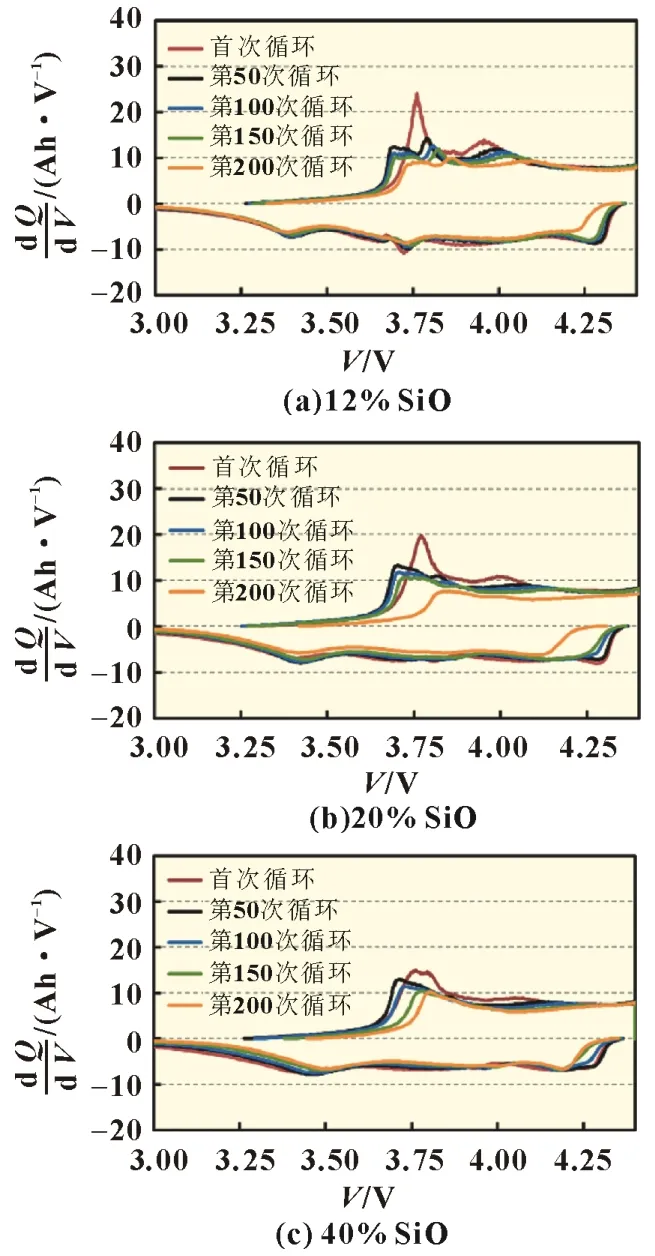
图4 不同SiO含量锂离子电池循环过程dQ/dV-V曲线
2.3.2 负极对循环的影响
为了考察电池充放电循环过程对负极的影响,了解负极变化对循环的作用,考察了循环前后满电电池负极的形貌变化。
图5 为不同SiO 含量锂离子电池循环前后负极的SEMmapping 图。电池循环前,12% SiO、20% SiO 和40% SiO 电池的SiO/石墨负极的厚度分别为116、94 和74 μm。分别循环220、210 和164 次后,12% SiO、20% SiO 和40% SiO 电池的SiO/石墨负极的厚度分别为179、210 和180 μm,循环后厚度分别增长了54.3%、123.4%和143.2%。SiO 含量越高,负极厚度增长越多。同时,除了负极片的厚度增长外,负极片上还出现了不同程度的裂痕,负极极粉和铜箔发生了不同程度的脱离,SiO 含量越高,负极片上的裂痕及与铜箔的脱离程度越严重。
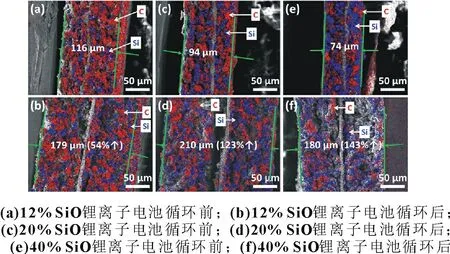
图5 不同SiO含量锂离子电池循环前后负极的SEM-mapping图
为了进一步了解SiO/石墨负极厚度增长的原因,对循环前后的负极片断面进行了SEM-mapping 测试。电池循环前,12% SiO、20% SiO 和40% SiO 电池的SiO/石墨负极的SiO 和石墨呈区域性分散,而循环后,由于材料膨胀造成SiO 和石墨的分布较循环前更均匀,说明SiO 的膨胀造成了负极片厚度的增加,同时还伴随着SiO 和石墨材料的相对位移,这会影响负极片粘结剂及导电剂网络的稳定性。
通过表面形貌的SEM 测试,考察了循环前后SiO 结构的变化。图6 为不同SiO 含量锂离子电池循环前后负极表面形貌SEM 图。测试结果表明,电池充放电循环后,SiO 颗粒发生了破裂,势必增加SiO 材料与电解液的接触面积,进而加剧负极侧副反应的发生,消耗电解液,造成Rs的增加。此外,SiO 负极颗粒的破裂会影响SiO 负极的导电性能,造成电化学阻抗的增加。

图6 不同SiO含量锂离子电池循环前后负极表面形貌SEM图
对负极的分析结果表明,SiO 负极充放电循环过程导致极片膨胀,同时伴随着SiO 和石墨材料的相对位移,破坏负极片粘结剂网络及导电剂网络。膨胀造成SiO 颗粒结构破裂,增加了负极侧副反应发生的几率,消耗电解液,导致电池内阻增加。
2.3.3 正极对循环的影响
硅基负极的嵌锂电位高于石墨负极[3],SiO 负极的掺入势必会导致正极充电电位的偏高,基于图2 和图4 及前文对LiCoO2-SiO/石墨电池充放电曲线及循环曲线分析结果,SiO含量的增加会加剧电池化学体系充放电过程中电化学极化现象,而在电池的全寿命周期内,随着充放电循环的进行,会加速电池极化的程度。为了考察充电电位对正极造成的影响,制备了LiCoO2为正极、Li 金属为负极的LiCoO2-Li扣式电池,并对充电至4.4、4.45、4.5、4.55、4.6、4.65 V 的LiCoO2-Li扣式正极进行断面形貌表征。
图7 为LiCoO2-Li 扣式电池充电至不同电位的正极颗粒断面形貌。结果表明,LiCoO2正极嵌锂后结构会发生破裂,而且随着充电电压的升高,颗粒结构破裂的现象越明显。对于固态颗粒,这种结构损伤是不可逆的,影响正极材料本体的导电、导离子性能,从而影响循环性能。此外,LiCoO2正极材料脱锂过多会导致微观结构坍塌,产生不可逆的相变,失去活性,降低容量,造成循环性能衰减[9-10]。

图7 LiCoO2-Li扣式电池充电至不同电位的正极颗粒断面形貌
综上所述,LiCoO2-SiO/石墨电池的充放电循环性能的衰减与SiO 循环过程中的膨胀及破裂有关,SiO 含量的增加会加剧电池化学体系充放电过程中电化学极化及电解液的消耗。正极侧的电化学极化会造成正极颗粒的结构破裂及晶体结构不可逆相变。以上因素都可能导致LiCoO2-SiO/石墨电池循环性能的衰降。所以,对于硅基负极,应持续降低体积膨胀、提升微观结构和电化学的稳定性;对于正极,提升本身结构稳定性是一个解决问题的方向,考虑到LiCoO2正极较高的充放电首次效率,更重要的应该是深入研究电池体系的正负极匹配性;此外,还需构建稳定的负极粘结剂及导电剂网络。
3 结论
通过循环过程的电化学分析及正负极形貌表征,研究了负极活性物质中SiO 含量为12%、20%和40%的LiCoO2-SiO/石墨软包电池体系循环衰减机理。SiO 负极微观结构的破裂造成负极粘结剂网络和导电剂网络损伤,加剧循环过程中的电化学极化。负极电极结构破坏导致负极极化现象加剧,提高了负极充电电位,造成正极电化学极化现象加剧,引发正极结构的不可逆损伤。改善正负极材料微观结构,提升材料稳定性以及优化体系设计等是实现硅基负极应用的关键。
