中性锌-空气电池的阴极非贵金属催化剂
2022-03-03杨孝昆邓中梁易清风
盛 况,杨孝昆,余 亮,邓中梁,易清风,2
(1.湖南科技大学化学化工学院,湖南湘潭 411201;2.新能源储存与转换先进材料湖南省重点实验室,湖南湘潭 411201)
锌-空气电池是一种将氧气的还原反应与金属锌的氧化反应在空间上隔离,从而将锌氧化反应的化学能转化为电能的化学电池,它的正极还原反应的活性物质来自空气中的氧气,其来源是无限的,电池放电时只消耗负极锌。锌-空气电池具有显著的优点:在使用和放置过程中安全可靠、稳定,并且环境友好,同时电池可以通过更换锌阳极的方式,实现快速的机械式充电;锌-空气电池的电荷容量大、功率高,是应用于电动汽车等的理想动力电源,具有广泛的应用前景。然而,锌-空气电池目前在使用和研究中也存在许多问题:空气电极催化剂的成本与性能需要进一步改进,制备能够高效电化学催化氧还原反应(ORR)、成本低廉且制备过程简单的非贵金属催化剂仍是锌-空气电池研究的重要内容;作为阳极的金属锌会发生腐蚀,从而引起电池自放电,尤其在碱性锌-空气电池中,阳极锌电极在碱性电解质溶液中会置换出水中的氢,本身溶解为锌离子;此外,金属锌中的杂质会与锌形成许多微小电池而发生电化学腐蚀,进一步加速了锌的自发溶解。
锌-空气电池在放电时,阳极(负极)锌发生氧化反应,而阴极(正极)发生来自空气中的氧气的还原。通常地,锌-空气电池采用强碱性溶液(NaOH或KOH)为电解质,电极反应表示为[1]:
阳极:Zn+4 OH-→Zn(OH)42-+2 e-
Zn(OH)42-→ZnO+2 OH-+H2O
阴极:O2+2 H2O+4 e-→4 OH-
总的电化学反应:2 Zn+O2→2 ZnO
这种碱性锌-空气电池还可以通过阴极(空气电极)的气体扩散层吸附空气中的二氧化碳,或者由于电池密封性差而吸收二氧化碳,从而导致电解液碳酸盐化,大大降低了电池的效率。与在碱性溶液中相比,金属锌在中性或准中性的电解质溶液中具有良好的稳定性,而且中性电解质溶液的碳酸盐化要比碱性溶液弱很多,并且中性电解质更加安全、环保[2]。然而,要保证这种中性锌-空气电池稳定地高效运行,开发在中性环境中能高效电催化氧还原反应的非贵金属催化剂尤为重要。本文总结了近年来非贵金属掺杂的碳氮管状复合物催化剂的制备以及它们应用于中性锌-空气电池方面的工作,探讨了不同制备条件对碳氮管状物的形状、大小和ORR 性能的影响。
1 碳氮管状复合物催化剂的制备
碳纳米管导电性优良,表面积巨大,此外,它的石墨层还携带一些功能性基团,具有特殊的催化效应,在催化ORR 方面具有重要作用。通常地,碳纳米管的电催化性能可以通过掺杂氮元素而得到改善。掺杂氮元素一般以吡啶型氮(398.6 eV)、吡咯型氮(400.2 eV)和石墨型氮(401.1~403.6 eV)[3]三 种形式存在,其中具有Lewis 碱特性的吡啶型氮能吸附O2分子及其中间体,其含量越多,对ORR 的电催化活性就越好[4-5]。此外,金属(如铁、镍、钴等[5-8])掺杂的碳材料也能形成对ORR具有强烈电催化活性的活性位点。因此,以不同金属盐为生长催化中心,以双氰胺为氮源和碳氮纳米片源,以不同有机化合物为碳源,将它们混合均匀形成前驱体;最后在高温(如800 ℃)下热解该前驱体,一步合成金属-氮共掺杂的管状碳复合物。不同前驱体的组成以及相应的管状碳复合物如表1 所示,复合物的形成示意图如图1 所示[5,9]。扫描电子显微镜法(SEM)和透射电子显微镜法(TEM)图证明了这种管状结构的存在,如图2 所示[5,10]。不存在金属盐时,只形成碳氮复合物纳米片,没有管状结构产生[图2(a)];只有镍存在时,形成均匀、但纳米管较大的管状结构[图2(b)];只有金属钴存在时,形成不均匀的管状结构,但在镍和钴按一定比例存在时,产生了均匀且管径更小的管状结构[图2(c)~(d)]。

表1 前驱体组成以及相应的管状碳复合物

图1 复合物形成示意图

图2 以葡萄糖为碳源制备的管状结构复合物的SEM图
作为管状结构生长的催化中心,金属盐的种类对形成的管状结构影响明显,研究了镍钴的硝酸盐(用n 表示)、氯化物(用c 表示)和醋酸盐(用a 表示)对形成的复合物结构的影响,其中,镍钴混合的硝酸盐或醋酸盐对形成的管状结构的影响如图3(a)~(e)所示。Ni 与Co 原子比为1∶1 时,管径在28 nm 左右[图3(a)];Ni 与Co 原子比为2∶3 时,管径在35 nm 左右[图3(b)和3(d)];Ni 与Co 原子比为3∶2 时,管径在20~28 nm[图3(c)和3(e)]。这表明Ni、Co 共存有利于形成较小管径的碳氮复合物管状结构[5,11]。
进一步研究发现,以聚苯胺为碳源时,没有形成碳氮复合物管状结构[12]。考虑到金属盐是管状结构形成的生长催化剂,如果金属盐能均匀地分散在某一载体上,则形成的管状物的管径可能会发生相应的变化。因此,在催化剂前驱体中加入碳纳米管和乙二胺,将金属盐与乙二胺形成配合物,并均匀分散于碳纳米管上,最后高温热解得到的碳氮复合物管状结构具有更小的管径[图3(f)],说明金属盐在这一体系中形成了颗粒更小的分散体,从而有利于形成管径更小的管状物[13]。采用蔗糖为碳源时,形成的催化剂Ni2Co3@s-CN 由卷曲态的纳米管和金属纳米颗粒组成[图3(g)],纳米管直径为12~22 nm[图3(h)],比葡萄糖为碳源的管径更小,并且从金属颗粒的晶格条纹间距看出,Ni和Co之间形成了合金[图3(h)插图][9]。
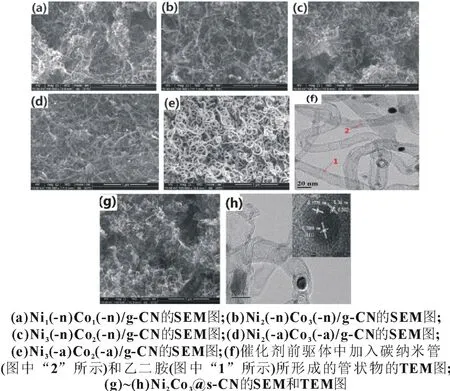
图3 不同金属盐、碳源及乙二胺制备的管状物的SEM和TEM图
2 催化剂的ORR 电活性
为了研究催化剂在中性锌-空气电池中的应用,测试了中性溶液中它们对ORR 的电催化活性。图4(a)是在0.5 mol/L KNO3溶液中以蔗糖为碳源制备的催化剂的循环伏安(CV)图[5,9]。图4(a)显示,在氧气存在下,催化剂表现出明显的阴极还原峰,且电流密度增加,而在电解液中不存在氧气时(N2饱和)没有观察到明显的还原峰。进一步从图4(b)看出,不同催化剂ORR 的峰电位有一定差别,并且电流峰大小也不相同,Ni2Co3@s-CN 催化剂对ORR 具有强的电活性。


图4 以蔗糖为碳源制备的催化剂在O2和N2饱和的0.5 mol/L KNO3溶液中的CV图
进一步利用旋转圆盘电极(RDE)研究了催化剂对ORR 的电活性,结果如图5 所示,其中,图5(a)比较了在1 600 r/min 时不同催化剂的极化曲线,Ni2Co3@s-CN 和Ni1Co1@s-CN 具有相近的ORR 起始电位,但前者的ORR 电流较大,并且Ni2Co3@s-CN 的极限电流密度大于Pt/C,表明Ni2Co3@s-CN具有优异的电催化活性。不同转速下Ni2Co3@s-CN 的极化曲线如图5(b)所示,出现了明显的电流平台,极限电流密度达到6.5 mA/cm2,进一步表明Ni2Co3@s-CN 对ORR 优异的电活性。通过Koutecky-Levich(K-L)曲线图,发现在中性溶液中,Ni2Co3@s-CN 上ORR 的电子转移数为3.7~3.9,表明ORR 过程几乎以四电子进行,即氧气完全还原为水,这对于提高锌-空气电池的能量转换效率是非常重要的。

图5 催化剂在O2饱和的0.5 mol/L KNO3的极化曲线
3 中性锌-空气电池性能测试
电池性能测试在自制电池模型中进行,作为阳极的锌片插在0.5 mol/L KNO3溶液中,阴极片为涂有催化剂的碳纸,其中涂有催化剂的一面直接与电解液接触,未涂催化剂的另一面相当于气体扩散层并与空气相通。以葡萄糖为碳源制备的催化剂CN-sheet、Ni@g-CN、Co@g-CN 和Ni2Co3@g-CN 作为锌-空气电池的阴极催化剂时,其放电性能如图6(a)所示[10],开路电压(OCV)分别为0.9、1.04、1.01 和1.13 V,其中Ni2Co3@g-CN 的OCV值与Pt/C(1.14 V)接近。在180 mA/cm2时,Ni2Co3@g-CN 的最大功率密度为65 mW/cm2,明显高于Pt/C。根据文献报道[14],锌-空气电池以MnOx作为阴极催化剂时,在中性氯化物溶液中的OCV约为1.2 V,在电池电压0.3 V 时的电流密度约为42.8 mA/cm2,最大功率密度只有12.7 mW/cm2,对应的电流密度也只有13.8 mA/cm2。表明所制备的阴极催化剂的性能大大优于现有文献结果。此外,进一步研究了电池在不同电流密度下的放电稳定性(终止电压0.1 V),如图6(b)所示,在电流密度分别恒定为50、100 和150 mA/cm2时,以Ni2Co3@g-CN 为阴极催化剂的电池分别持续放电202、93 和11 h,并且均出现了明显的电压平台;与Pt/C 催化剂比较发现,在50 mA/cm2的电流密度下,Ni2Co3@g-CN 的放电时间更长,放电电压平台更高。
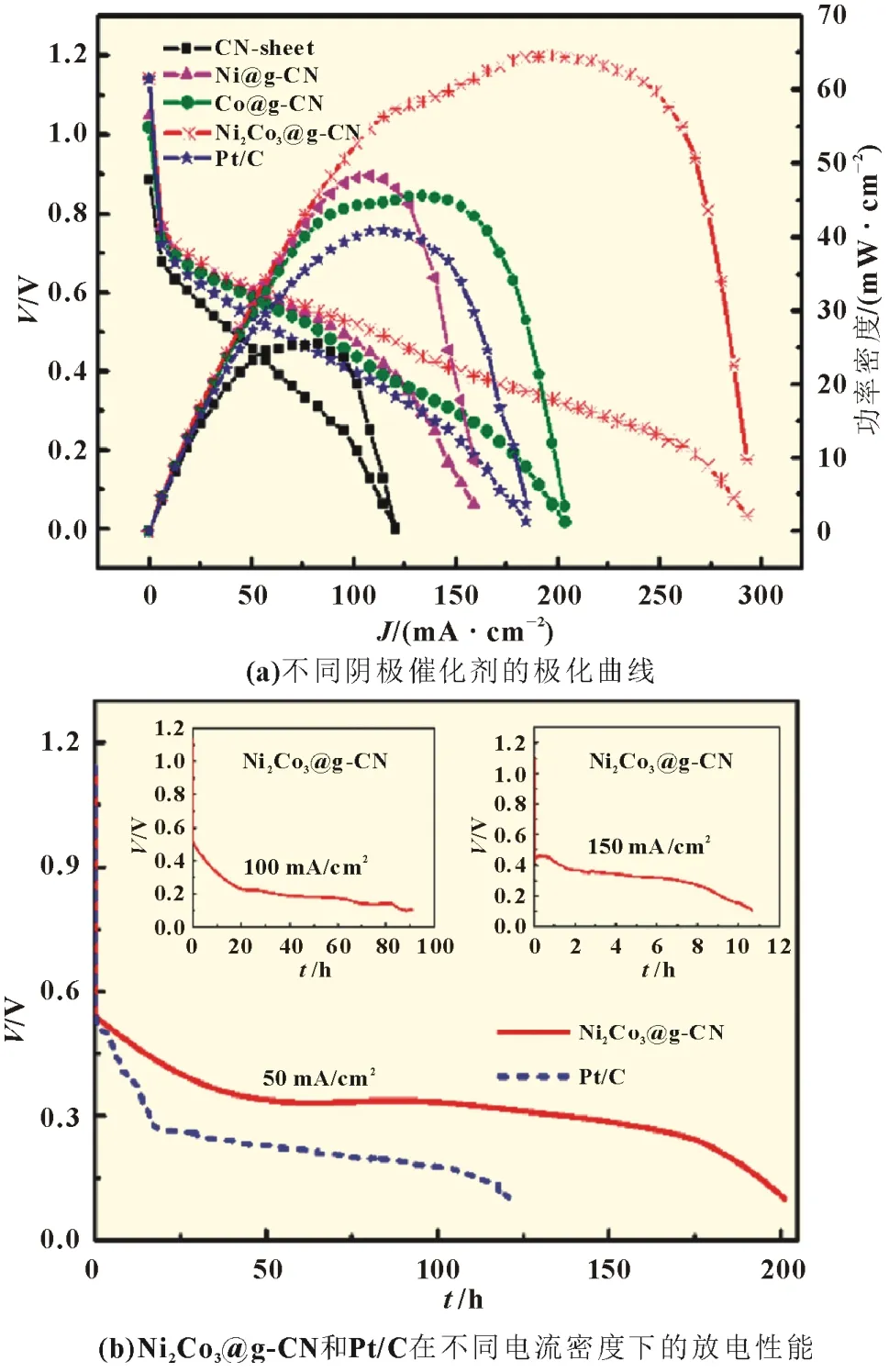
图6 以葡萄糖为碳源的催化剂的锌-空气电池在0.5 mol/L KNO3中的极化曲线以及Ni2Co3@g-CN和Pt/C在不同电流密度下的放电性能
以中性溶液为电解质时,锌-空气电池在工作过程中仅消耗阳极锌和空气中的氧气,但电解质的组成基本上保持不变,说明可以通过更换阳极锌片,实现机械式充电[15]。要实现这一目的,阴极催化剂空气电极必须稳定、可靠,能反复使用。为此,将电池在150 mA/cm2的超高电流密度下重复放电10 次,以检验空气电极的稳定性。实验中,电解液(0.5 mol/L KNO3)和空气电极保持不变,每次放电至终止电位后更换阳极锌片,再继续放电,结果如图7(a)所示,随着重复次数的增加,放电时间逐渐下降,第10 次的时间为5.5 h,约为第1 次(10.6 h)的一半,可能是碳纸的气体扩散层中渗透了少量电解质,阻挡了空气的迁移。将第10 次放电后的空气电极取出,并在室温下干燥15 h 后再在同样条件下放电,其持续放电时间达11 h,如图7(a)插图所示,达到了第1 次测试的效果。将以Ni2Co3@s-CN 为阴极催化剂的两个中性锌-空气电池串联后,可以轻松地点亮8 个发光二极管(LED),如图7(b)所示。结果表明,这类非贵金属掺杂的碳氮复合物是中性锌-空气电池优异的阴极催化剂[9]。
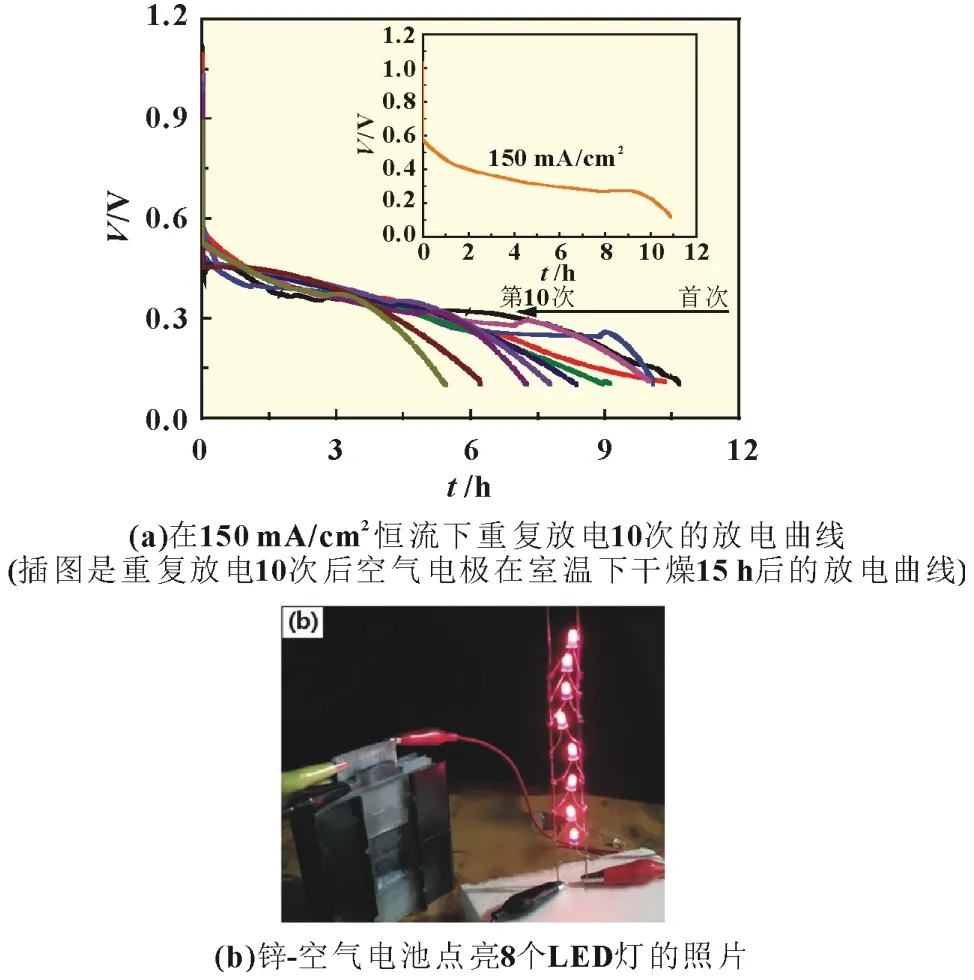
图7 Ni2Co3@g-CN为阴极催化剂的中性锌-空气电池的放电曲线以及以Ni2Co3@s-CN为阴极催化剂的电池点亮8个LED灯的照片
4 结论
以双氰胺为氮源,在不同非金属盐(铁、钴、镍盐)和有机物碳源存在下,采用简单的热解法制备具有管状结构的复合物。镍钴盐同时存在,或者以蔗糖为碳源时,形成管径为12~22 nm且分布更为均匀的管状结构。在中性溶液中,Ni2Co3@s-CN 对氧还原反应的起始电位为0.06 V(vs.Ag/AgCl),极限电流密度为6.5 mA/cm2,性能接近或超过商品Pt/C。在中性电解质溶液中,以制备的复合物作为阴极催化剂的锌-空气电池表现出优异的放电性能:放电功率密度达到65 mW/cm2;放电平台时间长且稳定;在100 和150 mA/cm2的大电流下仍能保持稳定放电;空气电极在150 mA/cm2的电流下循环10 次后,通过简单干燥处理即可恢复其性能;这种中性锌-空气电池适合机械式充电使用。
