曲妥珠单抗联合CTF化疗方案对乳腺癌晚期患者心肌酶谱及毒副反应的影响
2022-03-01赵伶伶
赵伶伶
(铁岭市中心医院肿瘤内科,辽宁 铁岭 112000)
乳腺癌为临床常见女性恶性肿瘤,且由于乳腺癌细胞失去正常活性,细胞结构被破坏,容易引起癌细胞脱落游走并随着血液循环系统散播至全身,严重威胁患者的生命安全[1]。CTF化疗方案[环磷酰胺+吡柔比星+5-氟尿嘧啶]为常用化疗方案,可有效抑制癌细胞DNA聚合酶,干扰其分裂过程,具有较好的抗肿瘤效果[2]。曲妥珠单抗为抗原癌基因人类表皮生长因子受体2(Her-2)的单克隆抗体,可抑制癌细胞的生长,对乳腺癌的Her-2过度表达具有显著疗效[3]。但目前关于曲妥珠单抗联合CTF化疗治疗乳腺癌的报道较少。基于此,本研究旨在探究曲妥珠单抗与CTF化疗联合应用于乳腺癌晚期患者的效果,现报道如下。
1 资料与方法
1.1 临床资料 回顾性分析2018年1月至2020年2月本院收治的80例乳腺癌晚期患者的临床资料,根据治疗方法不同分为对照组(n=41)与观察组(n=39)。对照组年龄49~62岁,平均(54.14±2.52)岁;病理分型:浸润导管癌20例,浸润小叶癌17例,导管内乳头状瘤4例。观察组年龄51~63岁,平均(55.04±2.46)岁;病理分型:浸润导管癌19例,浸润小叶癌17例,导管内乳头状瘤3例。两组临床资料比较差异无统计学意义,具有可比性。患者及家属均签署知情同意书,本研究获得医院伦理委员会审核批准。
1.2 纳入及排除标准 纳入标准:符合《中国抗癌协会乳腺癌诊治指南与规范(2015版)》[4]中相关诊断标准;参与研究前未接受其他系统性治疗;临床资料完整。排除标准:预计生存期<3个月;存在青光眼或甲亢病史;存在痛风或泌尿系结石病史。
1.3 方法
1.3.1 对照组 对照组给予CTF化疗方案。第1天、第8天静脉注射注射用环磷酰胺(Baxter Oncology GmbH,生产批号:170107、190102,规格:1 ml∶3 mg)600 mg/(m2·d);第1天、第8天静脉注射注射用盐酸吡柔比星(海正辉瑞制药有限公司,生产批号:170207、190102,规格:10 mg)30 mg/(m2·d);第1天、第8天静脉注射氟尿嘧啶注射液(上海旭东海普药业有限公司,生产批号:170302、190203,规格:10 ml∶0.25 g)500 mg/(m2·d),28 d为1个周期,共治疗5个周期。
1.3.2 观察组 观察组在对照组基础上静脉推注注射用曲妥珠单抗(Genentech Inc.,生产批号:180107、190301,规格:440 mg∶20 ml),第1周使用剂量为4 mg/(kg·d),之后维持剂量为2 mg/(kg·d),以28 d为1个周期,共治疗5个周期。
1.4 观察指标 ①心肌酶谱水平:采集两组治疗前后清晨8:00空腹静脉血,离心处理后使用试剂盒(郑州博赛生物技术股份有限公司,规格:96T)采用化学发光法检测心肌肌钙蛋白I(cTnI)水平;采用N-乙酰半胱氨酸法检测肌酸激酶(CK)水平;采用免疫抑制法检测肌酸激酶同工酶(CK-MB)水平。②毒副反应:根据抗肿瘤药物毒副反应标准[5]对毒副反应进行评价,白细胞含量(×109/L)3.0~3.9为I度,2.0~2.9为Ⅱ度,1.0~1.9为Ⅲ度;恶心短暂为I度,暂时性呕吐为Ⅱ度,呕吐需治疗为Ⅲ度;轻度脱发为I度,中度、斑状脱发为Ⅱ度,完全脱发为Ⅲ度;心功能轻微异常为I度,短暂的心功能不足但无需治疗为Ⅱ度,心功能不足且治疗有效为Ⅲ度。
1.5 统计学方法 采用SPSS 24.0统计学软件进行数据处理,计量资料以“±s”表示,组间比较采用独立样本t检验,组内比较采用配对样本t检验;计数资料采用[n(%)]表示,等级资料采用Z检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组心肌酶谱水平比较 治疗前,两组心肌酶谱水平比较差异无统计学意义;治疗5个周期,两组cTnI、CK、CK-MB水平均高于治疗前,且观察组高于对照组,差异有统计学意义(P<0.05),见表1。
表1 两组心肌酶谱水平比较(±s)
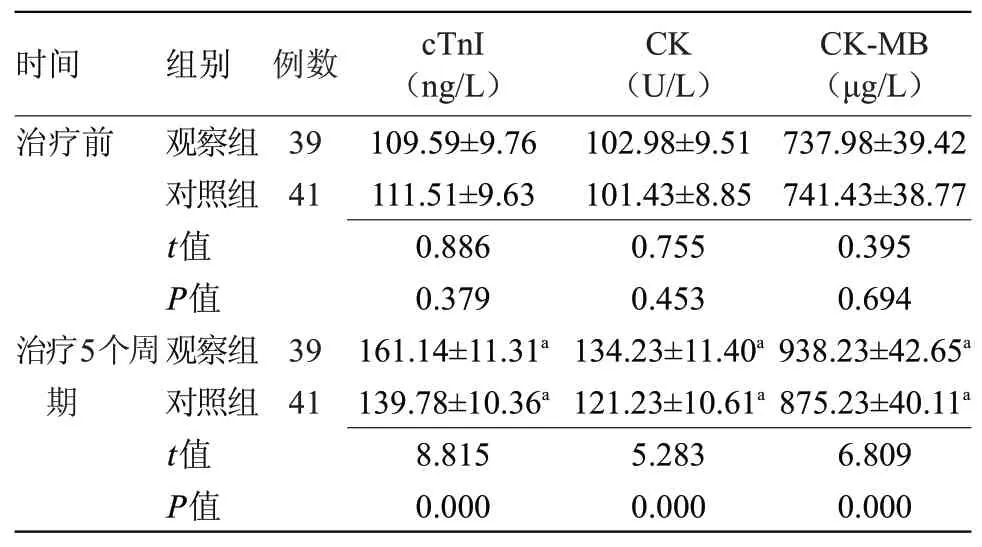
表1 两组心肌酶谱水平比较(±s)
注:cTnI,心肌肌钙蛋白I;CK,肌酸激酶;CK-MB,肌酸激酶同工酶。与本组治疗前比较,a P<0.05
?
2.2 两组毒副反应比较 化疗期间,两组白细胞降低、恶心呕吐、脱发及心功能比较差异无统计学意义,见表2。
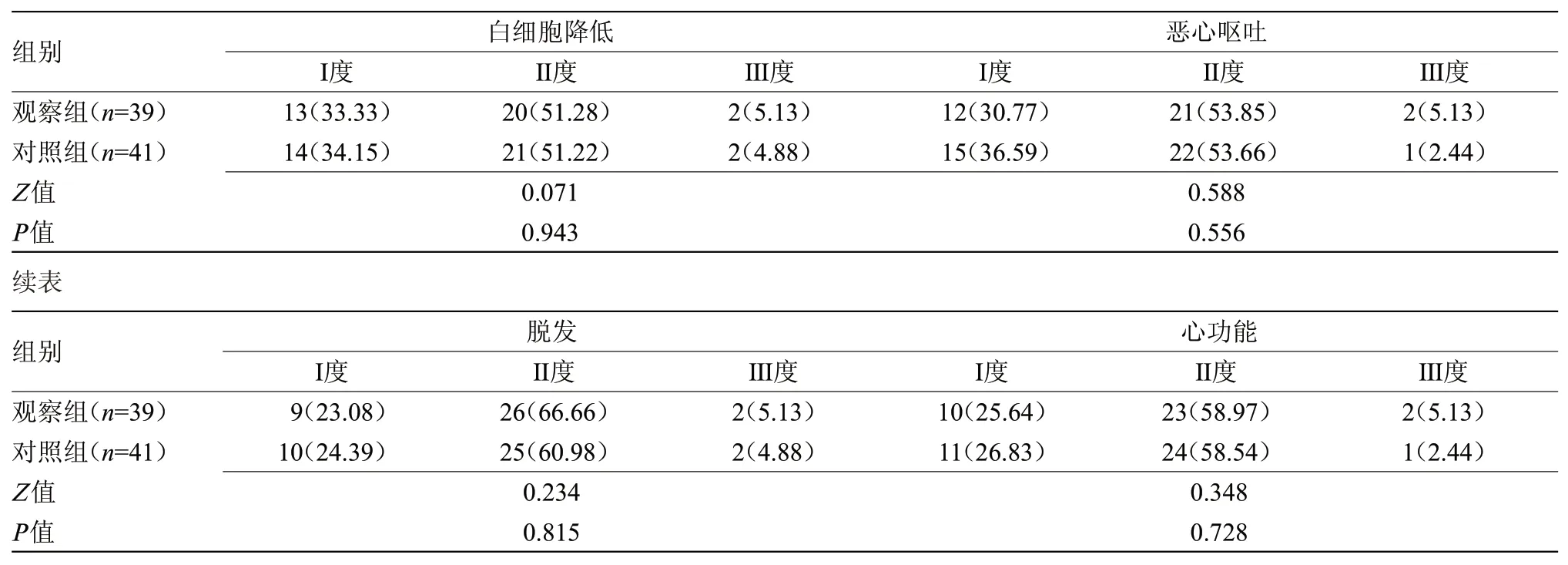
表2 两组毒副反应比较[n(%)]
3 讨论
乳腺癌多由家族遗传、物理因素、过量饮酒等引起,患者早期无明显症状,后期主要伴有乳腺肿块、乳晕异常等临床表现[6]。目前,针对乳腺癌患者临床多采取外科手术治疗、化疗、放疗、生物靶向治疗等,但近年来该病呈年轻化趋势,考虑到乳腺癌晚期患者失去手术指征,故化学药物疗法常作为治疗该类患者的首选方案。
本研究结果显示,治疗5个周期,两组cTnI、CK、CK-MB水平均高于治疗前,且观察组高于对照组,提示曲妥珠单抗联合CTF化疗可有效改善乳腺癌晚期患者心肌酶谱水平。分析其原因为,CTF化疗方案由环磷酰胺、吡柔比星、5-氟尿嘧啶等药物构成,其中环磷酰胺属于细胞毒性免疫抑制剂,服用后可被肿瘤内过量磷酰胺酶分解,生成具有活化效应的磷酰胺氮芥,破坏DNA的结构及功能;吡柔比星为蒽环类抗肿瘤药物,进入细胞核后可快速嵌入DNA核酸碱基对间,阻扰其转录过程,抑制mRNA的合成;同时,还可有效灭杀DNA聚合酶与拓扑异构酶的活性,进而延缓疾病进展;5-氟尿嘧啶在体内可转换为脱氧核苷酸,抑制RNA中蛋白质的合成,产生细胞毒性,具有较好的抗肿瘤活性[7]。而曲妥珠单抗是由抗体依赖的细胞介导的细胞毒反应的潜在介质,该药主要作用于Her-2受体的细胞外围部分,可有效干扰Her-2的合成,降低苏氨酸激酶的生理活性,致使原癌基因丧失功能,从而抑制细胞周期,起到杀伤肿瘤的效果,改善心肌酶谱水平,进而缓解癌症的发展[8]。此外,本研究结果还显示,两组白细胞降低、恶心呕吐、脱发及心功能比较差异无统计学意义,提示曲妥珠单抗联合CTF化疗不会给患者带来更多不良反应,安全性较高。这主要得益于曲妥珠单抗的高度特异性,该药可在发挥抗肿瘤作用时有效确保对周围健康组织产生较小的杀伤力[9]。但仍需注意,本研究所选病例数及研究对象有限,观察时间较短,结论可能与实际仍有偏差,研究仍有局限,还应扩大样本量,延长随访时间,深入研究曲妥珠单抗联合CTF化疗方案对乳腺癌晚期患者远期预后的影响。
综上所述,曲妥珠单抗联合CTF化疗可有效改善乳腺癌晚期患者的心肌酶谱水平,抑制病情的发展,且安全性较高。
