伊立替康联合FOLFOX4化疗对胃癌根治术后转移患者血清肿瘤标志物水平及生存质量的影响
2022-02-19周亮华王明元黄锦训
周亮华,王明元,黄锦训
胃癌为临床较常见的消化道肿瘤之一,其发病率位居全部恶性肿瘤第二位,且近年来该病发病率逐年升高[1]。目前,对于早中期胃癌临床多采用胃癌根治术治疗,以完整切除肿瘤病灶来遏制疾病进展,但相关报道指出,约50%的胃癌患者术后可能会出现转移、复发情况,预后不良发生风险较高[2]。化疗作为胃癌术后转移首选姑息治疗方案,其可抑制肿瘤细胞生长,延长患者生存期,但临床应用发现,单纯化疗整体效果有限。伊立替康是化疗常用辅助药物,其对细胞周期S期具有较强的特异性,可阻断肿瘤细胞DNA复制,且可阻止RNA合成,从而抑制肿瘤细胞增殖[3]。现观察伊立替康联合FOLFOX4化疗(奥沙利铂+5-氟尿嘧啶+亚叶酸钙)对胃癌根治术后转移患者血清肿瘤标志物水平及生存质量的影响,报道如下。
1 资料与方法
1.1 临床资料 选取2020年1月—2021年5月中国人民解放军联勤保障部队第九〇〇医院莆田医疗区收治的胃癌根治术后转移性胃癌患者86例,依据随机数字表法分为对照组与研究组,各43例。对照组:男24例,女19例;年龄47~72(60.64±3.39)岁;体质指数17.6~24.8(21.08±1.03)kg/m2;病理类型:高分化腺癌15例,中分化腺癌12例,低分化腺癌9例,其他7例;肿瘤分期:Ⅱ期12例,Ⅲ期31例。研究组:男26例,女17例;年龄46~70(60.17±3.45)岁;体质指数17.9~24.7(21.10±1.02)kg/m2;病理类型:高分化腺癌14例,中分化腺癌13例,低分化腺癌10例,其他6例;肿瘤分期:Ⅱ期9例,Ⅲ期34例。2组性别、年龄、体质指数、病理类型、肿瘤分期比较,差异无统计学意义(P>0.05),具有可比性。本研究经医院伦理委员会批准。
1.2 病例选择标准 纳入标准:经影像学、病理组织等检查确诊为胃癌,且伴有周围淋巴结、脏器等转移;胃癌根治术后发生转移;病灶可实体测量;预期生存时间≥3个月;Karnofsky功能状态评分(KPS)≥70分,体力状况评分(ZPS)≤2分;认知功能正常,可配合研究;患者及家属知情同意本研究。排除标准:合并脑、肝等重要脏器功能不全;伴有心肌梗死、脑梗死等严重心脑血管疾病;合并脑转移;凝血功能障碍;合并感染性疾病;合并脏器原发性肿瘤;沟通障碍;近1个月接受相关放化疗治疗;对本研究药物过敏。
1.3 治疗方法 对照组予以FOLFOX4化疗:第1天,予以85 mg/m2奥沙利铂(先声药业有限公司生产,国药准字H20093899,规格:50 mg)静脉滴注,于2 h内滴注完成;第1~2天,予以200 mg/m2亚叶酸钙(江苏奥赛康药业有限公司生产,国药准字H20060197,规格:100 mg)静脉滴注,于2 h内滴注完成,然后予以600 mg/m25-氟尿嘧啶(山西太原药业有限公司生产,国药准字H14022106,规格:0.25 g)静脉滴注,维持滴注22 h;化疗预处理:化疗前6 h、12 h予以4 mg地塞米松(安徽国森药业有限公司生产,国药准字H34021164,规格:0.75 mg)口服,并静脉滴注8 mg格拉司琼(重庆药友制药有限责任公司生产,国药准字H20055073,规格:3 mg),同时予以10 mg甲氧氯普安片(天津力生制药股份有限公司生产,国药准字H12020161,规格:5 mg)口服,且做好保暖,并提供营养支持。研究组采用伊立替康(江苏恒瑞医药股份有限公司生产,国药准字H20213373,规格:40 mg)联合FOLFOX4化疗,FOLFOX4化疗方案同对照组;化疗第1天,予以180 mg/m2伊立替康静脉滴注,于1.5 h内滴注完成。2组均以治疗21 d为1个化疗周期,共治疗2个周期。
1.4 疗效判定标准[4]完全缓解:检查可见肿瘤病灶全部消失,无新病灶,且实验室检查提示肿瘤标志物水平恢复正常,维持时间≥4周;部分缓解:所有肿瘤病灶最大径总和相比治疗前缩小≥30%,维持时间≥4周;疾病稳定:所有肿瘤病灶最大径总和相比治疗前缩小<30%,但增大<20%;疾病进展:肿瘤病灶最大径增加≥20%,或可见新发病灶。总有效率为完全缓解率与部分缓解率之和。
1.5 观察指标与方法 (1)血清肿瘤标志物水平:抽取2组患者治疗前、治疗2个周期后晨起空腹静脉血5 ml,以1 000 r/min转速离心处理15 min,采取血清分装于两支试管,并置于-20 ℃冰箱内贮存;其中一支以电化学发光法测定癌胚抗原(CEA)、糖类抗原19-9(CA19-9)水平,以酶联免疫吸附法(ELISA)测定再生基因蛋白Ⅳ(REG Ⅳ)水平。(2)血清基质金属蛋白酶9(MMP-9)与血管内皮生长因子(VEGF)水平:取另一支血清标本,以ELISA测定MMP-9、VEGF水平。(3)生存质量:采用癌症患者生活质量测定量表(EORTC QLQ-C30)[5]评估2组患者治疗前、治疗2个周期后的生存质量,该量表包括躯体功能、社会功能、情绪功能、总体健康4个维度,各维度总分均为100分,评分越高提示患者生存质量越好。(4)不良反应:记录2组患者治疗期间恶心呕吐、骨髓抑制、胃肠道反应、血小板下降等不良反应发生情况。

2 结 果
2.1 临床疗效比较 对照组完全缓解1例(2.33%),部分缓解7例(16.28%),疾病稳定20例(46.51%),疾病进展15例(34.88%),总有效率为18.61%(8/43)。研究组完全缓解4例(9.30%),部分缓解14例(32.56%),疾病稳定19例(44.19%),疾病进展6例(13.95%),总有效率为41.86%(18/43)。研究组总有效率较对照组高(χ2=5.514,P=0.019)。
2.2 肿瘤标志物及MMP-9、VEGF水平比较 治疗前,2组CEA、REG Ⅳ、CA19-9、MMP-9、VEGF水平比较,差异无统计学意义(P>0.05);2组治疗2个周期后CEA、REG Ⅳ、CA19-9、MMP-9、VEGF水平较同组治疗前降低(P<0.01);治疗2个周期后,研究组CEA、REG Ⅳ、CA19-9、MMP-9、VEGF水平较对照组低(P<0.01),见表1。

表1 对照组与研究组治疗前后肿瘤标志物及MMP-9、VEGF水平比较
2.3 EORTC QLQ-C30评分比较 治疗前,2组EORTC QLQ-C30中躯体功能、社会功能、情绪功能、总体健康评分比较,差异无统计学意义(P>0.05);2组治疗2个周期后EORTC QLQ-C30中躯体功能、社会功能、情绪功能、总体健康评分较同组治疗前升高,且研究组较对照组高(P<0.01),见表2。
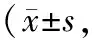
表2 对照组与研究组EORTC QLQ-C30评分比较分)
2.4 不良反应比较 2组恶心呕吐、骨髓抑制、胃肠道反应、血小板下降发生率比较,差异无统计学意义(P>0.05),见表3。
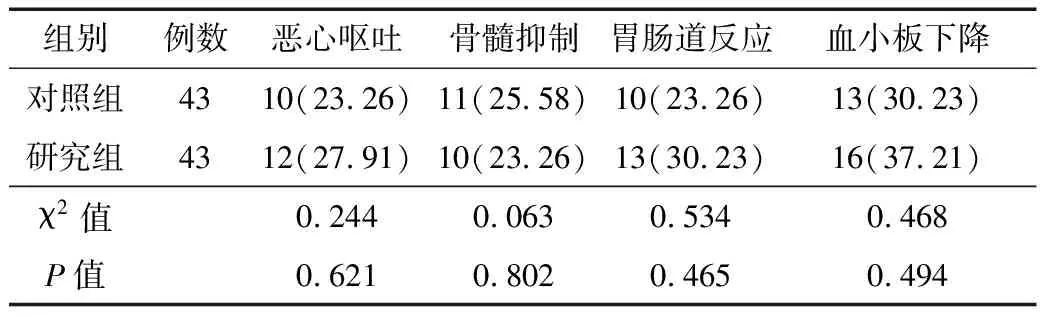
表3 对照组与研究组不良反应发生率比较 [例(%)]
3 讨 论
手术作为早中期胃癌首选治疗方案,其虽可切除病变组织,但部分患者术后可能会出现转移情况,且肿瘤细胞扩散速度较快、恶性程度较高,患者预后不良发生风险高[6]。
目前,临床多采用FOLFOX4化疗方案治疗术后转移性胃癌,该方案中奥沙利铂可避免部分耐药机制,且抗癌活性较强,可靶向损伤肿瘤细胞DNA,促使
细胞凋亡,且可协同5-氟尿嘧啶,增强抗癌敏感性,而亚叶酸钙是一种叶酸还原型甲酰化衍生物,可活化体内叶酸,增强奥沙利铂的抗癌作用[7]。有关FOLFOX4化疗方案的治疗效果已得到临床证实,但报道指出,在FOLFOX4化疗基础上辅以其他药物治疗,可进一步提高抗癌效果[8]。伊立替康是一种特异性抗肿瘤药物,其主要作用于细胞周期,可抑制细胞DNA拓扑异构酶Ⅰ,不可逆地阻断细胞DNA复制与转录,且其可产生的细胞毒性可作用于细胞S期,从而有效阻止细胞生长,发挥抗肿瘤作用[9]。同时有研究表明,伊立替康对缓慢生长、快速生长的肿瘤细胞均具有较好的杀伤作用,且辅助化疗可提高治疗总有效率[10]。本研究结果显示,研究组总有效率较对照组高,说明胃癌根治术后转移性胃癌患者采用伊立替康联合FOLFOX4化疗可提高临床疗效。究其原因在于,在FOLFOX4化疗基础上辅以伊立替康可更好地杀伤肿瘤细胞,抑制病灶生长、转移,从而提高整体治疗效果。
肿瘤标志物是评估肿瘤发展的重要指标,其常用标志物包括CEA、REG Ⅳ、CA19-9等,其中CEA、CA19-9为广谱指标,水平升高提示肿瘤转移、浸润等,而REG Ⅳ是一种分泌性蛋白,该蛋白可经多通道促使肿瘤细胞增殖,利于病灶发展[10]。肿瘤病灶的转移有赖于新血管的生成,其中VEGF为促血管生成因子,不仅可增加血管通透性,还可加速内皮细胞迁移,利于血管新生;而MMP-9为基质金属蛋白酶成员,其可降解血管弹力蛋白、胶原组织等,使肿瘤细胞侵袭周围正常组织[8]。本研究结果显示,研究组治疗2个月周期后CEA、REG Ⅳ、CA19-9、MMP-9、VEGF水平均较对照组低,说明胃癌根治术后转移性胃癌患者采用伊立替康联合FOLFOX4化疗利于降低血清肿瘤标志物水平与MMP-9、VEGF水平。分析原因在于,伊立替康联合FOLFOX4化疗可更好地抑制肿瘤细胞增殖,从而控制病灶,下调肿瘤标志物水平,阻断细胞扩散,可在一定程度上减少新血管生成,降低细胞侵袭能力,从而利于降低MMP-9、VEGF水平。在生存质量方面,研究组治疗2个周期后EORTC QLQ-C30中躯体功能、社会功能、情绪功能、总体健康评分均较对照组高,说明胃癌根治术后转移性胃癌患者采用伊立替康联合FOLFOX4化疗对提高患者生存质量有积极意义。分析原因在于,伊立替康辅助FOLFOX4化疗控制病灶生长后,相应临床症状减轻,可缓解患者身心负担,从而利于提升其生存质量。此外,本研究中2组恶心呕吐、骨髓抑制等不良反应发生率比较无差异,说明伊立替康联合FOLFOX4化疗不会增加不良反应发生,安全性较高,这一结果可能与伊立替康用药剂量较少有关。
综上所述,胃癌根治术后转移性胃癌患者采用伊立替康联合FOLFOX4化疗可提高临床疗效,降低血清肿瘤标志物水平与MMP-9、VEGF水平,延缓病情进展,减少新血管生成,提升生存质量,且不会增加不良反应发生。
利益冲突:所有作者声明无利益冲突。
