从富硒茶叶中提取碳钢酸洗缓蚀剂
2022-02-14郝鑫铭廖欣怡周晓荣廖瑞一苏肖雅馨顾源宋垚
郝鑫铭,廖欣怡,周晓荣,廖瑞一苏,肖雅馨,顾源,宋垚
(武汉轻工大学化学与环境工程学院,湖北 武汉 430023)
随着人们对环保和安全认识的逐渐提高,各国均限制有毒、污染环境的缓蚀剂的应用,开发环境友好型的缓蚀剂成为近年来的研究热点[1]。从天然植物中提取物质并用作缓蚀剂,是目前开发新型绿色缓蚀剂的途径之一[2]。具有价格低廉、毒性小或是没有毒性,可以直接排放的缓蚀剂备受研究者的青睐。目前已经有将大蒜、竹叶、柚子皮、薄荷叶等提取物应用于开发绿色缓蚀剂的研究报道[3-6]。中国作为传统的产茶大国,产量一直排名世界第一,占40%左右,其中绿茶的比例超过60%。在中国有近20个省份均有产茶工业,湖北省排名第5。恩施州富硒绿茶名列湖北十大名茶排行榜,来源丰富。绿茶有抗氧化、防衰老的功效,富硒绿茶更被认为是可增强这些功效的精品,且目前尚未有应用于缓蚀剂研究的报道。本研究选择本省出产的富硒绿茶,采用简单的水浸提取法制备用于HCl溶液中碳钢的缓蚀剂,并对其吸附行为和机理进行了分析。
1 实验
1.1 试剂及仪器
采用茶叶为富硒绿茶(宣恩县宝泰贡茶有限公司)。主要使用的化学试剂有无水乙醇和浓盐酸,均为国产分析纯试剂。配制溶液均使用去离子水。使用Q235型碳钢标准腐蚀试片(腐蚀面积为12 cm2)作为测定对象。
主要使用的仪器为:电子天平(AR224CN,奥豪斯仪器有限公司),电热恒温干燥箱(DUG-9147A,上海精宏实验设备有限公司),电化学工作站(CHI604E,上海辰华仪器有限公司),恒温水浴锅(HH-2,江苏省金坛市荣华仪器制造有限公司)。
1.2 碳钢腐蚀试片的预处理
先采用600~1000#金相砂纸依次对碳钢片进行打磨。然后,将打磨过的碳钢片分别用蒸馏水、无水乙醇清洗干净,置于玻璃干燥器中干燥2 h,用分析天平称重,记下碳钢片的初始质量(m0)。最后,将预处理后的碳钢片保存在干燥器中备用。
1.3 缓蚀剂的制备
采用水浸提取法。称取5 g干燥富硒绿茶,置于150 mL锥形瓶中,加入100 mL去离子水,密封。浸泡提取24 h,过滤,即得缓蚀剂原始溶液,浓度c记为50 g·L-1。
1.4 腐蚀溶液制备
用缓蚀剂原始溶液和浓盐酸(12 mol·L-1)、去离子水配制不同缓蚀剂浓度的腐蚀溶液,盐酸浓度固定为1 mol·L-1。
1.5 缓蚀效率测试
1.5.1失重法
恒定在25℃,进行全浸没实验,腐蚀时间设定为24 h。腐蚀后,取出碳钢片,观察并记录碳钢片表面的腐蚀情况,随后用软毛刷去除腐蚀产物,用纯水、乙醇依次清洗,晾干后在干燥器中干燥2 h,进行称重,记录数据,并利用公式(1)进行缓蚀效率计算[7]:
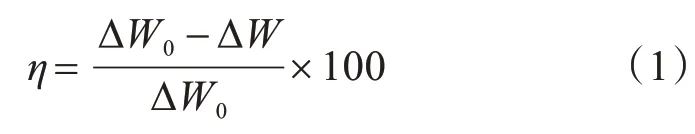
式中:η为缓蚀效率,%;ΔW0为不含缓蚀剂的碳钢片的平均失重,mg;ΔW为含不同缓蚀剂时的碳钢片的平均失重,mg。
用公式(2)计算碳钢片的腐蚀速率:

式中:v′为含缓蚀剂时碳钢片的腐蚀速率,g·m-2·h-1;ΔW为含缓蚀剂的碳钢片的平均失重,mg;As为碳钢片的腐蚀表面积,m2;t为腐蚀时间,h。当公式(2)中用ΔW0计算时,得v0',即不含缓蚀剂时碳钢片的腐蚀速率。
1.5.2电化学交流阻抗法
恒温25℃,预先在三电极电解池中注入适量的腐蚀溶液,以经过预处理的碳钢电极(0.5 cm2)作为工作电极,铂片电极为对电极,用饱和甘汞电极为参比电极,进行电化学交流阻抗谱测试。测试开路电位(OCV)直至达到稳态(3 min内电极电位的变化不超过1 mV)。在EIS(Electrochemical Impedance Spectroscopy)模式下,在OCV±5 mV的范围内,0.001~100 kHz之间进行测试。使用Zview软件根据等效电路模型进行拟合,以得到极化电阻值(Rct),根据公式(3)计算缓蚀效率。式中:IE(inhibition efficiency)为缓蚀效率,%;Rct为加入缓蚀剂后的电荷转移电阻,Ω·cm-2;Roct为不加入缓蚀剂后的电荷转移电阻,Ω·cm-2。
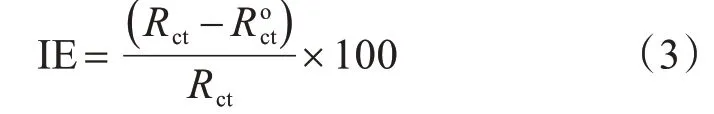
1.5.3极化曲线法
采用恒温25℃,在三电极电解池中,以经过预处理的碳钢电极(面积为0.5 cm2)作为工作电极,铂片电极作为对电极,用饱和甘汞电极为参比电极,以5 mV·s-1的扫描速率对碳钢电极在OCV±200 mV的范围内进行稳态极化曲线测试。用电化学工作站自带软件进行Tafel拟合,得到电化学腐蚀参数。
2 结果与讨论
2.1 失重法测试缓蚀效率
在含有不同浓度c的富硒茶叶提取物(SeTE)的1 mol·L-1HCl溶液中测试了碳钢试片的腐蚀失重,根据公式(1)计算出缓蚀效率(η),如图1所示。随着c的增加,SeTE的缓蚀效率增大,c为3 g·L-1时的缓蚀效率已经超过80%。c大于5 g·L-1以后,缓蚀效率随浓度的增加的变化率逐步减小。当c大于20 g·L-1时,缓蚀效率基本不变,维持在96%左右。测试结果表明,SeTE对Q235型碳钢具有优良的缓蚀性能。

图1 SeTE的缓蚀效率与浓度的关系图Fig.1 The relationship of corrosion inhibition efficiency of SeTE and concentration
2.2 SeTE缓蚀作用的热力学分析
缓蚀剂通常是吸附在金属的表面形成吸附层,从而起到抑制腐蚀的作用。通过对缓蚀剂的吸附行为进行热力学分析,可以获得吸附热力学参数,帮助研究者理解缓蚀规律。目前用于研究缓蚀剂的吸附行为的有Langmuir、Freundlich、Temkin三种等温吸附模型。将图1中的数据代入这三个公式进行拟合,发现符合Langmuir吸附模型[5],如公式(4)所示。

式中:c为缓蚀剂浓度,g·L-1;θ为表面覆盖度,按公式(5)计算;K为吸附平衡常数,L·g-1。
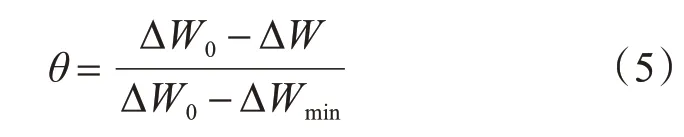
式中:ΔWmin为失重测试中的最小失重,mg;其余的同公式(1)。
根据Langmuir吸附公式做图2,拟合公式为:c/θ=0.5709+0.9902c,线性相关系数R为0.9999。斜率为0.9902,接近于1。计算得平衡常数Kads为1.7262 L·g-1。根据公式ΔGads=-2.303RTlg(55.5Kads)计算出该吸附过程的吉布斯自由能变化值ΔGads为-11.306 kJ·mol-1,其绝对值小于20 kJ·mol-1,表明富硒茶叶提取物在碳钢表面的吸附以物理吸附为主[5],缓蚀剂组分的分子与碳钢表面原子之间以分子间作用力黏附在一起。

图2 SeTE的c/θ-c图Fig.2 The c/θ-c relationship of SeTE
2.3 温度对SeTE缓蚀效率的影响
研究不同温度下缓蚀剂的缓蚀效率,有助于进一步理解缓蚀机理。在1 mol·L-1HCl溶液中和c为10 g·L-1的1 mol·L-1HCl溶液中的碳钢腐蚀失重数据如表1所示。可以看出,随着温度的升高,茶叶提取物的缓蚀效率降低,在55℃(328 K)时缓蚀效率降低至80%左右。这表明随着温度的升高,提取物在碳钢表面的吸附量降低,符合物理吸附的规律。表1还列出了碳钢的腐蚀速率(v0',v')。由表可知,随着温度的升高,碳钢的腐蚀速率增大,但相同温度条件下加入SeTE明显降低碳钢在1 mol·L-1HCl溶液中的腐蚀速率。
2.4 SeTE缓蚀作用的动力学分析
根据表1中不同温度条件下碳钢的腐蚀速率数据,绘制lnv′与1000/T的关系图,如图3所示。图中曲线a为1 mol·L-1HCl溶液,图中曲线b为含有SeTE10 g·L-1的1 mol·L-1HCl溶液。对图3进行线性拟合后,根据方程(6)进一步进行数据处理,通过斜率(-Ea/R)得到腐蚀反应的活化能动力学参数[5]。
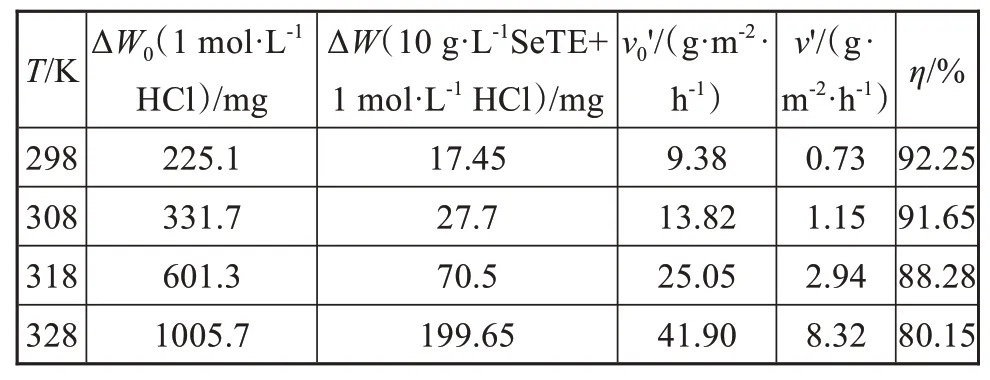
表1 碳钢在不含和含有SeTE的1 mol·L-1 HCl中的腐蚀参数Tab.1 The corrosion parameters of carbon steel in 1 mol·L-1 HCl with and without SeTE
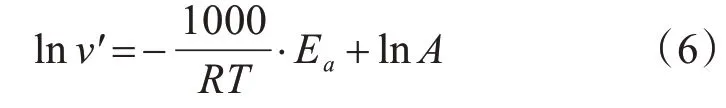
式中:v′为碳钢的腐蚀速率,g·m-2·h-1;Ea为腐蚀反应活化能,kJ·mol-1;A为指前因子;T为开尔文温度,K;R为气体摩尔常数,8.314 J·K-1·mol-1。
根据图3拟合可得,在1 mol·L-1HCl溶液中碳钢腐蚀反应的活化能为41.23 kJ·mol-1,在浓度c为10 g·L-1的含有SeTE的1 mol·L-1HCl溶液中碳钢腐蚀反应的活化能为66.67 kJ·mol-1。表明SeTE吸附在碳钢表面的腐蚀活性位点上,加大了反应速度控制步骤的能垒,降低了腐蚀反应的总速率。
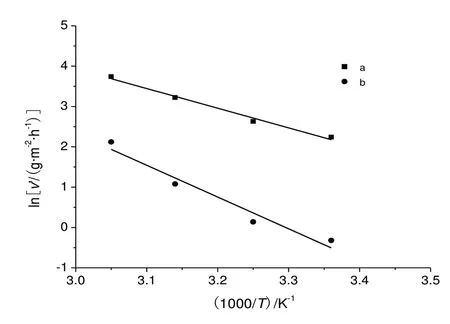
图3 碳钢在不含和含有SeTE的1 mol·L-1 HCl中的ln v′-(1000/T)图Fig.3 The ln v′-(1000/T)relation of carbon steel in 1 mol·L-1 HCl with and without SeTE
2.5 极化曲线法测试SeTE的缓蚀效率
在缓蚀剂的研究中,极化曲线测试也是一种表征缓蚀性能的常用方法。通过对曲线的Tafel极化区进行线性拟合,可以得到腐蚀电化学参数,如自然腐蚀电位(Ecorr)、自然腐蚀电流密度(Jcorr)、阴极和阳极Tafel斜率(bc,ba)等,计算出缓蚀效率并且分析缓蚀剂类型。在不含和含有Se TE(c=1 0 g·L-1)的1 mol·L-1HCl溶液中测试了稳态极化曲线,如图4所示。图中曲线a为1 mol·L-1HCl溶液,曲线b为SeTE10 g·L-1的1 mol·L-1HCl溶液。从图4拟合所得的腐蚀电化学参数列于表2中。可以看到,含有SeTE的1 mol·L-1HCl溶液中,碳钢的自腐蚀电位正移了32 mV,自腐蚀电流密度显著减小,计算所得缓蚀效率约为92%,与失重法测试结果一致。在添加SeTE的HCl溶液中,碳钢腐蚀的阴极和阳极Tafel斜率均发生了明显的变化,说明腐蚀反应的机理发生了变化,SeTE对腐蚀反应的阴极过程和阳极过程均有抑制作用,是一种混合型缓蚀剂[6]。

图4 碳钢在不含和含有SeTE的1 mol·L-1 HCl溶液中的极化曲线Fig.4 The polarize curves of carbon steel in 1 mol·L-1 HCl with and without SeTE
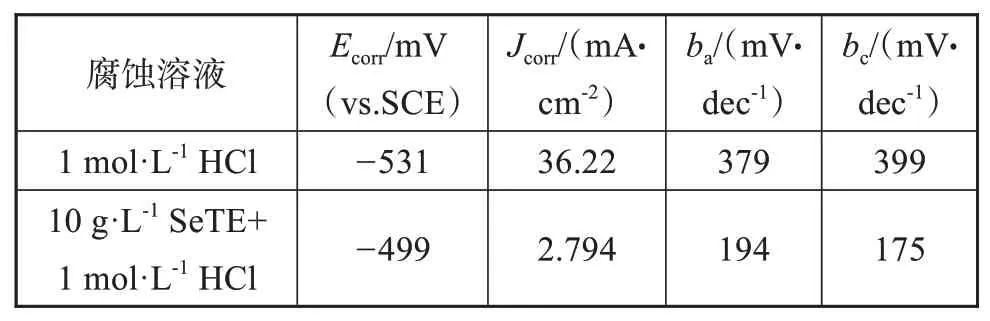
表2 碳钢在两种溶液中的腐蚀电化学参数Tab.2 The electrochemical corrosion parameters of carbon steel in two different solutions
2.6 电化学阻抗法测试SeTE缓蚀效率
在三电极电解池中测试了不含和含有SeTE(c=10g·L-1)的1 mol·L-1HCl溶液中的电化学阻抗谱,如图5所示。图中曲线a为1 mol·L-1HCl溶液,曲线b为SeTE 10 g·L-1的1 mol·L-1HCl溶液。用Zview软件对阻抗图谱进行拟合,等效电路如图5中的插图所示,拟合所得的电阻值列于表3中,其中Rs为溶液电阻值,Rct为腐蚀反应极化电阻值。根据公式(3)计算,缓蚀效率约为95%,与失重法和极化曲线法测试结果基本一致。阻抗测试结果表明,SeTE有效地抑制了碳钢与盐酸中的氢离子之间的电化学腐蚀反应,Rct值增大,对电子转移步骤有显著的影响,能够起到良好的缓蚀效果。
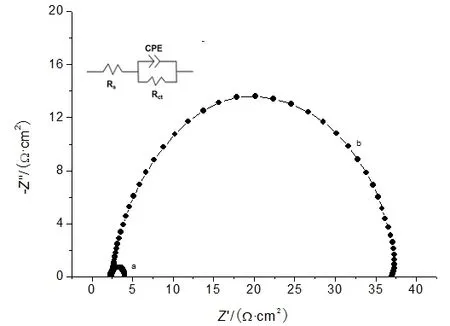
图5 碳钢在不同腐蚀溶液中的阻抗谱图Fig.5 The EIScurves of carbon steel in various aggressive solutions
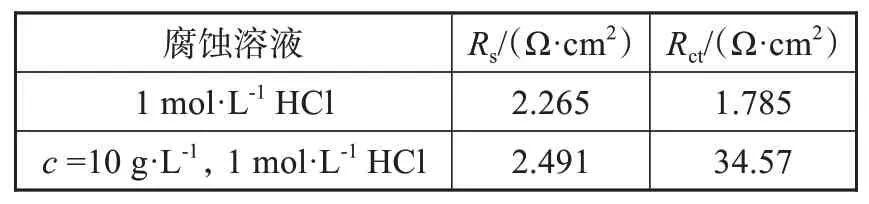
表3 碳钢在不同腐蚀溶液中的电化学阻抗参数Tab.3 The EISparameters of carbon steel in various aggressive solutions
3 结论
(1)用简单的水浸提取法制备含有SeTE的溶液,可用作1 mol·L-1HCl溶液中碳钢材料的绿色缓蚀剂。在25℃,当c达到20 g·L-1时,SeTE的缓蚀效率达到96%。
(2)失重法、极化曲线法和电化学阻抗法测试SeTE在c为10 g·L-1时的1 mol·L-1HCl溶液中对碳钢的缓蚀效率,结果均表明,25℃时其缓蚀效率达到92%。
(3)根据吸附热力学和动力学分析可知,本研究中的提取物SeTE在碳钢表面主要发生物理吸附,使腐蚀反应的表观活化能增大。根据拟合得到的电化学腐蚀参数可知,提取物属于混合型缓蚀剂,对腐蚀的阴极和阳极过程均有抑制作用。
