诃子对川楝子所致肝毒性的减毒作用机制初探
2022-02-12乌日汉陈玉花肖田梅毕力格丽丽孟香花宝乐尔韩晓静白梅荣
乌日汉,陈玉花,肖田梅,毕力格,丽丽,孟香花,宝乐尔,韩晓静,白梅荣✉
(1. 内蒙古民族大学,蒙医药研发工程教育部重点实验室,内蒙古 通辽 028000;2. 蒙医药研发工程教育部重点实验室,内蒙古 通辽 028000)
诃子在蒙药药性理论指导下具有“浩日音·达日拉嘎”(镇毒之王)之美名,也有调元之功效。两千多年来,在临床实践中逐渐形成的含有毒药味的常用蒙药复方中,98%以上均有诃子参与。研究证实,诃子能对抗长期用药导致的毒性反应,并对氧化应激所致的肝毒性损伤具有一定的减毒作用[1-2]。诃子与含剧毒的药物泵阿配伍使用,能起到减毒存效作用[3]。那么诃子在复方组成中是否起到减毒作用呢?以符合《中华人民共和国药典》和地方标准的代表性蒙药三子汤为例,三子汤由诃子25 g、川楝子15 g、栀子30 g 组成,具有清血热、解毒、分离“恶血”和“正血”的功能[4]。主治新旧血热症、希拉热、“恶血”与“正血”混合等,同时还具有缓解胶原诱导性关节炎(CIA)关节炎症、促进免疫功能、抗菌、抗凝血的作用[5],是蒙医临床疗效显著的地域性知名复方制剂。研究表明,三子汤中的川楝子具有肝脏毒性,然而诃子在此方中的应用是否起到配伍减毒作用,目前尚未见相关现代毒理学研究报道。基于此,本研究参照蒙医临床用药原则,采用亚急性毒性试验方法,以诃子和川楝子为研究核心,根据三子汤药物组成,将其拆分为川楝子组、诃子组、栀子组、川楝子加诃子组、川楝子加栀子组及诃子加栀子组,通过对SD 大鼠给予相应的药物溶液连续灌胃21 d,观察大鼠血清生化指标和病理组织学的改变情况,同时基于UPLC-MS 技术重点考察并比较诃子和川楝子共有代谢产物的变化规律,探讨诃子是否具有配伍减毒作用,进而评价三子汤安全性及复方组成的科学性和合理性。
1 实验材料
1.1 动物
SD 雄性大鼠64 只,SPF 级,体质量为(200±20)g,由辽宁长生生物技术股份有限公司提供[SCXK(辽)2015-0001]。饲养环境温度(23±1)℃,12 h 光照,大鼠自由饮水、进食。
1.2 药品与试剂
所有中药由内蒙古民族大学附属医院蒙药制剂室提供;谷丙转氨酶(ALT)、谷草转氨酶(AST)、总蛋白(TP)、甘油三酯(TG)、总胆固醇(CHO)试剂盒[罗氏诊断产品(上海)有限公司];纯化水(屈臣氏集团有限公司);质谱乙腈(美国Thermo Fisher Scientific 公司);甲酸(Sigma-Aldrich公司)。
1.3 仪器设备
质谱仪MASS(TripleTOF5600+,AB SCIEX™);台式高速冷冻离心机(Mikro 220R,Hettich);罗氏全自动生化分析仪(cobas c 311);移液器(Eppendorf N13462C,德国Eppendorf 公司);粉碎研磨仪(TL-48R,上海万柏生物科技有限公司);漩涡振荡器(QL-901,海门市其林贝尔仪器制造有限公司);色谱UHPLC(Nexera UHPLC LC-30A,岛津SHIMADZU)。
2 实验方法
2.1 给药剂量选择
为了评价诃子对三子汤是否有配伍减毒作用,筛选大鼠对三子汤散最大耐受量即临床等效量3 倍(3.857 1 g/kg)进行了实验研究,但通过预实验发现,临床等效量3 倍时,拆方后的川楝子组大鼠在染毒1 周内死亡60%以上,无法继续染毒,而临床等效量2 倍(2.571 4 g/kg)时川楝子既有肝毒性且无动物死亡;三子汤及其他各给药组在最大耐受量时均无大鼠死亡。因此,为了便于分析三子汤肝毒性机制是否与川楝子肝毒性一致,并分析诃子是否有配伍减毒作用,在实验中川楝子组采用了临床等效量2 倍剂量,其他给药组均采用了临床等效量3 倍剂量。
2.2 动物分组及取材
取SD 大鼠64 只,随机分为正常组、三子汤组、川楝子组、栀子组、诃子组、川楝子加诃子组、川楝子加栀子组和诃子加栀子组,每组8 只。从实验第1 天开始,各给药组均给予相应药物溶液灌胃,每日1 次,连续灌胃21 d,正常组灌胃等容量生理盐水。末次给药后,麻醉各组动物,取血,3 500 r/min 离心10 min 分离血清,部分血清用于检测AST、ALT、TG、CHO 和TP含量,部分血清置于-80 ℃用于检测代谢组学指标。采集肝组织固定于10%甲醛中,对肝组织进行常规脱水、浸蜡、包埋、切片和HE 染色,以检查肝组织病理组织学变化。
2.3 代谢物提取
血清样本于4 ℃解冻后,取100 μL 加入300 μL 甲醇,震荡提取于12 000 rpm,4 ℃下离心10 min,取上清液进样10 μL,用UPLC-MS检测。
2.4 UPLC-MS检测
本研究采用Waters BEH HILIC 色谱柱(100 mm× 2.1 mm,1.7 μm)。流动相A(0.1%甲酸水,乙酸铵)和B(乙腈),柱温35 ℃,流速0.3 mL/min,进样量10 μL。洗脱梯度:95%~50%B,0~16 min;50%B,16~20 min;50%~95%B,20~21 min;95%B,21~22.5 min。
质谱参数条件:分别采用电喷雾电离(ESI)正离子和负离子模式进行检测。ESI 源条件如下:离子源Gas1∶50,离子源Gas 2∶50;气帘气压力(CUR)∶25;界面加热温度:500 ℃(正离子)和450 ℃(负离子),离子喷雾电压浮动(ISVF)5 500 V(正离子)和4 400 V(负离子);TOF 质量扫描范围:100~1 200 Da,产物离子扫描范围:50~1 000 Da,TOF MS 扫描累积时间0.2 s,产物离子扫描累积时间0.01 s;二级质谱采用information dependent acquisition(IDA)获得,并采用high sensitivity 模式,去簇电压(DP)为± 60 V;碰撞能量为(35±15)eV。
2.5 数据处理
应用SPSS 22.0 进行统计学分析。采用t检验、秩和检验、单因素方差分析分别进行组间比较。以P<0.05代表差异具有统计学意义。
利用Analysis Base File Converter 软件将获得的原始数据转换成ABF 格式,再导入MS-DIAL 4.10 软件进行预处理。使用Mass Bank,Respect,GNPS 数据库进行比对。采用主成分分析(PCA)和正交偏最小二乘-判别分析法(OPLS-DA)分析各组样本。筛选VIP ≥1 及FC >1.5(或<0.5)和P<0.05 作为差异代谢物。再使用Metabo Analyst 4.0 分析代谢通路。
3 结果
3.1 各组大鼠肝功能生化指标检测比较
与正常组比较,川楝子组大鼠血清ALT、AST 水平显著升高(P<0.05),CHO、TP 水平显著降低(P<0.05);川楝子加栀子组TG 显著升高(P<0.05);诃子加栀子组、栀子组的ALT、AST显著下降(P<0.05);诃子组AST、TG 显著下降(P<0.05);三子汤组和川楝子加诃子组的AST、ALT、TG、CHO 和TP 水平均无显著变化(P<0.05)。结果提示川楝子组大鼠出现了明显的肝损伤,其他组大鼠未见明显肝损伤。见表1。
表1 各给药组大鼠肝功能生化指标比较(±s,n=8)
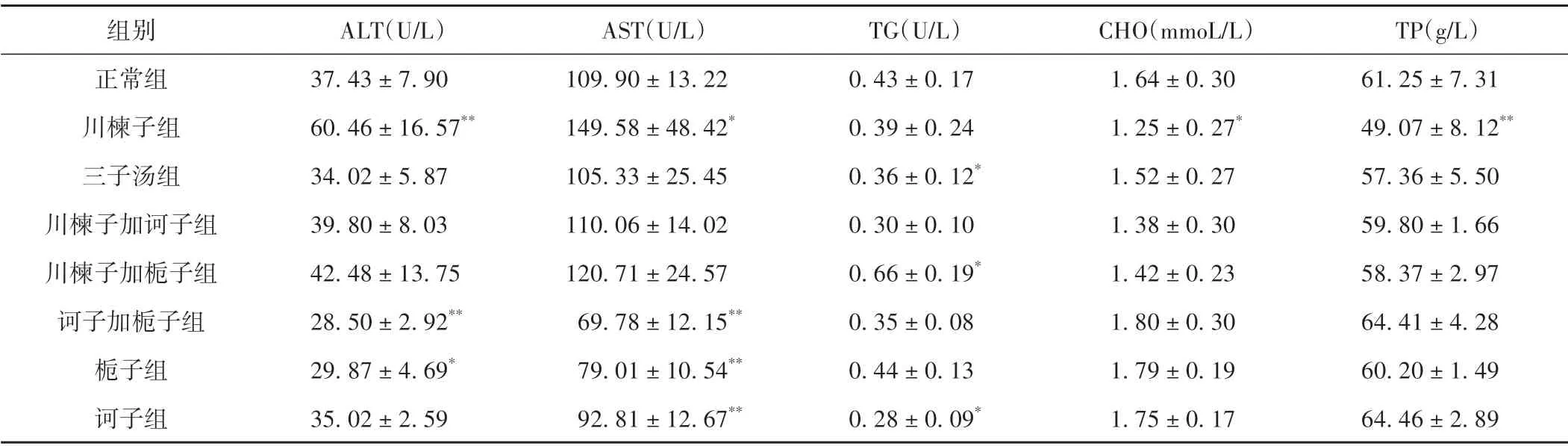
表1 各给药组大鼠肝功能生化指标比较(±s,n=8)
注:与正常组比较,*P <0.05,**P <0.01。
组别正常组川楝子组三子汤组川楝子加诃子组川楝子加栀子组诃子加栀子组栀子组诃子组TP(g/L)61.25±7.31 49.07±8.12**57.36±5.50 59.80±1.66 58.37±2.97 64.41±4.28 60.20±1.49 64.46±2.89 ALT(U/L)37.43±7.90 60.46±16.57**34.02±5.87 39.80±8.03 42.48±13.75 28.50±2.92**29.87±4.69*35.02±2.59 AST(U/L)109.90±13.22 149.58±48.42*105.33±25.45 110.06±14.02 120.71±24.57 69.78±12.15**79.01±10.54**92.81±12.67**TG(U/L)0.43±0.17 0.39±0.24 0.36±0.12*0.30±0.10 0.66±0.19*0.35±0.08 0.44±0.13 0.28±0.09*CHO(mmoL/L)1.64±0.30 1.25±0.27*1.52±0.27 1.38±0.30 1.42±0.23 1.80±0.30 1.79±0.19 1.75±0.17
3.2 各组大鼠肝组织病理学检测结果比较
肝组织病理检测结果显示,正常组大鼠肝小叶结构清晰,中央为中央静脉,肝细胞索和肝血窦大致呈放射状排列,肝细胞圆润、饱满,肝板排列规则、整齐。川楝子组大鼠可见少量肝细胞肿胀;川楝子加诃子组、诃子组和诃子加栀子组肝细胞胞质疏松淡染;川楝子加栀子组胞质疏松淡染,可见大小不一的水泡;栀子组胞质疏松,可见大小不一的水泡;三子汤和诃子组肝组织未见明显异常。见图1。

图1 各组大鼠肝组织病理切片图(HE,×200)
3.3 各组大鼠血清代谢物PCA结果比较
PCA 通过主要新变量对各组数据进行归类,去除重复性差和异常样本,可观察样品的聚集、离散程度。如图2 所示,正常组(8)与三子汤组(2)、川楝子加诃子组(4)有小部分重合,说明代谢物差异小。正常组与川楝子组(1)呈明显分离,说明代谢物有显著差异。正常组与川楝子加栀子组(3)、诃子加栀子组(5)、栀子组(6)呈明显分离,说明血清代谢物具有一定的差异性。正常组与诃子组(7)样品分布点靠近,表明诃子有回调潜在差异代谢物的趋势。

图2 各组大鼠血清代谢物PCA图
3.4 各组大鼠血清代谢物OPLS-DA结果比较
OPLS-DA 作为一种有监督的分析方法,能够筛选出差异代谢物。如图3 所示,正常组(8)与川楝子组(1)、三子汤组(2)、川楝子加栀子组(3)、川楝子加诃子组(4)、诃子加栀子组(5)、栀子组(6)的大鼠血清代谢物呈现出明显的分离趋势,说明代谢物谱存在显著差异,与诃子组(7)差异小。随后通过参数检验进行OPLS-DA 模型验证,模型具有良好的准确率和预测率(参数R2Y 和Q2均>0.5)。
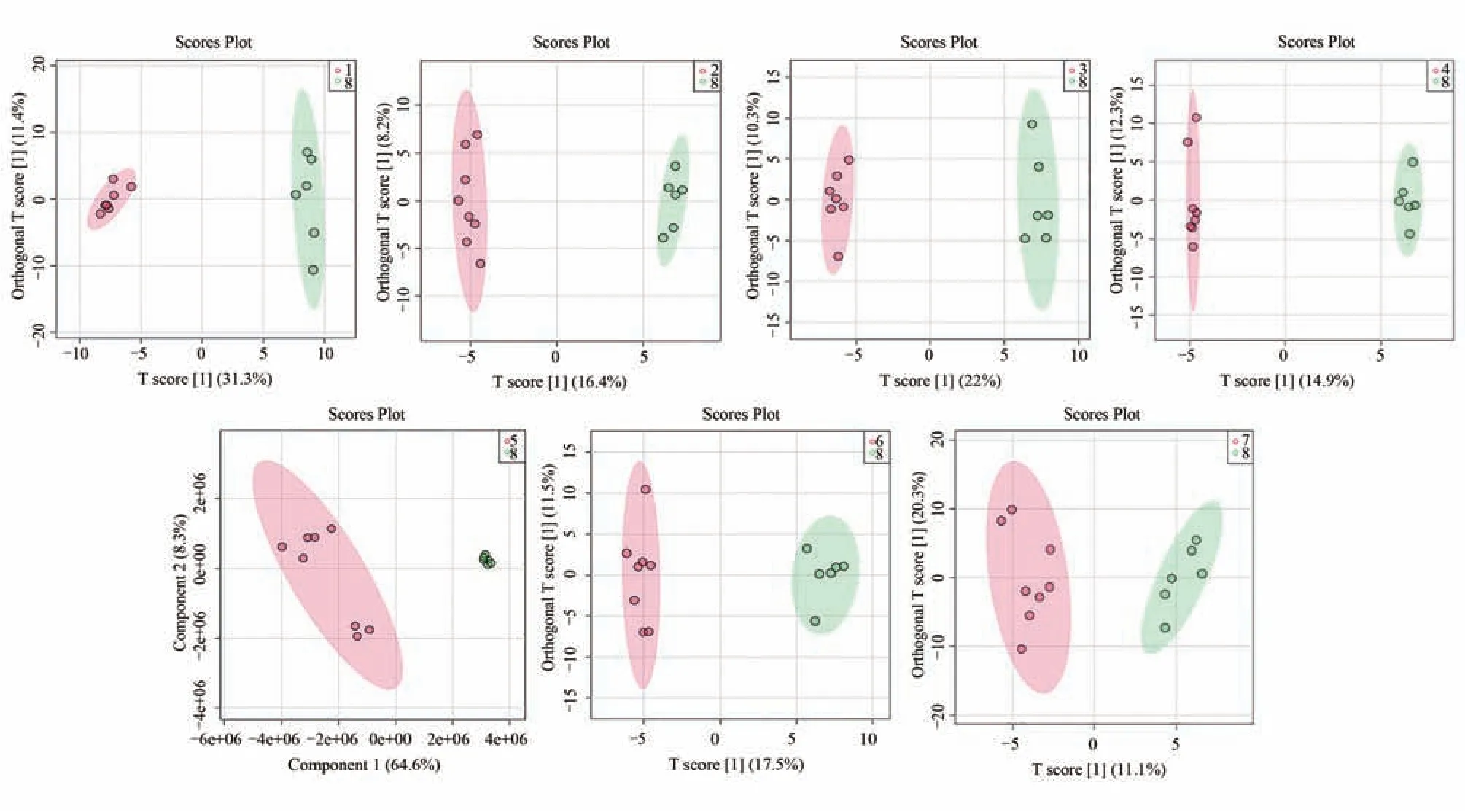
图3 各组大鼠血清OPLS−DA得分图(S−plot图)
3.5 差异代谢物的筛选
为筛选潜在差异代谢物,采用OPLS-DA 中VIP ≥1,且fold change >1.5(或<0.5)和P<0.05 的标准筛选,通过MassBank,Respect,GNPS 数据库进行检索分析,血清样本中共鉴定出12 个差异代谢物,其中包括代谢物种类、VIP 值、对应的分子式、保留时间及相对分子质量等信息。与正常组比较,川楝子组吡咯-2-羧酸、缬氨酸、胆红素、LPC 18∶2、LPC 16∶0、LPC 18∶1 显著升高,肉碱、sn-甘油-3-磷酸胆碱、胸腺嘧啶-β-D-葡萄糖苷、[5-乙酰氧基-3-(羟甲基)-2-氧基-6-丙烷-2-基环己-3-烯-1-烯基]3-甲基戊酸酯显著下降;三子汤组LPC16∶0、LPC 18∶2、LPC 18∶1 明显升高;川楝子加诃子组和川楝子加栀子组LPC 18∶2、LPC 18∶1、赖氨酸明显升高;诃子加栀子组LPC 18∶2、LPC 16∶0、谷氨酰胺(D)、葡萄糖、牛磺酰脱氧胆酸、尿嘧啶核苷、反式牛磺酸、糊精酸、二十二碳六烯酸、L-α-磷脂酰乙醇胺(大豆)升高;栀子组LPC 18∶2、LPC 16∶0、谷氨酰胺(D)、葡萄糖、牛磺酰脱氧胆酸、尿嘧啶核苷、反式牛磺酸、糊精酸、二十二碳六烯酸、肌苷升高,sn-甘油-3-磷酸胆碱下降;诃子组LPC 18∶2、谷氨酰胺(D)升高。 见表2、表3。
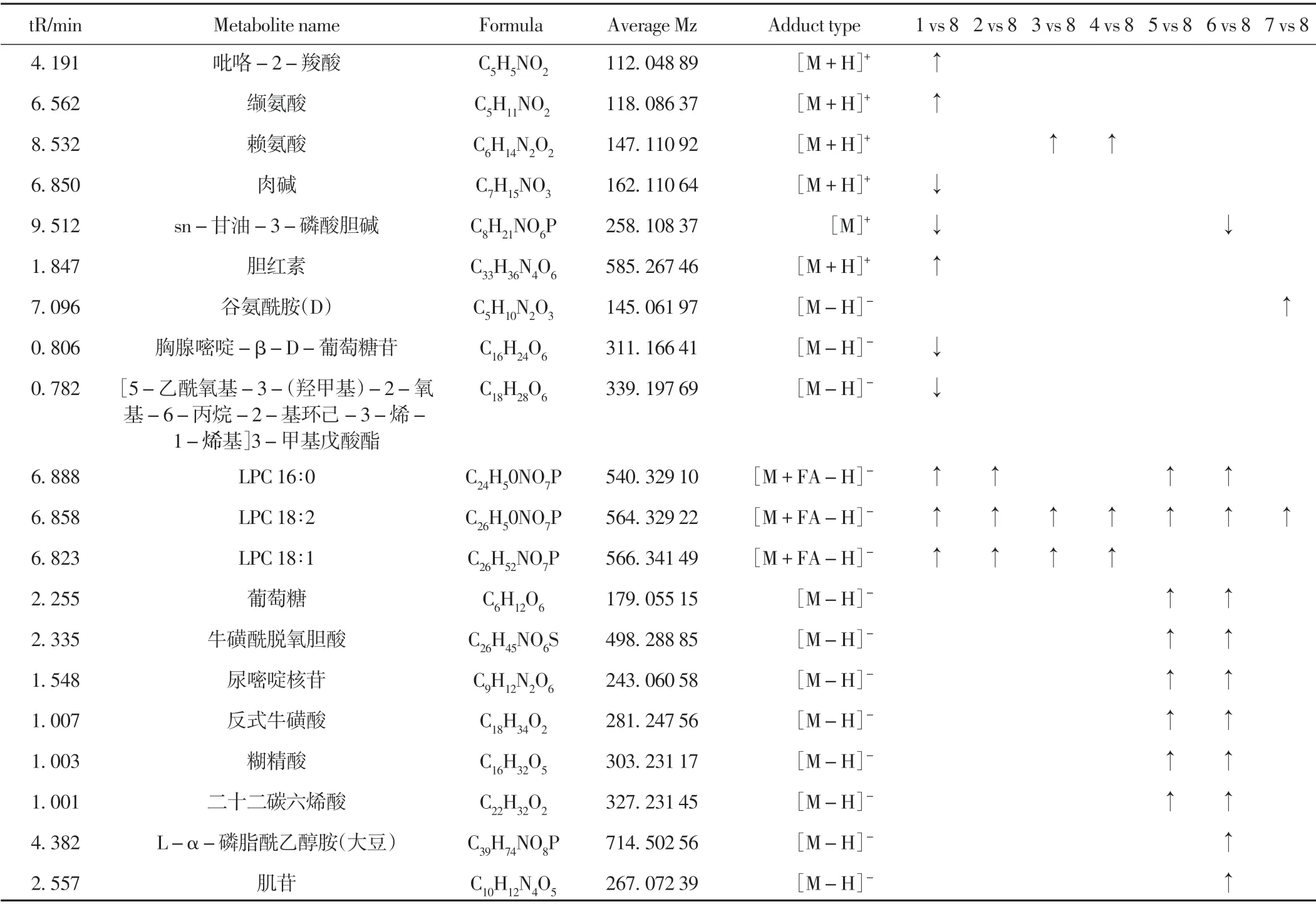
表2 基于UHPLC−MS 的血清差异代谢物鉴定

表3 血清差异代谢物的筛选
3.6 差异代谢物通路分析
将筛选出的差异代谢物导入MBRole 2.0 进行通路富集分析。结果显示,这些血清代谢物主要与ABC转运蛋白、氨基酸的生物合成、蛋白质消化吸收、嘧啶代谢、癌症的中心碳代谢、精氨酸生物合成、氨酰-tRNA 合成代谢、嘌呤代谢、FoxO 信号通路,甘氨酸、丝氨酸和苏氨酸代谢等10 条代谢通路密切相关。其中,与代谢物相关性最强的是ABC 转运蛋白,其次为氨基酸的生物合成代谢通路。见图4。
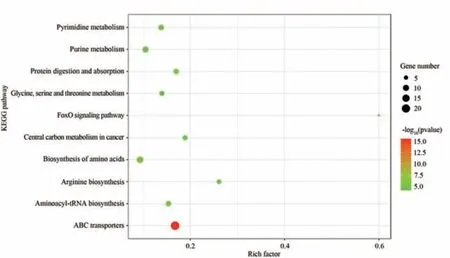
图4 血清样品代谢通路气泡图
4 讨论
4.1 诃子在血清生化和病理组织学层面缓解川楝子肝毒性作用评价
血清ALT、AST 可以敏感地反映肝细胞的完整程度。生化指标显示,与正常组比较,川楝子组大鼠血清ALT、AST水平明显升高,提示川楝子导致大鼠出现了肝脏损伤和功能障碍。而诃子加栀子组、栀子组的ALT、AST 水平显著下降(P<0.05),诃子组AST 水平下降(P<0.05),三子汤组、川楝子加诃子组的血清ALT、AST水平则无明显变化。病理组织学结果显示,川楝子组大鼠肝细胞肿胀,而三子汤组和诃子组肝细胞未见异常,其余各组肝细胞也仅可见胞质疏松淡染,这提示除川楝子组外,其余各组大鼠均未见明显肝损伤。以上实验结果说明,诃子与川楝子配伍能够降低川楝子的肝毒性,即推测诃子对三子汤复方有配伍减毒作用。
4.2 诃子在脂质代谢层面缓解川楝子肝毒性作用评价
溶血磷脂酰胆碱(LPC)是磷脂的一种,与动脉粥样硬化、血脂异常等代谢性疾病和心血管疾病密切相关。LPC 主要在肝脏代谢,在肝脏疾病和药物引起的肝毒性血清中,LPC 16∶0、LPC 18∶0、LPC 18∶2、LPC 18∶3和LPC 18∶1等多种LPCs的浓度均明显升高[6-10]。大量研究推测,LPC 将会成为肝脏疾病和肝毒性损伤的生物标志物,将在肝脏疾病和药物肝毒性的诊断与治疗中发挥重要作用。另外,较高水平的LPC 能够反映机体血浆脂质的转运能力。LPC 含量升高可抑制外周游离胆固醇的酯化,使之被载脂蛋白携带最终转运回肝脏代谢等脂质转运过程受限,增加血浆胆固醇含量,使肝脏功能受损进而发生脂肪变性[11-14]。本研究结果显示,与正常组比较,川楝子组血清LPC 16∶0、LPC 18∶1、LPC 18∶2 含量明显升高;与川楝子组比较,三子汤组血清LPC 16∶0、LPC 18∶2、LPC 18∶1 含量,川楝子加诃子组和川楝子加栀子组血清LPC 18∶2、LPC 18∶1 含量,诃子加栀子组和栀子组血清LPC 18∶2、LPC 16∶0含量,以及诃子组血清LPC 18∶2含量均显著降低。基于此,推测LPC 就是川楝子产生肝毒性和诃子缓解川楝子肝毒性的共有生物标志物之一。
4.3 诃子在氧化层面缓解川楝子肝毒性作用评价
肝脏是机体进行氨基酸代谢的关键场所,当其发生损伤时会影响氨基酸的代谢,使肝细胞内的氨基酸合成减少[15-16]。缬氨酸属于支链氨基酸,是人体必需的氨基酸和生糖氨基酸。缬氨酸水平的升高能影响肝脏和血清中ALT、AST 含量及部分非特异免疫指标[17]。本研究结果显示,川楝子组血清缬氨酸含量显著升高,提示川楝子使体内支链氨基酸含量上升,引起肝功能受损。吡咯-2-羧酸是羟脯氨酸代谢氧化主要产物,也是α-酮戊二酸发生转氨作用的产物[18]。吡咯-2-羧酸显著升高会影响氧化应激反应,可用于癌症的早期预测[18-19]。本研究发现,川楝子干预后血清吡咯-2-羧酸水平显著升高,可能通过加强氧化应激反应,进而影响氨基酸代谢来加重肝损伤。而诃子与川楝子配伍后,可回调缬氨酸和吡咯-2-羧酸含量。这一结果提示,川楝子肝毒性也与缬氨酸和吡咯-2-羧酸含量升高有关;诃子降低血清中缬氨酸和吡咯-2-羧酸含量可能是其缓解川楝子肝脏毒性的机制之一。
综上所述,诃子降低血清LPC 含量可能是其缓解川楝子所引发的肝细胞肿胀及升高血清AST、ALT 含量的主要机制之一;诃子与川楝子配伍后能够明显降低川楝子的肝脏毒性,大大提高三子汤安全性,诃子在该方中具有配伍减毒作用。可见,传统蒙药方剂三子汤复方组成具有高度的合理性和科学性。
