MMR蛋白表达与不同子宫内膜病变类型的相关性
2022-01-20刘晓娟马丽莎
刘晓娟 马 会 马丽莎 李 坤
1.河北北方学院附属第一医院(张家口,075000);2.河北省张家口市传染病医院
子宫内膜癌发病率仅次于宫颈癌[1]。错配修复基因(MMR)是一组参与DNA错配修复系统的关键基因[2-3],其功能丧失(dMMR)可导致基因组微卫星不稳定(MSI-H),进而导致基因组出现高突变表型[4],子宫内膜癌中dMMR发生率达20%~40%[5]。临床子宫内膜病变常见类型包括子宫内膜息肉、子宫内膜不典型增生、子宫内膜癌。子宫内膜息肉是常见的妇科良性疾病之一,由子宫内膜局部过度增生导致[6]。子宫内膜不典型增生即腺体存在细胞异型性,但未发展至浸润[7]。近年来子宫内膜癌的发病率呈上升趋势且趋于年轻化,美国癌症协会已将与非息肉性遗传性结直肠癌相关的基因突变者及可疑携带者列为罹患子宫内膜癌的高危人群,建议对子宫内膜癌高危人群应自35岁开始每年进行一次子宫内膜癌筛查。本研究通过检测不同子宫内膜病变类型的病理组织标本中MMR蛋白,探究MMR蛋白在不同病变组织表达差异,及其与子宫内膜癌临床指标相关性,为临床预防、治疗子宫内膜病变疾病提供参考。
1 材料与方法
1.1 受试者资料来源
回顾性收集2017年1月—2019年12月于本院治疗的子宫内膜病变患者,包括子宫内膜息肉、子宫内膜不典型增生、子宫内膜癌,收集患者年龄、体质指数(BMI)、产次、宫内节育器史等相关资料,对子宫内膜癌者收集临床病理指标等。纳入标准:诊断为子宫内膜不典型增生[8],非典型性质的单纯性增生或复杂拥挤的伴有非典型细胞的腺体增生,子宫内膜息肉病理确诊符合妇产科诊断病理学(第2版)诊断标准,子宫内膜癌病理诊断符合诊治规范[9];年龄18~75岁。排除标准:合并其他子宫、宫颈恶性病变或其他恶性肿瘤。本研究经本院伦理委员会审批,患者均签署知情同意书。
1.2 免疫组化分析
采用免疫组化SP法检测病理组织中MMR蛋白表达情况,使用来自北京中山杉金桥生物技术公司的单克隆抗体[MLH1(1:80)、MSH2(1:100)、MSH6(1:200)、PMS2(1:40)]。由两位病理医师进行盲法判定,计数5个视野或500个细胞,腺上皮细胞核内染色为棕黄色颗粒评估为阳性细胞,周围正常细胞如间质细胞、淋巴细胞作为对照。
1.3 结果判定
按美国病理学家协会CAP标准判定,即存在任何确定的病变组织细胞核染色为阳性判定为阳性,完全不表达判定为阴性,任一MMR蛋白(MLH1、MSH2、MSH6、PMS2)阴性即为dMMR,所有蛋白阳性判定为pMMR(MMR-proficient)[10]。
1.4 统计学处理
2 结果
2.1 基本情况
子宫内膜息肉、子宫内膜非典型增生、子宫内膜癌各60例,3组患者BMI、产次、宫内节育器史无差异(P>0.05),年龄子宫内膜癌组大于子宫内膜息肉组和子宫内膜非典型增生组(P<0.05)。见表1。
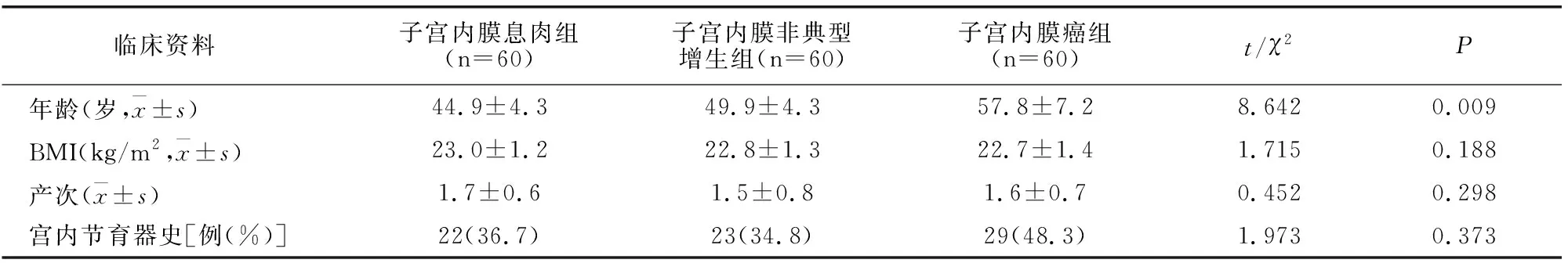
表1 各组一般资料比较
2.2 MMR蛋白表达情况
子宫内膜癌、子宫内膜非典型增生、子宫内膜息肉各组患者dMMR发生率分别为33.3%(20/60)、15%(9/60)、6.7%(4/60)(P<0.001)。MLH1、PMS2表达缺失发生比例,子宫内膜癌组与子宫内膜非典型增生组无差异(P=0.092)但均高于子宫内膜息肉组(P<0.05);PMS2表达缺失比例子宫内膜癌组与子宫内膜非典型增生组无差异(P>0.05)但均高于子宫内膜息肉组(P<0.05)。MSH2、MSH6表达缺失比例3组无差异(P>0.05)(表2)。
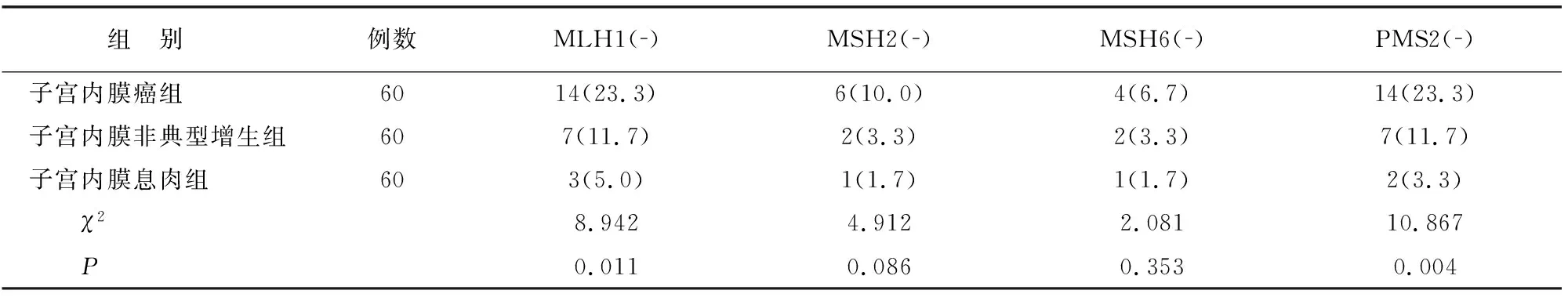
表2 不同子宫内膜病变组MMR蛋白缺失表达比较[例(%)]
2.3 子宫内膜癌MMR蛋白表达与临床病理指标
统计患者年龄、肿瘤分期、肌层浸润、淋巴结转移、肿瘤大小与子宫内膜癌dMMR发生相关性发现,肌层浸润≥1/2时dMMR发生率(58.9%)高于肌层浸润<1/2(23.3%),而在年龄、肿瘤分期、淋巴结转移、肿瘤大小之间均未发现dMMR发生率有差异(P>0.05)。见表3。
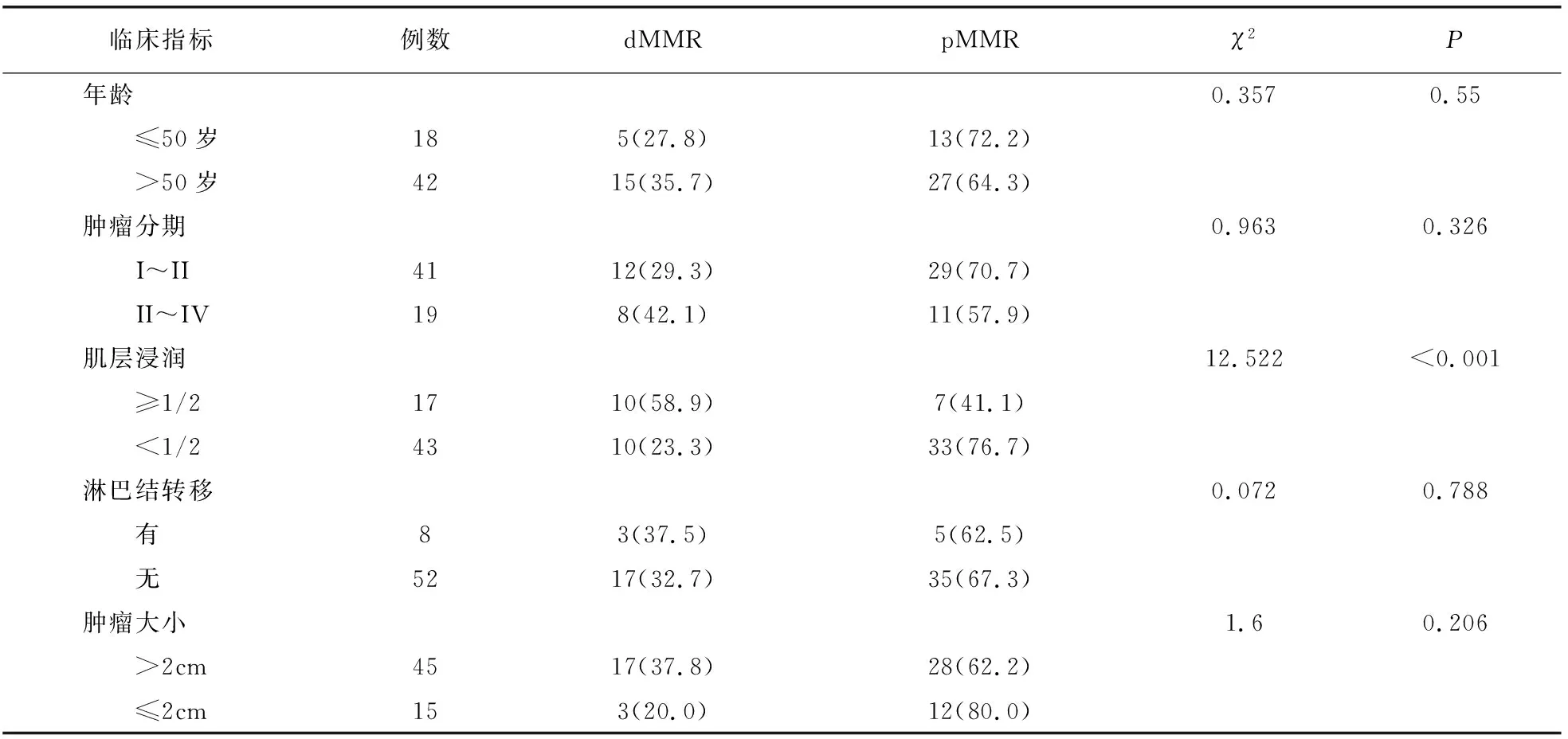
表3 子宫内膜癌不同MMR蛋白表达与临床病理指标比较[例(%)]
3 讨论
子宫内膜息肉是一种突出于子宫内膜表面的腺体和间质的局部性、无序增生。有研究认为他莫西芬通过诱导子宫内膜细胞KRAS突变(45%)进而引起子宫内膜间质细胞单克隆过度生长以及二次诱导引起的多克隆良性腺体增生导致子宫内膜息肉肿瘤的发生,子宫内膜息肉与基因表达、突变和免疫系统有相关性[11]。子宫内膜非典型增生是一种发生在子宫内膜的癌前病变,由异常细胞的过度生长,或是由子宫内膜增生引起[12]。随着分子生物学的发展以及精准医疗的进步,子宫内膜癌分型从雌激素依赖分型、世界卫生组织学分型到发展到TCGA分子分型。微卫星不稳定超突变型是一组分子诊断伴有错配修复蛋白缺失的病理类型,该类型患者具有较高的肿瘤突变负荷,是PD-1/PD-L1抑制剂的获益人群。MSI-H/dMMR状态的子宫内膜癌也在帕博丽珠单抗的临床试验中取得显著获益[13]。
子宫内膜增生活跃及子宫内膜癌实体瘤中dMMR发生率均较高[14]。本研究显示在不同类型子宫内膜病变中,子宫内膜癌dMMR发生率高于不典型增生和息肉,提示dMMR的发生与肿瘤发生可能有关,子宫内膜息肉dMMR发生率较低(6.7%),提示dMMR不适宜作为子宫内膜息肉的常规分子筛查指标。有研究表明多发性息肉与单纯增生性息肉亚型dMMR更常见[15]。作为子宫内膜癌的癌前病变,子宫内膜不典型增生也有较高的dMMR发生率,略低于子宫内膜癌。MMR蛋白参与全周期的细胞分裂DNA修复,MMR蛋白功能丢失增加了癌前病变发生发展的可能性。
本研究中子宫内膜癌MLH1与PMS2缺失率较高。MMR蛋白中,MLH1缺失率较高,而PMS2与MLH1形成异二聚体起协同作用,若MLH1表达缺失,则存在双蛋白缺失情况[16]。为进一步分析子宫内膜癌MMR蛋白表达与临床病理指标的相关性,本研究发现dMMR发生与肌层浸润有关,与年龄、肿瘤分期、淋巴结转移未见差异,与既往报道一致[17]。
综上所述,MMR蛋白参与了子宫内膜病变的发生发展。dMMR在不同类型子宫内膜病变均存在,提示了筛查的意义;dMMR在子宫内膜癌中发生率最高且与肌层浸润有关,提示MMR蛋白可能参与了子宫内膜恶性肿瘤的发生发展。
