替米考星肠溶颗粒在猪体内的残留消除试验
2022-01-17孙晨明潘超男叶丽青许燕茹苏治国
孙晨明,潘超男,葛 臣,叶丽青,许燕茹,苏治国
(江苏农牧科技职业学院,江苏 泰州 225300)
替米考星(Tilmicosin) 是一种畜禽专用大环内酯类抗生素[1],由顺式和反式两种异构体以85∶15 的比例混合而成[2],多用于由放线杆菌或巴氏杆菌引起的肺炎等呼吸系统疾病[3]。替米考星在我国亦已获准用于治疗猪和牛的巴氏杆菌病和鸡的支原体感染。以往替米考星批准用于猪的剂型只有预混剂,替米考星肠溶颗粒是采用先进的包衣技术,顶级的流化床设备研发的替米考星新型制剂,能有效避免高温对替米考星的破坏,提高药物的稳定性,同时解决传统替米考星预混剂在拌料给药时因苦味造成猪采食量降低、药物摄入量不足,影响动物生长性能及药物治疗效果等问题。
目前,国内外只有对替米考星预混剂在不同动物组织中的残留消除研究报道,残留检测的主要方法是高效液相色谱(HPLC)法,本试验对瑞普(天津)生物药业有限公司开发的替米考星肠溶颗粒新制剂开展替米考星在猪主要可食性组织中的残留检测,采用乙腈提取,C18固相萃取柱净化,HPLC紫外检测器测定猪肌肉、肝脏、肾脏和脂肪中的替米考星残留,研究其在猪体内残留消除规律,为替米考星肠溶颗粒在猪休药期的制定提供依据,以指导临床合理用药,保证消费者使用安全。
1 材料与方法
1.1 受试药物 替米考星肠溶颗粒:规格:20%(以替米考星计),批号:121001,生产企业:瑞普(天津)生物药业有限公司。推荐用法与剂量是混饲:每1 000 kg饲料,猪400 g(相当于加本品2 000 g,即每1 kg饲料加本品2 g),连用15 d。
1.2 仪器和设备 高效液相色谱仪,Waters 2695;检测器,Waters 2489;色谱柱,Agilent Eclipse XDB-C18色谱柱(5 μm,4.6 mm ×250 mm),美国Agilent Technologies公司;组织匀浆机B-400,瑞士Buchi公司;CR22GⅡ高速冷冻离心机;氮吹仪,Organomation Associates公司;感量0.000 01 g的Mettler AE240型分析天平,梅特勒-托利多公司;VTX-3000L型高速涡旋仪,Harmony公司;超纯水设备,美国Millipore公司;1~10 μL、20~200 μL和100~1 000 μL 可调微量移液枪,Eppendorf公司;C18 SPE柱,Bond Elut,6cc/500 mg,美国Agilent Technologies公司。
1.3 主要试液
1.3.1 配制二丁胺缓冲液(DBAP) 将85%磷酸100 mL缓慢加至900 mL纯水中配成10%磷酸溶液。将10%磷酸溶液700 mL加到168 mL 二丁胺中,充分混匀冷却后,用85%磷酸调pH至2.5,再加132 mL纯水定容[4-6]。
1.3.2 流动相 在1 000 mL的容量瓶中分别加入纯水700 mL、乙腈溶液105 mL、四氢呋喃50 mL、1 mol/mL 二丁胺磷酸缓冲液50 mL,最后用纯水定容至1 000 mL,0.22 μm 滤膜过滤备用。为有效防止有机溶剂挥发,各组分使用时密封并进行超声脱气15 min处理。
1.3.3 洗脱液 0.1 mol/L乙酸胺甲醇-乙腈溶液(2∶8)是由7.71 g乙酸胺先用200 mL甲醇溶解,再用790 mL乙腈混匀,待溶液冷却至室温后,用乙腈定容至1 000 mL配置而成。
1.4 方法
1.4.1 试验动物 选用28头健康的三元猪,公母各半,80~90 kg,随机分成6个组进行试验,购自江苏大丰中北畜牧场。采用耳标标记识别。用于试验的猪在试验前1个月以内未用相关抗菌药物。
1.4.2 给药 25头健康三元猪饲喂含有替米考星肠溶颗粒的饲料,试验期间自由采食,连用15 d,之后改用不添加任何药物的全价饲料继续饲养。另外3头三元猪做空白对照,试验期间每天清理猪粪,猪舍采用自然通风。
1.4.3 样品采集和保存 分别在停药后的第12小时、第3、6、9天和第14天时各随机选取5头猪宰杀并采集其可食性组织。猪经颈静脉放血处死后,每只猪取肌肉500 g左右(背最长肌),肝脏500 g左右(取整叶),双肾各取1/2(纵切),脂肪200 g。所取样品做好标记、包装保存在-20 ℃冰箱中备用。
1.4.4 测定替米考星残留量
1.4.4.1 前处理阶段 (1)提取:分别称取采集的肝脏、脂肪、肾脏和肌肉组织各2.0 g放于聚丙烯离心管中,先加入5 mL乙腈,先后振荡、超声3 min,然后在转速5 000 r/min下离心10 min,将上清液转移到另1个50 mL聚丙烯离心管中。剩余残渣用事先配好的2 mL 0.1 mol/L的磷酸二氢钾缓冲液(pH 2.5)和5 mL乙腈溶液重复提取1次。于聚丙烯离心管中合并2次上清液,最后用30 mL超纯水混匀。(2)净化:分别用10 mL甲醇和10 mL超纯水平衡SPE柱,控制流速约为每秒1滴,洗涤液分别用10 mL 超纯水和10 mL乙腈,干燥3 min后用3 mL 0. 1 mol/L乙酸胺甲醇-乙腈溶液(2∶8)进行洗脱,用5 mL 刻度试管收集洗脱液,氮气吹干处理。1 mL 流动相复溶残渣得到的复溶液经0.22 μm滤膜过滤,用进样针吸取100 μL滤液进行高效液相色谱分析[4-7]。
1.4.4.2 色谱条件 色谱柱选用Agilent Technologies公司生产的Eclipse XDB -C18色谱柱(5 μm,4.6 mm×250 mm);流动相是由体积比为10.5∶5∶5∶79.5的乙腈-四氢呋喃-二丁胺盐缓冲液-水混合液;检测波长:290 nm;流速:1 mL/min;进样量:100 μL; 柱温:35 ℃。
1.4.4.3 标准曲线 取空白脂肪和肌肉组织样品,添加系列标准工作液,分别制备0.1、0.2、0.4、0.5、1、2 μg/g和4 μg/g空白添加浓度,将一定浓度标准工作液加入到空白肝脏和肾脏中,空白添加浓度为0.1、0.2、0.4、1、2、4 μg/g和10 μg/g。7个浓度分设5个平行,按1.4.4.1方法进行处理。在1.4.4.2条件下,从低到高浓度进样测定分析。以检测的峰面积为纵坐标,标志物检测浓度为横坐标来绘制标准曲线,计算回归方程及相关系数。
1.4.4.4 检测限(LOD)与定量限(LOQ) 将适量标准工作液加入到空白组织中制成以下4个空白添加浓度:0.01、0.025、0.05 μg/g和0.1 μg/g。4个浓度分设5个平行,分别按1.4.4.1方法进行处理。检测限(LOD)以信噪比(S/N)=3确定,定量限(LOQ)由S/N=10确定。
1.4.4.5 添加回收率与精密度的测定 将适宜浓度的标准工作液分别加入到空白脂肪和肌肉组织样品,制备成0.05、0.1 μg/g和1 μg/g的空白组织添加样品,分别准确称取空白肝脏和肾脏组织样品,添加适宜浓度的标准工作液分别制备0.05、0.5 μg/g和5 μg/g的空白组织添加样品。按1.4.4.1方法进行处理后,添加浓度与对应浓度的替米考星标准液均做HPLC检测。每批3个浓度分设5个重复样品,共3个批次。依此计算标志物替米考星的回收率、批内与批间变异系数。
2 结果
2.1 色谱行为 替米考星和其他杂质在本试验确立的色谱条件分离较好,色谱峰形对称,基线平稳,替米考星反式异构体出峰时间在10.3 min左右,顺式异构体出峰时间在12.4 min左右,如图1所示。
2.2 标准曲线 在建立的色谱条件下,肝脏、脂肪、肌肉和肾脏组织空白添加平均浓度与其平均峰面积的回归方程为:y=144 624x-1 366.3(R2=0.999 9);y=150 000x-168.55(R2=0.999 9);y=135 206x-1 243.5(R2=0.999 9)和y=153 842x-10 684(R2=0.999 9),均呈现良好的线性关系。
2.3 LOD与LOQ 按照1.4.4.4方法求得猪各组织中替米考星的LOD和LOQ分别为0.025 μg/g和0.050 μg/g。
2.4 测得的回收率和精密度 肝脏和肾脏在0.05、0.5 μg/g和5 μg/g三个添加浓度水平,肌肉和脂肪在0.05、0.1 μg/g和1 μg/g三个添加浓度水平测得的回收率和精密度测定结果见表1。本方法的平均添加回收率在81.92%~86.53%,批内与批间变异系数均小于5%。
2.5 猪各组织中替米考星平均残留量及替米考星的消除 给药后测得猪组织中替米考星残留结果见表2。替米考星残留消除曲线如图2所示。表2是替米考星肠溶颗粒按推荐方案混饲给药连用15 d的残留检测数据,停药12 h后的结果显示,5头猪肾脏中替米考星的平均残留量为(1.771±0.675) mg/kg,全部超过我国规定的残留限量标准(1.0 mg/kg);肝脏是残留第2高的组织,但停药12 h后5头猪中仅有2头猪肝脏中替米考星的残留量超过限量标准(1.5 mg/kg),平均残留量为(1.454±0.888) mg/kg;停药12 h后5头猪中有4头猪的肌肉组织替米考星残留量超过限量标准(0.1 mg/kg);脂肪组织中残留量最低,停药12 h后5头猪中有3头猪的脂肪组织中替米考星残留量超过限量标准(0.1 mg/kg),2头猪脂肪组织中的残留量低于残留量限量标准。
停药3 d后在5头猪肝脏和肾脏组织中测得替米考星平均残留量分别为(0.568±0.238) mg/kg和(0.607±0.174) mg/kg,都低于我国规定的残留限量标准;来自3头猪的肌肉组织中替米考星残留量低于方法的检测限,2头猪的肌肉组织中替米考星残留量低于定量限;来自5头猪的脂肪组织替米考星残留量均低于仪器检测限。至停药第6天,来自5头猪的肝脏和肾脏组织中替米考星残留量仍高于定量限,脂肪和肌肉组织的替米考星残留量均低于检测限;至停药第14天时,仅有肾脏组中替米考星残留量仍能检出。
2.6 猪各可食性组织中替米考星休药期的计算 替米考星在猪各可食性组织中最高残留限量(MRL)是肝脏为1.5 mg/kg、肾脏为1 mg/kg、肌肉和脂肪均为0.1 mg/kg。将本试验实测的肝脏和肾脏替米考星残留量数据依据上述标准采用WT1.4休药期软件拟合,得出替米考星在猪肝脏休药期为6.17 d(图3),猪肾脏休药期为4.96 d(图4);至停药第3天后测得5头猪脂肪和肌肉组织中替米考星残留量均低于定量限,替米考星在猪脂肪和肌肉的休药期可依据实测残留量暂定为3 d。
3 讨论
动物性食品中替米考星残留检测研究较多,本试验参考农业部1025号公告-10-2008《动物性食品中替米考星残留检测——高效液相色谱法》[8]和刘德金等[9]建立的色谱条件基础上,将流动相比例从乙腈-四氢呋喃-二丁胺磷酸盐缓冲液-水(体积比100∶50∶50∶800)[10]调整为乙腈-四氢呋喃-二丁胺磷酸盐缓冲液-水(体积比105∶50∶50∶795),在保证峰形良好的前提下出峰时间有所缩短,这是由于在反相色谱中增加了乙腈这种有机溶剂的比例,使替米考星这种极性物质保留时间缩短,出峰时间前移。
替米考星为弱碱性化合物,微溶于水,与酸制成盐后易溶于水,易溶于如正己烷、丙酮、乙腈、四氢呋喃等有机溶剂[11],本试验参考刘彩等[6]的方法选择乙腈提取组织中的替米考星,因为乙腈不仅对替米考星有较高的溶解性,而且能有效除去提取液中的蛋白质和脂肪,使药物与其他干扰基质充分分离,提高药物的回收率。本试验采用固相萃取(SPE)分离技术用C18填料的萃取柱对提取液进行净化,与HPLC柱的固定相一样,保留机理与HPLC一致,具备良好的保留效果[12-13]。在所建立的检测方法下,猪可食性组织中替米考星的平均回收率均在80%以上,满足回收率要求。
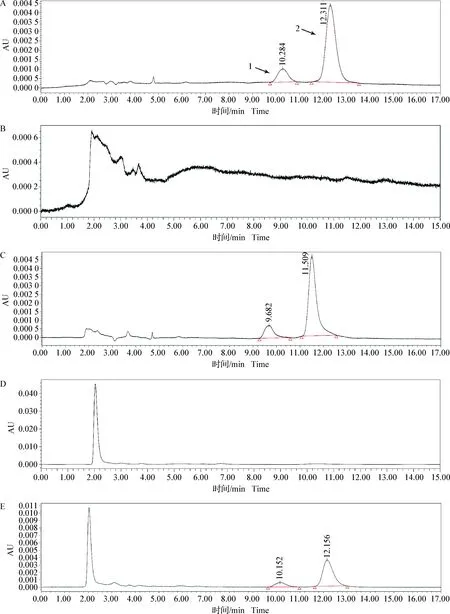
图1 猪部分组织中替米考星检测的色谱图Fig.1 Chromatograms of tilmicosin in swine tissues1:替米考星反式异构体色谱峰; 2:替米考星顺式异构体色谱峰; A:替米考星标准品色谱图(0.5 μg/mL); B:空白肌肉色谱图; C:添加肌肉样品色谱图(0.5 μg/g); D:空白肝脏色谱图; E:添加肝脏样品色谱图(0.5 μg/g)1:Chromatogram of tilmicosin transisomer; 2:Chromatogram of tilmicosin cisisomer; A:Chromatograms of tilmicosin standard (0.5 μg/mL); B:Chromatograms of blank muscle; C:Chromatograms of fortified muscle (0.5 μg/g); D:Chromatograms of blank liver; E:Chromatograms of fortified liver (0.5 μg/g)

表1 猪组织中的添加回收率和相对标准偏差Table 1 Recovery and RSD of tilmicosin in swine tissues
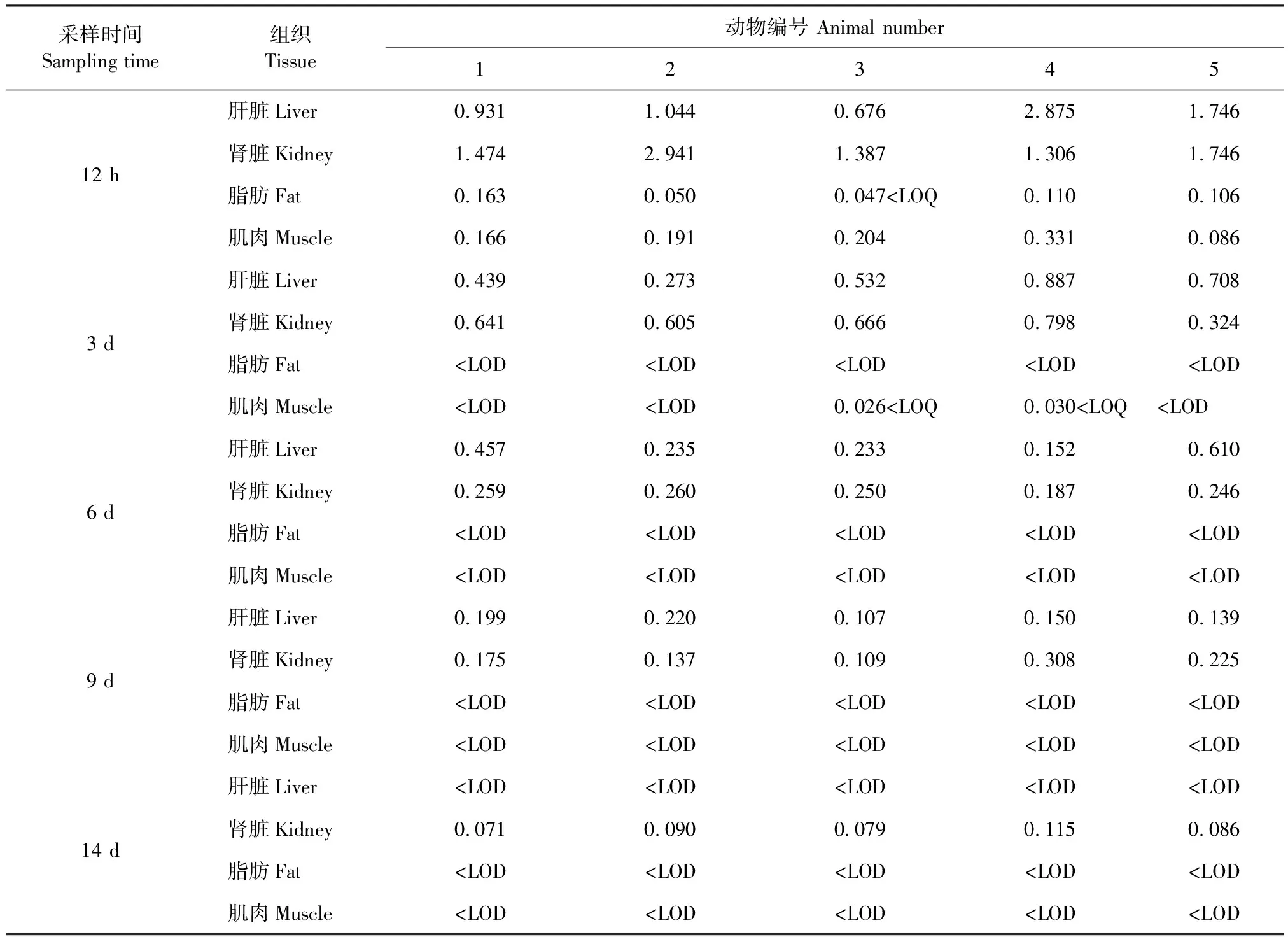
表2 停药后猪各可食性组织中替米考星的残留量Table 2 Residues of tilmicosin in edible tissues of swine after drug withdrawal (mg/kg)
残留消除试验显示,对替米考星肠溶颗粒混饲给药停药后在猪不同组织残留量进行比较,虽然同一采样时间点替米考星在不同组织没有统一的残留规律,但是其在肌肉和脂肪组织残留量较低,在肝脏和肾脏的残留量最高,这与刘彩等[6]的研究结果一致。而且肝脏和肾脏的药物残留量远高于皮脂和肌肉的残留量,消除时间分别在9 d和14 d以上,表明肝脏和肾脏为替米考星在猪体内的残留靶器官。食品中兽药最高残留限量标准中规定替米考星在猪皮脂、肌肉、肝脏、肾脏中的MRL分别为0.1、0.1、1.5 μg/g和1.0 μg/g。替米考星肠溶颗粒混饲连用15 d后,在停药后的第3天替米考星在以上组织中的残留量均低于国家最高残留限量,说明替米考星肠溶颗粒在猪体内代谢较快,且没有组织蓄积情况。
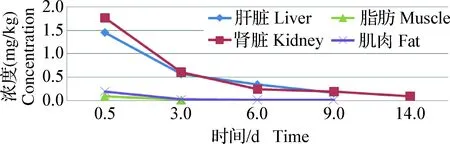
图2 替米考星肠溶颗粒混饲给药停药后替米考星在 猪组织中的残留消除曲线Fig.2 Residues eliminate curve of tilmicosin in swine tissues after the withdrawal of enteric-coated tilmicosin pellets

图3 按双单侧95%置信区间拟合休药期曲线图(肝脏)Fig.3 Plot of withdrawal time calculation for liver at the time when the one-sided 95% upper tolerance limit was below the MRL
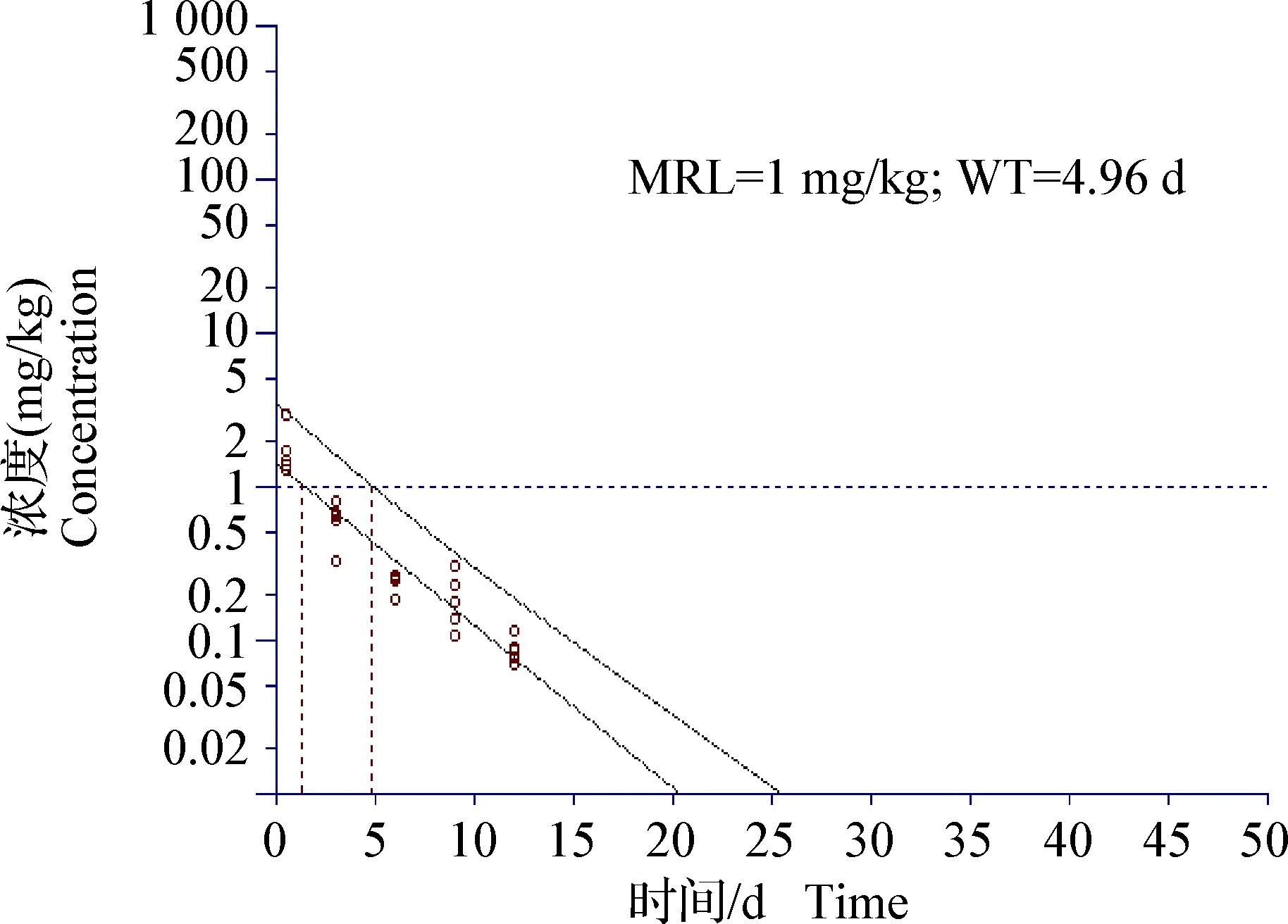
图4 按双单侧95%置信区间拟合休药期曲线图(肾脏)Fig.4 Plot of withdrawal time calculation for kidney at the time when the one-sided 95% upper tolerance limit was below the MRL
休药期(WDT)指食品动物从停止给药到许可屠宰或其产品(蛋、奶)许可上市之间的间隔时间。休药期的制定原则是药物或其他外源性化学物质必须从体内排出,或降至人在食用其组织或产品后不会危害人体健康的程度。本试验根据休药期计算软件和实测药物浓度得出皮脂、肌肉、肝脏、肾脏分别为3、3、6.17 d和4.96 d,这与国家药典规定的替米考星休药期14 d明显缩短,笔者认为这主要由替米考星肠溶颗粒剂不同生产工艺和试验动物个体差异造成。参照国家规定的替米考星最高残留量要求,建议替米考星肠溶颗粒按推荐给药剂量上限混饲给药时,在猪的休药期定为7 d。
