沙利度胺减轻肿瘤患者伊立替康化疗毒性及改善生活质量的临床效果分析
2022-01-04徐涛陈飞
徐涛 陈飞
1长沙市卫生职业学院 410199;2湖南省岳阳市中医医院肿瘤一科 414000
由于环境问题日益严重,人们生活方式、饮食结构不断发生变化及承受的工作、生活压力日益增大,肿瘤发病率呈现出不断攀升的态势,肺癌、胃癌及肝癌等位居前列[1]。手术治疗能够通过切除病灶的方式控制病情进展、抑制病情扩散,配合化学疗法及放射治疗能够进一步提升病情控制效果,延长患者生存周期。伊立替康在肺癌、结直肠癌等肿瘤治疗中应用广泛,但是患者用药后不良反应发生率较高,不但会对药物疗效造成影响,还会损害患者体质状况,影响其生活质量,因此,为了保证临床疗效及治疗安全性有必要为患者提供针对性的防控措施和手段[2-3]。作为非巴比妥类镇静药物,沙利度胺具有较好的抗肿瘤效应及较强的镇静作用,无宿醉效应,能够使恶心、失眠等症状得到有效缓解,除此之外,该药物还具有退热止痛、免疫调节、抗血管生成以及抗恶病质等功效[4-5]。本研究选取肿瘤患者58 例作为研究对象,患者自2017年4月至2020年10月在岳阳市中医医院进行化疗,本研究采用分组对照的方式对比和分析患者应用沙利度胺对减轻伊立替康化疗毒性以及改善患者生活质量所发挥的作用,分析如下。
1 资料与方法
1.1 一般资料 选取2017 年4 月至2020 年10 月在岳阳市中医医院进行治疗的肿瘤患者58 例,采用随机数字表法分为观察组与对照组,各29 例。观察组男17 例、女12 例,年龄37~84(59.56±3.21)岁,肿瘤类型:肝癌5 例、乳腺癌5 例、结肠癌5 例、肺癌8 例、其他6 例。对照组男16例、女13例,年龄34~82(60.21±3.15)岁,肿瘤类型:肝癌5 例、乳腺癌6 例、结肠癌4 例、肺癌7 例、其他7 例。所选患者意识清晰、知晓此次研究目的并自愿签署认知同意书。纳入标准:(1)经组织病理学确诊为肿瘤;(2)入组患者预计生存周期不短于3 个月;(3)所选患者无化疗禁忌。排除标准:(1)有凝血功能障碍或者近期有出血倾向者;(2)合并红细胞增多症及高脂血症等患者;(3)近期(入组前1 个月)服用过阿司匹林、抗血纤溶芳酸及蛇毒类止血药物的患者;(4)合并红细胞增多症或者高脂血症等血液疾病患者;(5)依照患者血象及肝肾功能提示无法耐受化疗者;(6)有药物滥用史或者乙醇滥用史者。两组肿瘤患者一般资料比较,差异均无统计学意义(均P>0.05),具有可比性。本研究经岳阳市中医医院医学伦理委员会批准。
1.2 方法 所有患者均接受伊立替康(江苏恒瑞医药股份有限公司,国药准字H20020687,规格40 mg)治疗,化疗前为所有患者实施血常规及肝肾功能等检查并进行体表面积计算,为所有患者实施基础治疗,若治疗过程中出现腹泻等不良反应时,需要及时依照说明书为患者提供对症治疗,若治疗过程中患者出现骨髓抑制等不良反应时应为其实施重组人粒细胞刺激因子、重组人白细胞介素11 等治疗。观察组患者在上述治疗基础上联合应用沙利度胺(常州制药厂有限公司,国药准字H32026130,规格50 mg)治疗,每晚睡前顿服沙利度胺100 mg,1次/d,每日服用1次,观察患者用药后反应情况,若没有明显不良反应可适当增加用药剂量,增加频率为100 mg/次,每间隔1 周增加1 次,最大用药剂量不可超过300 mg/d。治疗过程中必须密切观察患者用药后反应情况,若出现不良反应应适当减少应用剂量或者维持原剂量。每个疗程持续2~3 个月,连续治疗1个疗程。治疗期间每周进行血常规复查并进行X线、心电图及肝肾功能检查。
1.3 观察指标 (1)参考世界卫生组织(WHO)制定的化疗药物毒性反应分度标准评估化疗药物毒性反应情况,0度:没有毒性反应;Ⅰ度:有轻微毒性反应;Ⅱ度:有较为严重毒性反应;Ⅲ度:有严重毒性反应;Ⅳ度:有非常严重毒性反应。对比治疗后两组不良反应发生情况,主要包括胃肠道反应(便秘、腹泻、恶心、呕吐等)、骨髓抑制反应(贫血、白细胞减少、血小板减少等)、肝肾功能损害以及睡眠障碍、神经毒性、脱发等。(2)参考实体瘤疗效评价标准(由WHO 制定)对患者病情改善情况进行评估,参考如下标准进行评估。完全缓解(CR):肿瘤活性消失,患者病情完全得到控制;部分缓解(PR):与治疗前相比,肿瘤体积明显缩小(缩小幅度≥50%)、靶病区范围缩小(缩小幅度≥30%);稳定(SD):肿瘤体积缩小(缩小幅度≥25%~<50%),靶病区范围缩小(缩小幅度≥20%~<30%)或者靶病区范围扩大(<20%);进展(PD):检出新增病灶或者靶病区范围扩大(≥20%)。临床控制率=(CR 例数+PR 例数+SD 例数)/总例数×100%,临床总有效率=(CR 例数+PR 例数)/总例数×100%。(3)疗程结束后应用生活质量测评量表(QLQ-C30)对两组患者生活质量进行评估,主要评估项目包括社会功能、认知功能、情绪功能、角色功能及躯体功能,各维度评分范围为0~100分,评分越高则表明患者问题或者症状越多,生活质量越差。
1.4 统计学分析 以SPSS 23.0软件进行数据分析,计数资料采用[例(%)]表示,行χ2检验,符合正态分布的计量资料采用均数±标准差(±s)表示,组间行独立样本t检验,以P<0.05为差异有统计学意义。
2 结 果
2.1 不良反应 观察组胃肠道反应、骨髓抑制反应等不良反应程度均明显轻于对照组,差异均有统计学意义(P<0.05)。见表1。
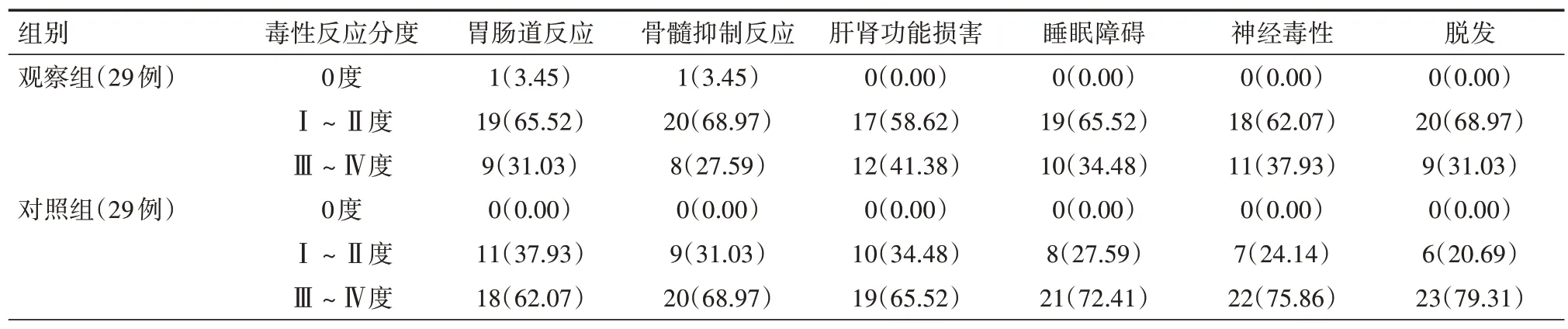
表1 两组肿瘤患者治疗后不良反应发生情况比较[例(%)]
2.2 临床疗效 观察组临床控制率及治疗总有效率分别为75.86%(22/29)、55.17%(16/29),均高于对照组48.28%(14/29)、24.14%(7/29),差异均有统计学意义(均P<0.05)。见表2。

表2 两组肿瘤患者临床疗效比较[例(%)]
2.3 生活质量 治疗前,两组肿瘤患者社会功能、认知功能、情绪功能、角色功能及躯体功能评分比较,差异均无统计学意义(均P>0.05);治疗后,观察组社会功能、认知功能、情绪功能、角色功能及躯体功能评分均低于对照组,差异均有统计学意义(均P<0.05)。见表3。
表3 两组肿瘤患者生活质量比较(分,±s)

表3 两组肿瘤患者生活质量比较(分,±s)
注:对照组接受伊立替康治疗,观察组患者在对照组治疗基础上联合应用沙利度胺进行治疗
3 讨 论
作为半合成水溶性喜树生物碱衍生物,伊立替康为DNA 拓扑异构酶抑制剂,进入人体后主要代谢产物为SN38,在卵巢癌、宫颈癌、肺癌及直肠癌等治疗中均有着广泛的应用,但是药物进入人体后容易引发不良反应,不但限制其临床应用,同时也会影响患者生存质量[6-7]。动物实验表明伊立替康在大鼠体内经羧酸酯酶作用后可转化为SN38,与伊立替康相比,SN38 对DNA 拓扑异构酶Ⅰ的抑制作用明显更强,对肿瘤病灶的破坏性更大,对肿瘤增殖细胞毒性作用更强[8-9]。有研究表明,SN38及伊立替康可同时对DNA 单链结构产生损伤作用,可对DNA 复制过程产生阻断有效作用,在胃癌、直肠癌、结肠癌等多种肿瘤疾病治疗中均有着广泛的应用[10]。
沙利度胺为人工合成谷氨酸衍生物,具有较好的抗炎、镇痛等效果,同时还能够发挥抗血管生成作用、免疫调节、抑制肿瘤作用以及改善睡眠等作用[11-12]。杀毒、抗肿瘤效果理想,可对肿瘤血管生成发挥抑制作用,能够有效抑制细胞表面黏附分子表达及肿瘤坏死因子-α(TNF-α),此外,沙利度胺还能够促进肿瘤患者恶病质状态改善,联合化疗对于提升患者生活质量可发挥非常重要的作用[13-14]。
此次研究中,两组对比,观察组胃肠道反应、骨髓抑制反应等不良反应程度均明显更轻,临床控制率及治疗总有效率均明显更高,社会功能、角色功能及躯体功能评分均更低,两组各项指标差异均有统计学意义(均P<0.05)。通过对比分析可知,接受伊立替康治疗的肿瘤患者联合应用沙利度胺有助于进一步减轻其不良反应,对于提高患者化疗耐受性、提升临床疗效以及改善患者生存质量均有重要意义。沙利度胺作用机制可能表现在以下方面:对胆汁分泌可产生抑制作用,有利于降低血浆中SN-8 与伊立替康浓度,从而可使肠毒性得到减轻;能够对肿瘤血管生成产生有效的抑制作用,具有协助抗肿瘤效用,有助于使患者自身抵抗力得到增强;能够保护胃肠道黏膜,进而可降低恶心呕吐等胃肠道反应发生率,有助于减轻患者不适感,可提高其化疗耐受度[15]。
综上所述,接受伊立替康治疗的肿瘤化疗患者应用沙利度胺能够有效减轻化疗期毒性反应,可提高安全系数,保证临床疗效并改善患者生存质量。
利益冲突:所有作者声明无利益冲突。
