miR-508-3p靶向AFF4/TGFβ1信号通路调控人牙髓细胞分化的机制研究*
2021-12-20杨正涛林方梁温利梅
杨正涛,林方梁,温利梅
(四川省自贡市第一人民医院,自贡 643000)
牙髓治疗普遍认可牙髓牙本质复合体的修复、再生,包括干细胞移植、细胞归巢、牙髓血运重建等技术[1]。虽然医疗水平不断进步,牙髓治疗的技术也得到了很大提升,但临床上仍存在很多问题。牙髓细胞具有很强的分化和再生牙本质牙髓复合体的能力,也是再生医学研究的重要对象。据报道,牙髓细胞分化的分子机制受碱性成纤维细胞生长因子(bFGF)、转化生长因子β(TGFβ)、神经生长因子(NGF)、血小板衍生生长因子(PDGF)和骨形态发生蛋白(BMP)等基因的调控[2]。微小RNA(miRNA)是一种非编码RNA,长度在18~25 个核苷酸,其通过识别靶基因,抑制靶基因mRNA 的翻译,从而在生物的发育、细胞增殖、凋亡、分化及肿瘤中发挥作用[3-4]。目前已发现,大量miRNA参与牙髓细胞的分化调控[5],其中包括新发现的miR-508-3p[6]。AF4/FMR2 家庭成员4(AFF4)是AF4/FMR2 家族的最末位成员。AFF1 和AFF4 都是重要的表观遗传调控因子,其在人骨髓间充质干细胞成骨分化过程中的作用不同,其中AFF4 在促进骨髓间充质干细胞成骨分化中起着关键作用[7]。本研究通过构建缺氧诱导的牙髓细胞模型,观察过表达miR-508-3p或敲减AFF4 对缺氧牙髓细胞分化的影响及相关机制。
1 材料与方法
1.1 主要试剂和仪器 DMEM 培养基、胎牛血清、胰蛋白酶均购自大连TaKaRa;pcDNA3.1(货号:HG-VPI0001)、pcDNA3.1-AFF4(货 号:GM-10405OP01)购自上海吉满生物科技有限公司;兔抗AFF4、DMP1、DSPP、OCN、ALP、TGFβ1、Smad、BMP抗体、辣根过氧化物酶标记的山羊抗兔二抗均购自上海艾博抗公司;荧光素酶报告基因试剂盒购自上海吉满生物公司;RNA 抽提试剂盒、RT-qPCR试剂盒、ECL均购自碧云天。半干转膜仪购自美国BIO-RAD公司,凝胶成像分析仪购自柯达公司。本试验所用所有引物、质粒、mimics-NC、miR-508-3p mimics、si-NC、si-AFF4 序列均由上海吉玛基因提供。
1.2 牙髓细胞的分离培养 收集2019 年2 月至2021年5月自贡市第一人民医院拔除的无病变健康前磨牙或第三磨牙。无菌条件下取出牙髓组织,PBS洗净,剪碎,用Ⅰ型胶原酶消化1 h。收集细胞,用20%胎牛血清的高糖DMEM 培养基置于37 ℃、5%CO2的培养箱中培养。待细胞贴壁后,隔2 d 换液1 次,0.25%胰酶消化传代。取第3~6 代的细胞用于实验研究。
1.3 缺氧牙髓细胞模型的建立与分组转染 用200 μmol/mL 的氯化钴(CoCl2)溶液处理牙髓细胞24 h,建立缺氧模型,记为实验组。用等量生理盐水处理的牙髓细胞为对照组。使用Lipofectamine®2000 脂质体将miR-NC 组(转染mimics-NC)、miR-508-3p组(转染miR-508-3p mimics)、si-NC组(转染si-NC)、si-AFF4 组(转染si-AFF4)、miR-508-3p+pcDNA 组(共转染miR-508-3p mimics 和pcDNA)、miR-508-3p+pcDNA-AFF4 组(共转染miR-508-3p mimics 和pcDNA-AFF4)转染至实验组牙髓细胞。转染48 h后,用RT-qPCR法检测转染效率。
1.4 RT-qPCR 实验 提取细胞总RNA,逆转录为cDNA,进行PCR 反应。miR-508-3p 内参为U6,AFF4、DMP1、DSPP、OCN、ALP 内参为GAPDH。用2-△△Ct法计算miR-508-3p、AFF4、DMP1、DSPP、OCN、ALP的表达。PCR反应条件:94 ℃变性2 min;94 ℃变性30 min;58 ℃退火30 s;72 ℃延伸2 min,共45 个循环。引物序列如下:miR-508-3p 上游:5’-ACACTCCAGCTGGGTACTCCAGAGGGCGTCACT-3’,下游:5’-TGGTGTCGTGGAGTCG-3’;DMP1 上游:5’-GTGAGTGAGTCCAGGGGAGATAA-3’,下游:5’-TTTTGAGTGGGAGAGTGTGTGCC-3’;DSPP 上游:5’-GGGACACAGGAAA-AGCAGAA-3’,下 游:5’-TGCTCCATTCCCACTAGGAC-3’;OCN 上游:5’-CTCACACTCCTCGCCCTATT-3’,下游:5’-TTGGACACAAAGGCTGCAC-3’;ALP上游:5’-CTATCCTGGCTCCGTGCTC-3’,下游:5’-GCTGGCAGTGGTCAGATGTT-3’;GAPDH上游:5’-GTTGTCTCCTGCGACTTCA-3’,下游:5’-GGTGGTCCAGGGTTTCTTA-3’;U6 上游:5’-GCTTCGGCAGCACATATACTAAAAT-3’,下游:5’-CGCTTC ACGAATTTGCGTGTCAT-3’。
1.5 Western blotting 实验 将细胞充分裂解,提取总蛋白,并进行定量、煮沸变性。SDS-PAGE 电泳,将蛋白转移至PVDF 膜,脱脂奶粉封闭,加入一抗AFF4(1∶1 000)、DMP1(1∶1 000)、DSPP(1∶500)、OCN(1∶1 000)、ALP(1∶1 000)、TGFβ1(1∶800)、Smad(1∶2 000)、BMP(1∶1 500)4 ℃孵育过夜;洗膜,加入山羊抗兔二抗溶液(1∶500)37 ℃孵育2 h,洗膜,ECL 显影、曝光。ImageJ 分析蛋白条带灰度值。以目的蛋白条带灰度值与内参GAPDH条带灰度值的比值作为目的蛋白相对表达量。
1.6 双荧光素酶报告基因实验 在线预测网站Starbase(http://starbase.sysu.edu.cn)预测到miR-508-3p 与AFF4 存在靶向关系。将AFF4 3’UTR WT、AFF4 3’UTR MUT分别与miR-NC、miR-508-3p、anti-miR-NC、anti-miR-508-3p 构建重组载体质粒,并共转染至293T 细胞。用双荧光素酶活性检测试剂盒测定细胞中萤火虫荧光素酶的荧光值与海肾荧光素酶的荧光值的比值。
1.7 统计学方法 用PEMS 3.2软件分析数据。计量资料以均数±标准差()表示,多组间比较采用方差分析,组间两两比较采用LSD-t检验,以P<0.05为差异具有统计学意义。
2 结果
2.1 miR-508-3p、AFF4 及牙髓分化指标在缺氧诱导牙髓细胞中的表达 与对照组相比,实验组细胞中miR-508-3p 的表达显著升高,AFF4、DMP1、DSPP、OCN、ALP 表达均显著降低(均P<0.01),见图1。
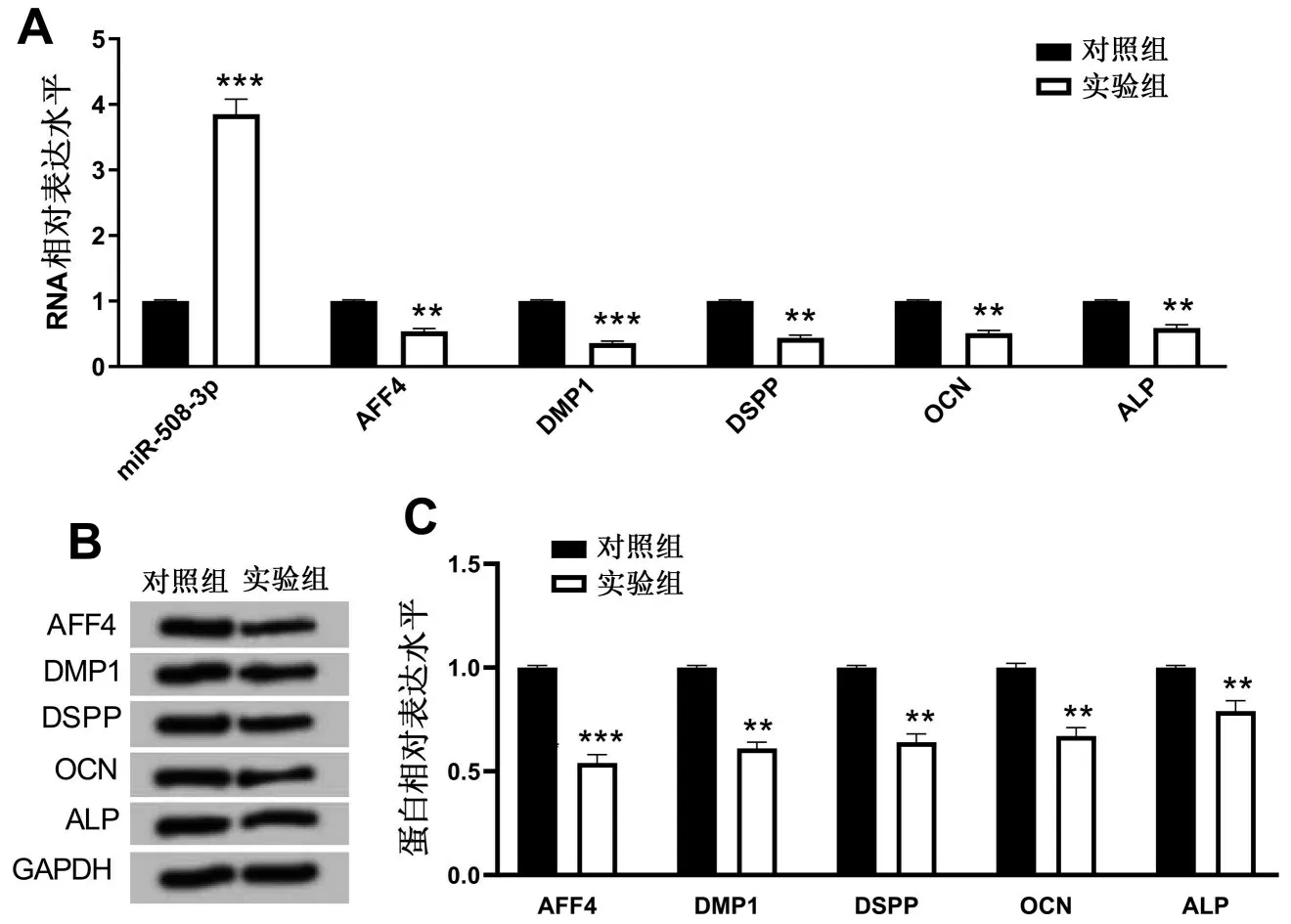
图1 miR-508-3p、AFF4及牙髓分化检测指标在缺氧诱导牙髓细胞中的表达
2.2 过表达miR-508-3p 或敲减AFF4 对缺氧诱导牙髓细胞分化的影响 与miR-NC 组相比,miR-508-3p组miR-508-3p表达显著升高,AFF4、DMP1、DSPP、OCN、ALP 的表达均显著降低(均P<0.01)。与si-NC 组相比,si-AFF4 组miR-508-3p 表达升高,AFF4、DMP1、DSPP、OCN、ALP 的表达均明显降低(均P<0.01),见图2。
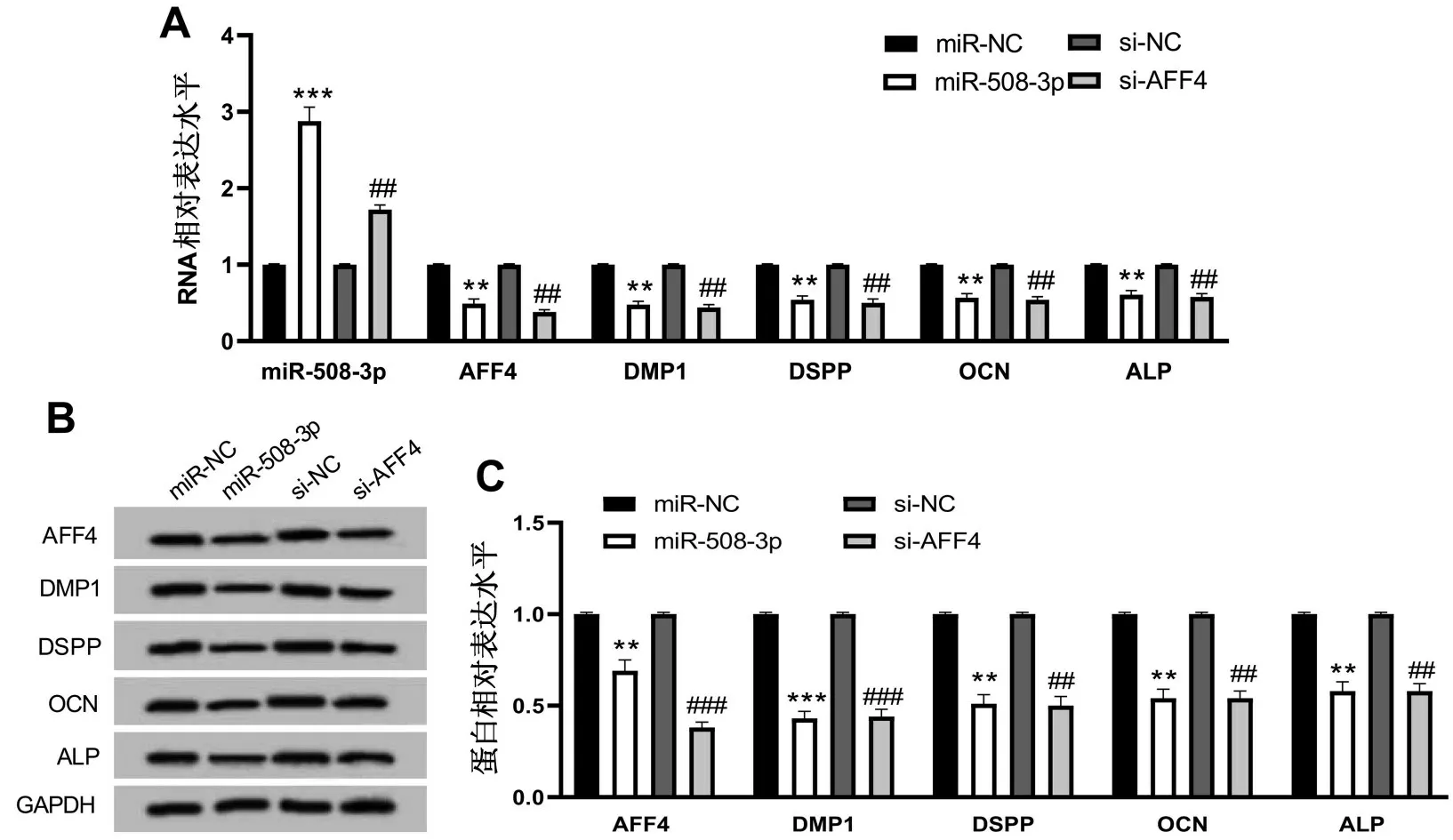
图2 过表达miR-508-3p或敲减AFF4对缺氧牙髓细胞分化的影响
2.3 miR-508-3p 靶 向AFF4 Starbase(http://starbase.sysu.edu.cn)预测到miR-508-3p与AFF4之间的互补碱基序列,见图3A。与miR-NC 组相比,miR-508-3p组AFF4 3’UTR WT细胞的荧光活性显著降低(P<0.01),而AFF4 3’UTR MUT 组细胞的荧光活性变化不明显,见图3B;与miR-NC组相比,miR-508-3p组AFF4 蛋白表达显著降低,与anti-miR-NC组相比,anti-miR-508-3p 组AFF4 蛋白表达显著升高(P<0.01),见图3C。
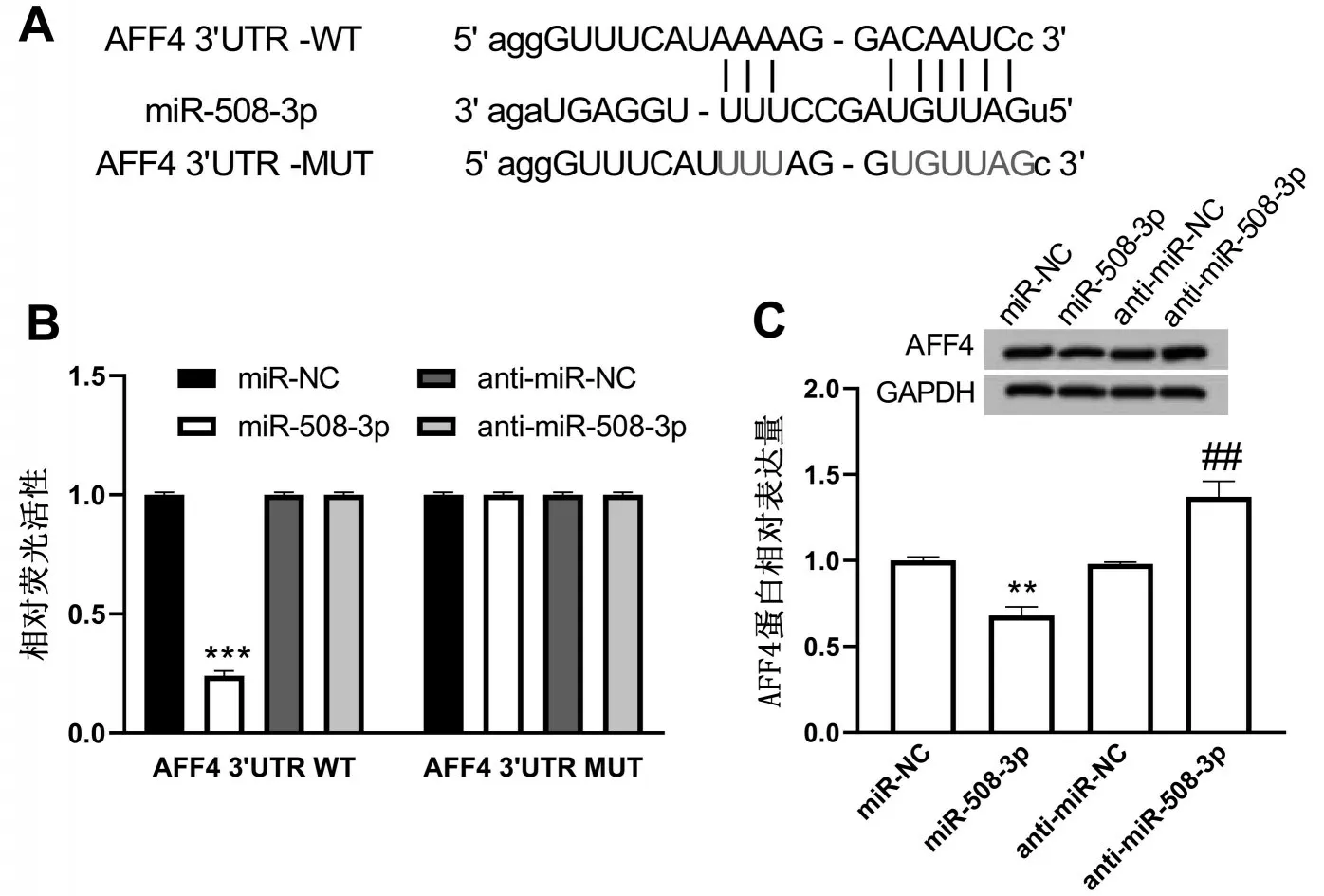
图3 miR-508-3p与AFF4的靶向关系
2.4 过表达AFF4 部分逆转过表达miR-508-3p 对缺氧诱导牙髓细胞分化的作用 与miR-508-3p+pcDNA 组相比,miR-508-3p+pcDNA-AFF4 组诱导牙髓细胞中miR-508-3p 表达显著降低,AFF4、DMP1、DSPP、OCN、ALP 的表达均明显升高(P<0.01),见图4。
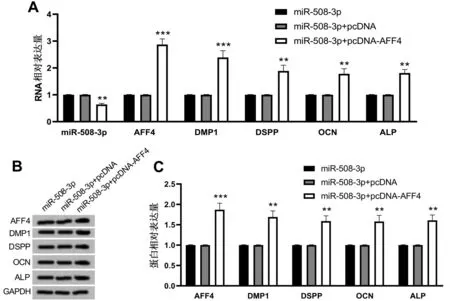
图4 过表达AFF4对miR-508-3p的抑制诱导牙髓细胞分化作用的调控
2.5 TGFβ1 信号通路在缺氧诱导牙髓细胞中受miR-508-3p、AFF4 调控 与miR-NC 组相比,miR-508-3p 组TGFβ1、Smad、BMP 蛋白表达均显著降低(P<0.01);与miR-508-3p+pcDNA 组相比,miR-508-3p+pcDNA-AFF4组TGFβ1、Smad、BMP蛋白表达均显著升高(P<0.01);与si-NC 组相比,si-AFF4组TGFβ1、Smad、BMP 蛋白表达均显著降低(P<0.01),见图5。
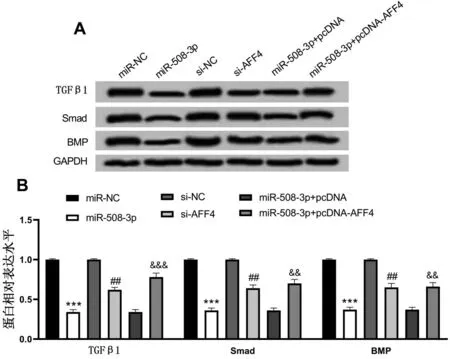
图5 TGFβ1信号通路关键蛋白TGFβ1的表达与miR-508-3p/AFF4的关系
3 讨论
牙髓细胞分化所处的环境含氧量虽然远远低于正常细胞培养的含氧量,但是若牙髓细胞长期受到炎症、外伤、牙菌斑侵蚀等,容易诱发牙髓组织的缺血缺氧[8-9]。袁晓琴等[10]在研究中使用化学法诱导牙髓细胞缺氧,模拟牙髓的缺氧环境,在此基础上发现,miR-210-3p参与牙髓在缺氧环境中的促增殖分化作用。因此,本研究建立了缺氧环境中的牙髓细胞模型,用于探究miR-508-5p、AFF4 在其中的功能及机制。
miRNA参与人类的多种疾病的发病过程,其中包括牙髓疾病[11]。Liu等[12]研究报道,miR-508-5p在牙周发育的过程中表达逐渐降低,过表达miR-508-5p 后,牙髓细胞的分化能力显著降低,miR-508-5p的这种抑制牙髓细胞分化功能可被非转移性黑色素瘤糖蛋白B(GPNMB)逆转,揭示miR-508-5p 通过靶向GPNMB 发挥抑制牙髓细胞分化的调节机制。于是,猜测miR-508-3p可能参与调控缺氧条件下牙髓细胞的分化过程。本研究检测了缺氧牙髓细胞中miR-508-5p 的表达发现,其明显升高,再次确定了miR-508-5p 在牙髓细胞分化中的抑制作用。本实验对miR-508-5p 过表达后的缺氧牙髓细胞进行检测,检测其中牙髓分化相关基因DMP1、DSPP、OCN、ALP 的表达发现,其可抑制牙髓分化的上述基因表达,这些结果与Liu 等[12]的实验结果相一致。通过荧光素酶实验进行深入探究发现,miR-508-5p可与靶向负调节AFF4的表达水平。推测这种靶向关系可能与miR-508-5p 的牙髓分化调节有关。这些实验结果揭示了miR-508-5p 在缺氧牙髓细胞中显著升高,发挥抑制牙髓细胞分化功能,这种抑制功能与靶向AFF4紧密相关。
近期,AFF4 在人类疾病发生发展中的调控功能的研究越来越多[13]。最近Xiao等[14]发现,AFF4参与牙囊细胞的成骨分化过程,敲减AFF4 能够下调成骨相关基因远端同源框5、核心结合因子a1 和骨γ-羧谷氨酸蛋白的表达,而慢病毒介导的AFF4过表达则具有相反的作用,并显著增强牙囊细胞的成骨能力,这种调控作用与AFF4上调ALKB同源蛋白1具有直接关系。Zhang 等[15]报道,慢病毒介导的AFF4 过表达能够促进牙髓细胞的成牙分化,而AFF4缺失则可抑制牙髓细胞分化,并且AFF4的这种功能与牙根形成关键因素核因子ⅠC相关。本研究发现,AFF4 在缺氧牙髓细胞中表达下调,敲减AFF4 可抑制牙髓分化相关基因DMP1、DSPP、OCN、ALP的表达,并且过表达AFF4还可逆转过表达miR-508-3p对DMP1、DSPP、OCN、ALP表达的下调作用。这说明了AFF4可逆转miR-508-5p对牙髓细胞分化的抑制作用。
大量研究报道,TGFβ1信号通路参与牙髓细胞损伤过程[16]。为了探究该通路是否受miR-508-3p、AFF4 的影响,本实验检测了TGFβ1 信号通路关键基因TGFβ1、Smad、BMP 的表达情况,结果显示,miR-508-5p 可抑制缺氧诱导的牙髓细胞中TGFβ1、Smad、BMP的表达,敲减AFF4也具有相似的功能,而过表达AFF4可逆转过表达miR-508-3p对TGFβ1、Smad、BMP 的抑制作用。这些实验结果展示了TGFβ1 信号通路的活性在缺氧牙髓细胞中受miR-508-3p 的抑制、AFF4 的 促进,揭示miR-508-5p/AFF4/TGFβ1信号通路在牙髓细胞分化中的调控机制。
综上所述,miR-508-5p 可抑制缺氧诱导的牙髓细胞分化,产生这种作用的机制与miR-508-5p靶向AFF4,抑制TGFβ1 信号通路活性有关,本研究结果可为牙髓再生提供理论参考。
猜你喜欢
杂志排行
广西医科大学学报的其它文章
- 基于Klotho/FGF23通路探讨天麻钩藤饮对大鼠静脉桥血管氧化应激及内膜增生的影响*
- 腹壁剖宫产瘢痕子宫内膜异位症恶变为透明细胞癌1例*
- 急性心肌梗死与2型糖尿病相关差异基因的GEO芯片分析*
- Effect of curcumin on palmitic acid-induced apoptosis and steroid production of ovarian granulosa cells by inhibiting HMGB1-mediated autophagy
- 白藜芦醇对人甲状腺乳头状癌细胞IHH4细胞恶性生物学特征及PI3K/Akt信号通路影响*
- 金丝桃苷对糖尿病肾病大鼠TGF-β1/smad通路及肾上皮间质转化的影响*
