拜耳法低铁赤泥制备硅钾肥工艺及硅钾活化机理研究
2021-12-17田江南郑诗礼吴应红
罗 扬,田江南,丁 健,,郑诗礼,吴应红
(1.香港大学土木工程系,香港,999077;2.香港生产力促进局,香港,999077;3.中国电力工程顾问集团华北电力设计院有限公司,北京,100120;4.中国科学院过程工程研究所,北京,100190;5.香港大学机械工程系,香港,999077)
'
赤泥是铝土矿生产氧化铝过程中所产生的固体废渣,目前,我国的赤泥年产生量已超过1亿吨,累积堆存量超过6亿吨,属于大宗工业固废[1],且其中大部分为拜耳法赤泥,该类赤泥浸出液pH值通常高达12~13,呈强碱性,主要以露天筑坝方式大量堆存,已对周边土壤、地表和地下水源造成严重污染[2-3]。对赤泥进行资源化利用是解决其污染问题的主要途径,但因赤泥碱含量高,造成实际利用困难,其综合利用率不足5%[4]。已有的诸多拜耳法赤泥综合利用方法主要是先对赤泥进行改性处理,充分利用并回收其中的有价金属等高附加值部分,再将改性赤泥经无害化处置后应用于建材领域,达到大规模消纳赤泥的目的。此外,为便于与现有的拜耳法溶出工艺衔接及控制能耗,在处理中尽量避免采用酸法或烧结法。但即便采取上述措施,依然没有从根本上解决赤泥大量堆存的问题,因此急需寻找新的赤泥利用途径。本课题组认为,针对赤泥的综合利用,除了考虑以上认知外,还应基于以下4个原则:一是吃渣量大;二是不能产生二次污染;三是工艺不能过于复杂;四是应具备可预计的产业化发展方向和政策保障。
众所周知,植物的正常生长发育离不开碳、氢、氧、氮、磷、钾等6种必须的大量元素,同时也需要硫、镁、钙、硅等中量元素以及铁、锰、钼、铜、硼、锌、氯、钠、钴、镍、钒等微量元素,尤其硅元素对植物生长的重要性被认为仅次于氮、磷、钾等3种元素。上述元素除碳、氢、氧等3种非矿物质元素外,其它元素均需植物从土壤中吸收[5],然而近30多年以来,由于我国农业生产大量甚至过量投入氮磷钾类化肥,忽视了对中、微量元素养分的系统补给,导致土壤中营养元素比例失衡,农产品产量和品质受到影响[6]。农业部全国农业技术推广中心2014年估测的数据显示,我国土壤中钙、镁、硫、铁、锰、铜、锌、硼、钼等中、微量元素含量在临界值以下的耕地面积分别达到总耕地面积的63%、53%、40%、31%、48%、25%、42%、84%、59%[7]。由此可见,中、微量元素缺乏已成为制约我国农作物产量和品质提高的主要因素,不过,随着化肥使用量“零增长”规划[8-9]的逐步实施,长期作为“配角”而被忽视的中、微量元素肥料将迎来重大发展机遇,而赤泥中含有大量植物生长所需的钾、硅、钙、铁、镁等多种元素,完全具备合成无机肥料的基本条件,这为赤泥的综合利用提供了新的思路。不过,由赤泥到无机肥料的转化面临两个主要问题:一是需要深度脱除赤泥中高含量的有毒元素钠;二是需要同步活化赤泥中的有益元素。故本文基于全组分利用和减量化的理念,在分析典型拜耳法赤泥主要物性的基础上,针对赤泥强碱性的特点,提出了低铁赤泥KOH水热脱钠制备无机硅钾肥的综合利用技术路线,开发了低铁赤泥KOH水热工艺并分析了KOH水热过程物相转化规律及赤泥中硅、钾等有益元素的活化机理,以期为赤泥在农业生产中的应用提供参考。
1 实验
1.1 原料
实验所用拜耳法低铁赤泥(以下简称赤泥)取自中铝河南铝业有限责任公司,经粉碎、100目筛分后,置于80 ℃烘箱内烘干备用。
1.2 水热反应
配制体积均为500 mL、浓度不同的KOH溶液若干组,分别与赤泥混合配制料浆,通过水热反应脱去赤泥中的有害钠元素并活化硅、钾等有益元素。考虑到液相与固相按低液固比(V(液)/m(固),mL/g)混合虽然可以有效地提高设备利用率和生产效率,但在实际生产中液固比过低会对物料输送和液固分离环节造成压力,故设定液固比为5,即每组KOH溶液与100 g赤泥混合。将装有混合料浆的反应罐置于高压反应釜内,拧紧密封后设置不同的反应温度及反应时间,反应釜搅拌桨的转速设定为450 r/min以消除反应中外扩散的影响。待混合料浆在一定温度下反应一段时间后,先通入冷却水降低釜内压力至常压,再开釜取出反应产物,借助真空抽滤对该产物进行液固分离,其中固相即脱钠赤泥样品经60 ℃去离子水浆洗2次后置于80 ℃烘箱内烘干备用。
1.3 样品的测试
采用JSM-7100F型扫描电镜(SEM)观察赤泥原料的显微组织;利用Perkin Elmer公司Optima 5300DV型电感耦合等离子体发射光谱仪(ICP-OES)测试赤泥原料及脱钠赤泥样品的元素含量,在进行ICP-OES测试前,赤泥原料及脱钠赤泥等固相样品需经过微波消解预处理,具体操作步骤为:称取0. 100 g样品置于聚四氟乙烯(PTFE)消解罐中,加入6 mL硝酸、2 mL盐酸及2 mL氢氟酸,在微波功率为800 W、升温速度为10 ℃/min的条件下,分别于150 ℃保温10 min、180 ℃保温5 min、210 ℃保温25 min,再自然冷却至室温,经充分赶酸后转移至100 mL容量瓶定容。借助X’Pert PRO MPD型X射线衍射仪(XRD)分析相关样品的物相结构。在肥料领域,有效硅、有效钾是指那些能被农作物吸收利用的可溶性硅和钾,赤泥样品中有效硅和有效钾含量的测定参照NY/T 2272-2012《土壤调理剂-钙、镁、硅含量的测定》[10-11]、NY/T 2273-2012《土壤调理剂-磷、钾含量的测定》及NY/T 2540-2014《肥料-钾含量的测定》[12],具体操作步骤为:称取0.500~4.000 g样品置于250 mL容量瓶中,加入150 mL浓度为0.5 mol/L、温度为28~30 ℃的稀盐酸溶液,瓶塞密封后摇动容量瓶使样品均匀分散于溶液中,之后将容量瓶置于28~30 ℃的恒温振荡器中,设定振荡频率保证样品能在容量瓶内自由翻动即可,振荡30 min后取出容量瓶冷却至室温,向其中加水稀释至刻度,混匀并干过滤,弃除初始滤液,对剩余滤液进行ICP-OES测试以确定其中的硅、钾含量。
2 结果与分析
2.1 赤泥原料的测试结果
经ICP-OES测试,赤泥原料的主要化学成分见表1,其XRD及SEM表征结果如图1所示。从图1(a)XRD分析结果可见,赤泥主要物相为方钠石Na8Al6Si6O24(OH)2.04·2.66H2O和钙铝榴石Ca2.93Al1.97(Si0.64O2.56)(OH)9.44,其微观组织呈大小不一的薄片状(图1(b))。
2.2 水热反应参数对赤泥成分的影响
2.2.1 反应时间
当KOH溶液浓度为5 mol/L、反应温度为200 ℃、反应时间分别为1、2、4、6 h时,赤泥中氧化钠、氧化钾、有效硅(SiO2)、有效钾(K2O)含量的变化及相应样品的XRD测试结果分别见图2和图3。由图2(a)可以看出,当反应时间为1 h时,赤泥渣相中的氧化钠含量由发生水热反应前的11.36%降至0.5%左右,降幅明显。当反应时间介于1~6 h时,赤泥渣相中的氧化钠含量变化波动不大,基本保持稳定,而氧化钾含量则持续增加,表明在此期间赤泥中不断有含钾物相生成,同时,氧化钠和氧化钾含量变化趋势的差异也表明,在本研究液固比条件下,含钠物相方钠石的分解和含钾物相的生成并不是同步发生的,在反应前期,含钠物相方钠石已基本完成分解,所以延长反应时间对氧化钠含量变化影响不大,而液相主体中的钾则通过与其它元素结合,在反应过程中持续析出新的含钾固相。从图2(b)中可以看出,反应后赤泥渣相中有效硅和有效钾含量均随反应时间的延长而不断增加,有效硅和有效钾含量变化趋势一致,表明二者有可能存在于同一物相中。由图3所示的样品XRD谱图可知,当反应时间为1 h时,反应后赤泥渣相主要由钙铝榴石和氧化铁组成,样品XRD谱图中的最强衍射峰出现在2θ为32.313°处,属于钙铝榴石的特征衍射峰(标准PDF卡片 077-1773),表明此时赤泥渣相中主要物相为钙铝榴石;当反应时间延长至2 h时,反应后渣相中除钙铝榴石和氧化铁外,在2θ为20.737°、34.618°处新出现了钾沸石(KAlSiO4)的特征衍射峰(标准PDF卡片 012-0134),同时在2θ为28.8°附近的衍射峰成为样品XRD谱图中的最强衍射峰,这是因为在2θ为28. 776°处还存KAlSiO4的特征衍射峰,该峰与钙铝榴石在2θ为28.823°处的特征衍射峰叠加导致该处衍射峰强度明显增大;当反应时间进一步延长至4 h和6 h时,赤泥渣相中的钙铝榴石和氧化铁依然存在,KAlSiO4特征衍射峰强度也进一步增大,这符合图2(a)中氧化钾含量随着反应时间延长而逐渐增加的趋势,表明反应时间越长,反应后赤泥渣相中KAlSiO4的含量越高。综上所述,虽然随着反应时间的延长,反应后赤泥渣相中有效硅和有效钾含量会不断增加,但仅需反应1~2 h,赤泥中的氧化钠含量即可降至0.5%左右,为了提高工艺设计中的生产效率,可设定KOH水热反应最佳反应时间为2 h。

(a)XRD

(a)Na2O与K2O含量变化

图3 不同反应时间条件下赤泥渣相的XRD谱图
2.2.2 反应温度
当KOH溶液浓度为5 mol/L、反应时间为2 h、反应温度分别为120、140、160、180、200 ℃时,赤泥中氧化钠、氧化钾、有效硅、有效钾含量的变化及相应样品的XRD测试结果分别见图4及图5。由图4(a)中氧化钠随反应温度的变化曲线可以看出,当反应温度为120℃ 时,发生水热反应后赤泥渣相中的氧化钠含量超过1%,但当反应温度升至140 ℃时,氧化钠含量迅速降至0.51%,当反应温度进一步升至200 ℃时,氧化钠含量降至0.31%,整体来说,当反应温度介于140~200 ℃时,氧化钠含量变化较平稳,整体呈减少趋势但降幅不大,这是因为赤泥中的含钠物相即方钠石相分解温度较低,在120 ℃左右已大量分解,当反应温度升至140 ℃及更高温度时,虽然能使该反应进行得更加彻底,但氧化钠含量变化幅度已趋于平缓;由图4(a)中氧化钾随反应温度的变化曲线可以看出,当反应温度从120 ℃升至160 ℃时,赤泥渣相中的氧化钾含量虽有小幅增加,但基本维持在2%左右,继续升高反应温度至180 ℃时,氧化钾含量达到4.97%,当反应温度进一步升至200 ℃时,氧化钾含量达到6.81%,这是因为赤泥中的含钾物相即KAlSiO4相生成温度较高,当反应温度超过160 ℃时才会有KAlSiO4相生成进入固相,此时氧化钾含量相比反应温度较低时的相应值增幅明显。从图4(b)中可以看出,随着反应温度的升高,赤泥渣相中有效硅和有效钾含量变化趋势一致,均先基本保持平稳而后迅速增加,增幅发生突变的温度节点也同为160 ℃。由图5所示的样品XRD谱图可知,当反应温度分别为120 ℃和140 ℃时,赤泥渣相样品的XRD谱图基本一致,其物相均由钙铝榴石和氧化铁组成;升高反应温度至180 ℃时,赤泥渣相中已出现KAlSiO4相;进一步升高反应温度至200℃后,反应后渣相中KAlSiO4相特征衍射峰进一步增强。综上所述,虽然反应温度介于140~160 ℃时,赤泥渣相中氧化钠含量已降至1%以下,但由于目标产物KAlSiO4相的生成温度在180 ℃左右,因此,可设定KOH水热反应最佳反应温度为180 ℃。

(a)Na2O与K2O含量变化

图5 不同反应温度条件下赤泥渣相的XRD谱图
2.2.3 KOH溶液浓度
当反应温度为180 ℃、反应时间为2 h、KOH溶液浓度分别为2、3、4、5 mol/L时,赤泥中氧化钠、氧化钾、有效硅、有效钾含量的变化及相应样品的XRD测试结果分别见图6及图7。由图6(a)可以看出,当KOH浓度为2 mol/L时,发生水热反应后赤泥渣相中氧化钠含量依然处于较高水平,为5.06%;当KOH浓度升高至3 mol/L时,氧化钠含量迅速降至0.5%左右;继续升高KOH浓度,氧化钠含量小幅降低,表明KOH浓度不低于3 mol/L即可实现赤泥基本脱钠的目标。与此同时,赤泥中氧化钾的含量则随KOH浓度的升高呈现出先明显增加而后基本保持稳定不变的趋势。从图6(b)中可以看出,随着KOH浓度的不断升高,赤泥渣相中有效硅和有效钾含量均呈现出先快速增加而后缓慢减少的变化趋势。由图7所示的样品XRD谱图可见,当KOH浓度为2 mol/L时,发生水热反应后赤泥渣相主要由方钠石Na8Al6Si6O24(OH)2.04·2.66H2O、钙铝榴石Ca2.93Al1.97(Si0.64O2.56)(OH)9.44、氧化铁和KAlSiO4等物相组成,结合图1(a)所示的XRD测试结果可知,赤泥原料中的主要物相如方钠石Na8Al6Si6O24(OH)2.04·2.66H2O等并未消失,这是此时赤泥中Na2O含量依然高达5.06%的根本原因。同时注意到,尽管KOH浓度较低,水热反应后的赤泥中仍出现了KAlSiO4相,表明该相的生成对碱浓度要求不高;当KOH浓度分别为3、4、5 mol/L时,发生水热反应后的赤泥物相均由钙铝榴石Ca2.93Al1.97(Si0.64O2.56)(OH)9.44、氧化铁和KAlSiO4组成,此时含钠物相方钠石Na8Al6Si6O24(OH)2.04·2.66H2O特征衍射峰已基本消失,这与赤泥渣相中的Na2O含量检测结果(图6(a))相吻合,表明当KOH浓度不低于3 mol/L时,赤泥中含钠物相方钠石经水热反应一定时间后即可发生较完全的分解。
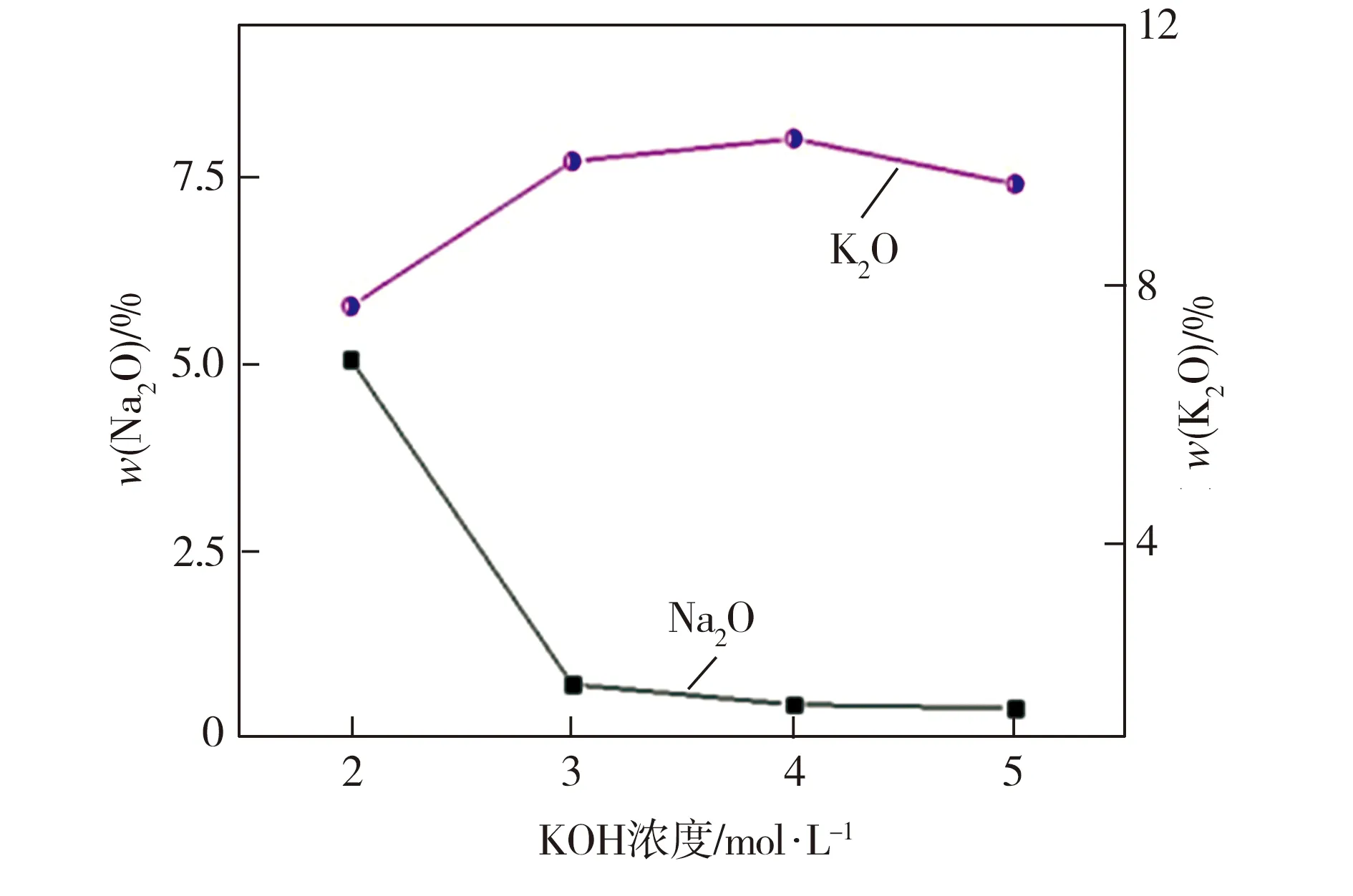
(a)Na2O与K2O含量变化

图7 不同KOH浓度条件下赤泥渣相的XRD谱图
基于上述水热反应参数对赤泥组成影响的分析,可以确定KOH水热处理低铁赤泥脱钠的最佳工艺参数为:反应时间2 h、反应温度180 ℃、KOH浓度3 mol/L。
2.3 KOH体系下硅、钾的活化机理
赤泥原料及在最佳KOH水热处理工艺条件下所得脱钠赤泥中的有效硅、有效钾含量见表2。由表2可见,赤泥原料中有效硅和有效钾占比分别为10.67%和0.58%,而经KOH水热处理后,赤泥中二者的相应值分别增至14.47%和7.91%,并且有效硅量占样品全硅量的比例RSi、有效钾量占样品全钾量的比例RK也分别由处理前的44.63%、31.02%相应增至50.38%、79.74%,二者占比的增幅差异明显,表明硅元素和钾元素的活化程度并不一致。

表2 样品中的有效硅和有效钾成分
经稀盐酸酸洗后的赤泥原料及在最佳KOH水热处理工艺条件下所得脱钠赤泥经稀盐酸酸洗前后的XRD分析结果见图8。由图8结合图1(a)可以看出,经酸洗处理后,赤泥原料的主要成分为二氧化硅和氧化铁,原有的方钠石、钙铝榴石、和CaCO3都已消失,表明在现有测试标准下,方钠石、钙铝榴石中的硅组分也被认为是可溶解并能被植物吸收的,因此赤泥原料中的有效硅含量测试值即达到10.97%,同时注意到赤泥原料经酸洗后所得样品XRD谱图中出现了很强的SiO2特征衍射峰,表明石英相是不能被溶解吸收的。至于脱钠赤泥样品,经酸洗处理后,其原有的钙铝榴石和KAlSiO4均已消失,这表明活化后赤泥中KAlSiO4相的生成是有效钾含量明显增加的原因,同时KAlSiO4也是有效钾组分的唯一来源。此外,对比赤泥原料、脱钠赤泥二者经酸洗后所得样品,在相同测试条件下,后者XRD谱图中石英SiO2特征衍射峰的主峰强度明显减弱,表明难溶的石英相含量有所降低,因此有效硅量占样品全硅量的比例由KOH水热处理前的44.63%增至50.38%。经分析总结,KOH水热处理赤泥时钾、硅的活化机理为:在水热处理过程中,有害的Na2O由赤泥原料转入溶液并发生分解,从而实现赤泥深度脱钠,新生成的KAlSiO4相中的硅、钾元素为完全活化的有效成分,同时,样品中部分石英相活化转型也生成KAlSiO4相,进一步提高了有效硅量在全硅量中的占比,期间发生的主要反应有

(1)

(2)

图8 酸洗前后样品的XRD谱图
3 结论
(1)采用KOH水热处理工艺,可以实现拜耳法低铁赤泥中有毒钠元素的深度脱除,且同步活化了其中的硅、钾等有益元素,将赤泥固废清洁转化为无机硅钾肥产品。
(2)KOH水热体系下脱钠工艺的最优参数为反应时间2 h、反应温度180 ℃、KOH浓度3 mol/L,在最优条件处理下,渣相中Na2O含量小于0.5%,有效硅含量为14.47%,有效钾含量为7.91%,分别占相应全硅及全钾量的50.38%和79.74%。
(3)在KOH水热过程中,主要是含钠物相方钠石分解转化为KAlSiO4,同时钠元素进入液相,而钙铝榴石不参与反应。
(4)钾沸石相的生成是有效钾含量提升的主要原因,同时水热处理过程中有部分石英相被活化,其由稳定的不可溶解形态转化为可吸收形态是有效硅含量提升的根本原因。
