肉芽肿性小叶性乳腺炎123例超声特征分析
2021-12-09常建东周瑞娟
林 韵, 林 云, 常建东, 周瑞娟
肉芽肿性小叶性乳腺炎(granulomatous lobular mastitis,GLM)是一种以女性乳腺终末导管小叶单元为中心的非干酪性的肉芽肿性炎性疾病,是临床乳腺外科较为少见的慢性炎症性疾病[1]。GLM由Kessler等[2]于1972年首先提出,约占乳腺良性疾病的1.80%[3]。近年来,GLM发病率呈逐年上升趋势[4],且多见于年轻女性,发病后患者会快速出现红肿、疼痛、脓肿、破溃等症状,乳房病损范围较大,常与皮肤及周围组织粘连,可并发窦道,病情凶险。若不及时治疗,难以彻底治愈,还可能并发关节疼痛、对侧乳房发病、下肢结节性红斑等症状。而且GLM易复发,复发率约为12%[5]。本研究通过回顾性分析2018年1月至2020年10月我院收治的123例GLM患者的病历资料,旨在探讨超声诊断GLM的临床应用价值。
1 资料与方法
1.1一般资料 收集2018年1月至2020年10月我院胸外乳腺科收治的123例GLM患者的病历资料,均为女性,年龄23~47(32.65±3.65)岁,肿块最长径9~90(43.22±2.35)mm,病程1~24(13.18±2.64)个月。合并下肢结节性红斑27例,关节疼痛11例,高泌乳素血症43例。
1.2纳入与排除标准 纳入标准:(1)术前或穿刺前在我院行常规超声检查;(2)经手术或粗针穿刺病理确诊为GLM。排除标准:(1)曾接受过GLM治疗的患者;(2)合并糖尿病、心脏病、肝肾功能衰竭患者;(3)合并精神障碍无法沟通者。
1.3方法
1.3.1 超声检查及分型方法 应用GE Logiq9型彩色多普勒超声仪进行检测,探头频率9.0~12.0 MHz。待患者准备就绪后由检测人员协助患者仰卧于检查床上,充分暴露乳房,探头涂抹耦合剂,先对患者乳房行全方位、多角度的常规超声检查,并记录患者病灶形态、大小、回声、钙化、周边回声有无增强等情况,以及有无累及皮肤、窦道,有无肿大淋巴结等信息。血流分级采用Alder分级法。其中:(1)结节型为病灶以低回声结节为主,边界清晰,形态不规则,部分结节内部伴有小无回声区。(2)团块型为病灶局限在一个象限,有连续的、边界不清的片状低回声,边界清晰,形态不规则,直径>3 cm,血流信号丰富。(3)脓肿型为病灶呈大片状无回声或混合回声,内见密集点状回声,周边回声增强,可见血流信号[6]。(4)窦道低回声区型为腺体内散在分布的多个不规则低回声区,常跨越多个象限存在,低回声区之间由窦道相通[7]。超声图像由2名具有5年以上工作经验医师进行分析诊断。
1.3.2 病理检查方法 病灶标本以中性甲醛进行固定,随之进行石蜡包埋切片,切片厚度为4~5 μm,使用苏木精-伊红(hematoxylin-eosin,HE)染色法进行染色,最后在光镜下观察病灶组织形态。
1.4统计学方法 应用SPSS26.0统计软件进行数据分析,计数资料以例数(百分率)[n(%)]表示,组间比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1123例患者超声检查结果 123例GLM患者中,经超声检查为结节型13例,团块型18例,脓肿型33例,窦道低回声区型59例。四种分型在病灶周边回声增强、血流信号丰富、窦道、腋下淋巴结肿大、累及皮肤超声表现上均有统计学差异(P<0.05)。其中结节型主要表现为血流信号丰富;团块型主要表现为血流信号丰富和腋下淋巴结肿大;脓肿型和窦道低回声区型均主要表现为周边回声增强、血流信号丰富和腋下淋巴结肿大。见表1。
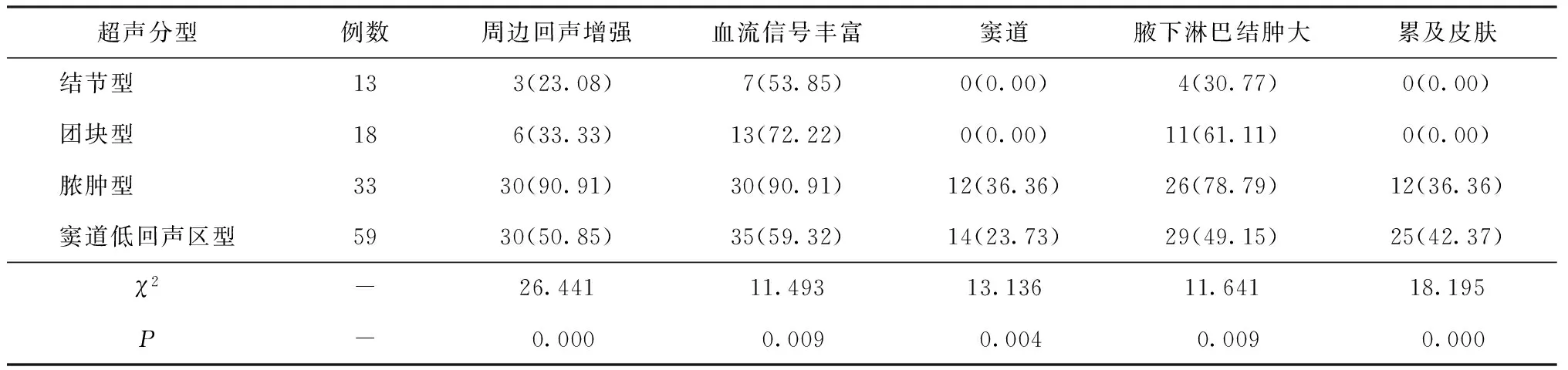
表1 不同分型GLM患者的超声表现[n(%)]
2.2不同分型GLM患者的典型超声表现及病理结果
2.2.1 结节型GLM患者的典型超声表现及病理结果 患者左乳见大小约26 mm×11 mm的低回声结节,形态欠规则,边界清,内部回声欠均匀(图1ⓐ)。彩色多普勒血流图(color Doppler flow imaging,CDFI)显示左乳结节内可见点状血流信号(图1ⓑ)。病理检查见肉芽肿周围类上皮样细胞增生包绕,周围多量淋巴细胞、少量浆细胞及中性粒泡浸润,并见少量多核巨细胞聚集(图1ⓒ;HE染色,×40)。
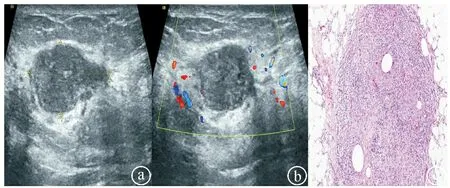
图1 结节型GLM患者的典型超声表现及病理结果图
2.2.2 团块型GLM患者的典型超声表现及病理结果 患者左乳见范围约47 mm×18 mm的低回声区,形态不规则,边界清,内部回声欠均匀(图2ⓐ)。CDFI显示左乳低回声区内见较丰富条状血流信号(图2ⓑ)。病理检查见肉芽肿结节形成小叶结构,结节中央见脂质空泡形成,周围多量淋巴细胞及少量中性粒细胞及浆细胞浸润(图2ⓒ;HE染色,×100)。
2.2.3 脓肿型GLM患者的典型超声表现及病理结果
患者左乳见大范围混合回声包块,长径及横径超过超声窗,前后径约25 mm,边界清,形态欠规则,囊壁增厚,内可见密集点状回声,探头加压可见漂浮(图3ⓐ)。CDFI显示左乳包块内及周边囊壁可见点条状血流信号(图3ⓑ)。病理检查见乳腺腺管腺上皮单层立方排列,周围存在肌上皮细胞,小叶内间质见多量淋巴细胞、浆细胞及少量中性粒细胞,部分区域组织细胞增生,肉芽肿形成(图3ⓒ;HE染色,×100)。
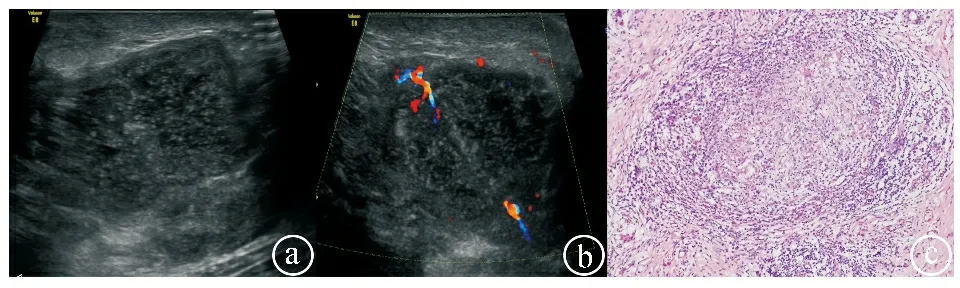
图3 脓肿型GLM患者的典型超声表现及病理结果图
2.2.4 窦道低回声区型GLM患者的典型超声表现及病理结果 患者左乳见数个低回声区,低回声区之间可见相通,并通向皮肤,形成窦道(图4ⓐ)。CDFI显示左乳低回声区内及周边见丰富血流信号(图4ⓑ)。病理检查乳腺组织被覆鳞状上皮,间质可见窦管样结构,窦管内鳞状上皮乳头状增生,部分上皮坏死、脱落,间质炎性肉芽组织增生,大量急慢性炎细胞浸润(图4ⓒ;HE染色,×40)。
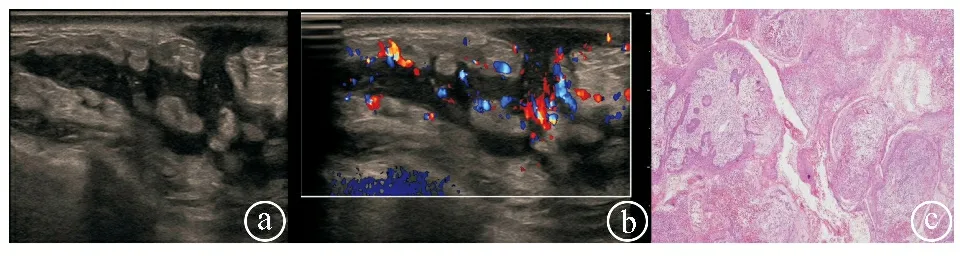
图4 窦道低回声区型GLM患者的典型超声表现及病理结果图
3 讨论
3.1GLM发病原因目前尚未明确,有研究认为GLM与乳腺导管内富含蛋白分泌物以及脂肪外渗引发机体免疫反应有关,也有研究认为其与棒状杆菌感染及高泌乳素血症有关[8-9]。对于GLM的超声分型研究较少且未有共识,有学者将GLM分为片状回声型、结节肿块型和弥散型,超声诊断符合率约为83.5%[10]。也有学者将GLM分为类淋巴结型、弥漫混合回声型、脓肿液化坏死型和多脓腔多窦道型[11]。以往由于临床医师对GLM认识不统一,故该疾病的诊疗过程也难以规范化[12]。对于小的单发脓肿者推荐试行穿刺抽吸,对于脓肿较大、多房脓肿或反复抽吸效果不佳者须行切开引流[12]。正确判断脓肿的形成有助于临床医师把握排脓的时机,而早期诊断脓肿形成也便于及早进行抽吸或引流[13]。
3.2本组研究根据超声图像特征将123例GLM患者分为结节型、团块型、脓肿型和窦道低回声区型,均表现为形态不规则、边缘不光整、未见钙化特征。本组患者中结节型GLM有13例,超声显示病灶形态不规则,边缘成角,血流信号丰富,与乳腺癌声像图相似。有学者认为超声造影有助于鉴别诊断,炎症肿块内常见无造影剂进入的单个及多个无回声区,呈网格状,且无增强区常表现为边界规则[14]。团块型GLM有18例,超声表现以血流信号丰富和腋下淋巴结肿大为主,且团块内部回声杂乱,因此超声检查中应注意两侧乳腺对比扫查。团块型GLM应注意与导管原位癌鉴别,有研究表明,GLM病灶超声表现为实质回声不均匀减低,肿块感不强,未出现钙化,而乳腺导管原位癌(ductal carcinoma in situ,DCIS)大多表现为低回声肿块,52.2%的DCIS存在微钙化[15]。本组病例有脓肿型GLM 33例,内部回声与脓肿形成时期相关。若脓肿早期超声表现为低回声区与无回声区混杂相间,此时穿刺抽脓往往效果不佳,脓肿中期当中性粒细胞崩解释放出蛋白溶解酶使坏死组织液化形成含有脓液的腔,超声表现为密集点状回声,当包块受探头加压时,可以看见点状回声浮动。包块的脓肿壁增厚,壁由新生的毛细血管和成纤维细胞组成,壁上有丰富的血流信号。GLM微脓肿的中心通常为有大量的肉芽组织及多种炎性细胞浸润,以中性粒细胞为主,还有单核细胞、淋巴细胞,而浆细胞较少见[16]。脓肿周边回声增强、血流信号增多,与文献报道相符[17]。本研究有窦道低回声区型GLM患者59例,超声表现为形态不规则的迂曲的管状低回声区,一端为盲端管道,另一端与皮肤相通形成窦道。管状低回声区之间往往相通,纵横交错,笔者认为此为GLM特征性表现。由于Cooper韧带为致密结缔组织,限制了炎症在局部发展,同时也使炎症沿Cooper韧带走行扩散,形成腺体内隧道样病灶,是皮肤窦道、瘘管、溃疡形成的组织学基础[18]。栾玉爽等[19]认为炎性病变突破腺体浅层筋膜出现窄颈征象后在相对疏松的皮下组织内蔓延,甚至累及皮肤层,造成皮肤破溃,形成窦道。有文献报道累及皮肤的GLM复发率较高[20]。本文中脓肿型及窦道低回声区型常范围较广泛,累及多个象限。
3.3通过对本研究资料分析,笔者认为GLM的超声图像较多样化,部分GLM患者超声分型中可能存在重叠,但通过总结,认为诊断GLM还是有一定的规律可循:(1)GLM是发生在终末导管小叶的乳腺炎,其超声表现与疾病的病理发生发展过程密切相关。炎症早期病灶较小时可单发,边界较清晰,病灶内部可发生微小脓肿,可有小片状无回声。当病情迁延发展,病灶增大,呈大片状低回声区或低回声团块,此时病灶内部大量炎细胞浸润,血流信号往往增多。当炎症发展到一定阶段,炎症得不到缓解,病灶往往累及多个象限,形成多个象限的包块,包块内大量炎性细胞浸润,脓肿形成,向皮肤方向发展。脓肿破溃后,脓腔皱缩,形成多条纵横交错的低回声区,此时应注意多个切面连续性扫查,寻找低回声区与低回声区之间的连通点。(2)与浆细胞乳腺炎及乳腺癌鉴别,其鉴别要点在于浆细胞乳腺炎多发生于绝经期前后妇女,病变部位通常发生于乳头、乳晕区域,乳腺大导管内多表现为乳管串珠样扩张,内透声差。而GLM通常发生于生育期妇女,具有哺乳不畅的病史,病变起源于外周,向中心发展,呈多条纵横交错的低回声区,周边组织回声增强。当乳腺癌合并变性坏死时亦可表现为实性肿块中囊性或出血改变,与脓肿期GLM不易鉴别,此时冲击触诊可见GLM脓肿随压力改变,坏死组织来回移动,密集点状回声可见缓慢蠕动。彩色多普勒显示乳腺癌血管走行不规则,位于实性部分中央,高速、高阻血流,而炎症性的血流走行于脓肿管壁周边。笔者认为超声造影中网格样高增强的特征性表现有助于鉴别诊断,提高诊断率。
综上所述,不同分型GLM的超声表现各有特点,可为临床疾病诊治提供依据。
