磁性膨润土的合成及其对亚甲基蓝吸附性能*
2021-11-24雷田旺张喜娜雷杨娜
裴 霏,刘 婷,雷田旺,张喜娜,王 娜,雷杨娜
(1.西安交通工程学院 土木工程学院,陕西 西安 710300;2.宝鸡文理学院 化学化工学院,陕西 宝鸡 721013;3.陕西省气候中心,陕西 西安 710300)
染料是一种广泛应用于造纸、皮革、纺织等行业的有机化合物[1]。然而染料污染是一个严重的环境问题,对人、动物和植物都有毒害作用。长期饮用含有过量染料的水,会对人类和动物的消化系统、肝脏和神经系统造成直接损害[2]。因此,含染料废水排放前必须进行净化处理。但大多数染料具有复杂的芳香结构,并且稳定,不能被氧化剂、光和热所降解[3]。目前,主要通过絮凝[4]、沉淀[5]、吸附[6]和离子交换[7]等水处理技术去除染料;其中吸附法具有操作简便、灵活、对环境无二次污染、价格低廉等优点[8-9]。活性炭由于吸附效率高,被广泛作为水处理吸附剂,但其价格昂贵且难以分离[10]。因此,开发一种吸附能力强、成本低、易于分离的吸附剂是目前的研究热点。
膨润土(H)是一种分布广泛的天然矿物,蒙脱土为其主要成分,蒙脱石由2个硅氧四面体和1个铝氧八面体夹心组成[11-12]。但天然膨润土吸附性能较弱,需要对其进行改良。近年来,研究表明将金属和金属氧化物纳米粒子(如铝[13]、氧化铁[14]和氧化锌[15])分布于膨润土层与层之间作为支柱,可有效扩大膨润土的层间距。而无机酸活化则可以使H+交换取代膨润土层之间的阳离子,从而提升其比表面积和吸附能力。由于膨润土溶于水时呈胶体状分散,不易从水体系中分离[16],吸附污染物后难以分离的缺点限制了其应用。
近年来,Fe3O4磁性纳米粒子在水处理、生物技术、催化等领域受到青睐[17];Fe3O4纳米颗粒具有固有的类过氧化物酶活性,可以催化废水中有机物的氧化[18];另外,Fe3O4具有磁性,易与废水分离,不会对环境造成二次污染。因此将磁性Fe3O4与膨润土结合,不但可增强膨润土的分散、吸附和催化性能,而且能够使膨润土在磁场驱动下从溶液中分离,可有效解决污染物分离问题。然而,由于膨润土的亲水性,大多数合成工艺局限于水溶液体系,难以得到高质量的磁性膨润土,通常含有大而不均匀的磁性纳米颗粒,易团聚、磁性低、比表面积小,在一定程度上限制了膨润土的性能[19-20]。因此,开发一种磁性纳米颗粒粒径分布较窄、分散性良好的优质磁性膨润土势在必行。
采用溶剂热法合成了比表面积较大、磁性较强的磁性膨润土(H-B@Fe3O4)。该复合材料中磁性纳米颗粒粒径分布较窄、分散性良好,对有机染料亚甲基蓝表现出较好的吸附性能,且易于分离和可回收利用。
1 实验部分
1.1 试剂与仪器
六水三氯化铁(FeCl3·6H2O)、盐酸(HCl)、乙二醇[(CH2OH)2]、钠基膨润土:国药集团化学试剂有限公司;亚甲基蓝(C16H18N3ClS,MB)、乙酸钠(NaAc)、柠檬酸三钠(Na3C6H5O7·2H2O):天津市天力化学试剂有限公司;以上试剂均为分析纯。
X射线粉末衍射仪(XRD):D8 Advance,德国布鲁克公司;比表面积测试仪:ASAP-2460,超导磁性测量系统仪:MPMS XL-7,麦克公司;高分辨冷场发射扫描电子显微镜(SEM):SU8010,紫外可见分光光度计:U-3900,日本日立公司。
1.2 酸化膨润土的制备
将10 g黏土加入200 mL浓度为1 mol/L的盐酸溶液中,水浴80 ℃反应12 h,将所得产品过滤,并用蒸馏水反复冲洗以完全去除产品中氯离子残留,t=80 ℃干燥,t=400 ℃煅烧1 h,得到盐酸酸化的膨润土(H-B)。
1.3 磁性膨润土的制备
采用水热法制备磁性膨润土。将10.8 g三氯化铁、200 mL乙二醇和2.667 g膨润土混合搅拌5 h,加入18 g NaAc和2.5 g柠檬酸三钠,再搅拌5 h。将混合物密封于高压釜中,t=200 ℃保持10 h。离心后用乙醇和蒸馏水反复洗涤产物,t=50 ℃干燥,制成磁性膨润土(H-B@Fe3O4)。
1.4 有机染料MB的吸附实验
量取50 mLρ(MB)=20 mg/L的溶液,添加10 mg的磁性膨润土,在室温下搅拌反应,每隔一段时间,取样进行磁分离;取上清液,采用紫外可见分光光度计测定MB溶液的吸光度,计算其脱色率。
2 结果与讨论
2.1 磁性膨润土的结构表征
H-B@Fe3O4复合材料合成与应用示意图见图1。

图1 H-B@Fe3O4复合材料合成及污染物去除的示意图
将膨润土直接引入盐酸溶液中,通过简单的水热即可制得H-B。比表面积测试结果表明,酸化后,比表面积从89 cm2/g增加至110 cm2/g,表明酸化后其比表面积、表面活性位点和吸附能力均有所增加[21]。可能是因为酸处理后,膨润土层间的交换阳离子被H+取代,从而增加了膨润土的比表面积和吸附容量[22-23]。
膨润土及其改性前、后的扫描电镜图片见图2。

a 原始膨润土

b H-B

c 多次乙醇清洗后的H-B@Fe3O4

粉体粒径/nmd Fe3O4粒径分布图图2 膨润土及其改性前、后的扫描电镜图片与Fe3O4粒径分布图
由图2a可知,膨润土是一种具有粗糙多孔表面的层状结构材料,可有效吸附水中的有机污染物。由图2b可知,酸化后的膨润土表面出现较多剥落、疏松、卷曲的断面,说明酸化过程中膨润土层部分脱落。由图2c可知,所形成的Fe3O4纳米球分散性良好,稳定分布于膨润土的表面和层状结构中,表明H-B与Fe3O4纳米粒子有很强的相互作用。由图2d可知,Fe3O4纳米球的平均粒径约为230 nm,且粒径分布较窄。
膨润土及其改性前、后样品的XRD谱图见图3。
由图3可知,酸化可去除膨润土中部分杂质。H-B@Fe3O4样品谱图在2θ=21.8°、26.7°处呈现出H-B特征衍射峰[23],表明所形成的复合材料中膨润土的结构没有被破坏;此外,复合材料谱图中呈现出明显的Fe3O4衍射峰(2θ=30°、35.5°、43°、53.4°、57°和62.5°),未发现其他杂质相的存在。结合SEM结果,表明成功制得了H-B@Fe3O4复合材料。

2θ/(°)图3 膨润土及其改性前、后样品的XRD谱图
2.2 磁性膨润土的磁性能
H-B@Fe3O4样品在室温下的磁滞回线见图4(a为MB吸附前,b为MB吸附后磁化分离)。

磁场强度/×10-3(A·m-1)图4 H-B@Fe3O4样品的磁滞回线
由图4可知,样品H-B@Fe3O4的饱和磁化强度为13.8 A/m,没有检测到剩磁现象,表明其磁性能良好,易与水分离。为进一步验证H-B@Fe3O4样品在水溶液中的磁性效果,其吸附亚甲基蓝染料后在侧边放置磁铁,很短的时间内即可完成磁分离,现象见图4右下角。结果表明,H-B@Fe3O4复合材料的磁性能使其易于通过磁铁等外部磁场进行分离,比高速离心的天然膨润土分离速度快,为吸附剂的快速分离提供了可能。
2.3 磁性膨润土的比表面积和孔径
Fe3O4和H-B@Fe3O4的氮气吸附/脱附等温线与孔径分布图分别见图5和图6。

p/p0图5 样品的氮气吸附/脱附等温线
由图5可知,H-B@Fe3O4的氮气吸附/脱附等温线为典型的Ⅳ型吸附等温线,滞后环较宽,表明H-B@Fe3O4复合材料的孔隙分布较宽且为介孔[24]。纳米Fe3O4的比表面积为2.6 m2/g,而H-B@Fe3O4复合材料的比表面积增至47 m2/g。表明磁性Fe3O4纳米粒子进入H-B的层状结构中,提高了H-B的孔隙率,有效增大了比表面积,有利于吸附性能的提高。
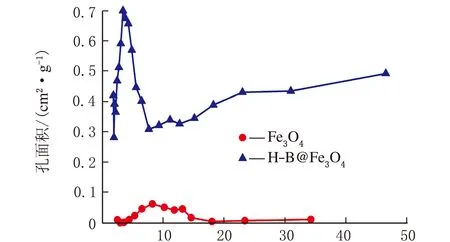
孔径/nm图6 样品的孔径分布图
由图6可知,H-B@Fe3O4复合材料的孔隙主要分布在2~10 nm,该结果与图5结论相一致。
2.4 磁性膨润土吸附MB的性能研究
H-B@Fe3O4添加量与MB去除率的关系曲线见图7。
由图7可知,吸附剂m(H-B@Fe3O4)=0~30 mg,MB去除率逐渐增加,且吸附速率逐渐加快;吸附剂m(H-B@Fe3O4)=20、30 mg时,两者的吸附速率接近,且均可在5 min内完成吸附,说明m(H-B@Fe3O4)=20 mg即可达到完全吸附效果。

吸附时间/min图7 H-B@Fe3O4添加量与MB去除率的关系曲线
m(H-B@Fe3O4)=20 mg时,吸附MB后溶液的吸光度随时间变化的曲线见图8。

吸收波长/nm图8 吸光度随时间变化的曲线
由图8可知,t<5 min对MB的去除率超过99.9%,表明H-B@Fe3O4是一种有效的吸附剂,可以有效去除MB。
2.5 影响磁性膨润土吸附性能的内在机制研究
溶液初始pH值与MB去除率关系见图9。
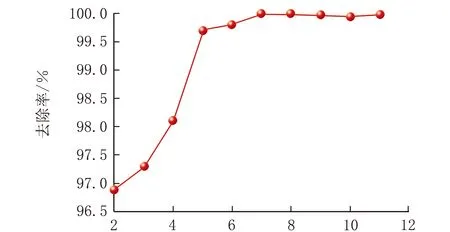
pH图9 MB去除率与pH值关系
由图9可知,随着溶液初始pH值逐渐增大,样品H-B@Fe3O4对MB的去除率逐渐增加;pH>7,对MB的去除率无明显影响,这可能是溶液初始pH值对吸附剂H-B@Fe3O4表面电荷有影响。
溶液初始pH值与H-B@Fe3O4样品表面Zeta电位的关系见图10。
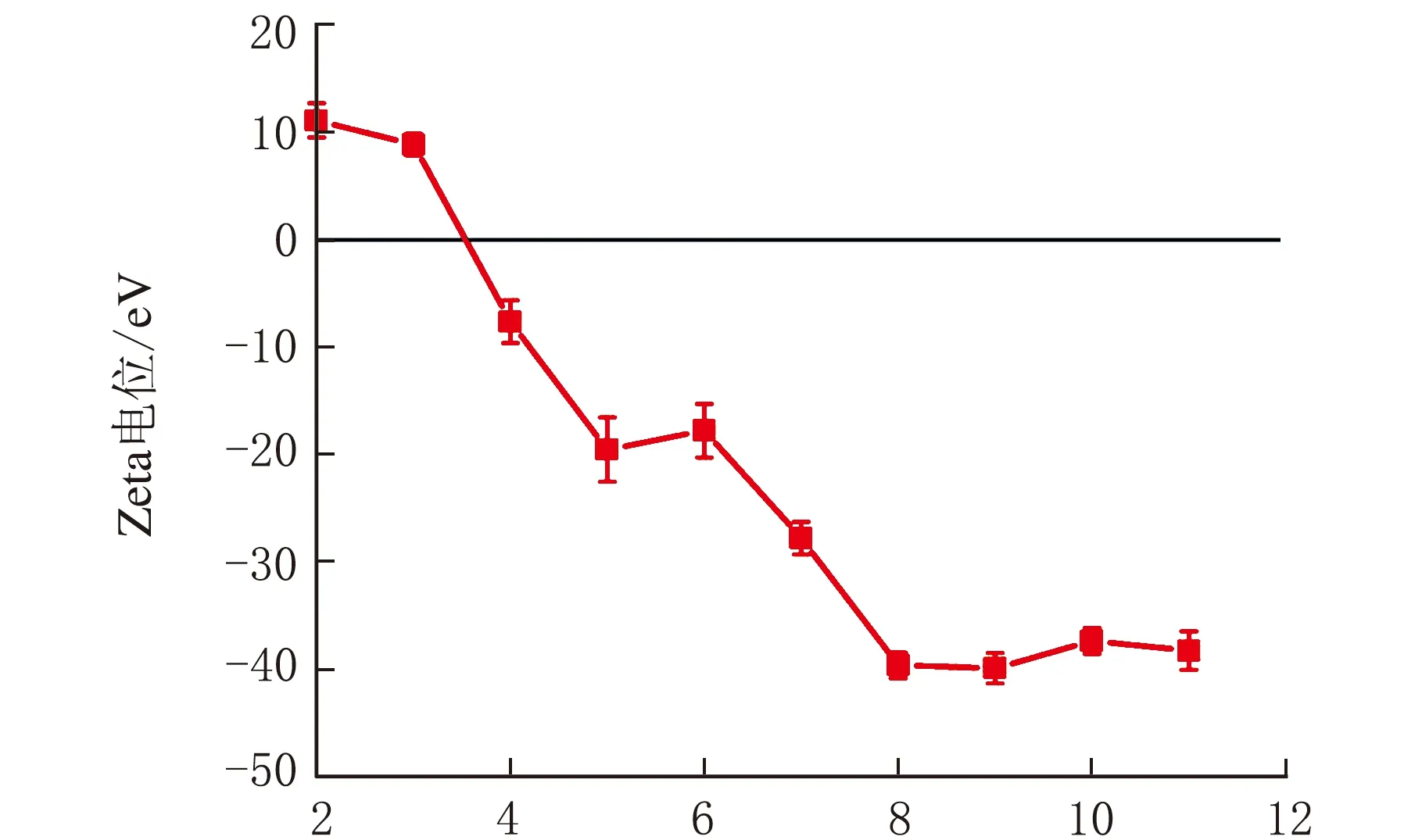
pH图10 H-B@Fe3O4表面Zeta电位与pH值的关系
由图10可知,H-B@Fe3O4表面的正电荷随着pH值的增加而减少,负电荷逐渐增加。MB在水溶液中带正电荷,因此pH=3.5~11,H-B@Fe3O4表面带负电荷,与MB表面电荷相反,致使其相互吸引,能有效去除MB。相比之下,pH<3.5,H-B@Fe3O4和MB表面均为正电荷,同电荷相互排斥,MB的去除主要是靠其中孔的负载和吸附作用;pH=7~8,负电荷增加,但是去除率不再增加,这可能是由于H-B@Fe3O4比表面积一定,当H-B@Fe3O4的表面电位达到-28 eV,在单位时间内就可达到吸附饱和,即使H-B@Fe3O4表面负电荷进一步增加,对MB的去除率也不再增加。
3 结 论
采用溶剂热法合成了H-B@Fe3O4复合材料,并将其应用于去除有机污染物MB。系统研究了H-B@Fe3O4用量、吸附时间与MB去除率的关系以及溶液pH值对MB去除率的影响及其内在机制。研究表明所制备的H-B@Fe3O4在t<5 min完成对MB的吸附,去除率高达99.9%,且H-B@Fe3O4具有较高的饱和磁强度,有利于污染物的磁化分离,此外,吸附MB后的H-B@Fe3O4易于脱除MB而实现循环利用。因此,研究提供了一种低成本、高效、易于分离和回收的复合磁性吸附材料的制备方法,可广泛应用于水中污染物的处理,具有极大的应用潜力。
