基于真实问题情境发展学生核心素养的教学
2021-11-20邓君
邓君


摘要:以魔术及“麦片中含铁粉是真的吗?”为切入口,设置真实问题情境学习铁盐和亚铁盐的性质和它们在生产生活中的应用,开展以化学实验为主的多种探究活动,提高学生解决实际问题的能力,促进核心素养的真正落实。
关键词:核心素养;真实情境;铁盐;亚铁盐
文章编号:1008-0546(2021)04-0048-06 中图分类号:G632.41 文献标识码:B
doi:10.3969/j.issn.1008-0546.2021.04.013
《普通高中化学课程标准(2017年版)》(简称新课标)指出:“重视开展素养为本的教学,倡导真实问题情境的创设,开展以化学实验为主的多种探究活动[1]。新课标对高中化学教学提出了更高的目标和要求,明确了学生学习该学科课程后应达成的正确价值观念、必备品格和关键能力。为此,教师在设计和开展教学活动时,根据教学内容为学生创设真实陌生的问题情境、设置挑战性任务,运用必备知识和关键能力去解决实际问题,将学科素养的培养落到实处。关于“铁盐和亚铁盐”的教学设计层出不穷,文献集中在离子转化关系的教学[2-3]、高考复习的教学设计[4-5]、创设生活情境进行实验探究的设计[6-7]。但是在诸多教学设计中,教师常常直接告知静态结论或者忽视问题情境的复杂性、应用性,未能发展学生应对生活实践问题情境与学习探索问题情境的综合素养。
鉴于此,笔者将以“铁盐和亚铁盐”的教学为例,结合真实问题情境,采用“体验—探究”教学模式,试图为构建学生核心素养的教学设计提供参考。
一、教材分析
“铁盐和亚铁盐”选自人教版《化学1》第三章第二节“几种重要的金属化合物”,是在初中介绍的金属和金属材料的基础上,进一步深化和提高,也是为物质的分类、离子反应、氧化还原反应等理论补充感性认识材料,更是对前面理论的应用和升华。本节课是在真实较为复杂的情境下进行Fe2+、Fe3+的检验及从氧化还原反应的视角认识Fe2+、Fe3+的性质,可以使学生在探究Fe2+和Fe3+的相互转化的实验方案中,对实验现象进行分析推理,得出合理结论,最终目的让学生在面临与化学有关的问题时,能从化学的视角做出更理智、更科学的判断或选择。
二、教学目标
1.通过魔术“黄酒变红酒”和“麦片中含铁粉是真的吗?”实验探究,学会Fe2+和Fe3+的检验方法,能根据观察和实验获得的现象,在分析过程中培养学生证据推理、科学探究的素养。
2.通过魔术揭秘及Fe2+和Fe3+相互转化的实验探究活动,对知识进行归纳整理,建构Fe2+和Fe3+的相互转化模型,在过程中培养学生模型认知和变化观念的素养。
3.通過了解实际生活生产中Fe2+和Fe3+的应用,体会理论知识在实际生活中的具体应用,培养学生科学态度与社会责任的素养。
三、教学策略
“体验—探究”教学模式操作程序如下:
创设情境(激发体验阶段)→探究释疑(实践体验阶段)→实践应用(体验生成阶段)→评价反思(反思体验阶段)
1.创设情境
魔术和网络新闻这些真实的问题情境,能够拉近学生与化学知识的距离,激发学生的好奇心,成为学生思考并解决问题的驱动力。
2.探究释疑
创设有思维梯度的学习任务,让学生进行不断地深度探究,将本质性知识形成清晰的知识框架。
3.实践应用
紧密联系生产和生活实际,培养学生尊重事实和证据,具有独立思考、敢于质疑和批判的创新精神。
4.评价反思
通过自我评价可以对外在的评价标准进行深刻领会,并使之转化为自我可以接受的评价准则,从而更好地用它来指导课堂教学。
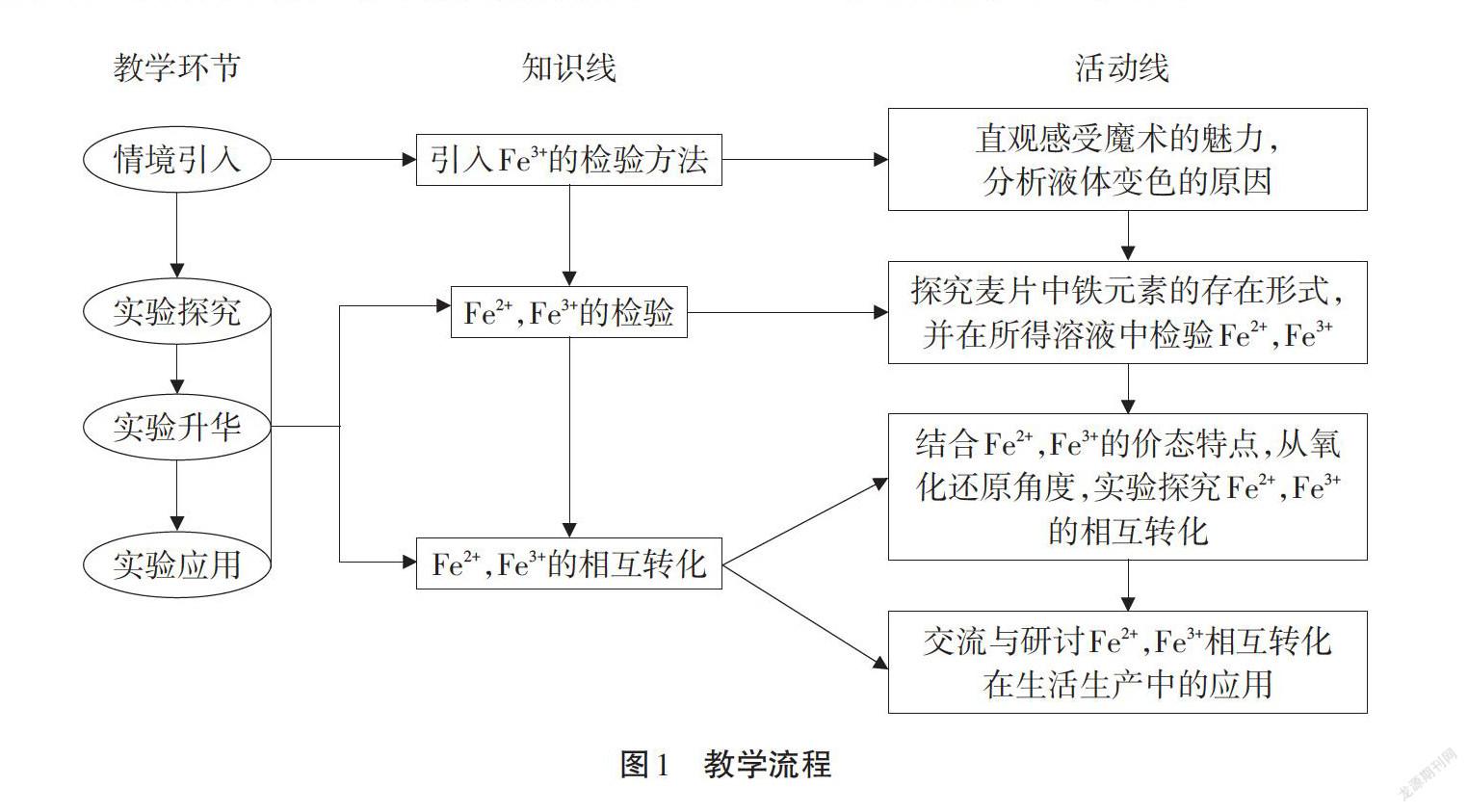
四、教学流程
教学流程如图1所示。
五、教学过程
1.情境引入——明确课堂目标
【引入】我不是刘谦,但我也可以像刘谦一样会变魔术,见证奇迹的时刻到了。这是一杯黄酒,另外一个是空酒杯,我将它倒进空酒杯,一杯纯正的红葡萄酒就出现了。我再加入维生素C粉末,红酒就变成苹果汁(见图2)。
【学生】尖叫、鼓掌
【教师】秘密就在课本中,请大家打开课本第61页,寻找答案。
【展示】硫酸铁等含有Fe3+的盐溶液遇到KSCN溶液时变成红色,我们可以利用这一反应检验Fe3+的存在。
【板书】铁盐和亚铁盐
【教师】魔术的奥妙在哪里?谁能为我这个魔术来揭秘呢?
【学生】黄酒是Fe3+溶液,另一个酒杯装有很少的KSCN溶液,看起来像空酒杯一样,一混合红葡萄酒就出现了。后来为什么变成苹果汁就不知道了。
【教师】非常好!为什么葡萄酒会变成苹果汁我们稍后揭秘。我们可以用KSCN溶液检验Fe3+,生成的硫氰化铁是红色的,注意不是沉淀。用K3[Fe(CN)6]溶液来检验Fe2+,产生蓝色沉淀。另外,还有没有其他方法来鉴别Fe2+,Fe3+呢?
【学生甲】观察溶液颜色,亚铁盐是浅绿色的,铁盐是棕黄色的。
【学生乙】加入NaOH溶液,Fe(OH)2是白色沉淀迅速变为灰绿色,最终被氧化为红褐色,而Fe(OH)3是红褐色沉淀。
【教师】不错。那我们就开启实验之旅吧。
设计意图:通过魔术表演,激发学生的学习兴趣,使乐学、善学这一核心素养在课堂上得以体现。
2.实验探究——掌握化学原理
【实验探究】有些商家为了将麦片中铁含量增加,直接把铁粉掺入麦片里。麦片中含有铁粉是真的吗?对人体是有益还是有害?请大家在20min内完成活动,各小组交流讨论,然后汇报成果。
(1)阅读麦片配料表(见图3),思考如何提取铁粉?如何溶解铁粉?溶液中的铁元素是Fe2+还是Fe3+?设计实验检验Fe2+,Fe3+。
(2)通过教师引导设计流程图(见图4),完成实验,记录现象,得出结论。
实验仪器:搅拌机、烧杯、试管、药匙、玻璃棒、胶头滴管、点滴板、密封袋、磁铁
实验试剂:麦片、稀硫酸、铁氰化钾溶液、硫氰化钾溶液、氢氧化钠溶液
实验步骤:分别取各品牌麦片一包,加水充分溶解,倒入搅拌机搅拌约20s,将液体倒入密封袋中,用强力磁铁放在密封袋上面,吸出黑色粉末并取出。
【实验现象】如图5所示
【板书】检验Fe2+,Fe3+
【教师】时间到了,大家非常积极,配合的也很默契,每组请一位同学进行汇报。铁元素存在的价态有哪些?大家如何提取铁粉?溶解过程有什么现象?请第1小组的成员分享你们的成果。
【成果汇报l】铁元素有0,+2,+3价,存在形式为Fe、Fe2+、Fe3+。用磁铁将铁粉吸出来,然后选择稀硫酸将其溶解,四种麦片中均有气泡生成。
【教师】很好,请在黑板上写出这个反应的化学方程式。
【学生板书】Fe+H2SO4=FeSO4+H2↑
【教师】如何检验所得溶液中的Fe2+和Fe3+?请第2组同学将本组探究情况跟大家交流汇报。
【成果汇报2】结果如表1所示。
【教师】根据实验现象,为什么观察法和沉淀法并没有达到实验的预期现象?
【学生丙】可能是铁离子浓度过小,通过肉眼无法辨别颜色。
【学生丁】可能反应后溶液是Fe2+,Fe3+的混合溶液,Fe2+含量多,灰绿色沉淀掩盖了Fe(OH)3红褐色沉淀,不能观察出来。
【教师】鉴别即两种或两种以上物质组合,通过实验予以区分。同学们归纳出来的是鉴别Fe2+,Fe3+的方法。而此时我们得到的是一杯混合溶液,里面可能存在Fe2+可能存在Fe3+,要确定溶液中是否存在二者,这样的过程称之为检验。观察法和沉淀法中两种离子相互干扰无法检验出二者。那么大家觉得在这杯溶液中检验Fe2+,Fe3+最好选用什么试剂?流程中试剂1,2分别是什么?
【学生戊】试剂1可用铁氰化钾K3[Fe(CN)6]溶液来检验Fe2+,试剂2可用KSCN溶液检验Fe3+。这两种方法比较灵敏,不相互干扰,用量少且现象明显。
【教师】请第3组同学对四种不同麦片品牌中的Fe2+、Fe3+的检验进行汇报交流。
【成果汇报3】四种麦片的实验数据(见表2)
【教师】这四种麦片中都含有Fe2+和Fe3+,分析产生Fe3+的原因是什么呢?
【学生】(1)麦片中加入的还原铁不纯,存在少量副产物。
(2)还原铁有部分被氧化,或者生成Fe2+后被空气氧化。
【教师】麦片中为何要添加还原铁?
【学生】补铁,还原铁粉进入胃中会转化为Fe2+,被人体所吸收。
【教师】还有其他作用吗?提示:铁露置在空气中最终会生成什么?形成铁锈的条件?
【学生】吸收空气中的氧气和水。
【教师】因此,还原铁粉又称为“双吸剂”,糕点中常会放一包黑色粉末,用于食品保鲜。一般来说,Fe2+较Fe3+有利于人体吸收。如何将Fe3+转化为更利于人体吸收的Fe2+呢?
设计意图:利用生活实验探究,不仅增进趣味性,更体现学以致用;既区别检验与鉴别的概念,又选出检验Fe2+,Fe3+的最佳试剂。本主题的设计是让学生勤于反思,通过问题解决实现学生核心素养的达成。
3.实验升华——形成知识框架
【教师】我们前面的魔术中,黄酒变红葡萄酒,大家都明白了暗含的秘密。说明溶液中有Fe3+,我再加入维生素C粉末,红酒就变成苹果汁。此时,有没有发生化学变化?溶液里还有没有Fe3+呢?如果是化学反应,属于什么反应类型?
【学生】有发生化学反应。红酒里已经有硫氰化钾,加入维生素C粉后,红色褪去,说明反应后已没有Fe3+。铁元素的化合价有发生改变,为氧化还原反应。
【教师】说得很好!从化合价的变化角度看,维生素C片起什么作用?作什么剂?
【学生】加入维生素C,维C把Fe3+转化为Fe2+,所以维C作还原剂。
【板书】Fe2+和Fe3+的转化
【学生活动1】设计实验将Fe3+转化为Fe2+
试剂:Fe2(SO4)3溶液、维生素C片、铜片,KSCN溶液,K3[Fe(CN)6]溶液。
(1)从氧化还原反应角度分析,Fe3+能不能转化为更利于人体吸收的Fe2+?
(2)验证你的猜想。
【教师】请采用不同还原剂做实验的第4组和第5组同學分别进行汇报交流。
【成果汇报4】取一支洁净的试管,加入少量的Fea(SO4)3溶液,加入铜片,溶液由黄色变为浅绿色(耗时较长)。再滴入1滴K3 [Fe(CN)6]溶液,出现蓝色沉淀(辅助检验)。说明铁离子转化为亚铁离子(见图6)。
【成果汇报5】取一支洁净的试管,加入少量的Fe2(SO4)3溶液,滴入几滴KSCN溶液,溶液变为红色。加少量研磨后的维生素C粉,红色褪去。再加入1滴K3[Fe(CN)6]溶液,出现蓝色沉淀(如图7)。说明维生素C粉、铜片这样的还原剂可以将Fe3+还原为Fe2+。
【教师】铜片、维生素C等还原剂能够将Fe3+转化为Fe2+,更有利于人体吸收。那要加入什么试剂可以将Fe2+氧化成Fe3+?
【学生】要加入氧化剂,比如高锰酸钾、氯水、过氧化氢等。
【学生活动2】设计实验将Fe2+转化为Fe3+
试剂:FeSO4溶液、新制氯水、双氧水,KSCN溶液。
【教师】请最后一组同学来分享你们的活动成果。
【成果汇报6】如表3所示
【教师】实验操作1和2哪一种更好?为什么?
【学生己】实验操作1更好,Fe2+易被氧化,先加KSCN溶液,溶液无明显现象,可排除原溶液中Fe3+的干扰。
【教师】请按实验操作3的同学来分享一下实验现象。
【学生庚】刚开始跟大家一样,溶液变红,但是,一段时间后,溶液中有较多气泡出现,并放热,随后有红褐色沉淀生成。
【教师】不错,同学观察现象非常仔细。有同学可以分析一下产生的是什么气体?产生气泡的原因是什么?生成的红褐色沉淀是什么?产生沉淀的原因又是什么呢?
【学生辛】可能双氧水加多了分解生成氧气。根据元素守恒和特殊的颜色现象可以判断出来,生成的红褐色沉淀应该是Fe(OH)3,原因是什么不清楚。
【教师】初中我们学过二氧化锰可以催化双氧水分解产生氧气,Fe3+也可以。感兴趣的同学可以自行设计实验进行验证。生成红褐色的原因是该分解反应放热,促进Fe3+的水解平衡正向移动。盐类的水解我们稍后会学习。
【板书】如图8所示。
设计意图:本节课模型构建的升华,掌握学习元素化合物的一般方法,同时拓展离子检验方法的思路及氧化还原理论的运用。
4.实验应用——体验知识达成
【教师】实验室如何保存FeSO4溶液?
【学生壬】可以加入少量铁粉,防止Fe2+被氧化。
【学生癸】在配制溶液时,用的蒸馏水应该要加热煮沸除去溶解氧。
【学生十一】这种试剂尽量现用现配,因为容易被氧化。
【教师】大家回答的非常棒!请大家观察这瓶FeSO4溶液的底部。
【学生】黑色粉末为铁粉,防止溶液被氧化。
【教师】不错,请同学们写出该反应的离子方程式。
【学生】Fe+2Fe3+=3Fe2+
【教师】在生活中,儿童缺铁性贫血医生会建议服用小儿硫酸亚铁糖浆,在服用时与什么同服更促进吸收?
【学生】维生素C片或富含维C的食物,维生素C可以将部分被氧化生成Fe3+转化为Fe2+,促进铁吸收。
设计意图:真实情境的引入,拓展学生的视野,身边处处有化学,升华学生对本节课学习方法的应用。
六、课后反思
1.创设情境,激活课堂教学
创设真实实验情境,引导学生探究性学习,不仅让学生体验到化学学科的独特魅力,也培养了学生实验探究的思维。本节课的开始教师借助魔术表演及新闻报道的引入,激发学生的求知欲。通过阅读麦片配料表,引导学生提取铁粉,溶解铁粉,设计实验检验Fe2+,Fe3+。最终找到在一杯Fe2+,Fe3+都可能存在的溶液中检验二者的最佳试剂。以生活化的视野引导学生联系实际生活,从生活中来,到生活中去,运用已有知识或合作探究能力来解决生活实践中的应用性问题。
2.尊重事实,解决实际问题
化学是一门以实验为基础的自然科学,尊重客观事实,用事实说话。通过“麦片中含铁粉是真的吗?”探究实验,学生知道在麦片中添加铁粉是真的,而且是有利于身体健康的。此外,既要充分利用学生的已有经验开展教学,又要对有些经验,尤其是有疑惑的内容进行实证,可以采用客观事实、化学实验等方式进行。在将Fe2+转化为Fe3+环节时,KSCN溶液滴加的顺序不一样,得到的现象一样,其实是某种实验操作不够严谨,没有排除原溶液中Fe3+的干扰。选用双氧水做氧化剂时,由于加入双氧水的量过多,有同学观察到其他现象。教师也应引导学生分析此产生现象的原因,对实验现象进行深度挖掘。因此,笔者经常在课堂上有意放慢教学节奏,留有足够的时间和空间让学生进行探究,思考、讨论,让学生体会到解决实际问题往往具有层次性、复杂性。
3.构建网络,体现思维进阶
构建化学知识网络可帮助学生理解化学,提高学习能力,提升科学素养。通过这节课铁盐和亚铁盐的知识学习,学生对所学知识进行系统的梳理、深化、整合,自主构建了Fe2+与Fe3+转化关系,思维得到了进一步的提升。所以,教师在教学过程中不仅仅是解决探究任务的本身,同时也要不断地联系生活,升华内容,特别是在探究环节结束的时候引导学生进行网络构建,使知识得以内化,情感得以提升。
参考文献
[1]中华人民共和国教育部.普通高中化学课程标准(2017年版)[S].北京:人民教育出版社,2018
[2]姚建军,仲淑娴.“Fe2+和Fe3+的性质与转化”教学设计及反思[J].化学教与学,2012(12):58-60
[3]赵仲霞,张泽俊,罗家刚.无机元素化合物知识教学设计研究——以铁及其化合物的性質为例[J].中学化学教学参考,2017(12):22-24
[4]虞琦,倪娟.基于学科观念培养的高三一轮复习课堂教学——以“铁及其化合物”为例[J].中学化学教学参考,2013(8):27-29
[5]耿亚萍.基于生活问题情境的化学核心素养的培养研究——以铁及其化合物复习为例[J].北学教育(中英文),2019,40(7):38-41
[6]王星乔,包朝龙,腾瑛巧.“补铁剂的选购与含铁量的测定”教学设计与实录[J].化学教学,2013(11):46-48
[7]马佩强,孟静.巧用情境线索渗透核心素养创设生机课堂——以“铁的重要化合物”的教学设计为例[J].化学教与学,2019(9):51-55
*本文系广州市教育科学规划“十三五”重点课题“基于学科核心素养的中学课堂教学策略转型研究”(201811552)、广东教育学会2018年度教育科研规划小课题“核心素养理念下的元素化合物知识‘体验—探究教学模式的研究”(GDXKT16781)的阶段性研究成果。
