基于网络药理学和分子对接研究化湿行瘀清热方治疗口腔扁平苔藓的作用机制※
2021-11-18邓倩澜路月亭路华林靳睿哲许彦枝刘铁军
邓倩澜 路月亭 路华林 靳睿哲 许彦枝 刘铁军 赵 乾
(河北医科大学第四医院口腔科,河北 石家庄 050019)
口腔扁平苔藓是一种病因不明的自身免疫性炎症疾病,据统计其发病率在0.5%~1.5%,多见于中年女性患者[1]。口腔扁平苔藓多发生于颊、舌部位,临床表现以网状、萎缩、糜烂型常见[2]。口腔扁平苔藓有癌变潜能,被世界卫生组织(WHO)定义为“癌前状态”,恶性转化率为0.5%~2%[3]。现代医学主要采取西药、手术、物理治疗方式控制该病进展,但部分患者疗效不甚理想。中医药在口腔扁平苔藓的预防治疗中发挥了重要作用。中医学将口腔扁平苔藓归为口疮、口糜范畴,为热毒与湿积聚、气血失和、湿热循经上逆熏蒸于口舌所致,以化湿醒脾、清热降火、活血化瘀为原则,形成了化湿行瘀清热方,在长期临床治疗中取得了较好疗效[4]。化湿行瘀清热方由黄柏、佩兰、砂仁、薏苡仁、茯苓、赤芍、红花、牡丹皮、甘草、白鲜皮、金银花11味药组成,然而其治疗口腔扁平苔藓的具体机制尚未阐明。
目前,网络药理学已成为一项成熟的技术,其基于系统生物学、生物信息学及多向药理学方法,系统研究药物靶点与疾病基因之间复杂多样的关系,从整体角度阐明各种药物有效成分的药理作用机制[5]。本研究采用网络药理学方法,预测化湿行瘀清热方治疗口腔扁平苔藓的有效活性成分、潜在靶点及相关信号通路,探究其治疗作用机制,并且通过分子对接对分析结果进行验证。
1 资料与方法
1.1 化湿行瘀清热方的活性成分及其作用靶点挖掘 使用TCMSP数据库[6](http://tcmspw.com/tcmsp.php) 和BATMAN-TCM数据库[7](http://bionet.ncpsb.org/batman-tcm/)获得化湿行瘀清热方剂中各组分的有效成分,以口服生物利用度(oral bioavailability,OB)≥30%,药物相似度(drug likeness,DL)≥0.18为条件,筛选有效成分对应的作用靶点。TCMSP是一个系统的药理学数据库和分析平台,整合了药物的化学成分和靶点、相关疾病的靶点及相互作用网络,有利于分析中药的作用机制。BATMAN-TCM数据库是一种中药分子机制生物信息学分析工具,该数据库基于中药成分的靶点预测和后续的网络药理学分析。OB用于描述药物的剂量进入人体循环的比例;DL指化合物与已知药物的相似性。使用UniProt数据库(http://www.uniprot.org/)和PERL编程语言(https://www.perl.org/,版本:5.30.1)获得药物有效成分靶点对应的基因符号。
1.2 口腔扁平苔藓相关靶点的获取 在GeneCards数据库(http://www.genecards.org)中,输入关键词“口腔扁平苔藓”,获得疾病靶点。
1.3 药物-疾病共同靶标筛选 将化湿行瘀清热方有效成分对应靶点的基因符号及疾病靶点导入到Venny2.1.0(https://bioinfogp.cnb.csic.es/tools/venny/)在线工具,得到药物和疾病的共同靶点,交集部分认为是化湿行瘀清热方治疗口腔扁平苔藓的关键靶点(药效靶点)。
1.4 药物-疾病调控网络的构建 使用PERL编程语言(https://www.perl.org/ver.5.30.1),筛选得到药效靶点对应的药物活性成分。将药效靶点与其对应的药物活性成分共同导入Cytoscape软件(http://cytoscape.org/,版本:3.7.2),构建化湿行瘀清热方活性成分与靶点的调控网络。
1.5 构建蛋白互作网络(PPI) 将药物-疾病共同靶点导入String 数据库(https://string-db.org/)构建PPI,限定物种为“人”,结果以TSV文件格式保存。将结果导入Cytoscape 软件绘制蛋白互作网络相互作用图,并使用“Network Analyzer”功能对网络进行分析,得到核心靶点。使用6个参数来评估蛋白互作网络的拓扑性质:自由度(Degree,DC),介度(Betweenness Centrality,BC),中心性(Closeness Centrality,CC),特征向量中心(Eigenvector Centrality,EC),基于局部平均连接的方法中心性(Local Average Connectivity-based method Centrality,LAC)和网络中心(Network Centrality,NC)。首先选择蛋白互作网络中6个参数值均大于中值的节点构建子网络;生成的子网络再通过“6个参数值均大于或等于中值”这一条件再次进行筛选,并构建核心蛋白互作网络。
1.6 基因本体论(GO)和京都基因和基因组百科全书(KEGG)富集分析 利用R软件中Bioconductor 安装包(http://www.bioconductor.org)的功能对药物-疾病共同靶点进行进行GO基因功能富集分析和KEGG通路分析。筛选条件为P<0.05,Q<0.05,以便进一步分析。
1.7 分子对接 分子对接是一种评价药物活性成分与药物靶点结合能力的方法。从PubChem数据库(http://pubchem.ncbi.nlm.nih.gov/)中下载靶点位于前4位的药物有效成分2D结构,并通过ChemOffice软件将2D结构转换为3D结构。在PDB(http://www.rcsb.org/)数据库中下载核心蛋白互作网络中的蛋白三维结构,通过PyMol软件,将蛋白中的水分子和小分子配体删除。利用AutoDock1.5.6软件将药物有效成分和核心蛋白的PDB格式转换为PDBQT格式,并寻找活性口袋。最后运行Vina进行分子对接。
2 结果
2.1 化湿行瘀清热方有效成分及潜在靶点 根据OB和DL (OB≥30%,DL≥0.18)的筛选条件,从化湿行瘀清热方中共获得169个不重复有效成分及260个相关靶点,其中有效成分白鲜皮18个,赤芍29个,茯苓15个,甘草92个,红花22个,黄柏37个,金银花23个,牡丹皮11个,佩兰11个,砂仁10个,薏苡仁9个,见图1。由于每种中药组分中含有效成分有重复部位,我们绘制韦恩图对每种组分中所含有效成分进行归纳,见图2,在化湿行瘀清热方中各组分分布范围较广的有效成分是豆甾醇、谷固醇、槲皮素、谷甾醇、木樨草素、山奈酚。图2中左侧柱状图代表化湿行瘀清热方各药物组分及所包含活性成分数目,上方柱状图代表药物共有的活性成分数量,中间黑色圆点代表含有此种活性成分的每种药物组分。
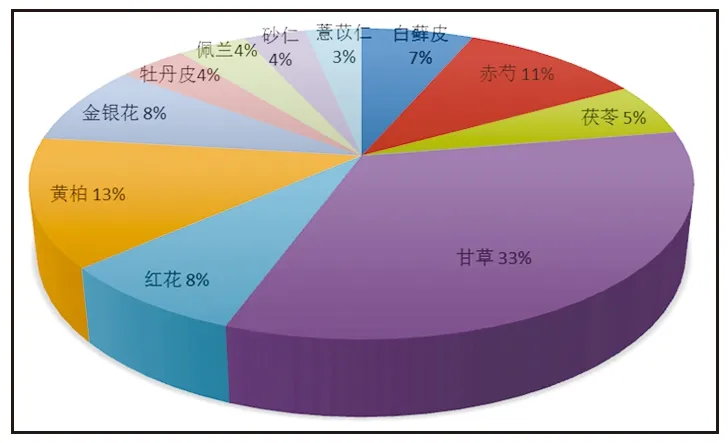
图1 化湿行瘀清热方各组分所含有效成分所占比例情况
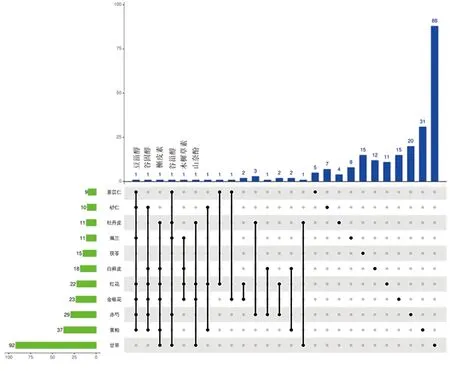
图2 化湿行瘀清热方各组分所含有效成分分布韦恩图
2.2 口腔扁平苔藓相关靶点 在GeneCards数据库中以“口腔扁平苔藓”为关键词进行搜索,经过检索共获得了387个疾病靶基因。
2.3 药物-疾病共同靶基因 利用R软件和Venny2.1.0在线工具对260个药物靶点和387个疾病靶点取交集,两者相交后,共获得了58个药物-疾病共同靶点,用于后续的网络药理学分析。
2.4 构建并分析药物有效成分-疾病靶点网络 应用PERL语言,我们共获得了58个疾病药物共同靶基因和对应的136个有效成分,通过Cytoscape软件构建药物有效成分-疾病靶点网络图,该网络共有194个节点,497条边,见图3,中心矩形代表药物的活性成分,外围矩形代表药物治疗疾病的靶点。白色矩形代表白鲜皮的有效成分,棕色代表赤芍,橙色代表茯苓,绿色代表甘草,红色代表红花,粉色代表黄柏,黄色代表金银花,深蓝色代表佩兰,灰色代表薏苡仁,淡粉色代表化湿行瘀清热方剂中2种或2种以上成分的共同成分。对靶点不低于5的有效成分信息进行整理,见表1。化湿行瘀清热方中靶点最多的化合物为槲皮素(MOL000098),其他依次为:木犀草素(MOL000006)、汉黄芩素(MOL000173)、山奈酚(MOL000422)等。槲皮素中有49个靶点,木犀草素中有29个靶点,汉黄芩素中有17个靶点,山奈酚中有16个靶点,表明它们在治疗口腔扁平苔藓中发挥更大的作用,可能是关键的有效活性成分。
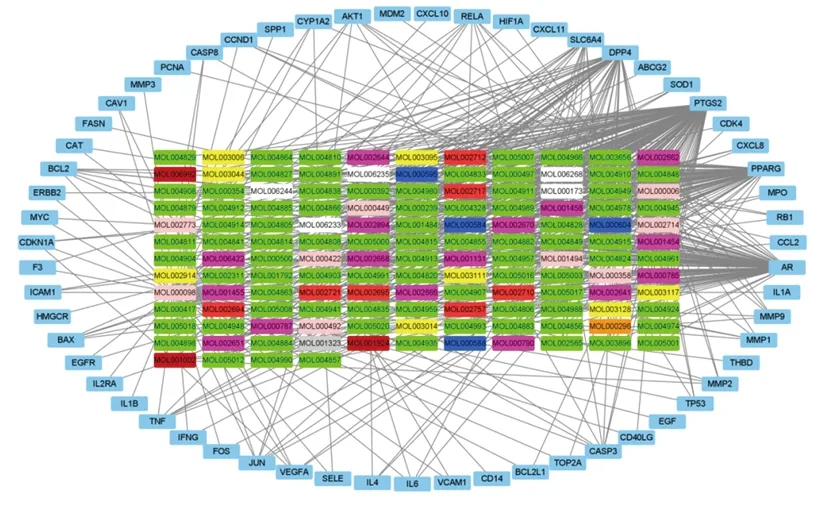
图3 活性化合物和疾病共同靶点的网络
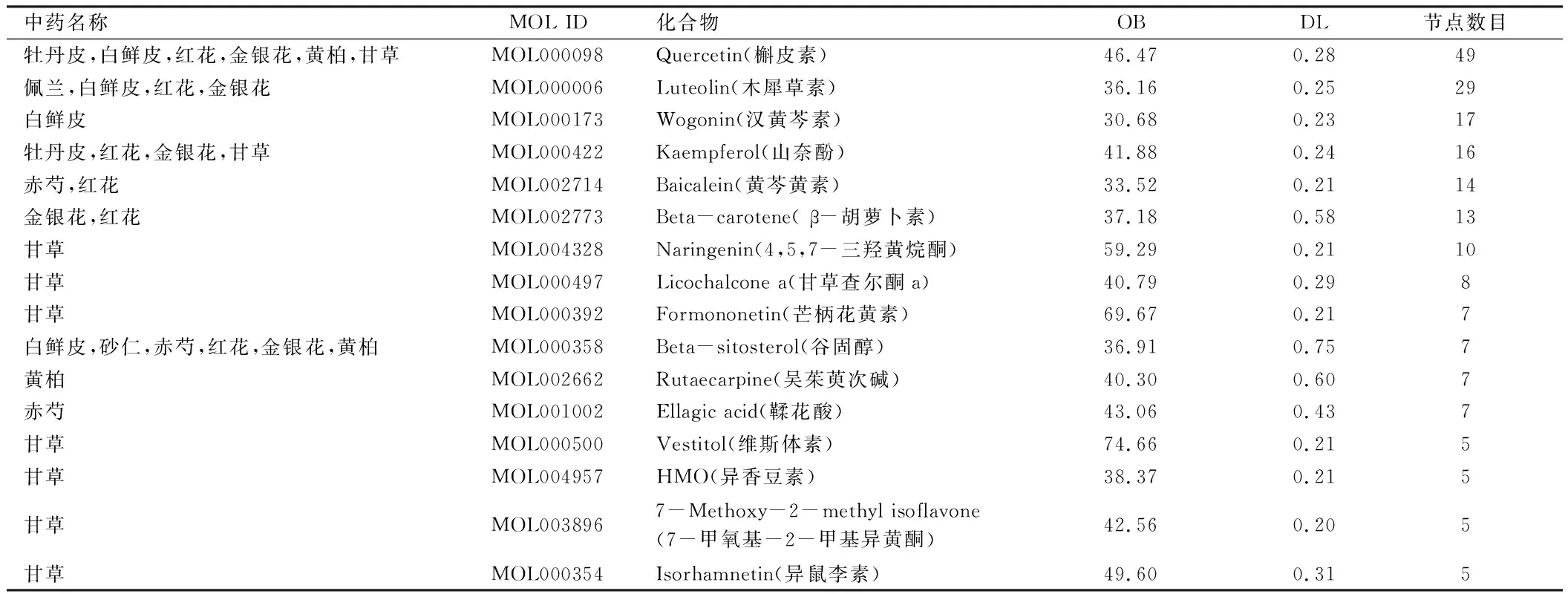
表1 化湿行瘀清热方中有效成分信息
2.5 蛋白互作网络(PPI) 原始PPI (图4A)通过DC、BC、CC、EC、LAC和NC的值进行2次筛选,最终得到核心蛋白互作网络。核心PPI由14个节点和168条边组成,如图4C所示。根据PPI的拓扑分析结果,图4A网络中各节点连接度的中位数为31,介度的中位数为16.741,紧密度的中位数为 0.683,特征向量中心为0.135,基于局部平均连接的方法中心性为24.151,网络中心为26.057,6个参数均超过中位数的靶点有25个,见图4B。图4B网络中各节点连接度的中位数为31,介度的中位数为24,紧密度的中位数为 1,特征向量中心为0.207,基于局部平均连接的方法中心性为22,网络中心为24,6个参数均超过中位数的靶点有14个,如图4C所示,推测这些靶点可能是化湿行瘀清热方治疗口腔扁平苔藓的关键靶点。
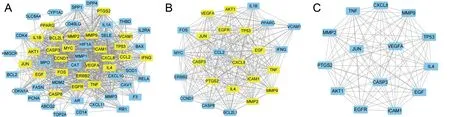
图4 核心PPI的构建过程
2.6 GO和KEGG富集分析 以P<0.05和Q<0.05为筛选条件,对这58个共同靶点基因进行GO富集分析,这些基因包括BP、CC和MF,最后我们得到了2169个GO项目。结果(图5)显示,化湿行瘀清热方通过调节多种生物过程(BP)发挥重要作用。主要5种是细胞对化学应激的反应(GO: 0062197),对金属离子的反应(GO:0010038),对脂多糖的反应(GO:0032496),对细菌来源分子的反应(GO:0002237),对辐射的反应(GO:0009314)。前五大细胞成分(CC)项(P<0.05)为:膜筏(GO:0045121),膜微区(GO:0098857),膜区(GO:0098589),细胞周期蛋白依赖性蛋白激酶全酶复合物(GO:0000307),质膜外侧(GO:0009897)。而主要的5个分子功能(MF)项(P<0.05)为:细胞因子受体结合(GO:0005126),细胞因子活性(GO:0005125),受体配体活性(GO:0048018),信号受体激活剂活性(GO:0030546),蛋白磷酸酶结合(GO:0019903)。通过运行R语言,对58个药物-疾病共同靶点进行KEGG通路富集分析,共获得131条KEGG通路。KEGG途径富集分析基于P< 0.05,结果(图6)显示排名前30的信号通路。根据P值大小、富集靶基因多少和治疗口腔扁平苔藓的相关性,认为重要的信号通路包括IL-17信号通路(hsa04657)和肿瘤坏死因子(TNF)信号通路(hsa04668)。为分析化湿行瘀清热方治疗靶点在白细胞介素17(IL-17)信号通路、TNF信号通路的作用,利用R语言,得到IL-17信号通路和TNF信号通路的模式图,见图7、8。
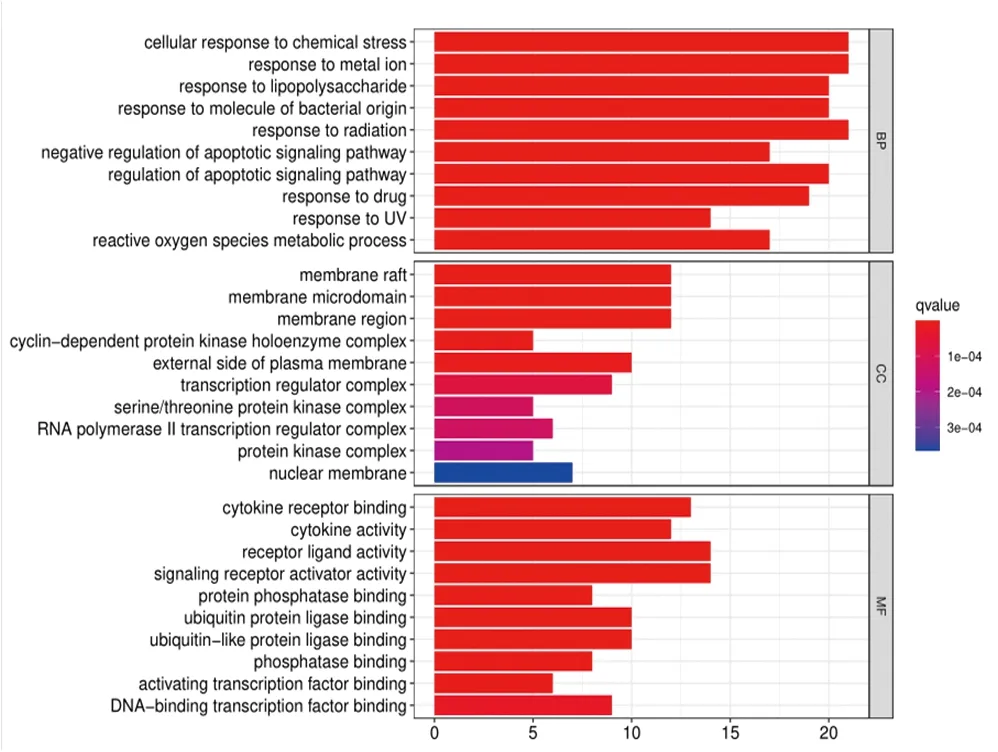
图5 58个药物疾病共同基因的GO富集分析
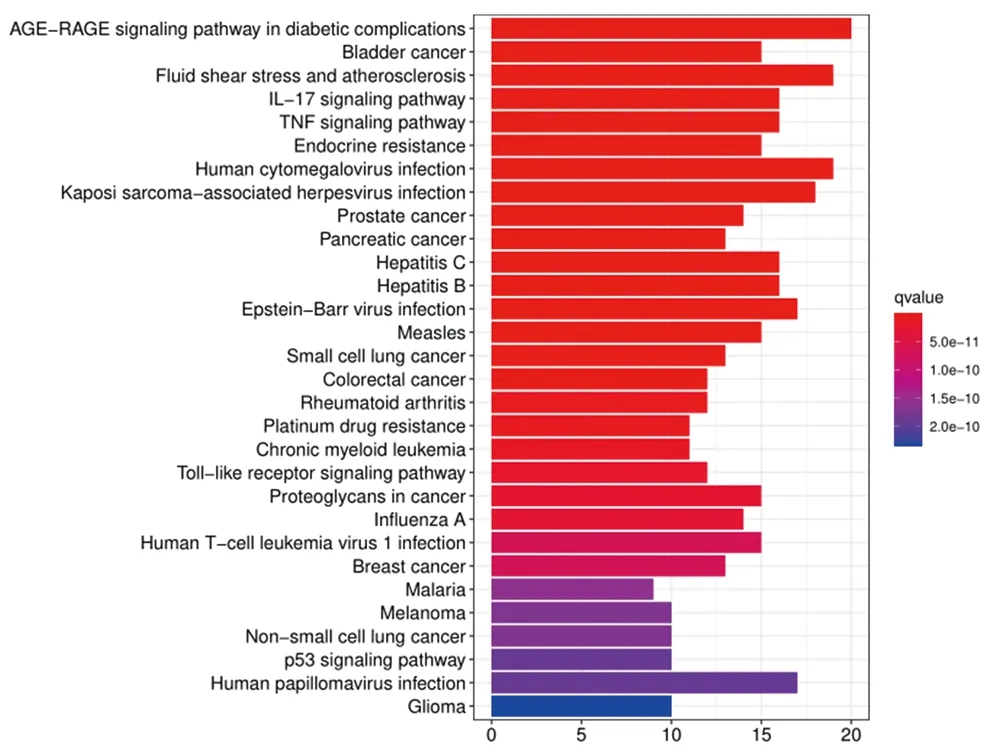
图6 58个药物疾病共同基因的KEGG富集途径
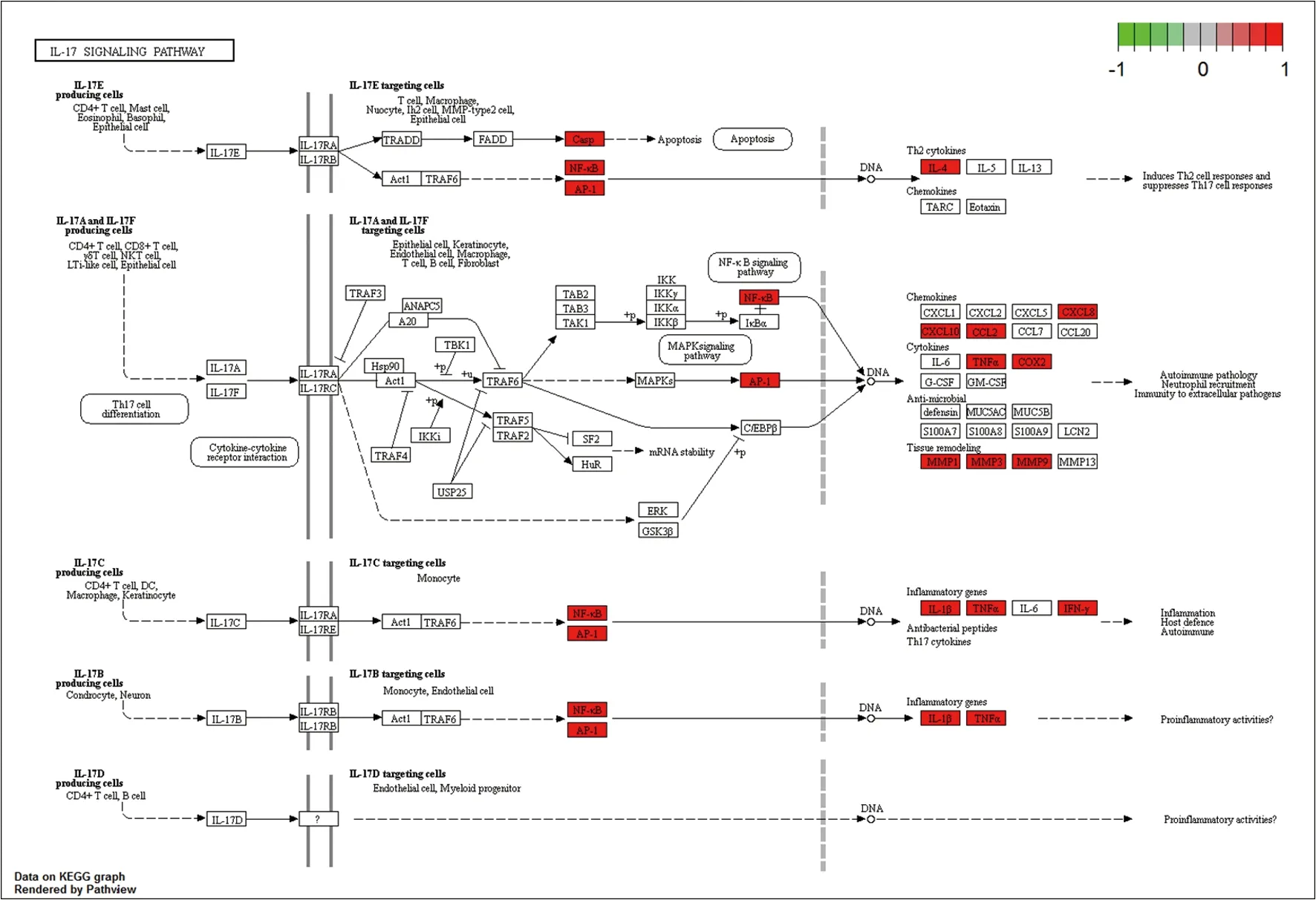
图7 IL-17信号通路
2.7 分子对接结果 为进一步验证化湿行瘀清热方治疗口腔扁平苔藓的的分子机制,从PubChem数据库中提取化湿行瘀清热方的关键有效成分作为配体,从PDB数据库中下载PPI核心网络中的关键靶点作为受体,使用AutoDock Vina软件进行分子对接。一般认为配体和受体结合的构象越稳定,结合能越低,作用的可能性越大,以小于或等于-5.0 kcal/mol的结合能作为判断标准。分子对接结果(表2)显示,化湿行瘀清热方的关键活性成分与关键靶点的结合能均小于-5.0 kcal/mol,表明化湿行瘀清热方剂的关键活性成分与口腔扁平苔藓治疗的关键靶点具有良好的结合活性。其中山奈酚与核心靶蛋白结合情况最佳,蛋白激酶B1(Akt1)是化湿行瘀清热方中关键化学成分结合活性最优的靶蛋白。结合能最高的前4组对接情况如图9所示,蓝色代表药物有效成分;绿色代表药物活性成分靶点;黄色虚线代表药物活性成分与靶点形成的氢键作用,其中Akt1通过氨基酸残基ASP-274、VAL-271和ASN-204与山奈酚形成氢键作用;基质金属蛋白酶-9(MMP-9)通过氨基酸残基ALA-189与槲皮素形成氢键作用,通过氨基酸残基LEU-188与木犀草素形成氢键作用;TNF通过氨基酸残基ILE-58与槲皮素形成氢键作用。
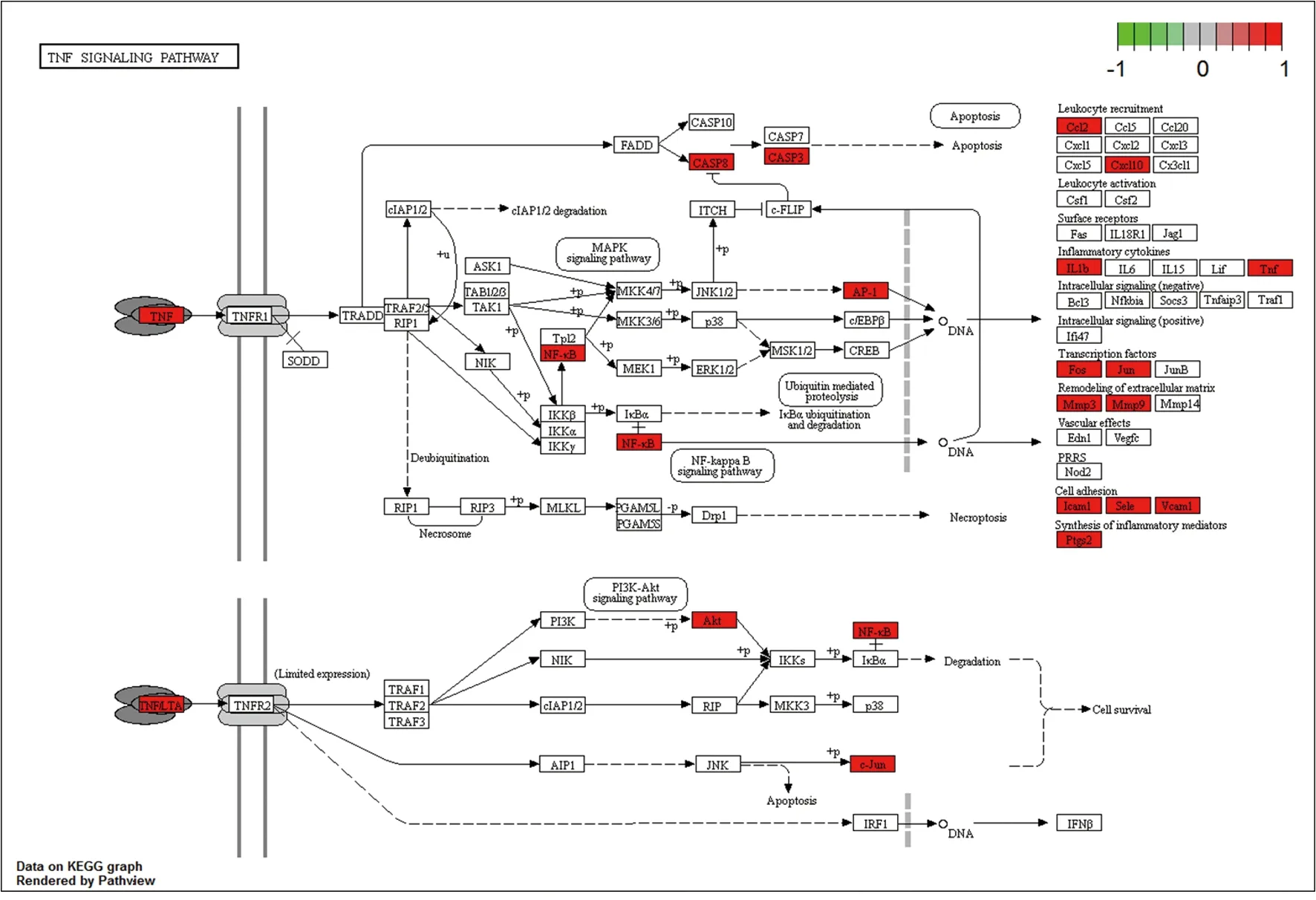
图8 TNF信号通路
3 讨论
目前,口腔扁平苔藓的病因尚不清楚,大多数研究认为口腔扁平苔藓是自身细胞毒性T淋巴细胞介导的免疫反应。中医学将口腔扁平苔藓归为口疮、口糜范畴,主要分为湿热蕴结型、气滞血瘀型、气阴两虚型和肝肾阴虚型,湿热蕴结型和气阴两虚型较常见[8]。化湿行瘀清热方以化湿醒脾、活血化瘀、清热降火为原则,主要由黄柏、赤芍、佩兰、甘草等11味中药组成。方中黄柏、砂仁清热燥湿,健脾化湿;佩兰、茯苓、薏苡仁健脾利湿;赤芍、红花、牡丹皮行气活血化瘀;白鲜皮、金银花清热燥湿;甘草加强清热益水之功。
现代药理研究表明,赤芍可降低血管通透性,改善微循环,促进免疫功能,有利于黏膜上皮修复[9];黄柏可抗炎抑菌,促进组织愈合[10];佩兰有抗炎、抗病原微生物作用[10];甘草可保护、修复黏膜[4]。前期研究显示,化湿行瘀清热方具有调节免疫、炎性反应,改善患者临床症状作用[4,8-12]。
本研究通过网络药理学,从化湿行瘀清热方的11味中药中提取了136种有效成分和对应的58个疾病靶点,并通过分子对接技术进行了验证。根据分析,每种有效活性成分作用于至少一个靶基因,每个基因至少受一种活性成分的调控,表明化湿行瘀清热方通过多组分、多靶点的方式作用于口腔扁平苔藓。靶点数量最多的化湿行瘀清热方活性成分为槲皮素(MOL000098)、木犀草素(MOL000006)、汉黄芩素(MOL000173)和山奈酚(MOL000422),它们可能是化湿行瘀清热方治疗口腔扁平苔藓的关键活性成分。槲皮素具有抗炎、抗病毒及镇痛作用,用于各种炎症[10-11]。槲皮素可抑制MMP-9产生,并通过阻断核转录因子κB(NF-κB)信号通路,减少白细胞介素6(IL-6)、细胞间黏附分子-1(ICAM-1)等炎症因子和趋化因子的产生[13],还可减轻脂多糖诱导的人口腔角质形成细胞损伤[14]。木犀草素是一种天然类黄酮,具有很强的抗氧化和抗炎作用[15]。研究显示木犀草素可能通过抑制NOD样受体热蛋白结构域相关蛋白3(NLRP3)/IL-1β信号通路,减轻牙周组织炎性反应、促进牙槽骨改建[16];木犀草素明显抑制人舌鳞癌细胞增殖,并且可通过抑制MMP-2和MMP-9的表达抑制人舌鳞癌细胞的侵袭和迁移[17],此外它可预防非酒精性脂肪性肝炎[18],抑制骨关节炎和神经炎进展[19-20]。汉黄芩素具有多种药理作用,包括抗炎、抑制肠道炎性反应和维持屏障功能。通过抗炎和抗氧化特性,汉黄芩素可减轻高血糖相关的心肌细胞损伤[21]。山奈酚属于黄酮类苷元,具有较强的抗炎作用[22],可降低牛皮癣皮肤损害中促炎性因子表达,包括IL-6、IL-17A 和肿瘤坏死因子α(TNF-α)[23]。本研究通过网络药理学对化湿行瘀清热方治疗口腔扁平苔藓的关键活性化合物进行预测,部分已在文献中报道,另外一些作用机制研究仍需进一步体内外实验验证。

表2 中药关键有效成分与核心靶点的结合能
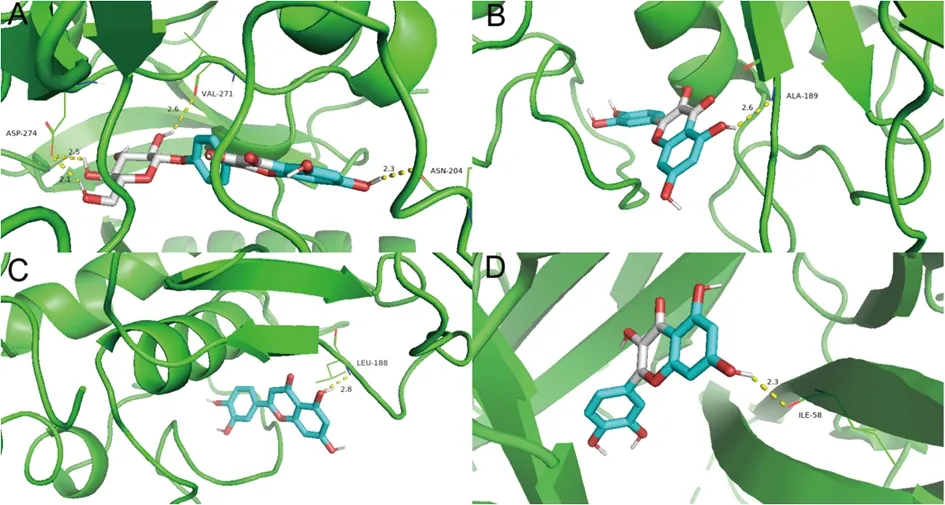
图9 山奈酚与Akt1(A)、槲皮素与MMP-9 (B)、木犀草素与MMP-9 (C)、槲皮素与TNF的分子对接模式图
我们研究核心PPI发现,化湿行瘀清热方的活性成分治疗口腔扁平苔藓的主要靶蛋白为Akt1、VEGFA、TNF、ICAM-1、MMP-9、CASP-3、MMP-2、EGF、EGFR、JUN、IL-4、CXCL-8、TP53、PTGS-2。口腔扁平苔藓是一种慢性炎症疾病。蛋白激酶B/雷帕霉素靶蛋白(Akt/mTOR)介导自噬反应可调节T淋巴细胞的免疫功能[24],此外,Akt/mTOR信号通路失调,影响正常的T淋巴细胞与角质细胞功能,以及使细胞因子调控网络失衡,影响口腔扁平苔藓的发展[25]。血管内皮生长因子A(VEGFA)经基因芯片检测,逆转录-聚合酶链式反应 (Reverse Transcription-Rolymerase Chain Reaction,RT-PCR)验证,发现在口腔扁平苔藓患者中表达增高[26],并具有很强的促进血管生成作用,进而介导口腔扁平苔藓慢性炎症的进展。TNF是炎性反应的关键调节因子,其促炎作用可通过改变白细胞黏附分子、促炎因子和基质金属蛋白酶的表达来体现[27-28]。细胞间黏附分子1(ICAM-1)不仅促进免疫和炎性反应,还可促进白细胞游离出血管[29],免疫组化结果显示,与正常皮肤相比,口腔扁平苔藓患者TNF和ICAM-1的阳性表达率较高,且二者之间存在显著相关性[30],受炎性介质TNF诱导,MMP-9、VEGF、ICAM-1表达增加,导致基底细胞液化变性,口腔扁平苔藓血管生成,以及淋巴细胞的浸润到特定部位[30-31]。高表达的MMP-9和胱天蛋白酶3(CASP-3)可促进角质形成细胞的凋亡[32],MMP-9和MMP-2与口腔扁平苔藓的发生及癌变有关[33]。表皮细胞生长因子/表皮细胞生长因子受体(EGF/EGFR)影响细胞的增殖、分化和迁移[34],糜烂型口腔扁平苔藓中EGFR表达较网状型及正常组织明显增高,EGF/EGFR信号通路可能参与糜烂型口腔扁平苔藓的癌变[35]。JUN属于转录激活因子-1(AP-1)转录因子复合物,调节炎性过程以及细胞的增殖分化[36],JUN与EGFR均是影响口腔扁平苔藓发生发展的关键因子[37],此外它们可能参与糜烂型口腔扁平苔藓的癌变过程[35]。IL-4表达水平可作为反映口腔扁平苔藓严重程度的标志物[38],IL-25通过增强IL-4和趋化因子CXCL-8表达可促进辅助型T淋巴细胞2(Th2)在口腔扁平苔藓疾病中的免疫反应[39]。前期临床试验表明,化湿行瘀清热方能明显降低患者唾液、血液中ICAM-1、MMP-9表达,改善患者临床症状[9,40]。
为深入研究化湿行瘀清热方治疗口腔扁平苔藓的作用机制,我们使用R语言对药物-疾病共同靶点进行GO和KEGG富集分析。GO分析结果表明化湿行瘀清热方治疗口腔扁平苔藓涉及的生物学过程主要是对细菌来源分子的反应,对脂多糖的反应及细胞因子活性、细胞因子受体结合、受体配体活性等分子生物学过程。KEGG富集分析结果表明,药物-疾病共同靶点主要富集在炎症免疫、病毒感染以及肿瘤相关通路,其中IL-17信号通路和TNF信号通路是化湿行瘀清热方参与治疗口腔扁平苔藓的关键通路。前期使用基因芯片技术筛选出与口腔扁平苔藓发病相关的8条通路,其中感染类疾病相关通路在口腔扁平苔藓的发生发展中发挥重要作用,这与此次网络药理学分析结果一致[41]。IL-17由辅助性T淋巴细胞17(Th17)细胞分泌,并被证实参与炎症、自身免疫等过程[42],IL-17可诱导角化细胞释放趋化因子配体20(CCL20),促进炎性细胞向扁平苔藓病损的迁徙和浸润[43],IL-23/IL-17通路的激活与MMP-9的高表达相关,并且参与了扁平苔藓的发病[44]。在口腔扁平苔藓中,NF-κB信号通路的激活,可促进TNF-α及IL-1β的高表达,口腔扁平苔藓患者唾液中,NF-κB依赖因子TNF-α、IL-1、IL-6和IL-8的高表达可用于诊断与治疗口腔扁平苔藓[45-46]。此外,复方甘草酸苷及养阴益气、理气活血中药治疗口腔扁平苔藓、降低TNF表达已得到研究[47-50]。由此可见,化湿行瘀清热方可能通过IL-17信号通路、TNF信号通路等发挥抗炎、抗感染作用,治疗口腔扁平苔藓。
分子对接结果表明,中药关键有效成分槲皮素、木犀草素、汉黄芩素和山奈酚与Akt1、MMP-9和TNF等核心靶点结合亲和力较强,说明化湿行瘀清热方可与受体蛋白稳定结合并发挥作用,作用机制多样活跃,具有潜在的研究价值。
口腔扁平苔藓是一种病因不明的免疫性炎症性黏膜疾病,可能由多种基因和因素引起,中医治疗强调各种中草药的组合,通过多方面、多角度的整体治疗,通过网络药理学分析化湿行瘀清热方治疗口腔扁平苔藓恰好证实这一点,然而中药方剂成分复杂,需进一步研究来支持本研究结果。
化湿行瘀清热方治疗口腔扁平苔藓在临床中取得了较好的疗效,本研究通过中药网络药理学,构建了药物疾病网络,发现了化湿行瘀清热方剂的主要活性成分和靶点并分析该药物的作用机制,通过分子对接对结果进行了验证,与前期研究及文献报道治疗口腔扁平苔藓的机制一致。这表明化湿行瘀清热方通过多成分、多靶点治疗口腔扁平苔藓,作用机制可能与IL-17信号通路和TNF信号通路相关。
