曲妥珠单抗联合含多柔比星脂质体治疗HER-2 阳性晚期乳腺癌临床疗效观察
2021-11-15刘小利荀雷
刘小利 荀雷
(河南科技大学第一附属医院甲状腺乳腺肿瘤外科,河南 洛阳 471000)
乳腺癌是乳腺细胞生长失去控制所引起的常见恶性肿瘤疾病之一,近年来,乳腺癌的发病率逐渐上升且年轻化,占据了女性发病的首位,据相关文献显示[1~2],乳腺癌中的HER-2 阳性乳腺癌占乳腺癌总数的20%~30%,其具有恶性程度高、病情发展迅速、容易发生淋巴结转移等特点。
临床上在对HER-2阳性晚期乳腺癌的治疗中主要以化疗为主,但是随着医学领域对癌症疾病进展的高度重视,对癌症的研究也逐渐深入,以HER-2 靶向联合治疗成为了一线治疗。有研究报道[3],曲妥珠单抗的靶点作用于HER-2,同时联合使用多柔比星脂质体抑制细胞DNA 的复制,能够有效杀死肿瘤细胞,达到抗肿瘤的目的。
本研究观察曲妥珠单抗联合含多柔比星脂质体治疗HER-2 阳性晚期乳腺癌临床疗效,为临床诊疗工作提供参考依据,现报告如下。
1 资料与方法
1.1 一般资料
选取2018 年5 月~2020 年9 月我院收入治疗的HER-2 阳性晚期乳腺癌患者,共80 例,为研究对象。根据治疗方式不同将80 例HER-2 阳性晚期乳腺癌患者分为基础组(40 例)和联合组(40例)。所有患者均为女性。
基础组:年龄29~73 岁,平均年龄(42.94±8.27)岁;体力状况评分[4]:0~1 分30 例,2 分10 例;HER-2(+)7 例,HER-2(++)16 例,HER-2(+++)17 例。
联合组:年龄30~70 岁,平均年龄(45.74±7.36)岁;体力状况评分:0~1 分28 例,2 分12 例;HER-2(+)5 例,HER-2(++)17 例,HER-2(+++)18 例。两组患者在年龄、体力状况、病情等基本情况上相比较,差异无统计学意义(P>0.05)。具有可比性。
1.2 纳入标准
(1)所有患者具有详细、完整的病例资料,包含肿瘤标志物等检查的结果;(2)所有患者均符合乳腺癌的诊断标准[5],并且已经过病理组织学检查明确诊断;(3)所有患者预计生存时间>3个月;(4)患者及其家属均已了解本次治疗方法,自愿参加并已签署知情同意书。
1.3 排除标准
(1)已排除合并重大恶性肿瘤的患者;(2)已排除有手术史、外伤史的患者;(3)排除合并精神障碍及心理疾病的患者;(4)排除耐受差无法进行化疗的患者。
1.4 方法
基础组予以盐酸多柔比星脂质体注射液(生产厂家:常州金远药业制造有限公司;国药准字:H20123273)治疗,具体治疗方法如下:盐酸多柔比星脂质体注射液20mg·m-2静脉滴注,环磷酰胺(生产厂家:山西普德药业有限公司;国药准字:H14023686)500mg·m-2静脉滴注;每周给药1 次,连用2 周后停药1 周,以此为一个疗程,持续治疗4 个疗程。
联合组在基础组治疗的基础上加用曲妥珠单抗(生产厂家:上海复宏汉霖生物制药有限公司;国药准字:S20200019)治疗,使用方法如下:患者初始计量为4mg·kg-1,静脉滴注60min,后续剂量减半,每3 周用药2mg·kg-1,静脉滴注30~60min,3 周为一个疗程,持续治疗4 个疗程。
1.5 评价指标
(1)两组患者治疗后临床疗效判定[6]:①完全缓解:目标病灶完全或基本消失,肿瘤标志物的血清水平降至正常,并且维持时间不少于4 周;②部分缓解:目标病灶最长径之和减少不低于30%,病灶部位无扩大,也没有新发病灶,肿瘤标志物的血清水平下降大于65%,并且维持时间不少于4 周;③未缓解:目标病灶最长径之和扩大超过20%,患者肿瘤标志物血清水平没有下降,反而升高超过40%,甚至出现新发病灶。总有效率=(完全缓解+部分缓解)/总例数×100%。
(2)记录患者入院前后的肿瘤标志物血清水平:癌胚抗原(Carcinoembryonic antigen,CEA)、CA153 乳腺癌抗原、组织多肽特异性抗原(Tissue polypeptide specific antigen,TPS)。
(3)观察两组患者治疗过程中有无发生恶心呕吐、头痛、肝功能异常、脱发及血液系统异常等不良反应。
1.6 统计方法
本研究数据均采用SPSS18.0 软件进行统计分析,计量资料通过平均数±标准差(X±S)描述,采用t检验;计数资料通过率或构成比描述,并采用χ2检验,以P<0.05 为差异具有统计学意义。
2 结果
2.1 两组临床疗效对比
治疗疗程结束后,联合组的临床总有效率为90.00%显著优于基础组的临床总有效率70.00%,两组之间疗效对比(P<0.05)。(详情见表1)。
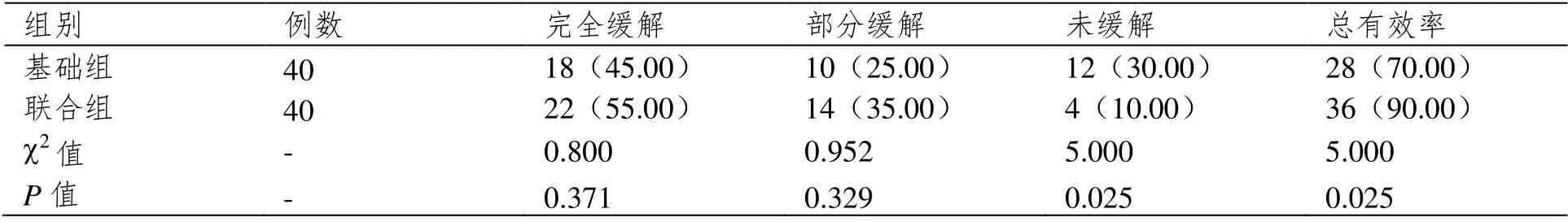
表1 两组临床疗效对比[n(%)]
2.2 两组治疗前后肿瘤标志物血清水平对比
两组患者治疗后的肿瘤标志物血清水平均较治疗前明显降低,且联合组下降水平优于基础组(P<0.05)。(详情见表2)。
表2 两组治疗前后肿瘤标志物血清水平对比[±SD]
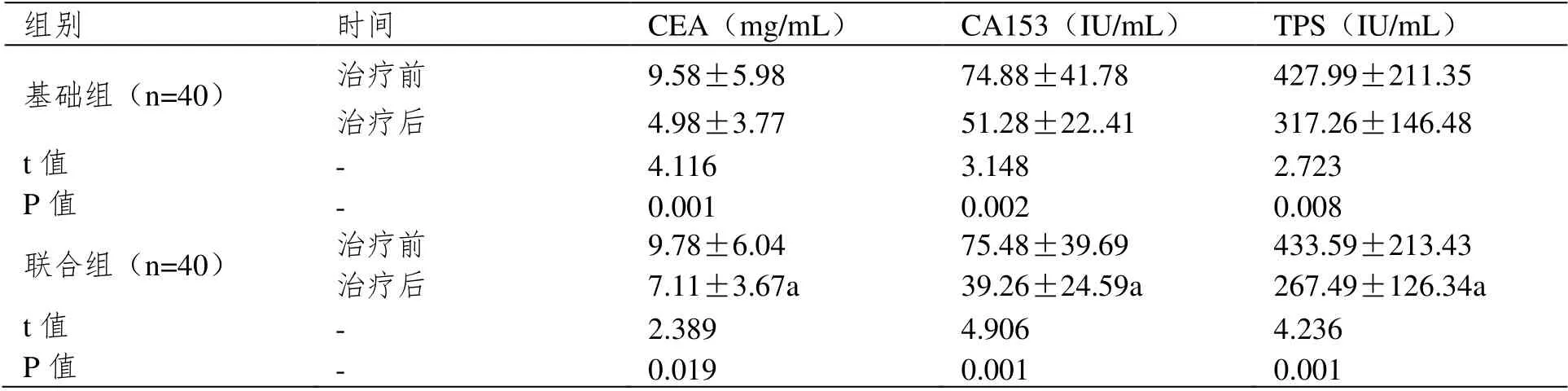
表2 两组治疗前后肿瘤标志物血清水平对比[±SD]
注:治疗后,与基础组对比,aP<0.05。
组别 时间 CEA(mg/mL) CA153(IU/mL) TPS(IU/mL)基础组(n=40) 治疗前 9.58±5.98 74.88±41.78 427.99±211.35治疗后 4.98±3.77 51.28±22..41 317.26±146.48 t 值 - 4.116 3.148 2.723 P 值 - 0.001 0.002 0.008联合组(n=40) 治疗前 9.78±6.04 75.48±39.69 433.59±213.43治疗后 7.11±3.67a 39.26±24.59a 267.49±126.34a t 值 - 2.389 4.906 4.236 P 值 - 0.019 0.001 0.001
2.3 两组不良反应对比
基础组患者有6 例出现恶心呕吐、2 例出现头痛、1 例出现脱发,不良反应总发生率为22.50%;联合组患者有4 例出现恶心呕吐、2 例出现头痛,不良反应总发生率为15.00%。两组患者不良反应发生率对比无差异,无统计学意义(P>0.05)。
3 讨论
乳腺癌的致死率较高,特别是HER-2 阳性的患者,机体状况差、治疗后复发转移的可能性大,生存期较短,在临床上引起了高度重视。乳腺癌肿瘤的增值指数高,病情进展迅速,并且激素受体呈阴性的比例更高,在临床上对乳腺癌治疗方式的选择取决于癌症的类型和分析,最常用的方式包括手术、化疗、放疗及激素治疗。
研究表明[7~8],单纯的化疗或内分泌治疗并不能达到稳定的临床效果,而靶向药物治疗可以针对性的作用于细胞癌变的具体过程中,抗肿瘤血管形成,在分子水平控制肿瘤细胞的分化,促进其消亡,从而达到乳腺癌治疗的临床效果。曲妥珠单抗是重组人源化单克隆抗体,具有抗HER-2的作用,也是乳腺癌治疗的靶向药物,通过介导HER-2 受体使细胞表面密度降低,达到抑制肿瘤细胞生长的作用,联合蒽环类广谱抗肿瘤药物多柔比星脂质体治疗HER-2 阳性晚期乳腺癌患者,具有长效、毒性低的优点。
本研究结果中,曲妥珠单抗联合含多柔比星脂质体治疗的临床总有效率高于单独使用多柔比星脂质体治疗的临床总有效率,并且不良反应发生情况少,证实联合用药临床治疗效果更为显著,能够改善患者预后。
综上所述,曲妥珠单抗联合含多柔比星脂质体治疗HER-2 阳性晚期乳腺癌临床疗效显著,不良反应发生情况少,能够改善乳腺癌患者的生活质量和预后,具有使用价值。
