多指标权重分析法结合影响因素试验优选紫前款甘散生产工艺
2021-11-11康诵垚王金泉王春元赵红琼杨芬芳郝智慧
康诵垚,王金泉,王春元 , 赵红琼,杨芬芳,郝智慧
(1.青岛农业大学 病原微生物与新药生物创制实验室,山东 青岛 266000;2.新疆农业大学动物医学学院,新疆 乌鲁木齐 830001;3.中国农业大学动物医学院,北京 海淀 100193)
紫前款甘散由紫菀、款冬花、枇杷叶、前胡、白前、甘草共 6 味药材配比而成,是在传统经典方法的基础上开发研制而成的一种中药复方散剂,根据中药材的现有药理、化学等研究资料[1-3],同时考虑实际生产[4-5]的特点,制备工艺采用“原方药材粉碎一过筛一混匀一分装成型”设计,目的是在保持原药方的化学组成的基础上,进一步提高含药量,同时达到使配制工艺流畅、大生产重复可行的目的。本试验在前期研究基础上,进行了中试放大生产,以确保工艺达到生产稳定性和可操作性,进而保证产品安全、有效和质量可控,并且初步研究影响其稳定性的各项因素,为紫前款甘散的生产、运输、储存等提供依据。
1 材料与方法
1.1 药材与试剂 原料药:紫菀(批号:171211)、款冬花(批号:170701)、枇杷叶(批号:180501)、前胡(批号:170701)、白前(批号:180301)、甘草(批号:180501),均购于豪州市济生堂中药饮片有限公司。紫前款甘散,批号:20181119、20181120、20181121,规格:500 g/袋,由青岛中仁药业有限公司提供。对照药材:枇杷叶(批号:121261~201303)、前胡对照药材(批号:120951~201706)、甘草对照药材(批号:120904~201519)。对照品:紫菀酮(批号:111581~20160,含量以 99.8%计)、白花前胡甲素(批号:111711~201703,含量以 98.8%计)、白花前胡乙素(批号:111904~201203,含量以 98.0%计)、熊果酸对照品(批号:110742~01823,含量以 94.7% 计),均购自中国食品药品检定研究院。
1.2 试验仪器 高效液相色谱仪Agilent 1200 型,安捷伦科技有限公司;显微镜BX-53型,奥林巴斯公司;电子天平AL204型,梅特勒-托利多公司;小型高速粉碎机WK-1600A型;水浴恒温摇床SHZ-C型,杭州川一实验仪器有限公司;玻璃干燥器、漏斗、坐标纸、铁架台、直尺。
1.3 方法
1.3.1 处方及制备 组成:紫菀、前胡、款冬花、甘草、枇杷叶、白前共6味药材。工艺路线:原方药材粉碎一过筛一混匀一分装成型[2]。成型制备工艺:单方药材饮片符合2015年版《中国兽药典》[6]中规定的各药材饮片的含水量要求进行一般粉碎处理,过24目筛,混合均匀,制成散剂。
1.3.2 含水量的测定 参照 2015 年版《中国兽药典》[6](二部)附录 0832 进行测定:取粉末3 g,平铺于干燥至恒重的扁形称量瓶中,精密称定,开启瓶盖在 100~105 ℃干燥5 h,将瓶盖盖好,移置干燥器中,放冷30 min,精密称定,再在上述温度干燥1 h,放冷,称质量,至连续2次称质量的差异不超过5 mg为止。由减失的质量计算含水量(%)。
1.3.3 物料含水量对粉碎效果的影响 按照处方中各药材比例平行取0.1个处方量药材饮片8份,进行干燥(50~60 ℃)、测定水分后,最大程度进行粉碎,每次15 s,每次粉碎完成之后过筛,称滤渣,直到相邻的2次粉碎之间的药渣量少于1 g或目测基本无变化,即粉碎完成,统计粉碎次数,计算出粉率[7]。
1.3.4 粉碎工艺重复性验证试验 各药材检测符合药典规定的各药材水分含量要求后,按处方配比称取0.2个处方量的药材饮片,共3份,粉碎15 s每次,每次粉碎完成之后过2号筛,重复4次,最后称取过2号筛粉末的重量计算出粉率。
1.3.5 混匀工艺的考察 将3批散剂粉末分别装入8#自封袋中,进行混匀,每次混匀10 s,依据2015年版《中国兽药典》(二部)附录散剂(外观均匀度)[6]评价药材粉末是否混合均匀。
1.3.6 小试生产工艺的重复性考察 按照已研究过的生产工艺生产3批小试样品,批号分别为2018061201、2018061202、2018061203,并根据《中国兽药典》(二部)附录0101中散剂通则进行相关项目的检查。
1.3.7 临界相对湿度的测定 将3个批次的样品细粉进行干燥并至恒重,将厚约2 mm的细粉置于已经恒重的称量瓶底部,精密称重后分别置于盛有不同湿度的饱和盐溶液干燥器中(称量瓶盖子打开),在25 ℃恒温培养箱中保持7 d后称重,计算吸湿百分数[8]。
吸湿率(%)=吸湿前后细粉重量差/吸湿前细粉重量×100%
1.3.8 松密度的测定 松密度又被称为堆密度(Bulk density),即单位容积粉末的质量,精密称定量筒(10 mL)的重量,再将药粉进行填充,在保证试验条件一致的基础上采用一定方式使量筒振动(振动直至药粉体积为10 mL并不再变化为止),精密称重药粉和量筒重量,根据公式ρ=m/v(其中ρ是松密度,g/mL;m为粉体的质量,g;v是粉体的填充体积,mL),即为松密度[9]。
1.3.9 休止角的测定 取制备的3批散剂(含水量约为5%),用串联漏斗法测定其休角,平行样每批次3份,测得散剂α均值[10]。
1.3.10 中试研究 根据《兽药研究技术指导原则》中对兽用中药、天然药物中试研究技术指导原则的要求下,对小试的生产工艺进一步,根据实际生产中的设备规模及生产成本核算进行适当调整,药材70 kg,全面考核其生产工艺指标,对药材和成品进行质量评定[11]。
1.3.11 影响因素试验 依照 2015 年版《中国兽药典》[6](二部)和《兽药研究技术指导原则》[11]的要求,取紫前款甘散3批(批号:20181119、20181120、20181121),按市售包装进行高温试验(60 ℃,10 d)、高湿试验(25 ℃,RH90%±5%,10 d)、强光照射试验[照度(4 500±500)lx,10 d]分别在第 0、5天和第10天,按稳定性重点考察项目取样进行检测。
2 结果
2.1 含水量的测定 结果表明饮片干燥6~9 h含水量约为6.299%,粉碎次数为3次,最高出粉率为94.44%,结果表明,各干燥组之间最大出粉率相差不大,基于生产工艺简单可行及节能减排的原则,在实际生产中单方药材含水量符合药典规定后,适当延长粉碎时长,直接粉碎即可,结果见表1。
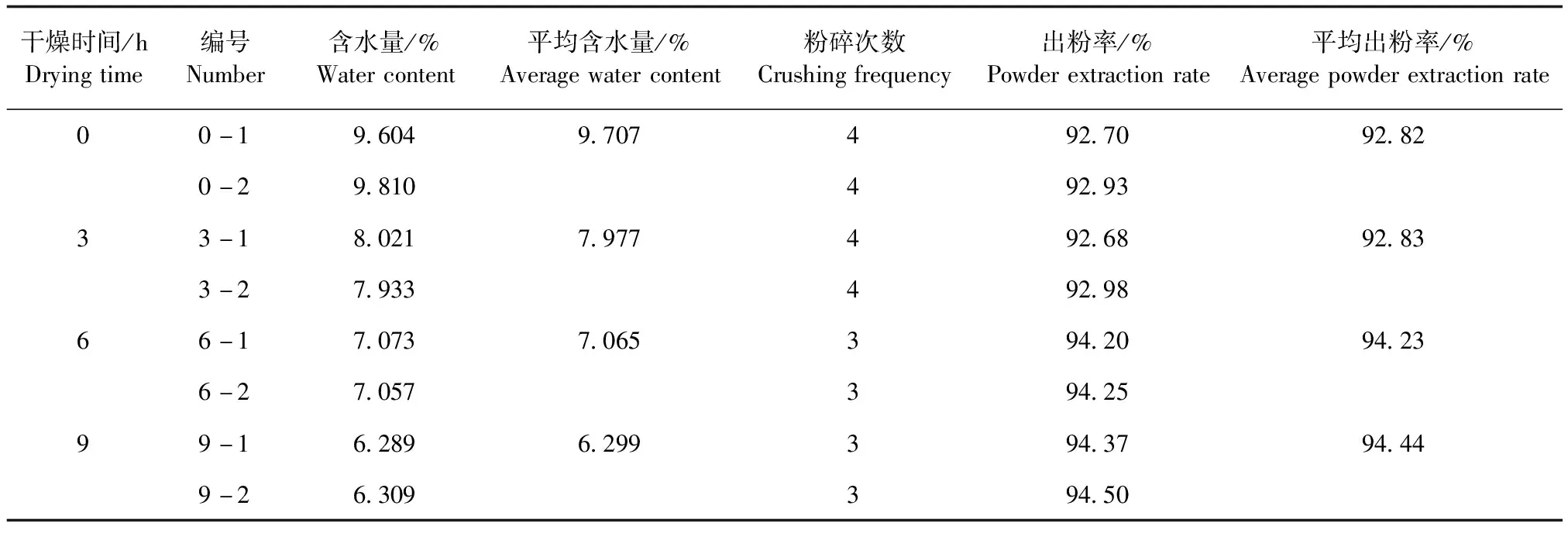
表1 物料含水量对粉碎效果影响的考察试验结果
2.2 粉碎工艺重复性验证 结果表明平均出粉率为92.34%,RSD为0.461 1,结果重复性好,最终确定实验室小试粉碎工艺为每次粉碎15 s,每次完成之后过筛,重复4次,最后称取过2号筛即得,结果见表2。

表2 粉碎工艺重复性验证试验结果
2.3 混匀工艺的考察 每组粉末混合,每次10 s,重复3次即符合散剂外观均匀度的要求,所得实验室小试混匀工艺为每次混匀10 s,重复3次即可。
2.4 小试生产工艺的重复性考察 试验结果可知,小试生产工艺稳定,符合《中国兽药典》[7](二部)附录 0101 中散剂通则中的相关规定,结果见表3。

表3 小试生产工艺的重复性考察试验结果
2.5 临界相对湿度的测定 根据表4中数据作图,纵坐标为吸湿百分率,横坐标为相对湿度,作图获得吸湿曲线并做切线,其临界相对湿度值为2条切线的交点所对应的横坐标,得到紫前款甘散的临界相对湿度(CRH)为69.85%。散剂在生产、分装等过程中应控制环境相对湿度在69.85%以下。

表4 吸湿率测定结果
2.6 松密度的测定 测得紫前款甘散的平均松密度为0.497 6 g/mL(RSD<1.05%),平均为(498±4.75)g/L,实际生产中装量为500 g时宜采用容积>1 000.9 cm3的包装,结果见表5。

表5 松密度试验测定结果
2.7 休止角的测定 测得紫前款甘散的平均休止角为 30.07°(RSD<0.95%),平均值为(30.07± 0.26)°,理论认为当休止角的角度越小时,表明其受到的摩擦力越小,其粉体的流动性越好,α≤45°说明紫前款甘散的流动性可以满足生产过程中需求,结果见表6。

表6 3批散剂的休止角α测定结果
2.8 中试研究 由表7可知,按所投料量来计算,理论应生产140袋(500 g/袋)成品,实际生产成品135袋,其成品率不低于96%。工艺生产条件符合工厂大生产要求,可操作性较强,成品药材、半成品质量可控,成品质量稳定。

表7 中试生产成品的质量检测数据
2.9 影响因素试验 紫前款甘散的性状、薄层鉴别、含水量及外观均匀度均未发生明显变化,说明在高温、高温及强光照射条件下放置10 d,各组分的稳定性较好。见表8、9、10。

表8 高温试验结果

表9 高湿试验结果
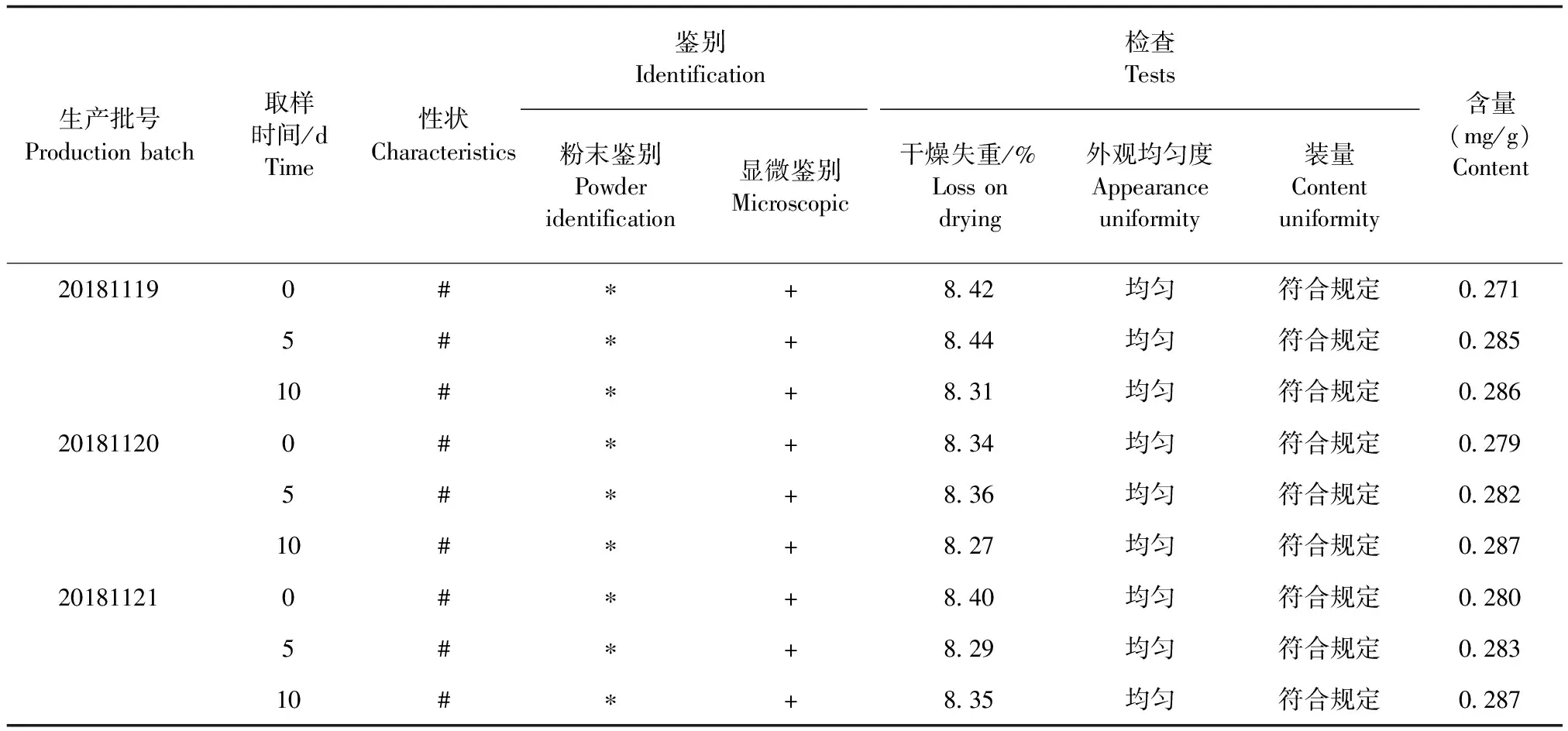
表10 强光照射试验结果
3 结论
散剂作为中药的传统剂型,具有易吸收、起效快、制作工艺简单等特点。在我国用药历史上有着不可替代的优势[12-14]。在前期研究基础上,本试验在实验室范围内进一步考察优选紫前款甘散的制备成型工艺,考察工艺参数,进一步提高了该制剂的质量并放大工艺进行中试生产使其能实际生产推广,利于中药现代化的发展。
根据试验结果对处方中药材饮片含水量进行考察,当含水量从9.707%经烘干至6.299% 时,药材粉碎时间只增加了15 s,出粉率相差1.62%,说明在实际生产中基于生产工艺简单可行及节能减排的原则,在单方药材含水量符合药典规定的前提下,适当延长粉碎时长,直接粉碎即可,然后又对其粉碎工艺的重复性进行了考察,其平均出粉率达到92.34%。在出粉率方面,现在制剂生产时的出粉率也在 90.00%左右,没有明显差别,物料利用率相近,说明其粉碎工艺稳定可行。采用吸湿增重法测定紫前款甘散的的临界相对湿度为 69.85%,说明本品极易吸湿,因此在实际生产时其环境湿度应<69.85%,外包装的密封性要好,并贮存于阴凉、干燥的环境中。粉末的流动性对于生产工艺非常重要[15],粉末的流动性可以通过对休止角的测定来判断,在重力场中,休止角是指在粉体堆积层的自由斜面上粒子滑动时,所受的重力和粒子之间的摩擦力达到平衡而处于静止状态时所测得的最大角,理论认为,当休止角的角度越小时,表明其受到的摩擦力越小,其粉体的流动性越好,一般认为休止角≤45° 时可以满足生产过程中对粉体流动性的要求,通过串联漏斗法对紫前款甘散的休止角进行了重复测定,α为(30.07± 0.26)°,<45°说明紫前款甘散可以满足生产过程中的流动性需求。松密度的测定在指导产品包装中起着非常重要的意义,采用质量体积法测定松密度为(498±4.75)g/L,说明该散剂较轻,密度较小,在包装规格的选择过程中,根据实际情况尽量选择略大一点的包装。对其小试工艺在工厂进行了放大生产,其成品率>96%并且成品质量检测后均符合规定,证明该制剂工艺适用于实际生产。根据影响因素试验结果来看,除在相对湿度为>92.5%的高湿条件下原料药物吸湿性有改变,有轻微吸潮,内容物色泽性状未发生变化外,其他相关考查项目均符合规定。不论是温度还是光照条件的改变,对成品均无显著的影响。湿度试验结果显示,本制剂的内容物有轻微改变,表明紫前款甘散具有一定程度的吸湿性,但吸湿后主要成分的含量没有明显降低,综合衡量各种影响因素,故建议紫前款甘散及原料药在生产、运输、贮存过程中应尽量保持干燥,避免高湿环境,从而保证本制剂使用安全、稳定、有效。
综上所述,本试验方法简便易行、稳定可靠,可为紫前款甘散的实际生产应用提供可靠保证。
