Bilobalide的全合成
2021-10-27郭文改
郭文改,顾 凡
(温州大学,浙江 温州 325000)
1 天然产物Bilobalide
银杏提取物在中国民间医学中被使用,已经有5000多年的历史,长期以来被认为是中药的主要成分,广泛用于老年人的脑血管疾病和外周循环疾病的治疗。随着科技水平的不断提升,白果内酯目前被广泛作为神经精神病药物,用于治疗神经病、脑病和脊髓病、抗衰老等。
Bilobalide属倍半萜内酯,是目前从银杏叶中发现的唯一的1个倍半萜内酯化合物。1967年,在Major R. T.等人[1]首次从银杏中提取出Ginkgolides之后,1969年,Weinaes K.等人[2]也成功地从银杏中提取出了Bilobalide。
1971年,Nakanishi K.等人[3]通过质谱发现,Bilobalide是一种稀有的含叔丁基的物质,采用核磁共振对质子进行表征后发现,C-9是季碳原子,NOE表明与叔丁基直接相关联的是氢。最终,确定分子式为3个五元内脂和1个五元环。
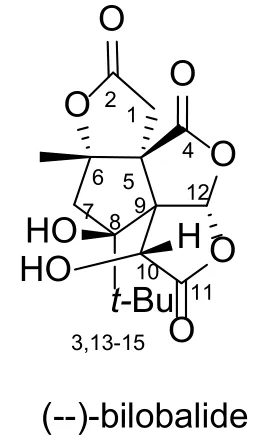
2 Bilobalide的合成方法
Bilobalide在银杏叶和根皮中的含量极低,且尚未被发现存在于其他植物中,这给Bilobalide的提取和纯化带来了很大难度。此外,Bilobalide超级拥挤的立体结构和不稳定性,也给合成带来了极大的挑战。截止到目前,只有3个课题组完成了Bilobalide的全合成。
2.1 Corey E. J.合成法(24 steps synthesis)
首次合成(±)-Bilobalide的合成路线[4]:
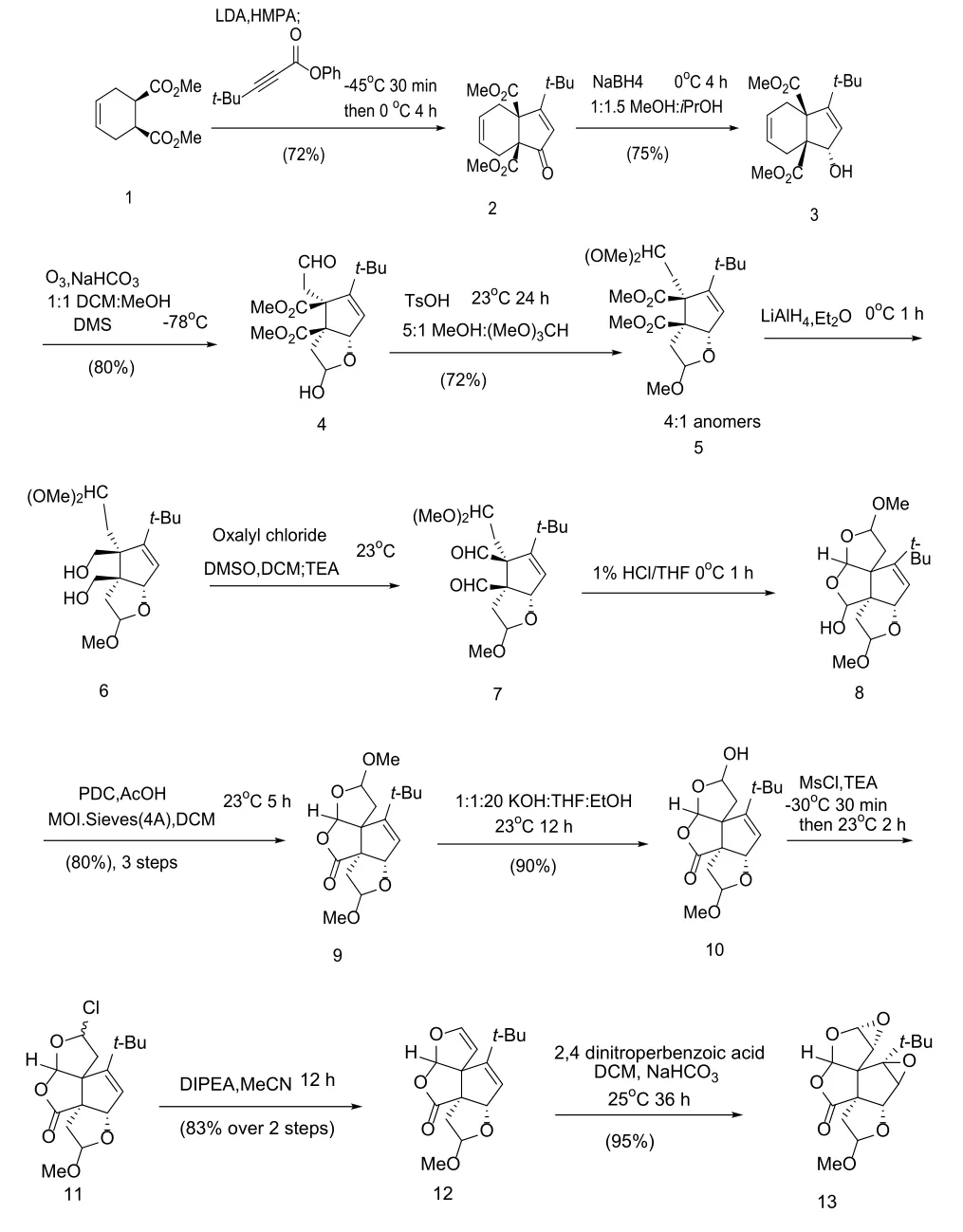
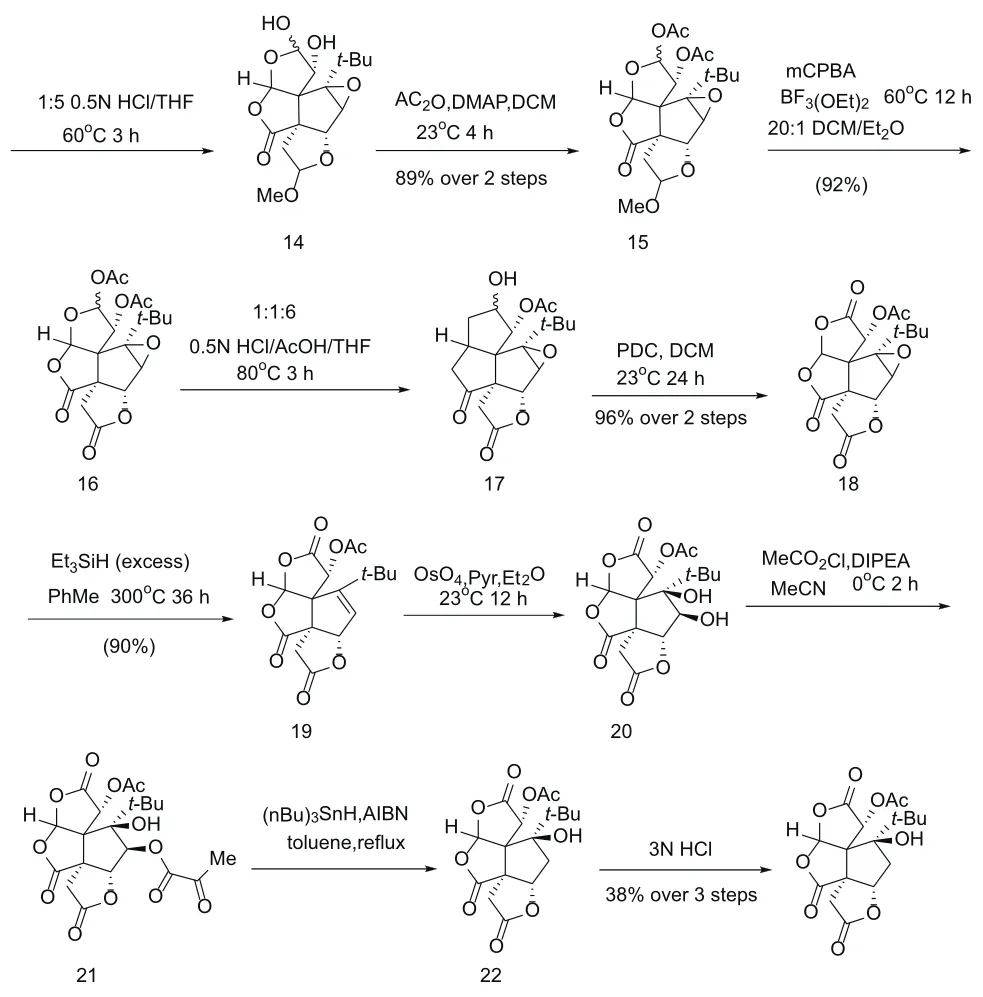
具体步骤:化合物2包含了Bilobalide合成需要的所有碳原子。以化合物1为原料,通过一步反应来生成化合物2,用硼氢化钠对化合物2进行还原,得到具有立体选择性的化合物3,化合物3通过臭氧化反应得到中间产物,中间产物通过二甲基硫醚还原得到化合物4。保护羟基和醛基,然后将2个酯基用氢化铝锂还原后,再经过一步氧化得到化合物7。在酸性条件下,化合物7经过环化、分子筛纯化和重铬酸吡啶盐氧化后得到化合物9,甲氧基被羟基选择性地取代后得到化合物10。化合物10通过氯化反应,脱去1分子的氯化氢后生成化合物12。对化合物12进行环氧化,然后将环氧化产物选择性地转化为二醇,二醇再在酸酐条件下形成醋酸酯。化合物15在酸性条件下转化为2分子的内脂化合物16,酸性条件下选择性地对酯水解,然后经重铬酸吡啶盐氧化,得到化合物18。此时对环氧化合物进行氢化,似乎就可以得到Bilobalide,但在实际中这种情况很难实现。化合物18脱氧得到烯烃,再在四氧化锇的氧化下得到双羟基化合物。将另1个羟基脱去得到化合物22后,再在酸性条件下生成Bilobalide。
合成难点:要使用高选择性的反应,以使反应合成理想的目标物质。一步合成化合物2是前所未有的;从化合物7到化合物9的环化反应和氧化反应非常难。
缺点:合成步骤繁琐;合成需经多步氧化和还原过程才能完成;合成产率低。
2.2 Michael T. Crimmins合成法(17 steps synthesis)
逆合成分析[5]:
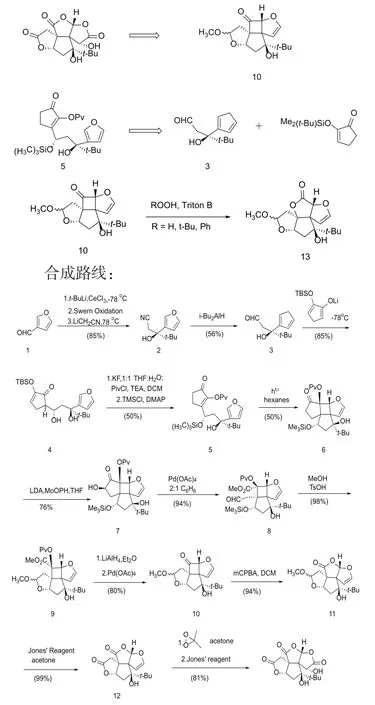
具体步骤:以商业化的3-呋喃甲醛为原料,在t-BuCeCl2中生成二级醇,通过Swern氧化转化为酮。酮在锂化腈的作用下生成化合物2。在酸性条件下,化合物2在二异丁基铝氢化物的作用下,将氰基转化为醛基。将化合物3加入化合物2当量的锂烯酮中生成异构体4,再通过氟化钾处理异构体。水解TBS产生烯醇,发生酰基化反应,然后通过TMSCl对羟基进行保护,得到化合物5。在光照下生成80%的混合物后,分离得到50%的理想产物6,再在MoOPH下通过氧化反应生成羟基酮。羟基酮通过裂解产生乙醛8,乙醛8形成缩醛后,通过两步反应,形成环丁基羰基10。根据研究者的经验,可通过Baeyer-Villiger氧化,生成11种酯。筛选了大量溶剂和过氧化物后,未得到目标内脂11,而是形成了另一种酯13。化合物10在间氯过氧苯甲酸的作用下,5min就可以生成内脂11。内酯11通过缩醛氧化和烯醇醚转化,可以生成Bilobalide。采用琼斯试剂对缩醛进行部分氧化,可形成内酯12,接下来再尝试将烯醇醚转化为羟基内酯。先将烯烃进行环氧化,再进一步采用琼斯试剂,即可生成Bilobalide。
合成难点:构建Baeyer-Villiger oxidation;光照下形成环丁基;光加合产物通过5步反应转化为环丁基酮10,比之前的路线有了重大的改进。
缺点:过程复杂;合成需要多步氧化还原过程来完成。
2.3 Masaki Ohtawa & Ryan A. Shenvi合成法
合成路线[6]:Wittig Olefination反应(一步或两步):
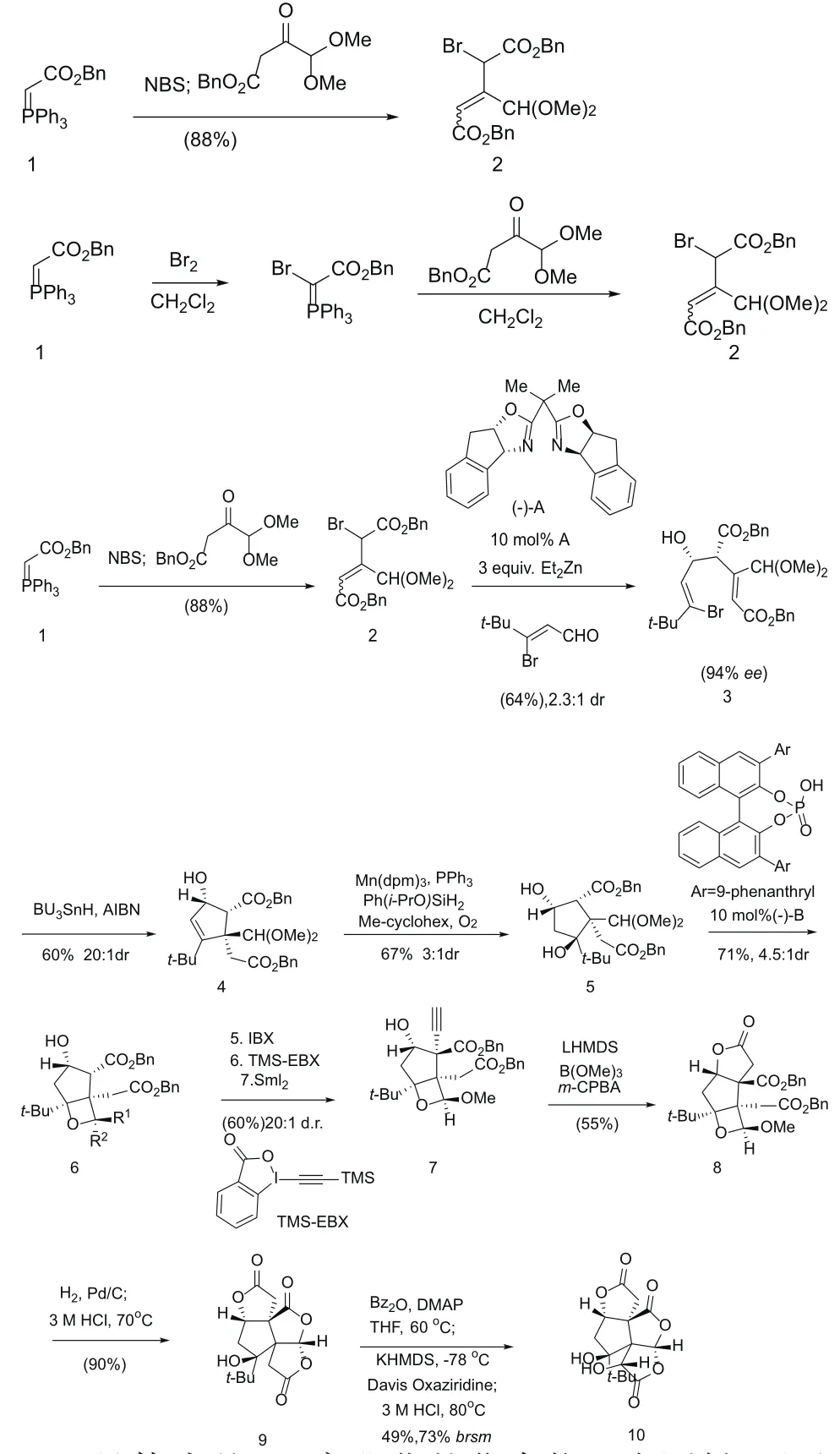
具体步骤:以商业化的化合物1为原料,通过Wittig Olefination 反应,一步生成化合物2。化合物2通过不对称Reformatsky反应生成化合物3,该步产生的副产物为原位脱溴产物。化合物3通过Giese 反应形成1个五元环4,五元环4发生Mukaiyama hydration反应,以化学选择性在金属氢化物氢的转移机制下与水合受阻的烯烃生成化合物5,在磷酯作用下形成氧杂环丁烷。氧杂环丁烷通过3步反应(IBX氧化成β-酮酯,TMS-EBX发生亲电炔基化,再进行还原)生成化合物12,再通过炔烃氧化生成1个内酯环8,内酯8通过脱保护,环合生成三内酯,再通过羟基化反应生成Bilobalide。
合成难点:构建不对称的Reformatsky反应;通过手性磷酯构建氧杂环;引入炔基。
优点:合成步骤简单,合成过程的每一步都非常经典。
3 总结
Bilobalide是从银杏叶中提取出来的天然产物之一,Bilobalide结构的拥挤且不稳定,给合成带来了很大的困难。1987年E.J.Corey等人首次完成了Bilobalide的全合成,1993年Michael T. Crimmins等人报道了Bilobalide的全合成方法。该方法巧妙地使用了光加合反应,通过选择性的缩醛氧化和烯醇醚氧化,完成了Bilobalide的全合成。2019年,Masaki Ohtawa & Ryan A. Shenvi课题组通过10步反应,完成了Bilobalide的全合成,该方法的关键之处是不对称Reformatsky反应,通过合成第1个手性季碳后,再通过炔烃氧化来生成内酯。
