人类表皮生长因子受体2表达与胃癌组织学的相关性研究
2021-10-10刘江帕合热迪尼玉素甫李建刚马博李亮王俊王彤阿合提别克
刘江,帕合热迪尼·玉素甫,李建刚,马博,李亮,王俊,王彤,阿合提别克
人类表皮生长因子受体2(human epidermal growth factor receptor 2,HER2)表达状态是评估进展期胃癌和胃食管结合部癌抗HER2治疗指征和效果的一个重要生物标记物。目前,普遍认为HER2阳性进展期胃腺癌在诊疗方案上与HER2阴性胃癌差别明显[1,2]。不同组织学类型的胃癌其细胞分泌功能、侵袭特点、蛋白基因表达状况等不同[3,4],导致不同组织类型胃癌对化疗、抗HER2靶向治疗等辅助治疗的效果良莠不齐[1,5,6],并且抗HER2耐药的尴尬结局为实施规范的临床诊疗增加不确定性。基于此,本研究通过初步分析胃癌胃镜活检标本HER2表达情况,及HER2表达与胃癌组织学特点的相关性,了解不同胃癌组织的HER2表达差异,为胃癌精准抗HER2治疗予以组织学提示。
1 资料与方法
1.1 一般资料
收集2017年1月至2020年1月在新疆医科大学第二附属医院普外科、肿瘤科收治的胃癌患者87例(男性54例,女性33例)作为胃癌组,另选同期在本院消化内科住院治疗的慢性浅表性胃炎患者21例(男性13例,女性8例)作为正常胃黏膜组。基线资料:胃癌组年龄均数(57.07±6.91)岁,既往胃镜检查(2.41±1.91)次;临床分期:Ⅰ期+Ⅱ期47例,Ⅲ期+Ⅳ期40例;浸润深度T1+T2 58例,T3+T4 29例;分化程度:高分化+中分化53例,低分化+未分化34例;有淋巴结转移50例,无淋巴结转移37例;Lauren组织学分型:肠型63例,弥漫型24例。正常胃黏膜组年龄均数(58.67±10.62)岁,既往胃镜检查(2.14±1.68)次。两组患者年龄、基础疾病情况、既往胃镜检查次数等临床资料比较无显著差异。本研究经新疆医科大学第二附属医院伦理委员会批准。所有胃癌患者均按美国癌症联合会(AJCC)第8版胃癌标准进行TNM分期,组织学分类按2010版WHO胃肿瘤组织学分类。纳入标准:本院病理证实为胃癌;内镜检查前一周内无影响胃黏膜功能药物用药史;语言表达能力正常、能配合各项检查者。排除标准:胃转移癌;严重心、肺、肝等脏器功能不全者;行辅助治疗、免疫治疗者;凝血功能障碍者。
1.2 方法
所有纳入的患者均常规行内镜检查获取内镜标本,分析内镜下不同部位取材的标本的HER2表达情况,每个病例取材数不少于5块,尽量避开坏死部,记录每个病例的取材部位。IHC检测:将获得的胃组织(手术或内镜标本)在30 min内完成编号、切片等处理,室温下于新配置的10%中性缓冲福尔马林溶液内固定,固定时长在12~24 h,完成后续的制片过程后行IHC染色,详细操作过程及质量控制按所购DAB染色试剂盒[商品名:免疫组织化学试剂盒(兔、小鼠),上海经科化学科技有限公司,生产批号:WB1210-1]的说明书和HER2检测指南及共识进行[7,8]。HER2评定方法:IHC0或1+分记为HER2阴性,IHC2+或3+记为HER2阳性。HE染色法:将所获得胃组织制备成5 μm厚石蜡切片,65℃孵育30 min,二甲苯溶液浸泡5 min,新鲜二甲苯溶液再次浸泡脱蜡5 min,100%乙醇浸泡8 min,90%乙醇浸泡2 min,80%乙醇1 min,70%乙醇2 min,PBS溶液冲洗2 min,擦拭干净后HE染色试剂盒染色(商品名:Solarbio,北京索莱宝科技有限公司,生产批号:G1120)。首先200 μL苏木素染色液染色15 min,流动水冲洗10 min,PBS冲洗2 min,分化液分化30 s。然后400 μL伊红染色液染色30 s,流动水冲洗5 min,完成脱水、透明、封固操作后,由两名高年资病理科医生独立交叉阅片。
1.3 观察指标
两组患者HER2阳性率;内镜下不同活检部位组织HER2的阳性率;病理特征指标包括胃管状腺癌和其他类型胃癌HER2阳性率,以及镜下有、无印戒细胞的胃癌的HER2阳性率。
1.4 统计学方法
采用SPSS 23.0进行统计学分析,计数资料用率(%)表示,分类比较采用χ2检验或Fisher确切概率法。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者HER2表达比较
胃癌组HER2阳性率为17.2%(15/87),明显高于正常胃黏膜组0.0%(0/21),差异有统计学意义(P<0.05)。
2.2 胃癌中不同活检部位HER2表达阳性率比较
浅表弥漫部(环瘤体中心周围的浅表弥漫病变,图1A)、溃疡隆起部(瘤体中隆起的溃疡病变,图1B)、溃疡床(瘤体内的溃疡病变,图1C)及肿块突起部(瘤体突起的病变,图1D)HER2阳性率分别是100%、90%、44%、100%,见表1。

图1 胃镜下不同取材部位A:浅表弥漫部;B:溃疡隆起部;C:溃疡床;D:肿块突起部

表1 HER2表达与活检标本部位相关性
2.3 胃癌组中,HER2表达与胃癌组织学相关性分析
镜下表现为管状腺癌及不含印戒细胞HER2阳性率明显高于其他组织学类型胃癌和含印戒细胞,差异有统计学意义(P<0.05)。见表2。
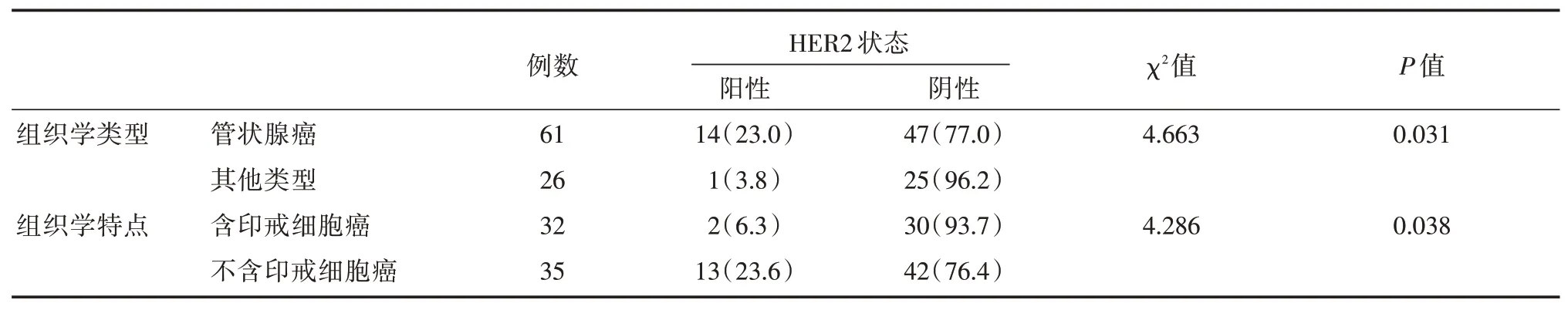
表2 胃癌组HER2表达与胃癌组织类型及特点关系[n(%)]
3 讨论
据统计,HER2在肠型、弥漫型和混合型(Lauren分型)胃癌中阳性率为分别为3%~23.5%、0%~6%和0%~20%[9-11]。但具体到不同组织类型中HER2阳性率仍未见一致报道。临床上,同一胃癌标本中镜下观察到两种以上组织学类型并存的情况常见[12],这使胃癌实施精准抗HER2治疗增加不确定性。本研究中胃管状腺癌中HER2阳性率为23.0%,其他类型胃癌HER2阳性率为3.8%,差异有统计学意义(P=0.031),与之前一些研究报道相近[10,11]。
研究证实内镜活检标本在胃癌HER2检测中能获得与手术标本相近的结果[13-15]。尽管如此,目前国内在对内镜活检标本进行HER2状态分析仍不及手术标本,部分是由于HER2的异质性表达或受限于内镜的经验基础。本研究中,通过分析胃癌患者内镜下不同活检部位的HER2阳性率,结果提示:在肿瘤浅表弥漫部、溃疡隆起部、溃疡床及肿块突起部检测的HER2阳性率分别是100%、90%、44%、100%,发现HER2在胃癌浅表弥漫部比溃疡床部阳性率更高。既往有研究认为,在腺体形成区域和异型增生上皮区域中阳性率高于肿瘤侵袭区域[16,17]。当然需要注意的是,Subasinghe等[18]认为胃癌活检标本中,肿瘤中心与肿瘤外围组织HER2异质性可达30%以上。因此,指南[3,19]推荐内镜标本应该在5个以上时可满足HER2检测需要,本研究所取的标本数也达到推荐的要求,结果可靠。这提示在内镜下评估HER2状态时应该重视肿瘤浅表弥漫部和溃疡床的组织。
目前,在晚期乳腺肿瘤中以曲妥珠单抗为主的抗HER2靶向药应用日趋广泛,HER2靶向治疗联合化疗的疗效在进展期HER2阳性胃癌中也较可观,其生存优势在包括ToGA在内的一些研究中得以证实。本研究结果显示镜下未见印戒细胞的胃癌患者中HER2阳性率为23.6%,较含印戒细胞者更高,两组比较有显著差异(P=0.038),印戒细胞可能影响胃癌组织中HER2表达水平,这与Machado-Neves等[20]的研究结果一致。由于典型胃印戒细胞癌细胞在胃壁侵袭进展过程可以向低黏性肿瘤细胞转化[21],而使HER2阳性胃癌病例中不含印戒细胞的病例数相对增加,可能使研究的结果出现放大效应。本研究回顾的病例数相对较少,还需进一步的大样本研究证实。本研究以慢性浅表型胃炎为对照,虽可以消除HP、慢性黏膜炎症、肠道菌群微环境等一些混杂因素,但由于慢性浅表型胃炎病变常局限黏膜浅层,对于一些浸润深度达黏膜肌层或浆膜的癌性病变,上述混杂因素对本研究结果的影响可能难以完全均衡。此为本研究的不足之处。
总之,内镜活检标本评估HER2表达时应有针对性地取材,胃癌组织病理中见不到印戒细胞的胃癌组织HER2阳性率可能更高。因此,当病理提示未见印戒细胞而黏膜层存在大量炎性细胞浸润或黏液细胞时,应该警惕假阴性的可能性,避免影响进一步靶向抗HER2治疗。
