3D腹腔镜与普通腹腔镜、开放根治性膀胱切除+肠道原位新膀胱术围手术期疗效的比较
2021-09-30夏照明土应果郭民杨建昌李智斌李元杨旺秋
夏照明 土应果 郭民 杨建昌 李智斌 李元 杨旺秋
膀胱癌是泌尿系统最常见的恶性肿瘤之一,我国膀胱癌的发病率为5.80/10万,男女发病率分别为8.83/10万和2.61/10万,膀胱癌在所有男性恶性肿瘤中位居第7位,在所有女性恶性肿瘤中位居第17位[1-2]。膀胱癌对人们的生命健康造成严重的威胁,初次就诊的膀胱癌患者中有四分之一为肌层浸润性的膀胱癌,对于肌层浸润性非转移膀胱癌,膀胱根治性切除术(radical cystectomy, RC)+盆腔淋巴结清扫(pelvic lymph node dissection, PLND)是公认标准的治疗方案[3],对于多发、复发的高危非肌层浸润性膀胱癌,RC术是最有效的治疗方式。随着医疗技术的发展,在国内一些大的医疗中心,机器人辅助RC术已经非常成熟,但是大部分医院主流的手术方式仍是腹腔镜RC术[4]。无论是腹腔镜还是机器人手术,都不能完全取代传统的ORC术,ORC术在肌层浸润性膀胱癌的治疗中仍然起着举足轻重的作用。本文回顾性分析了2008年9月至2020年6月在我院行RC术+乙状结肠(或回肠)原位新膀胱术148例患者的临床资料,对3种术式的临床疗效进行了比较,现报告如下。
对象与方法
一、一般资料
148例患者术前均行腹部增强CT检查、膀胱镜检及肿瘤组织活检确诊,其中142例为肌层浸润性膀胱尿路上皮癌,2例为膀胱多发非肌层浸润性高级别尿路上皮癌,1例为复发的膀胱嗜铬细胞瘤,2例膀胱腺癌,1例膀胱鳞状细胞癌。115例为膀胱初发肿瘤,33例为复发性膀胱癌,148例患者均由我科同一医生主刀行RC术+乙状结肠(或回肠)原位新膀胱术。纳入标准:①经影像学及病理诊断为肌层浸润性膀胱尿路上皮癌(T2~T3)、膀胱腺癌、膀胱鳞癌、多次复发的膀胱嗜铬细胞瘤、多次复发的非肌层浸润性高级别尿路上皮癌;②心肺功能、肝肾功能、凝血功能无明显异常,无严重基础疾病,可以耐受RC术者;③膀胱三角区、膀胱颈口、尿道无肿瘤,尿道无狭窄及其他尿道疾病。排除标准:①肿瘤位于膀胱三角区或膀胱颈口,尿道有肿瘤,尿道有狭窄及其他尿道疾病等不适合行原位新膀胱术者;②年龄大于75岁;③结肠镜检查发现结肠病变同时合并有回肠病变者;④身体状况欠佳,基础疾病多,凝血功能障碍、心肺功能不全等不能耐受手术者。其中109例行RC术+乙状结肠原位新膀胱术,39例行RC术+回肠原位新膀胱术,开放手术62例,腹腔镜手术32例,3D腹腔镜手术54例,其中男135例,女13例,白族57例,汉族91例,年龄45~75岁,平均年龄(66.81±5.18)岁。患者合并高血压24例、合并糖尿病14例、合并肾功能不全5例、合并心脏病5例。其中T1肿瘤2例,T2期肿瘤109例,T3期肿瘤37例。
二、术前准备及简要手术步骤
术前请内科相关科室会诊,内科疾病控制平稳,术前3 d开始口服甲硝唑片及阿米卡星,静脉补充维生素K,补充足够能量,术前1 d流质饮食,口服番泻叶或蓖麻油进行肠道准备,术前晚上清洁灌肠。行开放根治性膀胱切除术(open radical cystectomy, ORC)。患者取仰卧位、头低脚高,取下腹部正中切口长约18 cm,常规行淋巴结清扫,清扫范围为髂外淋巴结、髂内淋巴结及闭孔淋巴结,分离出双侧输尿管至膀胱壁段,然后顺行切除膀胱、精囊、前列腺(或女性子宫),距离回盲部15~20 cm取长度约40 cm的回肠或直接取长度约25 cm的乙状结肠作新膀胱,手工进行肠道端端间断吻合,用直线切割缝合器将取下来的肠管做成“U”型新膀胱:取一段带系膜的乙状结肠,肠管中间对折,将近端和远端并拢,将直线切割吻合器张开经乙状结肠近端口和远端口插入进行切割吻合。将双侧输尿管远端与新膀胱两侧壁进行吻合,再将新膀胱与尿道进行吻合。行腹腔镜根治性膀胱切除术(laparoscopic radical cystectomy, LRC)及3D腹腔镜根治性膀胱切除术(3D laparoscopic radical cystectomy, 3D-LRC)的患者先建立气腹,建立腹腔镜操作通道,腹腔镜下完成双侧淋巴结清扫及RC术,然后取腹部正中切口,开放手术游离部分回肠或者乙状结肠,取合适长度的肠管作新膀胱用,手工进行肠道端端间断吻合,然后制作U型新膀胱,接下来将双侧输尿管与新膀胱侧壁进行吻合,最后行新膀胱与尿道的吻合(手术步骤同开放手术)。
比较3组患者的性别、年龄、肿瘤临床分期、膀胱切除时间、淋巴结清扫时间、淋巴结清扫数量、术中出血量、围手术期并发症的发生情况、术后排气时间、术后新膀胱尿控、术后住院天数的差异。
三、统计学方法
结 果
一、基本资料的比较
3D-LRC组、LRC组及ORC组3组在年龄、性别、民族、体重指数(body mass index, BMI)、合并症、肿瘤分期方面比较,差异无统计学意义(P>0.05),见表1。
二、术后并发症的比较
患者手术均顺利完成,术中未更改手术方式,3D-LRC组术中出血量明显小于LRC组及ORC组(P<0.05),ORC组术后排气时间及术后住院天数明显长于LRC组及3D-LRC组,差异有统计学意义(P<0.05),3D-LRC组膀胱切除时间以及淋巴结清扫时间短于LRC组(P<0.05),淋巴结清扫的数量多于ORC组(P<0.05)。3组患者围手术期并发症的发生率以及新膀胱尿控方面比较无明显差异(P>0.05),见表2、表3。
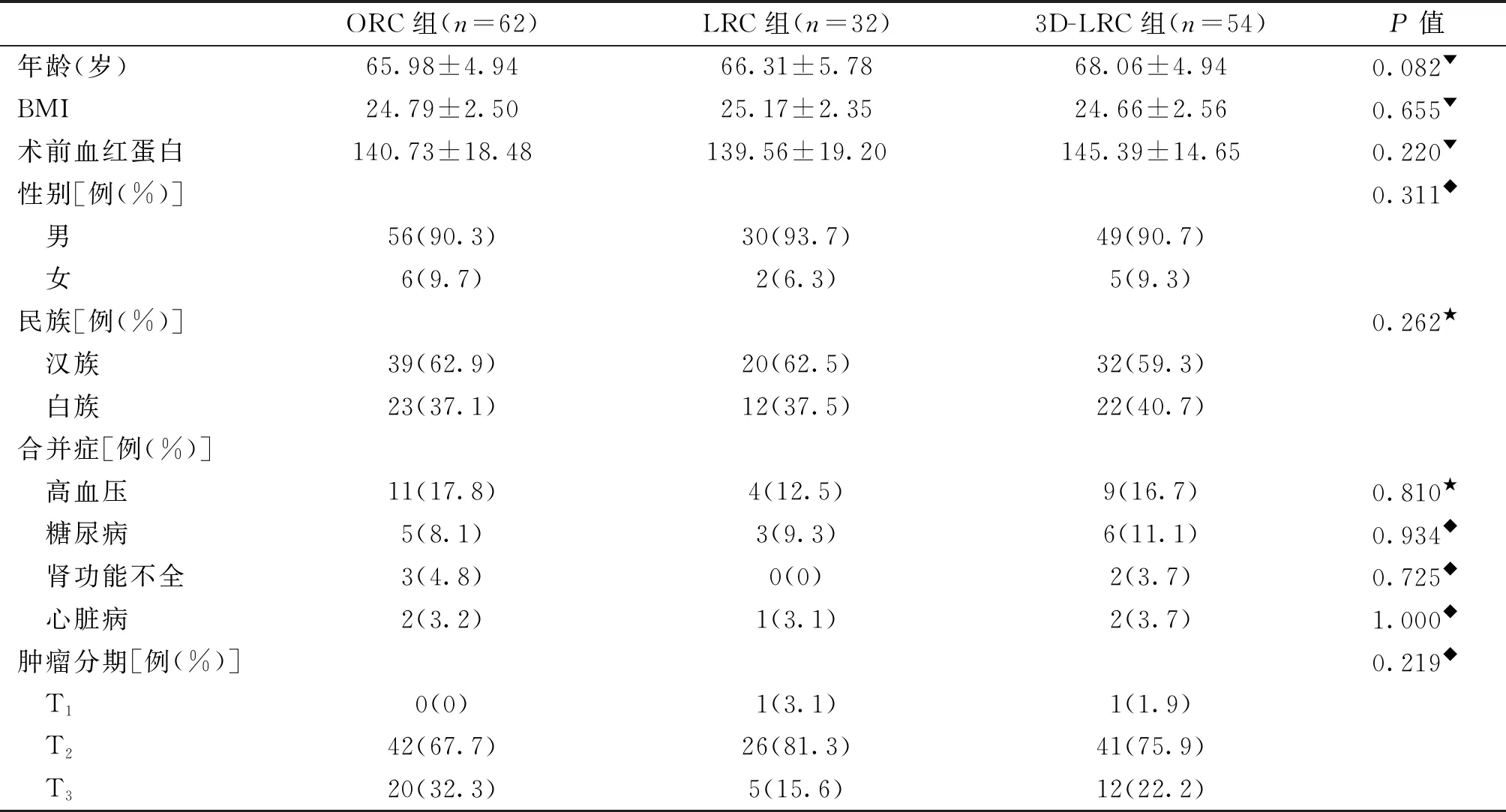
表1 3组患者一般资料的比较
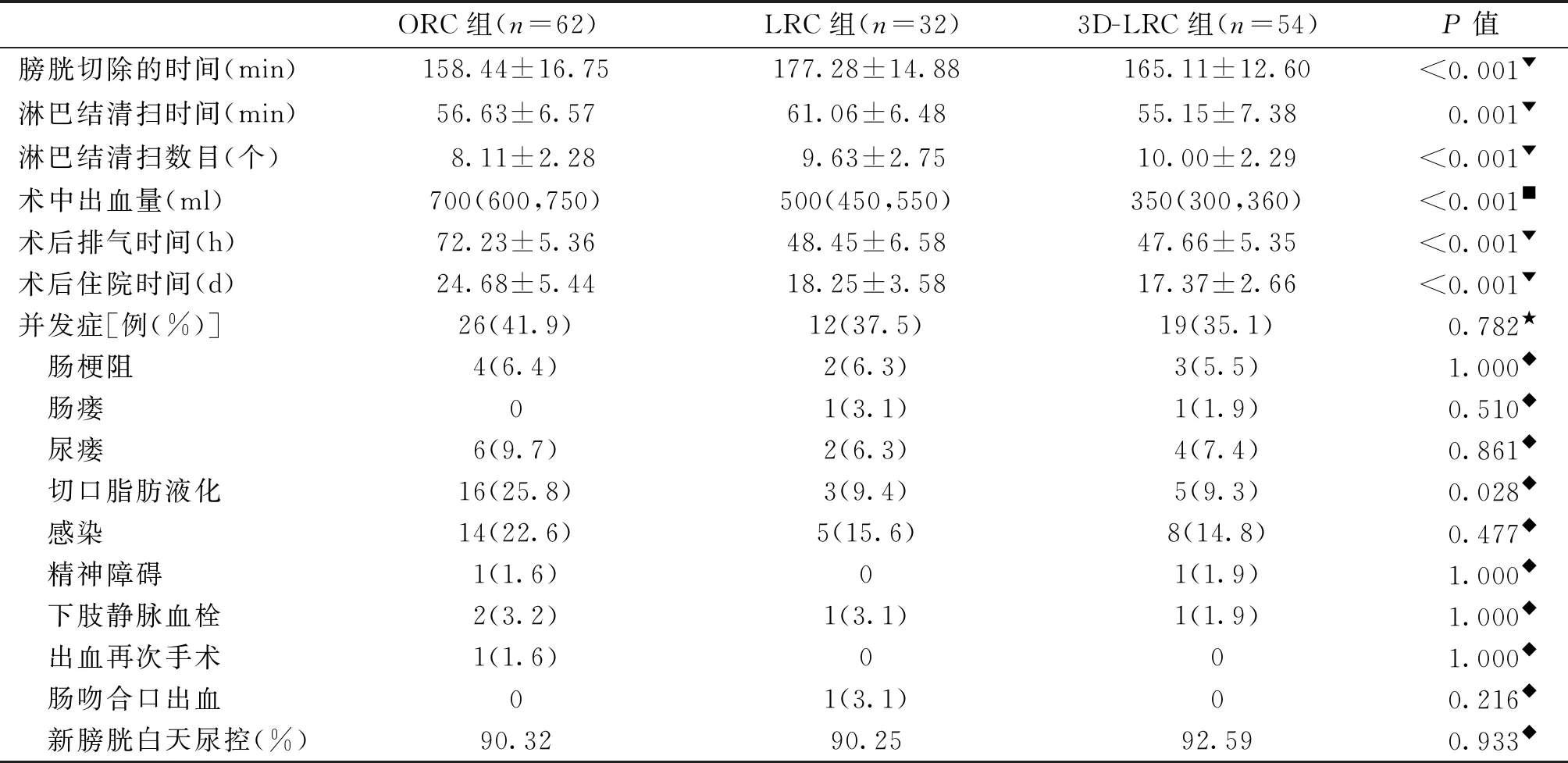
表2 术中情况及围手术期并发症的比较
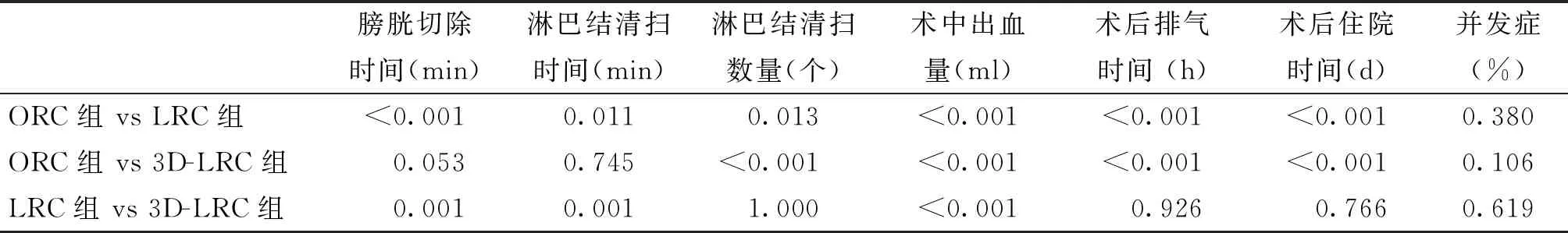
表3 3组有统计意义指标的并发症的比较
讨 论
RC术是肌层浸润性膀胱尿路上皮癌、膀胱腺癌、膀胱鳞状细胞癌的标准治疗方法[3,5-6],目前RC术方法主要有ORC术、LRC术和机器人辅助腹腔镜膀胱根治性切除术3种,调查显示[4]3种手术方式的比例分别占39.6%、57.6%和2.7%,LRC术仍然是RC术的主要手术方式。手术的步骤包括膀胱切除+PLND+尿路重建或是尿流改道3个主要步骤,是泌尿外科最复杂、难度最大的一类手术[7]。在腹腔镜技术出现之前,RC术均采用开放手术的方式进行,随着腹腔镜技术的发展,外科手术逐渐进入了微创时代。1993年,Sánchez等[8]报道了首例腹腔镜下RC术的病例,黄健等[9]于2002年率先在国内开展LRC术+原位回肠新膀胱术,随后,国内各大医院陆续开展LRC术。本文对ORC术、LRC术、3D-LRC术3种RC术的方式进行对比研究,我们的数据显示3D-LRC组膀胱切除时间以及淋巴结清扫时间短于LRC组,淋巴结清扫的数量多于ORC组,3D-LRC组的术中出血量明显少于LRC组及ORC组,术后排气时间及术后住院天数明显短于ORC组,3组患者围手术期并发症的发生率以及新膀胱尿控方面比较无明显差异。在进行普通2D腹腔镜RC术时,由于盆腔的操作空间相对狭小,二维的成像没有立体感,对组织的层次分辨不够清楚,加上注意力长时间高度集中,容易造成视觉疲劳,可能会出现错觉,甚至会出现动作上的偏差;与传统的2D腹腔镜相比,3D腹腔镜显示高清的三维立体图像,得到真实视觉中的三维立体手术视野,有利于病变部位的辨识并进行精确的切除,可以减少血管、神经的损伤,使手术更加顺畅,缩短手术时间,提高手术效率。3D腹腔镜还可以十分清晰的辨认组织器官的深度、组织的层次、组织器官的毗邻关系。在清扫髂外淋巴结、髂内淋巴结、闭孔淋巴结的时候优势十分突出,术中可以更加干净、彻底、有效的进行淋巴结的清扫,最大程度的避免髂血管及闭孔神经的损伤,还可以明显提高术者手术的稳定性[10]。此外,由于3D-LRC手术时间明显缩短,术中出血少,患者术后恢复更快,可以缩短患者术后住院时间。
RC术+肠道原位新膀胱术有较高的围手术期并发症的发生率,本研究数据显示ORC组围手术期并发症的发生率为41.9%,LRC组围手术期并发症的发生率为37.5%,3D-LRC组并发症发生率为35.1%,ORC组围手术期的并发症的发生率依次高于LRC组及3D-LRC组,但是统计学无显著差异。尽管3D腹腔镜在手术操作中有明显的优势,但3D腹腔镜手术并未明显降低手术并发症的发生率。Minervini等[11]报道,RC术+回肠原位新膀胱术并发症总体发生率在28%~58%之间,我们3组患者并发症的发生率与Minervini所报道的相似。我们发现前四位的并发症分别为切口脂肪液化、感染、尿瘘、肠梗阻(表2),ORC组脂肪液化的发生率明显高于LRC组及3D-LRC组。研究表明[12],切口暴露时间过长,压迫、钳夹等机械刺激导致脂肪组织氧化、分解和产生无菌性炎症,最终导致脂肪液化,ORC组脂肪液化发生率高的原因考虑与上述因素有关。此外,据我们观察,切口引流不畅、皮下积液、营养不良、组织水肿也是导致切口脂肪液化的因素。何围等[13]研究发现3D腹腔镜保留性神经的RC中具有明显优势,可以更好的保留血管神经束,还可以降低术者视觉疲劳程度,由于技术的限制,我们没有开展此方面的研究。
综上所述,不管采取哪种手术方式,RC术+乙状结肠(或者回肠)原位新膀胱术围手术期并发症的发生率仍然较高,3D-LRC术与ORC术比较,具有术中出血少、淋巴结清扫更彻底、术后肠道恢复快、切口并发症少,术后住院时间短的优势。RC术操作复杂,对术者技术要求较高,对于经验不是很丰富的外科医生,选择3D腹腔镜手术可能会提高效率、降低术中并发症的发生。
