莪术油乳膏外用对大鼠的长期毒性实验研究
2021-09-27李文静包亚男
李文静 刘 军 包亚男 洪 博
齐齐哈尔医学院药学院,黑龙江齐齐哈尔 161006
莪术性温,味辛、苦,来源于姜科植物蓬莪术、广西莪术或温郁金的干燥根茎[1-2]。有行气破血、消积止痛的功效,属活血化瘀要药[3-4]。具有抗肿瘤、抗菌、升高白细胞、抗炎等药理作用[5-8]。莪术中主要含挥发油、黄酮类、萜类等化学成分[9-11]。其中,莪术油的临床应用较广泛,具有行气活血、消积止痛、活血化瘀、增强机体免疫能力之功效[12-14]。多项实验研究证实,莪术油可改善乳腺癌癌前病变大鼠的血液黏度等指标,其活血化瘀的药理作用可能是防治乳腺癌的作用机制之一[15-17]。
正常乳腺组织恶化成带有恶性肿瘤的乳腺组织是一个渐进的过程,在乳腺癌变之前这一发展过程是可逆的。根据中医理论,血瘀是乳腺癌癌前病变重要辩证,所以,本研究在以往的文献研究基础上,着眼于中医药的活血化瘀理论,结合大量的前期试验数据研制了莪术油乳膏用于乳腺增生的防治。该制剂制备工艺简单且质量可控,为进一步完善该制剂的开发,长期毒性试验是必不可少的,本研究旨在考察外用药莪术油乳膏对实验大鼠长期连续经皮给药的毒性反应及皮肤局部用药的安全性。
1 材料与方法
1.1 主要仪器及试剂
BP211D 精密电子天平(上海耀壮检测仪器设备有限公司,精密度为0.1 mg);Velocity 14R 台式离心机(澳大利亚Dynamica 公司);ADVIA2120 型全自动血球分析仪(德国西门子公司);AU5421 型全自动生化分析仪(日本Olympus 公司)。莪术(批号:20150329)药材购自亳州市国峰药业销售有限公司,产地为安徽亳州,经齐齐哈尔医学院中药研究室郭丽娜教授鉴定为姜科植物蓬莪术Curcuma phaeocaulis的干燥根茎。乳膏基质[齐齐哈尔医学院药学院提供,由十六醇、聚乙二醇(polyethylene glycol,PEG)-8 蜂蜡、单硬脂酸甘油酯、甘油、月桂醇硫酸钠、白凡士林和纯化水组成]。
1.2 研究对象
雌性美国斯泼累格·多雷(Sprague Dawley,SD)大鼠体重为200~230 g,购自于北京维通利华实验动物技术有限公司,实验动物使用许可证编号:SCXK(京)2007-0001,本研究经过动物伦理委员会审核同意开展。动物饲养环境:温度20~25℃,相对湿度40%~70%。换气次数10~15 次/h,照明时间每日12/12 h 交替照明。
1.3 方法
1.3.1 制剂制备 莪术油提取:取粉碎后的莪术药材10 g,置于挥发油提取装置的烧瓶中,最终得提取液为50 mL。取莪术油提取物10 mL,加入白凡士林18 g,十六醇28 g,PEG-8 蜂蜡18 mL 和单硬脂酸甘油酯32 g 于研钵中,置水浴加热至75℃熔化,作为油相。另取月桂醇硫酸钠24 g、甘油70 mL 和蒸馏水500 mL加热至同样温度,作为水相。将水相细流状搅拌条件下加至油相中,温度降至60 ℃时加入主药,继续研磨直至冷却即得。置于棕色试剂瓶中保存备用,乳膏中莪术油含量为0.014 mL/g。
1.3.2 动物分组及给药 将30 只雌性SD 大鼠随机分为空白对照(乳膏基质)组,完整皮肤组和破损皮肤组3 组,每组10 只。给药前24 h 用电推给大鼠胸部剃毛,脱毛部位为以乳头为圆心,1 cm 为半径的圆。破损皮肤组用针头在剃毛后大鼠皮肤上划“井”字至渗血[18]。将待测乳膏及空白基质分别应用于对应组的大鼠胸部,用药剂量为10 mg/cm2,每天2 次,连续给药3 个月。
1.3.3 一般情况观察 试验期间每日记录各组大鼠的摄食、行为活动、精神状态、食欲等日常情况,及大鼠有无死亡情况。每周固定时间给大鼠称重1 次,并适当调整给药剂量。期间如果发现有中毒反应的大鼠应马上隔离,并观察、记录,如何有死亡大鼠应及时进行病理学检查。
1.3.4 血液样品测定 用全自动血球分析仪对大鼠腹主动脉血进行血常规检查:红细胞(red blood cell,RBC)、白细胞(white blood cell,WBC)、血红蛋白(haemoglobin,HGB)、中性粒细胞百分比(neutrophil percentage,NEUT)、血小板计数(platelet count,PLT)、单核细胞百分比(monocyte percentage,MONO)、淋巴细胞比值(lymphocyte ratio,LYMPH)、嗜酸细胞百分比(eosinophilic percentage,EO)、嗜碱细胞百分比(basophile percentage,BASO)。
取血球分析剩余的全血离心10 min(速度4000 r/min,半径10 cm),用全自动生化分析仪检测血液生化各项指标:谷草转氨酶(aspartate aminotransferase,AST)、谷丙转氨酶(aminotransferase,ALT)、谷氨酰转肽酶(gamma-glutamyl transferase,GGT)、总胆汁酸(total bile acid,TBA)、总胆红素(total bilirubin,TBil)、血清前白蛋白(preserum albumin,PA)、尿素(Urea)、尿酸(uric acid,UA)、肌酐(creatinine,Crea)。
1.3.5 病理检查3 个月后,对各组大鼠进行解剖,观察心、肝、脾、肺、肾、卵巢等主要脏器的外观及硬度等有无明显病变。通过公式(质量/体重×100%)计算各主要脏器系数,主要脏器及皮肤标本进行HE 染色试验(200×)。
1.4 统计学方法
采用SPSS 22.0 统计学软件进行数据分析,计量资料用均数±标准差(±s)表示,组间比较采用单因素方差分析及LSD-t检验,以P<0.05 为差异有统计学意义。
2 结果
2.1 三组大鼠一般情况结果的比较
实验期间,三个实验组大鼠生长发育良好,均未出现中毒反应,且无死亡现象。各组大鼠行为活动比较,差异无统计学意义(P>0.05),肉眼观察脏器的形态和硬度等均未见异常。各组大鼠的食量和体重在正常范围内增长,给药前后的体重组间比较,差异无统计学意义(P>0.05);给药前后的体重同组比较,差异有统计学意义(P<0.05)(表1)。
表1 三组大鼠给药前后体重的比较(g,±s)
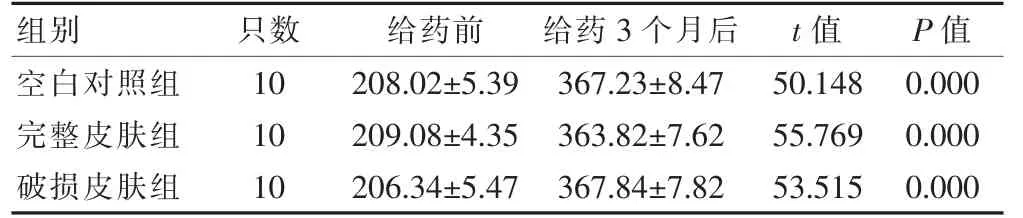
表1 三组大鼠给药前后体重的比较(g,±s)
组别只数给药前给药3 个月后t 值P 值空白对照组完整皮肤组破损皮肤组10 10 10 208.02±5.39 209.08±4.35 206.34±5.47 367.23±8.47 363.82±7.62 367.84±7.82 50.148 55.769 53.515 0.000 0.000 0.000
2.2 三组大鼠血常规指标的比较
连续外用给药3 个月后,破损皮肤组的WBC 高于空白对照组,破损皮肤组的HGB 低于空白对照组,差异有统计学意义(P<0.05);BASO 在三组中无表达,EO 在三组表达水平接近,均为0.03%;其余指标组间比较,差异无统计学意义(P>0.05)(表2)。
表2 三组大鼠血常规指标的比较(±s)
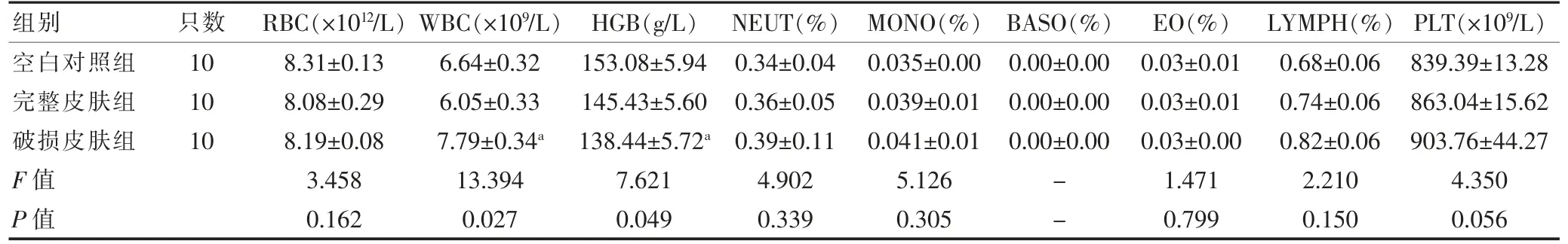
表2 三组大鼠血常规指标的比较(±s)
与空白对照组比较,aP<0.05;“-”表示无数据
组别只数 RBC(×1012/L)WBC(×109/L)HGB(g/L)NEUT(%)MONO(%)BASO(%)EO(%)LYMPH(%)PLT(×109/L)空白对照组完整皮肤组破损皮肤组F 值P 值10 10 10 8.31±0.13 8.08±0.29 8.19±0.08 3.458 0.162 6.64±0.32 6.05±0.33 7.79±0.34a 13.394 0.027 153.08±5.94 145.43±5.60 138.44±5.72a 7.621 0.049 0.34±0.04 0.36±0.05 0.39±0.11 4.902 0.339 0.035±0.00 0.039±0.01 0.041±0.01 5.126 0.305 0.00±0.00 0.00±0.00 0.00±0.00--0.03±0.01 0.03±0.01 0.03±0.00 1.471 0.799 0.68±0.06 0.74±0.06 0.82±0.06 2.210 0.150 839.39±13.28 863.04±15.62 903.76±44.27 4.350 0.056
2.3 三组大鼠血液生化指标的比较
连续外用给药3 个月后,破损皮肤组的PA 水平高于空白对照组,差异有统计学意义(P<0.05);其余指标组间比较,差异无统计学意义(P>0.05)(表3)。
表3 三组大鼠血液生化指标的比较(±s)
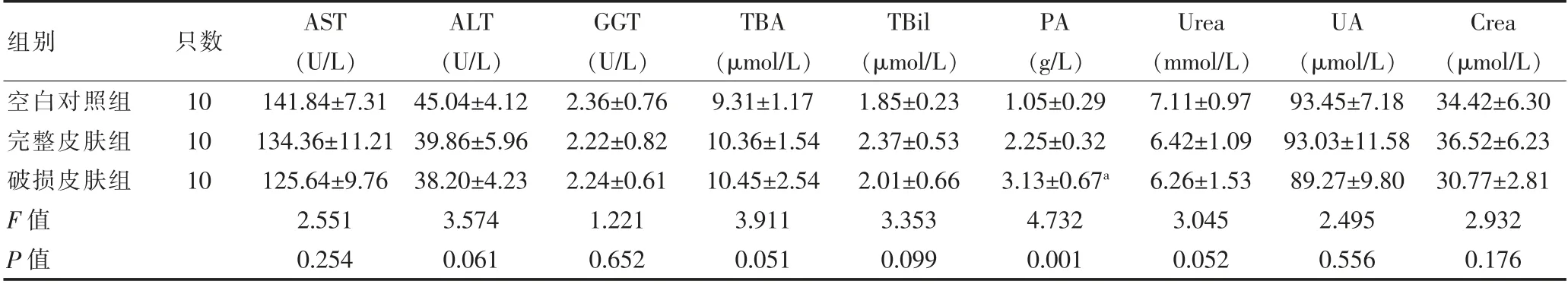
表3 三组大鼠血液生化指标的比较(±s)
与空白对照组比较,aP<0.05
组别只数AST(U/L)ALT(U/L)GGT(U/L)TBA(μmol/L)TBil(μmol/L)PA(g/L)Urea(mmol/L)UA(μmol/L)Crea(μmol/L)空白对照组完整皮肤组破损皮肤组F 值P 值10 10 10 141.84±7.31 134.36±11.21 125.64±9.76 2.551 0.254 45.04±4.12 39.86±5.96 38.20±4.23 3.574 0.061 2.36±0.76 2.22±0.82 2.24±0.61 1.221 0.652 9.31±1.17 10.36±1.54 10.45±2.54 3.911 0.051 1.85±0.23 2.37±0.53 2.01±0.66 3.353 0.099 1.05±0.29 2.25±0.32 3.13±0.67a 4.732 0.001 7.11±0.97 6.42±1.09 6.26±1.53 3.045 0.052 93.45±7.18 93.03±11.58 89.27±9.80 2.495 0.556 34.42±6.30 36.52±6.23 30.77±2.81 2.932 0.176
2.4 三组大鼠主要脏器系数结果的比较
各组大鼠的脏器系数比较,差异无统计学意义(P>0.05)(表4)。
表4 三组大鼠主要脏器系数结果的比较(%,±s)
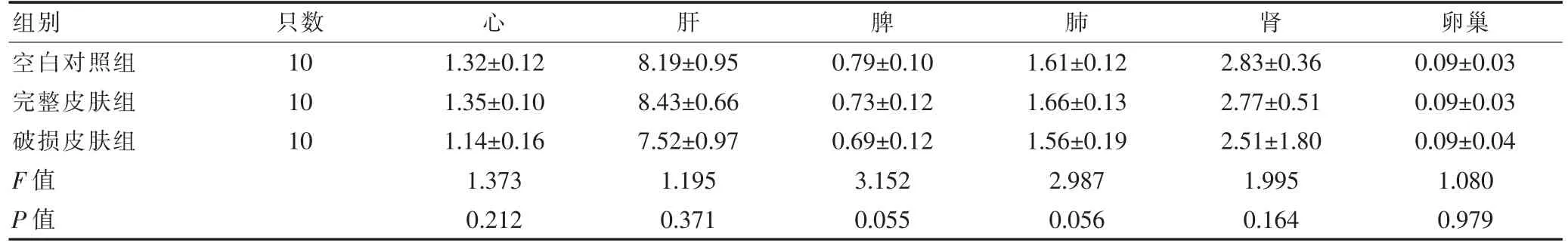
表4 三组大鼠主要脏器系数结果的比较(%,±s)
组别只数心肝脾肺肾卵巢空白对照组完整皮肤组破损皮肤组F 值P 值10 10 10 1.32±0.12 1.35±0.10 1.14±0.16 1.373 0.212 8.19±0.95 8.43±0.66 7.52±0.97 1.195 0.371 0.79±0.10 0.73±0.12 0.69±0.12 3.152 0.055 1.61±0.12 1.66±0.13 1.56±0.19 2.987 0.056 2.83±0.36 2.77±0.51 2.51±1.80 1.995 0.164 0.09±0.03 0.09±0.03 0.09±0.04 1.080 0.979
3 讨论
乳腺增生症与内分泌功能紊乱密切相关,治疗包括一般治疗、药物治疗和手术治疗[19]。一般治疗是指平时注意清淡饮食,禁食辛辣刺激及含有雌激素的食物,保持良好的心情和规律作息。如果疼痛症状比较明显,可以选择服用一些中成药来进行药物治疗,如乳癖消等,或一些激素类西药,比如三苯氧胺等[20];但是有一些乳腺增生形成结节,性质难以明确的需要手术治疗。其中,药物是最常用的治疗手段,但口服药物的副作用限制了其应用。中药外用制剂在乳腺增生的治疗上具有靶向性好、毒副作用小等特点。
本研究中,莪术油乳膏对大鼠体重无明显影响,比较各组大鼠行为活动,差异无统计学意义(P>0.05),肉眼观察脏器的形态和硬度等均未见异常;皮肤破损组的HGB 水平低于空白对照组,差异具有统计学意义(P<0.05);皮肤破损组PA 水平高于空白对照组,差异具有统计学意义(P<0.05);其余指标与空白对照组比较,差异无统计学意义(P>0.05)。个别指标在破损皮肤组的差异表现可能是皮肤破损后,外用药物刺激所致,但对于正常皮肤组各指标均无显著影响,提示对正常皮肤无刺激等副作用。
综上所述,本研究的外用莪术油乳膏对实验大鼠未见明显的长期毒性。
