替诺福韦对高载量慢性乙型肝炎病毒感染孕妇母婴阻断效果观察
2021-09-24张波涛邓生炜黄育脉
张波涛,邓生炜,黄育脉
(广西医科大学附属武鸣医院感染性疾病科 广西 南宁 530000)
慢性乙型肝炎(CHB)是一种因感染乙型肝炎病毒(HBV)的疾病,我国是HBV感染高发国家,目前HBV感染已成为全世界公共健康问题。HBV主要经血液、性接触、母婴传播(MTCT)。替诺福韦(TDF)是一种妊娠B级药物,主要用于治疗HBV感染孕妇,但其在高载量CHB病毒感染孕妇母婴阻断中的应用效果尚不完全清楚,为此,本研究选择122例患者进行分组研究,旨在探讨TDF在CHB病毒感染孕妇母婴阻断中的效果,报道如下。
1.资料与方法
1.1 一般资料
选择2017年1月—2020年1月诊治的110例高载量CHB病毒感染孕妇作为观察对象,根据临床诊断分期分为两组,现症乙肝组26例,年龄24~36岁,平均年龄(30.52±4.18)岁,孕周<12周11例,孕周12~24周15例;病毒携带组84例,年龄20~34岁,平均年龄(27.61±4.18)岁,孕周>24周;选择同期12例高载量CHB感染孕妇作为对照组,年龄20~32岁,平均年龄(26.82±4.05)岁。三组患者一般资料无显著差异(P>0.05),有可比性。纳入标准:(1)符合C H B诊断标准[3];(2)孕前乙型肝炎e抗原(HBeAg)阳性,HBV-DNA≥106U/L;(3)单胎孕妇;(4)入组前未接受过抗病毒治疗;(5)患者及家属对研究知情,签署知情同意书。排除标准:(1)丙型肝炎;(2)合并梅毒;(3)既往有抗病毒治疗;(4)合并脂肪肝、酒精性肝病、自身免疫性疾病、遗传代谢性肝病;(5)合并糖尿病。
1.2 方法
现症乙肝组(符合慢性乙型肝炎治疗指征即开始服药)和病毒携带组(于第24周后开始服药)均口服富马酸替诺福韦二吡呋酯片(TDF)(成都倍特药业股份有限公司,国药准字H20163436),300 mg/次,1次/d,分娩后停药。对照组不接受任何抗病毒治疗。三组胎儿娩出后12 h内,在臀大肌注射100 IU乙肝免疫球蛋白(H B I G)及三角肌注射第1针乙肝疫苗10μg,于婴儿第1、6个月注射第2、3针乙肝疫苗,剂量与第1针剂量相同。
1.3 观察指标
(1)于治疗前、分娩前、分娩1个月进行HBV-DNA定量检测,采用ABI Prism 7500荧光定量PCR仪检测HBV-DNA,试剂盒购自中山大学达安基因股份有限公司。于治疗前、分娩前、分娩1个月采用德国罗氏Cobas E 601电化学发光免疫分析仪ALT。(2)检测婴儿7月龄乙肝两对半及其DNA。(3)婴儿7月龄抗一HBsAg阳性和HBV-DNA为阴性判定为阻断成功。(4)记录胎龄、胎儿体重、头围、身长及Apgar评分。Apgar评分包括皮肤颜色、呼吸、心搏速度、肌张力及运动、反射5个项目,总分10分,0~3分为重度窒息,4~7分轻度窒息,8~10分为正常[4]。
1.4 统计学分析
采用SPSS 23.0统计软件进行数据处理。正态分布的计量资料采用均数±标准差(±s)表示,组间比较采用t检验,计数资料用频数和百分比(%)表示,组间比较采用χ2检验。P<0.05为差异有统计学意义。
2.结果
2.1 三组HBV-DNA定量及ALT水平比较
三组治疗前HBV-DNA、ALT水平比较,差异无统计学意义(P>0.05),现症乙肝组、病毒携带组分娩前、分娩后1个月后HBV-DNA、ALT水平与对照组比较,明显降低,差异有统计学意义(P<0.05),现症乙肝组与病毒携带组分娩前、分娩后1个月HBV-DNA、ALT水平比较,差异无统计学意义(P>0.05),见表1。
表1 三组术后恢复情况比较(±s)
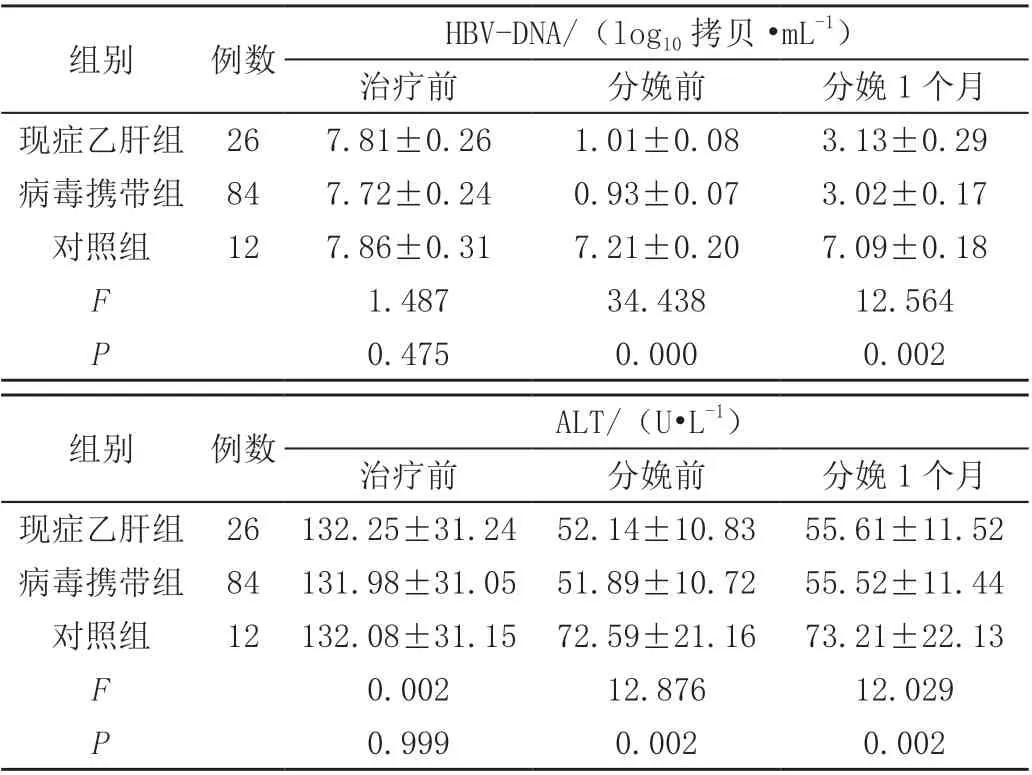
表1 三组术后恢复情况比较(±s)
注:与对照组比较,P<0.05。
组别 例数 HBV-DNA/(log10拷贝•mL-1)治疗前 分娩前 分娩1个月现症乙肝组26 7.81±0.26 1.01±0.08 3.13±0.29病毒携带组84 7.72±0.24 0.93±0.07 3.02±0.17对照组 12 7.86±0.31 7.21±0.20 7.09±0.18 F 1.487 34.438 12.564 P 0.475 0.000 0.002组别 例数 ALT/(U•L-1)治疗前 分娩前 分娩1个月现症乙肝组26 132.25±31.24 52.14±10.83 55.61±11.52病毒携带组84 131.98±31.05 51.89±10.72 55.52±11.44对照组 12 132.08±31.15 72.59±21.16 73.21±22.13 F 0.002 12.876 12.029 P 0.999 0.002 0.002
2.2 三组婴儿7月龄乙肝两对半及DNA检查
现症乙肝组与病毒携带组7月龄抗一HBsAg阳性均为100.00%,HBV-DNA定量均为阴性;对照组7月龄抗-HbsAg阳性率为91.77%,HBV-DNA 1例阳性,与现症乙肝组和病毒携带组对比,差异无统计学意义(P>0.05)。
2.3 三组母婴阻断成功率
现症乙肝组与病毒携带组母婴阻断成功率均为100.00%,对照组母婴阻断成功率为91.77%(11/12),三组对比差异无统计学意义(P>0.05)。
2.4 三组新生儿情况
三组胎龄、胎儿体重、头围、身长及Apgar评分比较,差异无统计学意义(P<0.05),见表2。
表2 三组新生儿情况比较(±s)
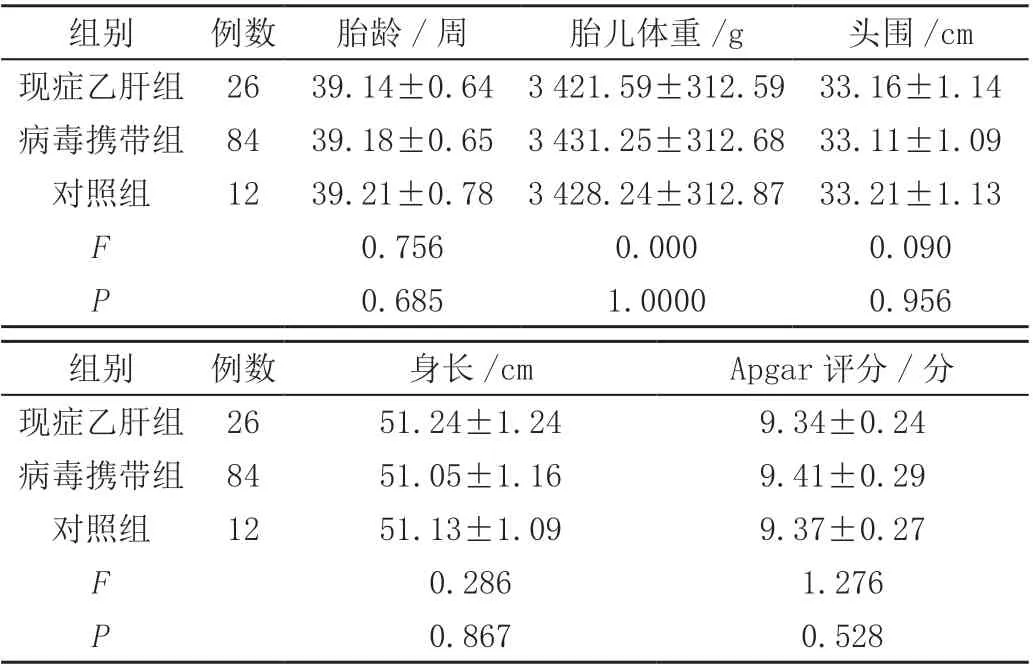
表2 三组新生儿情况比较(±s)
组别 例数 胎龄/周 胎儿体重/g 头围/cm现症乙肝组26 39.14±0.64 3 421.59±312.59 33.16±1.14病毒携带组84 39.18±0.65 3 431.25±312.68 33.11±1.09对照组 12 39.21±0.78 3 428.24±312.87 33.21±1.13 F 0.756 0.000 0.090 P 0.685 1.0000 0.956组别 例数 身长/cm Apgar评分/分现症乙肝组26 51.24±1.24 9.34±0.24病毒携带组84 51.05±1.16 9.41±0.29对照组 12 51.13±1.09 9.37±0.27 F 0.286 1.276 P 0.867 0.528
3.讨论
CHB是一种严重威胁人类健康的慢性传染病,该症因感染HBV所致,目前我国HBV感染者约9 300万,其中CHB约有2 000万,未经有效治疗的CHB可发展为肝硬化、肝细胞癌,严重威胁患者生命[5]。我国是HBV高发国家,且以青年和妇女居多,导致育龄期女性HBV感染率也相对偏高。HBV传播途径包括血液、性接触、母婴垂直传播三种,其中以母婴垂直传播为主要途径。相关数据表明,在所有HBV感染患者中,因MTCT引起的HBV感染占40%~50%,新生儿一旦发生HBV感染则会成为HBV携带者[6]。因此,针对HBV感染孕妇,孕期给予有效母婴阻断方案尤为重要。研究指出,宫内感染是造成HBV母婴传播重要传播途径,母体血清HBV-DNA水平越高,宫内胎儿HBV感染风险越高,且母体HBV-DNA病毒复制是造成母婴阻断失败的独立危险因素。白秀丽等研究表明,孕妇HBV-DNA与宫内传播呈正相关关系,当孕妇HBV-DNA<1.0×106IU/mL时,采用乙肝疫苗与乙型肝炎免疫球蛋白联合接种方式能够完全独断HBV传播,而当HBV-DNA>1.0×106IU/mL时,阻断率仅为68%。由此可见,母体血清中病毒载量与新生儿感染存在密切关联,通过传统主被动免疫并不能实现完全母婴阻断,尤其是高载量CHB病毒感染孕妇,母婴阻断效果相对更差,因此,孕期予以抗病毒治疗,通过降低母体分娩前HBV-DNA水平,可提高母婴阻断成功率。
综上所述,替诺福韦可降低高载量CHB病毒感染孕妇HBV-DNA及ALT水平,实现乙肝母婴传播的阻断,安全性高。
