贝伐珠单抗靶向治疗联合FOLFIRILOX化疗方案治疗晚期结直肠癌的效果及对患者免疫功能的影响
2021-09-18王人灵唐冬艳叶大胜
王人灵 唐冬艳 叶大胜
[摘要]目的探究貝伐珠单抗靶向治疗联合 FOLFIRILOX 化疗方案治疗晚期结直肠癌的效果及对患者免疫功能的影响。方法选取2016年1月至2020年12月开平市中心医院行晚期结直肠癌治疗的80例患者,基于不同治疗方法分为对照组与观察组,每组各40例。对照组予单纯 FOLFIRILOX 化疗,观察组则予以贝伐珠单抗靶向治疗联合 FOLFIRILOX 化疗。分析比较两组治疗后血清中免疫功能及肿瘤标志物指标、治疗效果及不良反应发生情况。结果观察组血清中3项免疫功能指标及3项肿瘤标志物指标均显著低于对照组( P <0.05);观察组总有效率(62.50%)及控制率(90.00%)均显著高于对照组(37.50%、62.50%)( P <0.05);观察组不良反应总发生率(17.50%)稍高于对照组(12.50%),但差异无统计学意义( P >0.05)。结论贝伐珠单抗靶向治疗联合 FOLFIRILOX 化疗方案治疗晚期结直肠癌能够有效降低血清中肿瘤标志物浓度,有效提高治疗有效率及疾病控制率,且不增加患者不良反应。
[关键词]结肠癌;晚期;贝伐珠单抗;靶向; FOLFIRILOX 化疗方案;免疫功能
[中图分类号] R735.34 [文献标识码] A [文章编号]2095-0616(2021)24-0196-04
Effect of targeted therapy with bevacizumab combined with FOLFIRILOX chemotherapy in the treatment of advanced colorectal cancer and its influence on patients' immune function
WANG Renling TANG Dongyan YE Dasheng
The Second Department of Oncology, Kaiping Central Hospital, Guangdong, Kaiping 529300, China
[Abstract] Objective To explore the effect of targeted therapy with bevacizumab combined with FOLFIRILOX chemotherapy in the treatment of advanced colorectal cancer (ACC) and its influence on patients' immune function. Methods A total of Eighty patients with ACC treated in Kaiping Central Hospital from January 2016 to December 2020 were selected. Based on different treatment methods, they were divided into the control group and the observation group, with 40 cases in each group. The control group was given FOLFIRILOX chemotherapy alone, while the observation group was given targeted therapy with bevacizumab combined with FOLFIRILOX chemotherapy. The immune function, tumor markers, therapeutic effect and adverse reactions in serum of the two groups after treatment were compared. Results Three indexes of immune function and three indexes of tumor markers in serum of observation group were significantly lower than those of control group (P <0.05). The total effective rate and control rate in the observation group (62.50% and 90.00%) were significantly higher than those in the control group (37.50% and 62.50%)(P <0.05). The total incidence of adverse reactions in the observation group (17.50%) was slightly higher than that in the control group (12.50%), with no statistically significant difference (P >0 .05). Conclusion The targeted therapy with bevacizumab combined with FOLFIRILOX chemotherapy can effectively reduce the concentration of tumor markers in serum, effectively improve the treatment efficiency and disease control rate, and do not increase the adverse reaction of patients with ACC.
[Key words] Colorectal cancer; Advanced stage; Bevacizumab; Targeted; FOLFIRILOX chemotherapy regimen; Immune function
随着社会人群生活方式及饮食结构的改变,进一步导致了人群胃肠道疾病及肿瘤的高发趋势[1-2]。结直肠癌为临床常见的恶性肿瘤,其发病率高居不下,仅次于肺癌和乳腺癌,且具有极高的病死率。结直肠癌高发于中老年,且男性病发率明显高于女性[3]。其病变部位位于肠黏膜上皮细胞,该病早期不引起明显症状而易被忽略,随着病程进展可出现局部腹痛、血便、腹泻、便秘等临床症状[4]。临床上常以5氟尿嘧啶、奥沙利铂、伊立替康作为晚期结直肠癌的治疗基础药物,虽然在提高生存期上有一定效果,但疗效仍不乐观[5]。研究发现,贝伐珠单抗靶向作用于内皮细胞并抑制其有丝分裂过程,从而达到控制肿瘤细胞生长的功效[6-7]。也有文献报道贝伐珠单抗靶向治疗联合 FOLFIRILOX 化疗方案能够取得良好的疗效。故开展评估贝伐珠单抗靶向治疗联合 FOLFIRILOX 化疗方案治疗该症效果的专项研究,现报道如下。
1资料与方法
1.1一般资料
选取2016年1月至2020年12月开平市中心医院行晚期结直肠癌治疗的80例患者。基于不同治疗方法分为对照组与观察组,每组各40例。对照组中男21例,女19例;年龄49~75岁,平均(54.68±3.04)岁;直肠癌18例,结肠癌22例;病理类型:高分化腺癌13例,中分化腺癌19例,低分化腺癌8例。观察组中男22例,女18例;年龄50~75岁,平均(55.96±2.85)岁;直肠癌17例,结肠癌23例;病理类型:高分化腺癌15例,中分化腺癌18例,低分化腺癌7例。两组患者一般资料比较,差异无统计学意义( P >0.05),具有可比性。纳入标准:①遵从医嘱,本人及家属知情并签订同意书,另外本研究通过医院医学伦理委员会批准;②临床病历完整清楚,符合 WHO 晚期结直肠癌的判断标准[8],且病理学诊断确诊;③预期生存期>6月者。排除标准:①心、肝、肾等脏器功能严重损伤者;②意识清楚,无精神障碍症者;③研究涉及药物过敏者;④病情加重或其他原因而无法坚持参与本研究者。
1.2方法
两组对象均采取FOlFIRlLOX化疗治疗,具体措施为:第1天进行伊立替康(江苏恒瑞医药股份有限公司,国药准字 H20061276)静脉滴注,剂量为180 mg/m2;第1天,奥沙利铂85 mg/m2,第1~2天,予以亚叶酸钙(江苏恒瑞医药股份有限公司,国药准字 H20061276)静脉滴注,剂量为200 mg/m2;第1~2天,予以2600 mg/m2氟尿嘧啶(上海旭东海普药业有限公司)静脉滴注维持22 h。以14 d 为1周期进行治疗,疗程共持续4个周期。观察组在对照组基础上增以贝伐珠单抗注射液(德国 Roche Diagnostics GmbH,注册证号 S20120068)静脉滴注,剂量为5 mg/(kg ·d)。每隔14 d 治疗1次,共持续4次。两组治疗过程中均予以胃黏膜保护、止吐等常规护理措施。
1.3观察指标及评价标准
分析比较两组治疗后血清中免疫功能及肿瘤标志物指标、治疗效果及不良反应发生情况。免疫功能指标包括:血清白蛋白(ALB)、免疫球蛋白IgG、IgA。肿瘤标志物指标包括:癌胚抗原(CEA)、肿瘤相关黏液抗原(CA242)、糖链抗原19-9(CA19-9)。比较两组临床疗效,疗效可分为四个级别[9]:若症状体征消失,且病灶完全消失,则评判为完全缓解(CR);若症状体征部分消失,且基线病灶直径缩小≥30%,则判定为部分缓解(PR);若症状体征无加重,且基线病灶直径缩小<30%或未变化,则判定为稳定(SD);若症状体征加重,且基线病灶直径增加≥20%或出现新病灶则判定为进展(PD)。总有效率(ER)=(CR+PR)例数/总例数×100%;控制率(DCR)=(CR+PR+SD)例数/总例数×100%。计算两组不良反应发生率,不良反应包括呕吐、厌食、头晕、腹胀。
1.4統计学分析
应用 SPSS 22.0统计学软件对研究所涉及统计、运算、分析进行处理。计量资料以( x ±s)表示,采用 t 检验,计数资料以[n (%)]表示,采用χ2检验, P <0.05为差异有统计学意义。
2结果
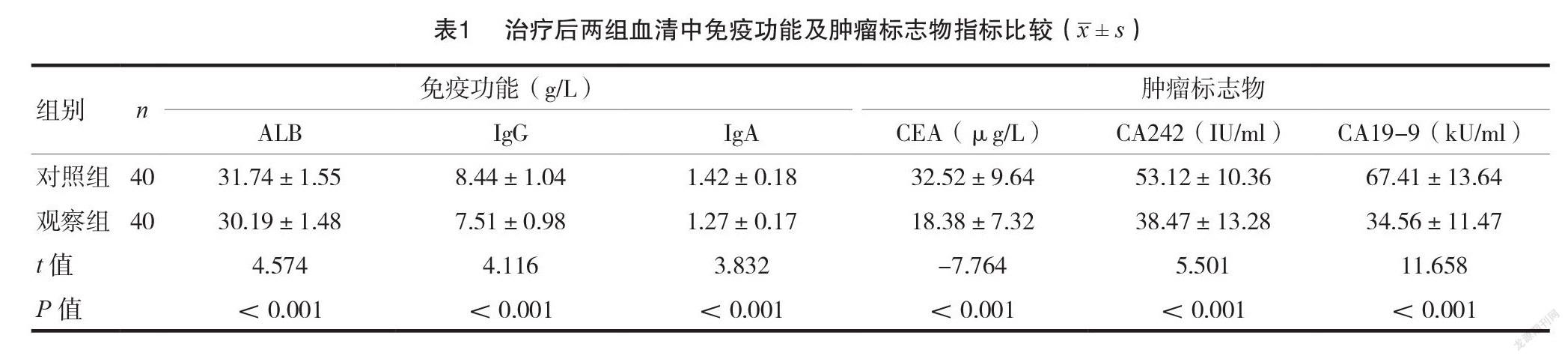
2.1治疗后两组血清中免疫功能及肿瘤标志物指标比较
治疗后,观察组血清中3项免疫功能指标及3项肿瘤标志物指标均显著低于对照组,差异有统计学意义( P <0.05),见表1。
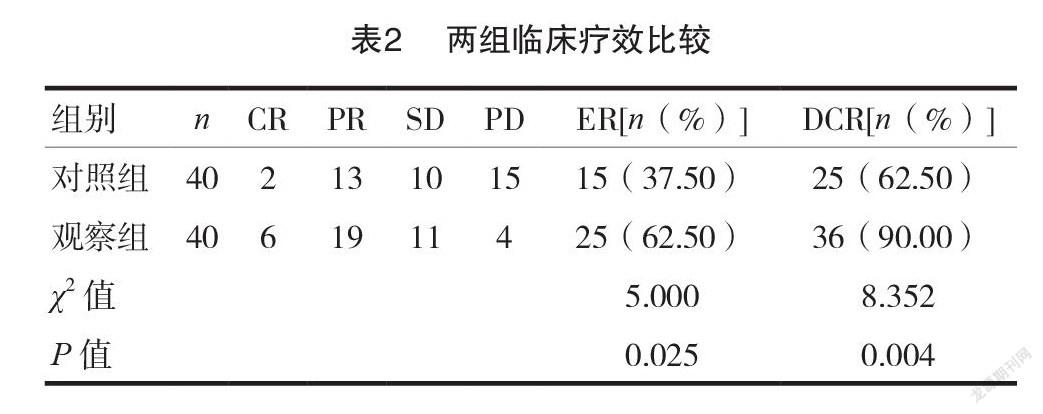
2.2两组临床疗效比较
观察组总有效率及控制率均显著高于对照组,差异有统计学意义( P <0.05),见表2。
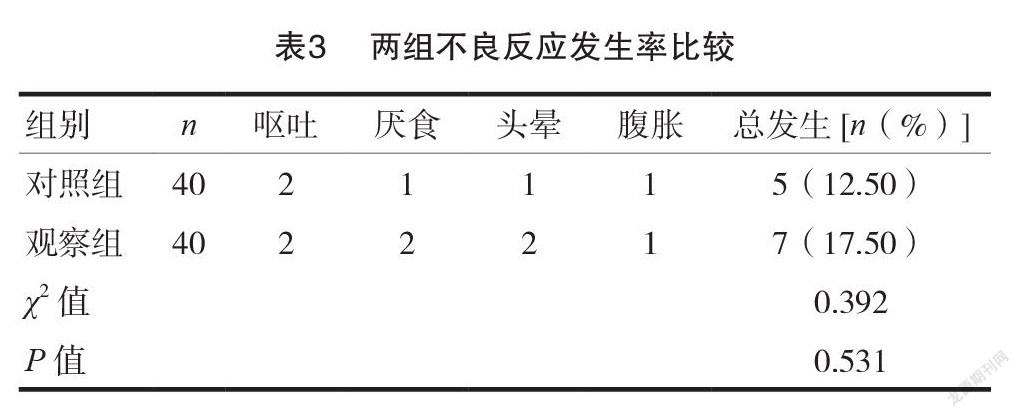
2.3两组不良反应发生率比较
观察组不良反应总发生率(17.50%)稍高于对照组(12.50%),但差异无统计学意义( P >0.05),见表3。
3讨论
结直肠癌为临床上常见的恶性肿瘤,又称大肠癌,主要涵盖结肠癌和直肠癌。其发病主要与遗传、饮食及生活习惯等因素有关[10]。结直肠癌常见于中老年,且男性发病率较女性更高。该病早期无显著症状,仅表现为腹泻、腹痛等局部症状,随着病程进展可出现不同程度全身症状[11]。因临床对早期结直肠癌的诊断方法仍较为匮乏,故常导致病情拖延至中晚期就医而被确诊。而当癌症进入中晚期时,往往肿瘤细胞严重转移,导致严重全身症状发生,患者因失去最佳手术时机,往往需要化学治疗。化疗是指通过化学药物治疗的方式以达到杀死癌细胞的目的[12-13]。临床常以伊立替康为治疗晚期结直肠癌的主化疗药物,取得了一定效果,但结果仍不理想。近年来,随着医学的发展,科学家发现肿瘤化疗中分子靶向药物具有重要价值。分子靶向药物主要通过阻断肿瘤细胞的分裂,抑制其不断侵袭正常细胞的能力,达到控制肿瘤细胞的生长、扩散的目的。因此,临床治疗方案可采用化疗联合分子靶向药物来治疗晚期肿瘤。贝伐珠单抗则是一种能通过抑制血管内皮生长因子而达到抑制癌症细胞转移的重组人源化、人鼠嵌合单克隆抗体[14-15]。本研究即对贝伐珠单抗靶向治疗联合FOlFIRlLOX化疗方案治疗晚期结直肠癌的效果及对患者免疫功能的影响展开探究。
有研究表明多数肿瘤患者在并发过程中常伴有大量新生血管形成的过程。肿瘤的附着、生长及转移均需要养分,而局部血管密集可为癌细胞提供足够养分为其提供侵袭正常细胞的能源,而加速肿瘤的转移[16]。血管内皮生长因子(VEGF)又称血管通透因子,对于血管生成起促进作用,其主要结合相应受体,而促进血管内皮细胞生长,因此其为临床靶向治疗的重点关注对象之一[17]。贝伐珠单抗进入人体后能够通过特异性与 VEGF 受体-2(VEGFR-2)竞争性结合 VEGF-A,抑制 VEGF 发挥包括降低血管的渗透性、抑制肿瘤血管内皮细胞增生以及内皮细胞迁移与存活的生物学作用,从而完成抗血管异常生成等抑制肿瘤血管生成、生长以及转移的效果[18-19]。CEA、CA19-9及 CA242为临床上重要的肿瘤标志物,其在血清中的浓度直接反应患者癌症的病情严重程度与发展阶段。CEA 糖蛋白为中晚期肿瘤的广谱标志物,能够对结直肠癌的病程及发展情况起重要指示作用;CA19-9糖抗原胃肠道相关抗原,对结直肠癌的诊断起辅助作用; CA242为唾液酸化的糖抗原,其在结直肠癌诊断中具有较高的灵敏度及特异性[20]。
本研究结果显示,治疗后观察组血清中3项免疫功能指标及3项肿瘤标志物指标均显著低于对照组,差异有统计学意义( P <0.05);提示联合治疗较单独化疗具有更为理想的抑制肿瘤效果。而血清中免疫球蛋白 IgG、IgM 及 ALB 的含量也与肿瘤的进展相关,肿瘤分化程度更高,发展更为严重常导致体内免疫球蛋白过量表达以发挥抗肿瘤功能,而血清中免疫球蛋白及 ALB 浓度趋于减少,预示着机体处于恢复好转,肿瘤得以控制等状况[21]。观察组总有效率(62.50%)及控制率(90.00%)均显著高于对照组(37.50%、62.50%),差异有统计学意义( P <0.05);结果表明观察组能够显著提高患者的治疗有效率,有效地控制了疾病的发展,避免病情进一步恶化而病死等严重不良转归。除有效性外,安全性也是药物临床应用的重要判定指标之一。在治疗过程中两组呕吐、厌食、腹胀及头晕不良反应发生情况差异无统计学意义,预示联合治疗并不增加不良反应发生的风险。因贝伐珠单抗能够特异性阻断肿瘤细胞血管的生成,因此可能出现凝血功能障碍,最显著不良并发症则为出血,结直肠癌患者可能会出现皮肤黏膜或胃肠道出血及便血的发生[22]。但在本研究中無出血症状的发生,显示出贝伐珠单抗若严格按照说明书剂量范围使用具有较高安全性,不易造成出血等不良并发症的发生。有报道显示 VEGF 促进内皮细胞生长能够有助于前列腺素及一氧化碳的产生,从而舒张血管,而抑制其则可导致高血压的发生。但还与年龄等因素有一定关联,并且与年龄增长成正比关系。观察组不良反应总发生率(17.50%)稍高于对照组(12.50%),但差异无统计学意义(P >0.05)。该结果证实运用贝伐珠单抗靶向治疗联合FOlFIRlLOX化疗方案并未增加不良反应发生的风险。综合所有结果,充分证实联合治疗手段能有效控制疾病发展并对消除临床表征及病灶有一定作用,且不增加如呕吐、腹胀、出血、厌食等不良反应,因此是一种安全有效的方案。
综上所述,在晚期结直肠癌患者中运用贝伐珠单抗靶向治疗联合FOlFIRlLOX化疗方案能够有效降低血清学中肿瘤标志物水平,能够有效缓解症状体征,有助于病灶的消除,并且不增加如呕吐、厌食、头晕、腹胀不良反应,值得在临床中推广。
[参考文献]
[1]张伟鹏,徐元元,刘苇,等.FOLFOXIRI 与 SOX 化疗方案治疗晚期结直肠癌的近期效果比较[J].肿瘤研究与临床,2018,30(8):548-552.
[2]李东玲,周京旭,朱茗祺,等.西妥昔单抗和贝伐珠单抗治疗晚期结直肠癌的有效性和安全性比较[J].现代生物医学进展,2019,19(8):1482-1485.
[3]邢丽,张勇,李娟,等.晚期结直肠癌一线化疗联合贝伐珠单抗疗效与 k-ras基因状态的关系[J].河北医学,2018,24(6):886-890.
[4]徐蕾,邢丽,李明,等.KRAS 基因状态对晚期结直肠癌一线化疗联合贝伐珠单抗疗效的预测价值[J].蚌埠医学院学报,2019,44(5):593-596.
[5]张定国,阮建,阮秀丽.XELOX 与 FOLFOX6应用于晚期结直肠癌治疗的临床观察[J].实用癌症杂志,2018,33(4):618-620.
[6]纪荣佳,管凯,庄建发,等.贝伐珠单抗联合化疗治疗晚期大肠癌的疗效和安全性的 meta 分析[J].海军医学杂志,2018,39(6):526-532,544.
[7]高玉芹,卫刚要,魏军功,等.贝伐珠单抗联合化疗治疗结直肠癌肝转移的疗效观察[J].中国肿瘤临床与康复,2018,25(3):262-265.
[8]Bosman FT,Cameiro F,Hruban RH,et al.World health organization classification of tumours of the digestive system[M].Lyon:IARC Press,2010.
[9]顾瑞冬,马兴群,王琳.晚期结直肠癌抗血管生成药物疗效评价的研究进展[J].临床肿瘤学杂志,2019,24(1):81-86.
[10]欧阳运洁,刘利民,戴广海,等.贝伐珠单抗联合化疗治疗晚期十二指肠癌的临床疗效分析[J].实用肿瘤杂志,2019,34(6):524-528.
[11]郑玲利,袁明勇,蒋婷,等.贝伐珠单抗联合化疗/ EGFR-TKI 治疗晚期肺癌安全性的 Meta 分析[J].药物流行病学杂志,2018,27(3):145-152.
[12]李小妹,顾艳,杨柳.FOLFIRI 联合艾迪注射液治疗晚期结直肠癌的疗效及对免疫功能的影响[J].癌症进展,2018,16(10):1257-1260.
[13]张轶雯,方罗,钟里科,等.贝伐珠单抗在我院抗肿瘤治疗中的应用分析[J].中国药房,2018,29(16):2252-2256.
[14]张音洁,王晰程,李健,等.三药联合方案治疗晚期转移性结直肠癌的疗效和安全性比较[J].中国肿瘤临床,2019,46(4):178-183.
[15]王霞,王会志,姜润学.贝伐珠单抗联合腹腔热灌注化疗治疗结直肠癌并发恶性腹水的临床分析[J].实用药物与临床,2020,23(10):905-908.
[16]张泽,修光宏,王晓东.晚期直肠癌放化疗对预后的影响因素分析[J].癌症进展,2018,16(5):658-662.
[17]梁振雄,王若天,符敏,等.贝伐珠单抗联合 XELOX 化疗对结直肠癌疗效,血清 CRP 水平及生存时间的影响[J].实用癌症杂志,2020,35(2):326-329.
[18]苏爱江,孙永琨,毛爱琴.贝伐珠单抗联合化疗对晚期结直肠癌的疗效及免疫功能的影响[J].现代消化及介入诊疗,2018,23(2):195-197.
[19]韩建雄,骆成俊,杨波,等.贝伐珠单抗联合不同化疗方案治疗转移性结直肠癌的疗效及安全性分析[J].解放军医药杂志,2019,31(10):27-30.
[20]董明君,戴晓宇,赖福记,等.贝伐珠单抗联合雷替曲塞或卡培他滨治疗老年晚期结直肠癌的疗效及安全性观察[J].浙江医学,2019,41(23):2540-2542.
[21]邓文静,余更生,刘爱,等.贝伐珠单抗联合 mFOLFOX6治疗转移性结直肠癌的临床疗效及左右半结肠癌的疗效差异[J].现代肿瘤医学,2020,28(5):779-783.
[22]贾建宾,聂双发,李磊,等.贝伐珠单抗联合 FOLFOX-6化疗方案对晚期结肠癌患者细胞凋亡及相关蛋白表达的影响[J].中国医药,2018,13(10):1518-1521.
(收稿日期:2021-06-29)
