芳基亚磺酸钠作为含硫砌块合成吡咯并[1,2-a]吲哚
2021-08-25李梦婷宁志涛王璐瑶杜正银
李梦婷,王 丹,宁志涛,王璐瑶,杜正银
(西北师范大学 化学化工学院,甘肃 兰州 730070)
0 引言
吡咯并[1,2-a]吲哚是天然产物[1,2],抗癌药[3]和抗肿瘤药[4]中常见的结构片段。在图1中列举了一些含有吡咯并[1,2-a]吲哚骨架的生物活性分子,例如lisatisine A具有抗病毒的作用,Flinderole C作为一种抗疟药,Mitomycin C (MC)具有抗癌功效,化合物D具有抗肿瘤功效等。由于含有吡咯并[1,2-a]吲哚结构片段的化合物具有很好的药用价值,因此近年来吡咯并[1,2-a]吲哚衍生物的合成引起了化学家们的极大兴趣。据已有文献报道,通过N-炔丙基吲哚的串联自由基环化/异构化反应能够合成了一系列吡咯并[1,2-a]吲哚衍生物,而自由基串联环化反应作为高效的构建杂环化合物的重要策略被广泛应用[5]。在图2中可以看到,合成的化合物具有四种可能的结构F、G、H和I,这主要取决于合成化合物的反应条件。唐果课题组[6]和朱成建课题组[7]以二苯基膦氧化物为自由基试剂,使用N-炔丙基吲哚和二苯基膦氧化物在不同的反应条件下,利用过渡金属催化合成了2-膦酰基-9H-吡咯并[1,2-a]吲哚F。前不久,Reddy课题组报道了N-炔丙基吲哚与以碳为中心的酰基自由基试剂反应,合成了单酰基和双酰基吡咯并[1,2-a]吲哚F[8]。这些转化足以证明N-炔丙基吲哚可作为良好的自由基受体。
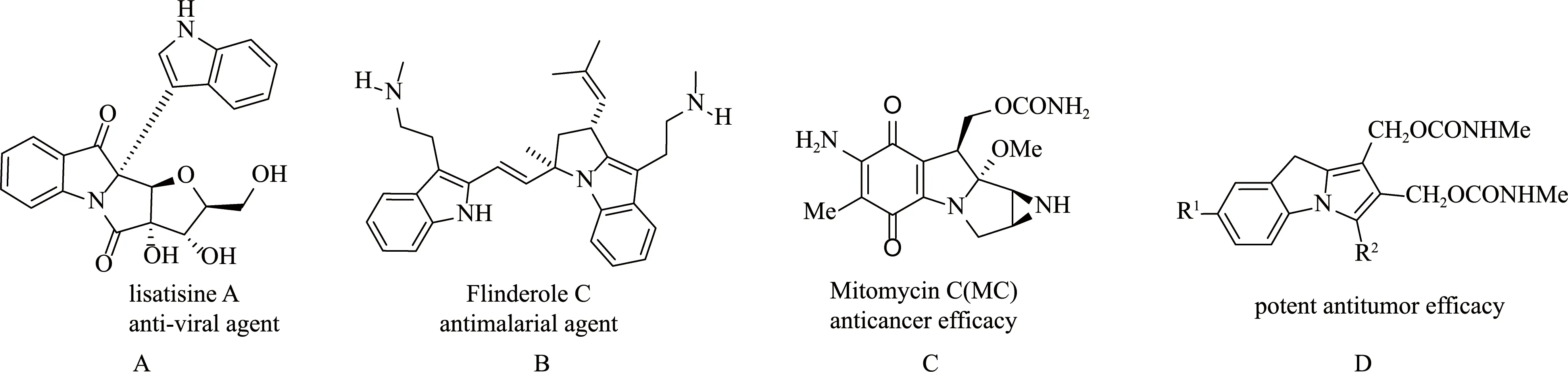
图1 具有生物活性的吡咯并[1,2-a]吲哚衍生物
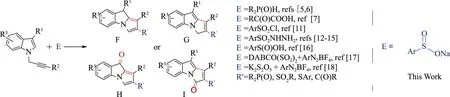
图2 N-炔丙基吲哚的串联自由基环化/异构化反应
在自然界中普遍存在许多含硫的有机化合物[9]。在有机分子中引入含硫基团可以大大增强其生物活性[10]。目前已经有研究小组引入了含硫基团以促进N-炔丙基吲哚的串联自由基环化/异构化反应。张鹏波课题组报告了N-炔丙基吲哚与磺酰氯在光催化剂fac-Ir(bpy)3的催化下,以CH2Cl2为溶剂,加入2.0当量Na2CO3反应12 h,可以有效的合成2-磺酰化9H-吡咯并[1,2-a]吲哚衍生物F[11]。此外芳基磺酰肼也可作为含硫基团与N-炔丙基吲哚反应,以获得不同的吡咯并[1,2-a]吲哚衍生物。唐果课题组已经报道使用NaI为催化剂和TBHP氧化条件下可生成2-磺酰化9H-吡咯并[1,2-a]吲哚衍生物F[12],而成江课题组使用CuSO4和K2S2O8时反应生成了2-硫代3H-吡咯并[1,2-a]吲哚衍生物G[13]。同样梁永民课题组分别使用CuCl2-TBHP和Cu(NO3)2-TBHP反应体系制备了2-磺酰化9H-吡咯并[1,2-a]吲哚-9-酮H[14]和2-磺酰化3H-吡咯并[1,2-a]吲哚-3-酮I[15]。2019年,王磊课题组开发了一种使用芳基亚磺酸作为磺酰化试剂合成2-磺酰化9H-吡咯并[1,2-a]吲哚F的方法[16]。但是,该反应必须在N2气氛中进行,并且需要2.0当量的AgOAc作为氧化剂。DABCO·(SO2)2[17]和K2S2O5[18]作为二氧化硫的方便来源,与四氟硼酸芳基重氮盐、N-炔丙基吲哚三组分反应原位形成芳基磺酰基来制备2-磺酰化9H-吡咯并[1,2-a]吲哚F。近年来,使用苯亚磺酸钠作为新型的含硫结构单元构建S-C键已成为研究的热点[19-21]。因苯亚磺酸钠在空气中稳定,价格便宜且易于获得,因此引起了化学家广泛的重视。于是可以利用磺酰化试剂芳基亚磺酸钠在无过渡金属I2促进的温和反应条件下与N-炔丙基吲哚发生串联自由基环化反应,以实现9H-吡咯并[1,2-a]吲哚衍生物的合成。
1 实验部分
1.1 试剂与表征
实验中所用的石油醚和乙酸乙酯为工业品,使用前需进行蒸馏纯化,其他所有试剂均为市售分析纯。核磁共振氢谱(1H NMR): 400 MHz核磁共振仪或600 MHz核磁共振仪。核磁共振碳谱(13C NMR): 150 MHz核磁共振仪。CDCl3为溶剂,TMS作为内标。化学位移(δ)以ppm给出,偶合常数(J)以赫兹(Hz)给出。熔点是在X-4型显微熔点测定仪上测定,熔点未校正。ZAB-HS双聚焦高分辨质谱仪测定高分辨质谱。
1.2 实验步骤
向20 mL 反应管中依次加入1 (0.15 mmol),2 (0.45 mmol),I2(0.15 mmol)和六氟异丙醇(2 mL)。旋紧反应管盖子,将反应混合物在油浴中于120 ℃搅拌12 h。反应液减压蒸馏去除溶剂后,通过硅胶柱层析分离反应体系,石油醚和乙酸乙酯作为洗脱剂,得到所需产物。产物大多数为已知化合物,有一种新的化合物,得到的目标产物经核磁1H NMR和13C NMR进行表征,与文献表征结果一致,具有代表性的化合物的表征数据如下:2-((4-(Tert-butyl)phenyl)sulfonyl)-1-phenyl-9H-pyrrolo[1,2-a]indole.Pale yellow solid; mp 101-102 °C.1H NMR(600 MHz, CDCl3): δ 7.93 (s, 1H), 7.49 (d,J= 8.4 Hz, 2H), 7.39-7.29 (m, 8H), 7.27-7.25 (m, 2H), 7.20-7.18 (m, 1H), 3.82 (s, 2H), 1.24 (s, 9H);13C NMR(CDCl3, 150 MHz): δ 156.0, 139.6, 139.5, 135.2, 134.0, 132.5, 129.8, 128.0, 127.9, 127.2, 127.2, 127.0, 126.1, 125.4, 125.2, 117.5, 115.3, 110.8, 34.9, 31.0, 29.1. ESI-HRMS: [M+Na]+C27H25O2NNaS, cald, 450.1498; found, 450.1493.
2 实验结果与讨论
2.1 实验条件探究与优化
在此使用1-(3-苯基丙-2-炔-1-基)-1H-吲哚和4-甲基苯亚磺酸钠作为模板反应,对反应中底物的物料比﹑I2的用量﹑碱﹑氧化剂﹑溶剂和温度进行了筛选,结果如表1所示。最初,我们选用1-(3-苯基丙-2-炔-1-基)-1H-吲哚(1a,1.0 equiv)和4-甲基苯亚磺酸钠(2a,3.0 equiv)进行反应。当加入1.0当量I2作为催化剂,乙醇作为溶剂时,在80 ℃氩气气氛下反应进行12 h后,得到了所需产物2-甲苯基-9H-吡咯并[1,2-a]吲哚3a,产率为48%(entry 1)。为了提高产物产率,我们试图增加2a和I2的量。实验结果表明使用2.0当量的I2会导致3a收率降低至15%,探究其原因是由于形成了复杂的反应混合物(entry 2)。当增加2a为4.0当量时生成3a的产率为46%,产率并没有明显的变化(entry 3)。在没有添加I2作为催化剂的情况下,反应没有发生,由此可见,I2的存在对该反应至关重要(entry 4)。当反应时间从12 h延长至15 h时,产物产率增加至53%(entry 5)。接下来我们研究了碱和氧化剂对产物产率的影响。结果表明,加入Na2CO3和Cs2CO3导致反应体系比较复杂,获得3a的收率分别为5%和12%(entries 6 and 7)。在反应中同时加入1.0 当量的叔丁基过氧化氢(TBHP)和1.0 当量的I2时获得了23%的收率(entry 8)。随后我们对不同溶剂(如乙醇、四氢呋喃、1,4-二恶烷、二甲基亚砜、硝基甲烷、1,2-二氯乙烷、甲苯和六氟异丙醇(HFIP)进行了筛选(entries 1,9-15)。发现六氟异丙醇对该反应最有利,以66%的产率获得了3a。之后我们就以六氟异丙醇为反应溶剂,进一步探究了反应温度,发现在59 ℃的回流条件下获得了痕量的目标产物,而当在密封的反应管中120 ℃氩气气氛下进行反应时,获得了3a的产率为70%(entries 16 and 17)。该反应也能够在空气气氛于120 ℃条件下进行,得到71%的3a(entry 18)。根据上述实验结果,我们选择的最优条件是在1.0当量I2促进下,N-炔丙基吲哚与芳基亚磺酸钠物料比为1:3,六氟异丙醇为溶剂,120 ℃反应12 h,得到9H-吡咯并[1,2-a]吲哚产率最高。
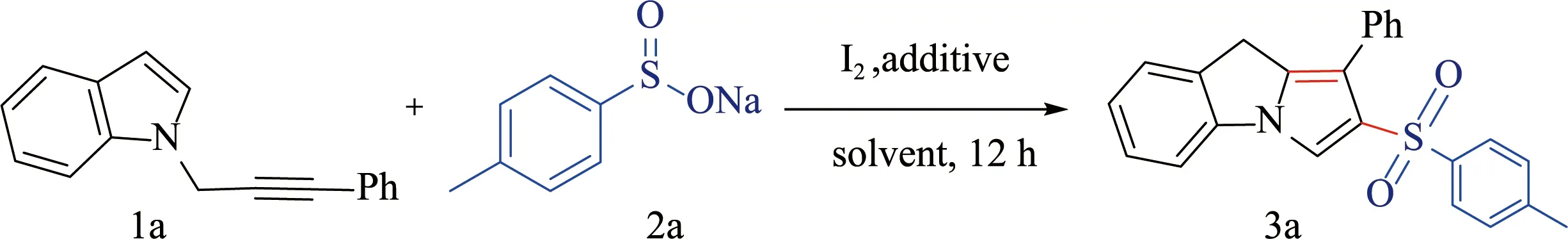
表1 优化反应条件a
2.2 实验底物适用范围的拓展
通过上述我们得到的最佳反应条件,我们对底物的适用范围进行研究。结果如图3所示。用各种芳基亚磺酸钠2与1-(3-苯基丙-2-炔-1-基)-1H-吲哚1a化合物进行底物的拓展。发现给电子基芳基亚磺酸钠和4-叔丁基苯亚磺酸钠在该反应中均能顺利进行,得到相应的产物3a,3b和3c,产率分别为71%,63%和58%。各种含有吸电子基团的芳基亚磺酸钠,例如4-F,4-Br和4-CF3,也可以19%-34%的产率转化为相应的2-磺酰化9H-吡咯并[1,2-a]吲哚(3d-f)。2-萘基亚磺酸钠在该磺酰化/环化反应中也是能够进行的,尽管得到目标产物3g收率较低为16%。其次,还研究了连接在底物1碳碳三键上不同取代基R1对反应的影响。当R1是给电子基团4-甲基,3-甲基,4-乙基和4-叔丁基时,底物1与2a的反应能够顺利进行得到相应的产物3h-k,产率约为60%。在此条件下,芳环上的卤素原子氟,氯和溴也具有良好的官能团耐受性,以38%-62%的产率得到了预期的产物3l-n。此外,4-CF3和4-CN作为强吸电子基团可能因为电子效应导致反应性不太好,分别以30%和29%的产率得到相应的产物3o和3p。最后,我们研究了吲哚骨架中苯环上不同位置的各种取代基。令我们高兴的是,在吲哚环上包含3-甲基,7-甲基,6-甲基和5-甲氧基的底物表现良好,以51%-73%的收率获得了目标产物3q-3t。卤素原子(例如6-F和6-Cl)取代的吲哚也能顺利进行该反应,并以中等收率得到所需的产物3u-3v。由此看出,取代基的电子效应对产物的产率具有明显的影响。
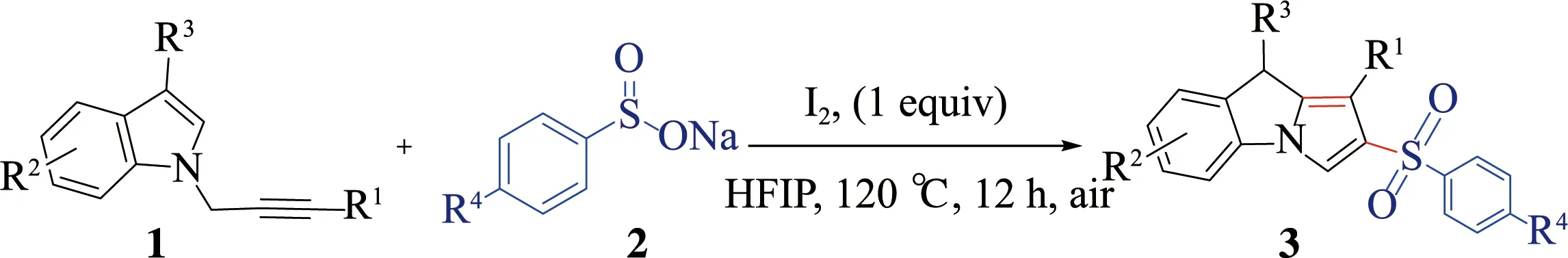
注:a:Reaction conditions: 1 (0.15 mmol), 2 (3.0 equiv), I2 (1.0 equiv), HFIP (2 mL) in air at 120 ℃ for 12 h in a sealed pressure tube。
2.3 反应机理探讨
为了验证碘促进的N-炔丙基吲哚与芳基亚磺酸钠的串联自由基环化反应的机理,在标准反应条件下我们进行了一些加入自由基捕获剂的对照实验(图4)。结果表明,当4.0当量的2,2,6,6-四甲基哌啶氮氧化物(TEMPO)被添加时,没有发现任何目标产物,说明该反应被完全抑制。当添加4.0当量的2,6-二叔丁基-4-甲基苯酚(BHT)和1,1-二苯基乙烯时,反应被部分抑制,分别仅获得33%和42%的3a。值得注意的是,当添加1,1-二苯基乙烯时,通过ESI-HRMS分析检测到了1,2-二苯基-2-甲苯基乙烯的捕获产物([M+H]+C21H19O2S,计算值为335.11003,检测值为335.11001)。这些结果表明该转化可能涉及串联自由基过程,并且在反应过程中形成了磺酰基自由基(图4)。
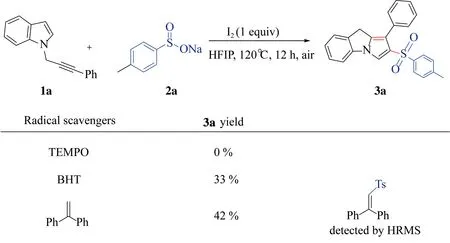
图4 对照实验
由已报道文献[7]和上述对照实验结果可知,该反应可能为自由基反应(图5)。首先,当对甲基苯亚磺酸钠被I2氧化时,就会形成对甲基苯磺酰基自由基。然后对甲基苯磺酰基自由基进攻1a的碳碳三键,形成了自由基中间体I。中间体I经过自身分子内环化形成自由基中间体II。然后,自由基中间体II被I2氧化,发生电子转移形成阳离子中间体III。最后,阳离子中间体III去质子化生成中间体化合物IV,中间体化合物IV将进一步异构化为所需产物3a。
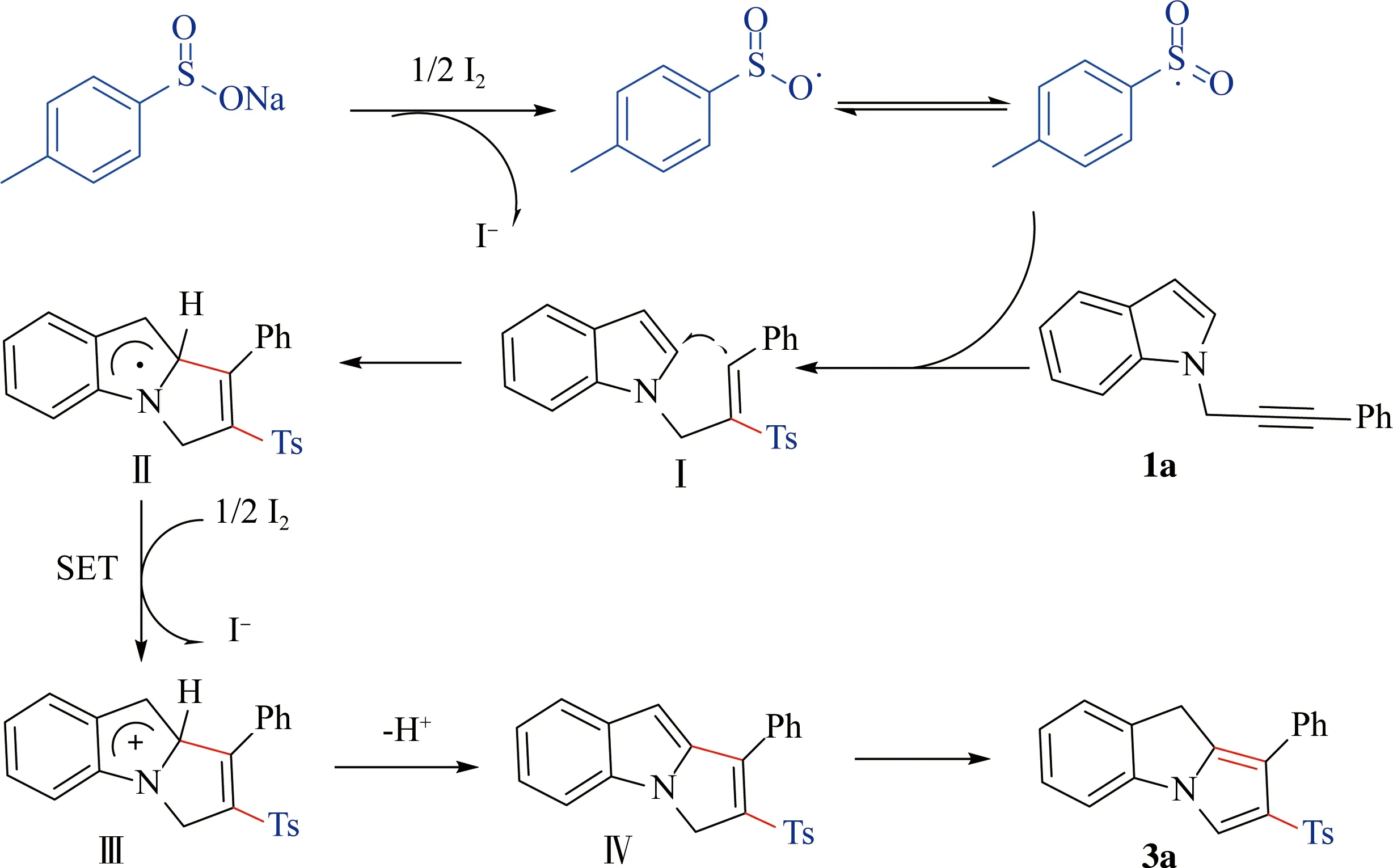
图5 可能的反应机理
3 结论
总之,我们已经开发了一种由N-炔丙基吲哚和芳基亚磺酸钠为反应底物,通过串联自由基磺酰化/环化/异构化反应的方法来合成2-磺酰化9H-吡咯并[1,2-a]吲哚。我们在温和的反应条件下以中等至良好的产率获得了所需的产物。简单的操作,良好的官能团耐受性和容易获得的原料使该方案成为获得9H-吡咯并[1,2-a]吲哚的有效合成方法。
