原发性肝脏血管肉瘤患者生存影响因素分析:基于SEER数据研究
2021-08-24冯政凯吴阳
冯政凯 吴阳
郑州大学第一附属医院肝胆胰外科 郑州 450052
血管肉瘤是血管或淋巴管内皮细胞、肌肉、脂肪等间叶组织起源的具有高度恶性和侵袭性的恶性肿瘤。原发性肝脏血管肉瘤(Primaryhepaticangiosarcoma,PHA)约占所有血管肉瘤的5%,占所有肝脏原发恶性肿瘤的2%[1]。由于其低发病率、高度恶性和较快的病情进展,现有研究多为单中心或多中心回顾性少量有限的病例报道性研究,尚无PHA临床特征、治疗方法,以及影响生存相关因素的研究。监测,流行病学和最终结果(TheSurveillance,EpidemiologyandEndResults,SEER)数据库由美国于1973年成立,目前该数据库覆盖了美国17个地理区域,纳入了美国28%人口的癌症统计登记[2]。SEER定期收集有关患者人口统计学、原发肿瘤部位、肿瘤形态和诊断阶段、癌症治疗的初始过程,以及生命状态信息随访的数据,在过去的20年内,SEER登记被广泛应用于肿瘤学的研究[3]。截至目前,我们未发现利用SEER数据库对PHA进行的流行病学研究。因此,本研究利用SEER数据库的大样本病例、时间跨度,以及数据公开等优势,纳入了1975—2016年SEER数据库登记的PHA病例(是迄今最大样本量的PHA研究),以分析影响PHA生存的影响因素。
1 资料与方法
1.1数据资料提取SEER数据库1975—2016年登记的所有PHA患者,肿瘤学疾病的国际分类,第三版组织学编码9120(angiosarcoma,血管肉瘤),结合位点编码C22.0(liver,肝脏)来确定PHA患者。提取变量:性别、年龄、种族、SEER分期、手术治疗、放射治疗、化疗、生存时间、生存状态等。根据SEER分期对肿瘤进展程度进行分类:Localized(局限,肿瘤局限于肝脏),Regional(局部进展,肿瘤直接扩展或局限于区域淋巴结)和Distant(远处转移)。2003年之前,外科手术治疗编码:移植(70),手术切除(20~32),局部消融(10)。2004年起移植被编码为(61),手术切除编码为(20~60),肿瘤局部灼烧为(10~17)。
1.2数据方法连续变量采用均数±标准差或中位数(IQR,四分位数) 表示;分类变量以数字和百分比(%)表示。计算生存率及生存曲线绘制采用寿命表法和Kaplan-Meier方法绘制。COX风险比例模型进行单因素和多因素分析,将单变量因素P<0.05的纳入多变量分析,双侧P<0.05认为差异有统计学意义。所有统计分析均使用SPSS26.0软件(IBMSPSS26.0,Armonk,NY,USA)实现。
2 结果
2.1临床资料本研究共计纳入1975—2016年登记的有完整治疗及随访资料的PHA患者301例,见表1。

表1 PHA患者临床特征
2.2PHA患者的生存特征本研究中PHA患者的整体1a、3a生存率分别为13.0%(95%CI9.0%~16.9%)和6.0%(95%CI4.0%~7.9%),中位生存时间为1.7个月。手术治疗组中位生存时间为6.0(IQR,2.0~25.0)个月,与未手术治疗组差异显著(P<0.001)。化疗组的中位生存时间为5.0(IQR,2.0~13.0)个月,与未化疗(或未知)组的差异显著(P<0.001)。放射治疗组的中位生存时间为4.0(IQR,1.0~12.0)个月,与未放射治疗(或未知)组无显著差异(P=0.069)。
2.3影响PHA患者整体生存的COX单因素和多因素分析对各变量进行COX单因素分析,结果显示:性别、年龄、肿瘤SEER分期、手术治疗、化疗等因素是影响PHA患者生存的独立危险因素,见表2。将以上因素纳入COX多因素回归分析,结果显示:年龄、肿瘤SEER分期、手术治疗、化疗等是影响PHA患者长期生存的独立危险因素(P<0.05),见表3。年龄≥60岁患者的死亡风险是年龄<60岁患者的1.842(95%1.429~2.374,P<0.001)倍。未手术治疗或未治疗患者较手术治疗患者的死亡风险增加1.895(95%CI 1.348~2.653, P<0.001)倍。未化疗较化疗患者的死亡风险增加2.153(95%1.650~2.809,P<0.001)。年龄<60岁、早期的SEER肿瘤分期、手术和化疗等是PHA患者生存的保护因素。
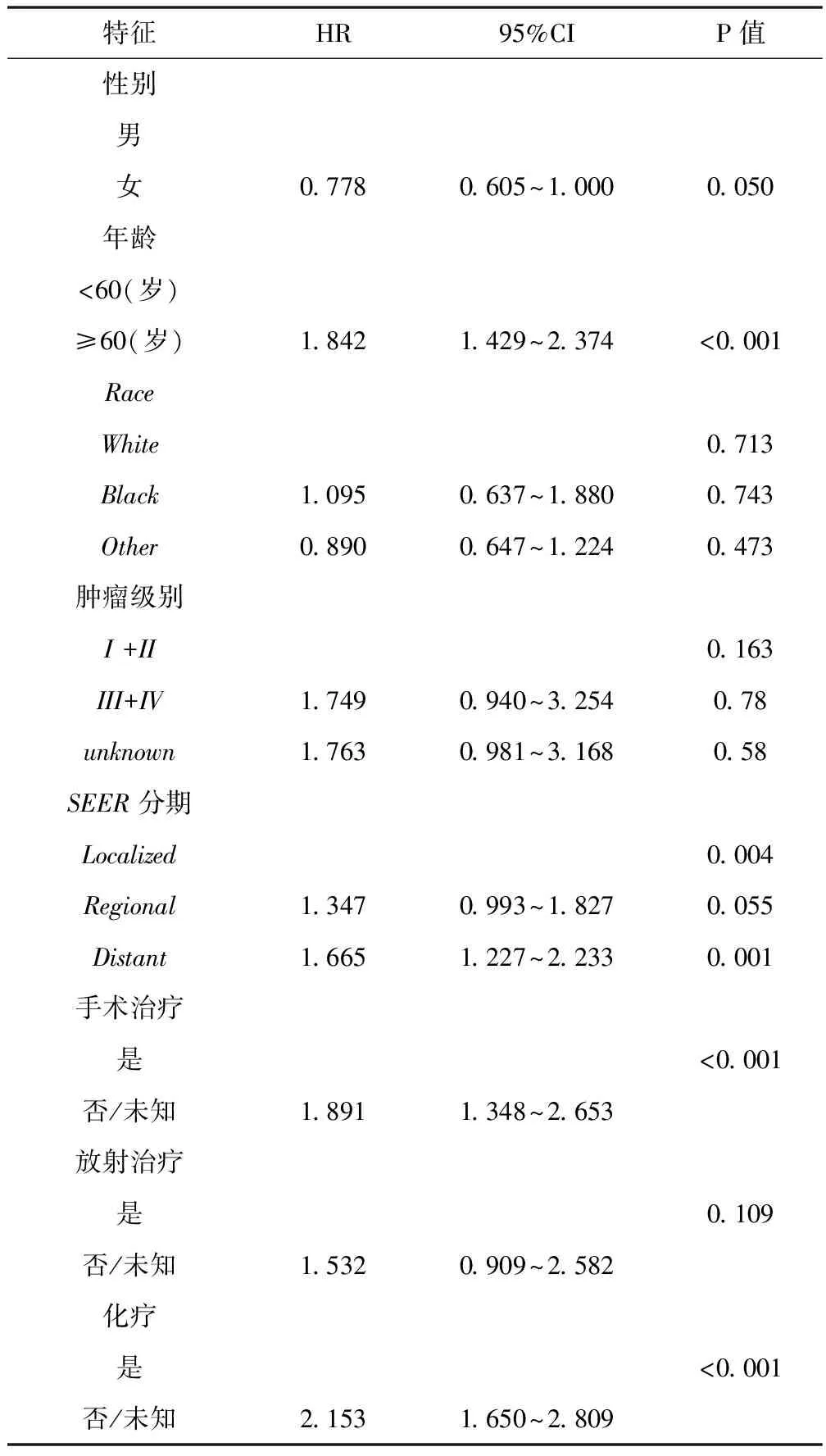
表2 影响PHA患者生存的COX单因素分析

表3 影响PHA生存的COX多因素分析
3 讨论
PHA是一种罕见的高度恶性的血管源性肝脏原发恶性肿瘤。发病原因尚不明确,可能与氯乙烯、砷、二氧化钍、镭、杀虫剂、放疗和辐射等接触史和暴露史有关[4-5]。PHA患者缺乏特异性临床症状,常表现为腹痛、腹胀、乏力和体质量减轻[5-6]。亦有报道显示破裂出血、异常凝血和急性肝功能衰竭等可为首发症状[7-8]。有研究建议DIC合并肝血管性肿瘤影像学征象时,应高度怀疑PHA[9-11]。
既往研究显示,PHA的中位生存时间为1~8个月[10-11],本研究为1.7个月,与Ryan[10]等的研究结果相近。可能原因是本研究纳入大量未治疗或姑息性治疗的病例,亦可能是现有诸多研究纳入的病例较多为手术治疗和效果较好的患者[12-13]。目前肝移植[14-15]、手术切除[16]、肿瘤消融、TACE(肝动脉化疗栓塞术)[17-18]、化疗[19]、放射治疗、分子靶向治疗[20-21]等,均有用于PHA治疗的报道。一些研究表明,手术切除仍是首选治疗方法,术后患者获得了较为理想的预后生存效果[6,12,21]。本研究中手术治疗患者的中位生存时间为6.0个月,优于放疗和化疗组。肝移植作为早期肝癌的最佳治疗方法,在PHA的治疗中常因早期复发和较快的病程进展已不被推荐[14,22]。欧洲肝移植登记处已将PHA列为肝移植的绝对禁忌证[17]。Li[15]等对1980—2017年75篇文章共纳入184例患者进行了最大样本量的汇总研究,总体中位生存时间为8个月。亚组分析显示,手术切除、化疗、肝移植和支持治疗的中位生存时间分别为15、10、5、1.3个月,并且建议对于可切除的PHA患者应首选手术切除。研究表明,约40%PHA患者确诊时已经存在局部或远处转移失去手术机会,化疗或姑息性化疗能够改善不可切除PHA患者的生存状态[15,19]。本研究中肿瘤的局部进展或远处转移等因素是PHA患者长期生存的独立危险因素,且化疗组的中位生存时间为5.0个月,仅次于手术治疗组。COX比例模型多因素分析表明,化疗是PHA患者长期生存的保护因素,因此对失去手术机会的PHA患者可行化疗。PHA破裂出血患者的生存时间往往少于1个月,TACE是首选治疗方法,在一定程度上也能预防肿瘤出血和改善伴有或不伴有肝内转移的PHA患者的预后生存期质量[18]。由于本研究中缺乏导管治疗信息,因此无法将TACE治疗与其他治疗方式进行比较研究。
综上所述,PHA是一种罕见的预后极差的肝脏恶性肿瘤,年龄<60岁、局部进展或远处转移患者的预后较差。PHA患者确诊时多已失去手术机会,对于可切除的患者,手术是改善预后生存期最理想的治疗方式;对于失去手术机会的进展期或远处转移的PHA患者,化疗亦可获得较为理想的预后生存期。
