急性脑梗死患者血清脂蛋白a、MMP-9、D-D水平及其与颈动脉粥样硬化的相关性
2021-08-21荆晓晴王美丽
任 蔚,荆晓晴,王美丽
(宁夏第五人民医院石嘴山中心医院,石嘴山 753200)
急性脑梗死(acute cerebral infarction,ACI)是一种临床常见病,多见于中老年人群,具有较高的发病率、致残率、致死率[1]。据不完全统计[2],近70%的脑卒中患者为ACI。目前,ACI与恶性肿瘤、心肌梗死并列为致残率最高的三种疾病[3]。动脉粥样硬化(AS)是引发ACI的重要原因和病理基础[4]。ACI是一种多因素诱导性疾病,长期炎性反应损伤血管内皮细胞,血液高凝状态下形成血栓是引发ACI的重要因素。基于此,本研究选择宁夏第五人民医院2017年3月至2020年3月收治的75例ACI患者,通过检测脑损伤标记物基质金属蛋白酶-9(MMP-9)、血液高凝状态标记物D-二聚体(D-D)、AS形成独立危险因子脂蛋白a[LP(a)],分析ACI患者颈AS斑块形成与血清LP(a)、MMP-9、D-D水平的相关性。
1 资料与方法
1.1 一般资料
选择本院2017年3月至2020年3月收治的75例ACI患者作为观察组,选择同期门诊体检的75例健康人员作为对照组。观察组女性30例、男性45例;年龄42~81岁,平均(61.52±2.17)岁;体质量指数(BMI)为20~27 kg·m-2,平均(23.56±0.47)kg·m-2。对照组女性32例、男性43例;年龄43~80岁,平均(61.54±2.14)岁;BMI为21~27 kg·m-2,平均(23.59±0.44)kg·m-2。两组年龄、性别、BMI差异均无统计学意义(P均>0.05)。本研究经医院伦理委员会批准。
1.2 纳入、排除标准
纳入标准:1)观察组患者均符合《中国无症状脑梗死诊治共识》[5]中对“ACI”的诊断标准;2)均为首次发病;3)均在48 h内确诊;4)临床资料齐全、完整;5)患者家属均已签署与本项研究有关的知情同意书。排除标准:1)合并器官功能衰竭、障碍者;2)合并外科手术者;3)合并急慢性感染性疾病者;4)合并糖尿病、甲状腺功能亢进者;5)研究未开展前接受过对症治疗者;6)处于哺乳期、妊娠期女性;7)存在乙醇、药物滥用史者;8)继发性高血压者;9)合并帕金森、癫痫等疾病者。
1.3 方法
1.3.1 血清LP(a)、MMP-9、D-D水平测定 抽取所有患者空腹静脉血5 mL,以10 cm离心半径、3000 r·min-1速率离心10 min,分离血清,以酶联免疫吸附法(ELISA)检测血清LP(a)、MMP-9水平;以全自动凝血仪(型号:日本希森美康CA-1500)检测D-D水平。试剂均由上海信裕生物技术有限公司提供,操作严格按照相关说明书进行。所有患者检验操作均由检验科的工作人员完成,确保检验操作流程无失误。
1.3.2 颈AS检测 采用彩色多普勒超声测量颈外动脉、颈内动脉、颈总动脉及分叉部位内中膜厚度(IMT),IMT大于1.0 mm表示增厚,局部IMT大于1.2 mm,突向管腔,即可判定为斑块形成[6]。以此为依据将ACI患者分为颈动脉正常组、颈AS组。
1.3.3 斑块性质判断 动脉管壁呈偏心性增厚状态,具有光滑表面,伴有强回声且回声均匀为稳定性斑块;斑块相对于周边组织为混合性或低回声,表面不平整、粗糙则为不稳定斑块[7]。
1.4 观察指标
比较观察组和对照组、颈动脉正常组和颈AS组、斑块不稳定组和斑块稳定组血清LP(a)、MMP-9、D-D水平。
1.5 统计学方法
2 结果
2.1 观察组、对照组血清LP(a)、MMP-9、D-D水平比较
观察组血清LP(a)、MMP-9、D-D水平均高于对照组(P均<0.05),见表1。
表1 观察组、对照组血清LP(a)、MMP-9、D-D水平比较(±s)

表1 观察组、对照组血清LP(a)、MMP-9、D-D水平比较(±s)
?
2.2 颈动脉正常组、颈AS组血清LP(a)、MMP-9、D-D水平比较
75例ACI患 者 中,28例 颈 动 脉 正 常,占37.33%;47例颈AS,占62.67%。颈AS组血清LP(a)、MMP-9、D-D水平均高于颈动脉正常组(P均<0.05),见表2。
表2 颈动脉正常组、颈AS组血清LP(a)、MMP-9、D-D水平比较(±s)

表2 颈动脉正常组、颈AS组血清LP(a)、MMP-9、D-D水平比较(±s)
?
2.3 斑块不稳定组与斑块稳定组血清LP(a)、MMP-9、D-D水平
75例ACI患 者 中,33例 不 稳 定 斑 块,占44.00%;42例稳定斑块,占56.00%。斑块不稳定组血清LP(a)、MMP-9、D-D水平均高于斑块稳定组(P均<0.05),见表3。
表3 斑块不稳定组与斑块稳定组血清LP(a)、MMP-9、D-D水平比较(±s)

表3 斑块不稳定组与斑块稳定组血清LP(a)、MMP-9、D-D水平比较(±s)
?
2.4 血清LP(a)、MMP-9、D-D水平与ACI患者颈AS程度、斑块性质相关性
血清LP(a)、MMP-9、D-D水平与ACI患者颈AS程度、斑块性质均呈正相关性(P均<0.05),见表4。
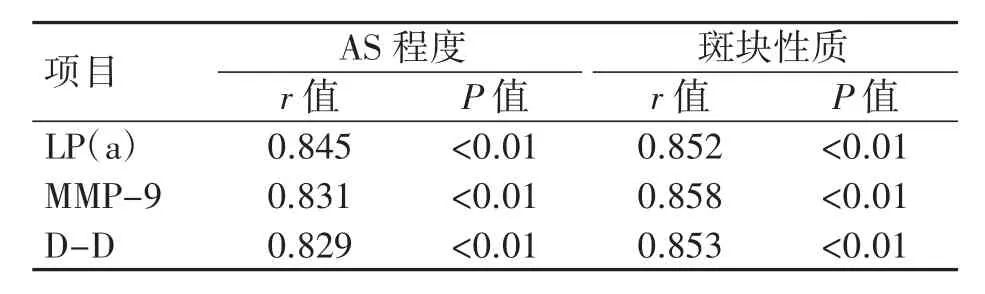
表4 血清LP(a)、MMP-9、D-D水平与ACI患者颈AS程度、斑块性质相关性
3 讨论
近年来,随着我国人们生活方式、饮食结构改变及人口老龄化进程的推进,ACI发病率明显增高[8]。有研究表明[9]:糖尿病、高血脂、高血压、吸烟、高龄等是引发ACI的独立危险因素。将近40%的ACI患者存在肢体功能障碍[10]。随着临床对ACI研究的深入,发现颈AS斑块破裂、脱落形成的栓子堵塞颅内动脉是引发ACI的重要原因[11]。AS与多种脑血管疾病的发生、发展有关,在脂质聚集的基础上,会伴有慢性炎性反应、基质降解。故及早发现、评估颈AS以及斑块性质,对于预防ACI发生发展意义重大。
LP(a)是一种大分子脂蛋白,富含大量的胆固醇,血脂沉积在血管壁,具有促进血栓形成和AS的作用。高水平的LP(a)是AS的独立危险因素。研究表明[12],LP(a)水平与遗传因素有关,与脂代谢、性别、年龄等无相关性。LP(a)作为一种独立的脂蛋白,受急性免疫反应、肾衰的影响较小,对于AS的发生具有良好的预知作用。Lee等[13]认为,血清LP(a)水平与ACI病变程度、病变范围呈正相关。本研究结果显示:观察组血清LP(a)水平高于对照组,颈AS组血清LP(a)高于颈动脉正常组,斑块不稳定组血清LP(a)水平高于斑块稳定组。血清LP(a)水平与ACI患者颈AS程度、斑块性质呈正相关性,表明ACI患者血清LP(a)水平较高,随着颈AS程度加重、斑块不稳定性增加,血清LP(a)含量也会逐渐升高,可作为ACI病情评估的一项重要指标。
MMP属于锌离子、钙离子依赖性蛋白酶,参与了人体中枢神经系统的病理、生理过程。MMP-9是MMP的重要家族成员,属于分解细胞外基质的多源糖蛋白,由血管内皮细胞、小胶质细胞、中性粒细胞分泌。MMP-9主要作用在Ⅳ及Ⅴ型明胶原,其中Ⅴ型的明胶原作为粥样斑块底膜的重要组成部分,在ACI病情发展中占有重要作用。有研究表明,MMP-9在AS发生、发展过程中发挥重要作用,MMP-9的作用机制是将Ⅴ型胶原酶激活,诱导其进入平滑肌细胞,促进AS斑块破裂[14]。MMP-9覆盖在斑块表面的纤维环被破坏,会将斑块稳定性降低,增加斑块的易损性。本研究结果显示:观察组血清MMP-9水平高于对照组,颈AS组血清MMP-9高于颈动脉正常组,斑块不稳定组血清MMP-9水平高于斑块稳定组。血清MMP-9水平与ACI患者颈AS程度、斑块性质呈正相关性,表明ACI患者机体血清MMP-9呈高表达状态。
D-D是纤维蛋白单体经过活化因子XⅡ交联之后,由纤溶酶水解而产生的一种降解产物,可以对纤溶过程做出准确反应。D-D可反映纤维蛋白的溶解功能,血清D-D水平升高,与机体受到多种因素的影响而形成血栓有着极为密切的联系。ACI发生、发展过程中,最先出现的是形成纤维蛋白原,进而发生纤溶亢进,最终导致血清D-D水平升高。本研究结果显示,观察组血清DD水平高于对照组,颈AS组血清D-D水平高于颈动脉正常组,斑块不稳定组血清D-D水平高于斑块稳定组。血清D-D水平与ACI患者颈AS程度、斑块性质呈正相关性。表明ACI患者血清D-D水平普遍较高,且颈AS及不稳定斑块患者血清D-D水平要明显高于颈动脉正常、稳定斑块患者,与Christersson等[15]研究结果接近。
综上所述,ACI患者血清LP(a)、MMP-9、DD水平呈高表达状态,与颈AS程度以及斑块性质呈正相关性,应当引起临床重视,通过加强血清LP(a)、MMP-9、D-D水平检测,及早评估、预测ACI发生风险,尤其对病损程度较重、病变范围较广的ACI患者提出预警。
