美沙拉嗪肠溶缓释片的制备与体外释放度考察
2021-08-19赵世娟严家瑞史婷严真尹莉芳
赵世娟,严家瑞,史婷,严真,尹莉芳
(中国药科大学药学院药剂系,江苏省缓释智能制剂及关键功能性辅料开发与评价工程研究中心,江苏 南京 210009)
溃疡性结肠炎是一种慢性终生性炎症性疾病,病因不明,可能由遗传易感性、环境等多种因素共同导致肠道免疫功能失调,从而导致肠道炎症,临床出现腹泻、血便、直肠出血、里急后重和腹痛等症状,特点为反复发作。调查显示,全球范围内,溃疡性结肠炎的发病率逐年上升[1-3]。
美沙拉嗪结构简单、安全性高,自20世纪40年代以来就用于治疗溃疡性结肠炎,目前用作一线治疗药物[4],作用机理未完全明确,在结肠黏膜处通过干扰多条炎症途径发挥抗炎作用[5],而普通制剂口服后被胃肠道近端迅速吸收,仅少量到达结肠,需多次给药,患者依从性差。为克服上述不良反应,结肠靶向美沙拉嗪制剂的研制成为研究热点[6]。
目前,国内市场上的美沙拉嗪制剂有栓剂、灌肠液、颗粒剂和肠溶片等,其中,口服制剂每天3~4次用药,患者顺应性差。美国上市的美沙拉嗪肠溶缓释片(商品名:Lialda)每天一次用于轻度至中度溃疡性结肠炎的诱导和维持缓解,极大提高了患者的顺应性,随后在英国、日本等国家上市。本课题以Lialda作为参比制剂,以体外释放为指标,筛选最优处方。
1 仪器与试药
AR223CN千分之一天平(奥豪斯仪器有限公司);MT-ME104/MT-XS105DU分析天平/MT-FE28 pH计(梅特勒-托利多仪器有限公司);热熔挤出机[安拓思纳米技术(苏州)有限公司];DP-30A单冲压片机(北京新龙立科技有限公司);YPD-300C型智能片剂硬度测定仪(上海黄海药检仪器有限公司);CHC-38高效包衣机(创志机电科技发展有限公司);RC-806D智能溶出试验仪(天津天大天发科技有限公司);UV-1800紫外分光光度仪(岛津有限公司)。
美沙拉嗪原料药(批号:2-20200615,牡丹江恒远药业股份有限公司);美沙拉嗪肠溶缓释片(批号:1165486,Shire Development Inc);巴西棕榈蜡(批号:2020030562,河南福美生物科技有限公司);硬脂酸(批号:20200203,湖州展望药业有限公司);羧甲基纤维素钠(CMC 7MF PH/CMC 7HXF PH,批号:NPF-0016/C192223,Ashland);羧甲淀粉钠/二氧化硅/硬脂酸镁(批号:191140/200111/200354,安徽山河药用辅料公司);滑石粉(批号:201901128,广西龙广滑石开发股份有限公司);丙烯酸树脂(批号:B191203218/B200405203,Eudragit L100/Eudragit S100,Evonik);柠檬酸三乙酯(批号:200304,蚌埠丰原涂山制药有限公司);二氧化钛/氧化铁红(批号:20200604/20200527,宁波一品生物技术有限公司);聚乙二醇6000(批号:20200305,江西阿尔法高科药业有限公司)。
2 方法与结果
2.1 释放度测定方法的建立
2.1.1 检测波长 文献报道,美沙拉嗪在0.1 mol·L-1盐酸溶液、pH 6.4和pH 7.2磷酸盐缓冲液中的溶解度(37 ℃)均高于2 mg·mL-1[7]。取美沙拉嗪原料药25 mg,精密称定,置50 mL量瓶中,分别加入上述3种介质溶解、稀释至刻度,摇匀,配制成浓度为0.5 mg·mL-1的储备液。分别精密量取2 mL储备液,置50 mL量瓶中,相应介质稀释至刻度,摇匀,作为供试品溶液,在190~500 nm波长范围内扫描,结果显示美沙拉嗪在3种释放介质中的最大吸收波长分别为303、330、331 nm,分别选择美沙拉嗪在各介质中的最大吸收波长作为检测波长。
2.1.2 线性关系 按照“2.1.1”项下方法配制储备液,分别精密量取0.5、1.0、1.5、2.0、2.5、3.0、3.5和4.0 mL,置50 mL量瓶中,相应介质稀释至刻度,摇匀,配制系列浓度溶液,分别在“2.1.1”项下美沙拉嗪在各介质中的最大吸收波长处测定吸光度。
以美沙拉嗪浓度C(μg·mL-1)为横坐标,吸光度A为纵坐标,进行线性拟合。结果显示,在0.1 mol·L-1盐酸溶液中,美沙拉嗪浓度在5~35 μg·mL-1范围内线性良好,回归方程为Y=0.022 7X+0.005 9(r=0.999 9);在pH 6.4磷酸盐缓冲液,美沙拉嗪浓度在10~40 μg·mL-1范围内,线性良好,回归方程为Y=0.019 4X-0.011 7(r=0.999 9);在pH 7.2磷酸盐缓冲液中,美沙拉嗪浓度在5~35 μg·mL-1范围内,线性亦良好,回归方程为Y=0.021 8X+0.000 3(r=0.999 9)。
2.1.3 释放度测定方法 参照美国食品药品监督管理局(FDA)溶出方法数据库中参比制剂的释放方法、《美国药典》USP40-NF35中美沙拉嗪肠溶片标准[8],采用溶出度与释放度测定法(《中国药典》2020年版通则0931第二法)测定[9],转速100 r·min-1,温度(37±0.5)℃,释放分为3个阶段:①在0.1 mol·L-1盐酸溶液750 mL中释放2 h时取样,0.45 μm水系微孔滤膜滤过2 mL,续滤液即为供试品溶液,配制浓度为20 μg·mL-1的对照品溶液,在303 nm波长处分别测定吸光度,计算释放量,应不大于标示量的1%;②取酸中释放2 h后的供试片,浸入预热至37 ℃的pH 6.4磷酸盐缓冲液950 mL中,释放1 h时取样,0.45 μm水系微孔滤膜滤过2 mL,续滤液即为供试品溶液,配制浓度为20 μg·mL-1的对照品溶液,在330 nm波长处分别测定吸光度,计算释放量,应不大于标示量的1%;③取pH 6.4磷酸盐缓冲液中释放1 h后的供试片,浸入预热至37 ℃的pH 7.2磷酸盐缓冲液960 mL中,经1、2、4、6、8 h分别取样10 mL,取样后补充pH 7.2磷酸盐缓冲液10 mL,0.45 μm水系微孔滤膜滤过2 mL,取续滤液稀释后作为供试品溶液,配制浓度为30 μg·mL-1的对照品溶液,在331 nm波长处分别测定吸光度,计算各个取样点的累积释放度。
2.2 美沙拉嗪肠溶缓释片的制备 参考专利CN1217665C[10],美沙拉嗪肠溶缓释片的制备过程如下:将处方量美沙拉嗪与黏合剂熔融制粒,冷却至室温,加入羧甲基纤维素钠和羧甲淀粉钠混合均匀,加入硬脂酸镁、二氧化硅和滑石粉总混后压片,将所得片剂用丙烯酸树脂聚合物包衣。
2.2.1 片芯处方筛选
2.2.1.1 原料药粒径的考察 美沙拉嗪为BCS Ⅳ类药物[11],难溶性药物粒径大小可能会影响溶出或释放速度。采用不同粒径的美沙拉嗪原料药制备片芯,考察原料药粒径对片芯释放的影响,按照“2.1.3释放度测定方法”第3阶段测定,释放曲线见图1,结果表明,原料药D90在28.58~98.81 μm范围内,药物释放速度无明显差异,分析可能原因,虽然原料药为难溶性药物,但在pH 7.2磷酸盐缓冲液中的溶解度(37 ℃)为5.6 mg·mL-1,介质体积为960 mL,满足漏槽条件,且为缓释制剂,因此,原料药D90在28.58~98.81 μm范围制剂释药速度无明显差异,选择D90为98.81 μm的原料药进行研究。
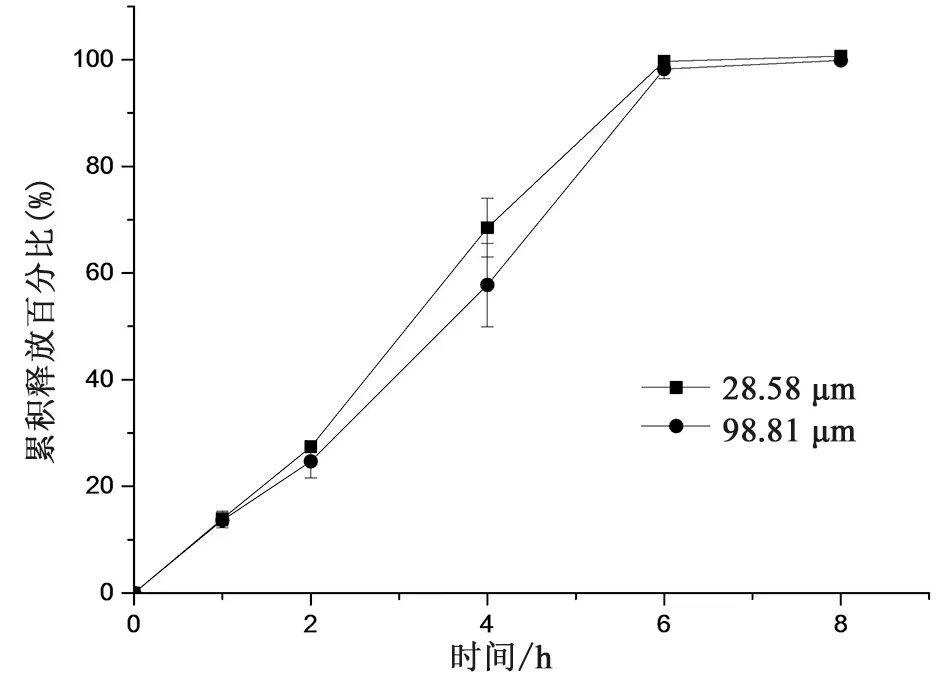
图1 原料药粒径对释放的影响
2.2.1.2 熔融黏合剂用量的考察 熔融黏合剂(巴西棕榈蜡、硬脂酸)通过与API熔融制粒,作为亲脂性基质,减慢肠液对片芯的渗透,控制药物释放。熔融黏合剂和API分别以1∶80、1∶16和1∶9的质量比熔融制粒制备片芯,考察不同熔融黏合剂用量对释放的影响,按照“2.1.3释放度测定方法”第3阶段测定,结果表明,熔融黏合剂和API以1∶80的质量比制粒时,所得颗粒可压性差,压片过程中裂片;以1∶16和1∶9的质量比制备的片芯释放曲线见图2,药物释放速度无明显差异,美沙拉嗪为高载药量药物,为减少辅料用量,选择熔融黏合剂与API质量比为1∶16制备处方。
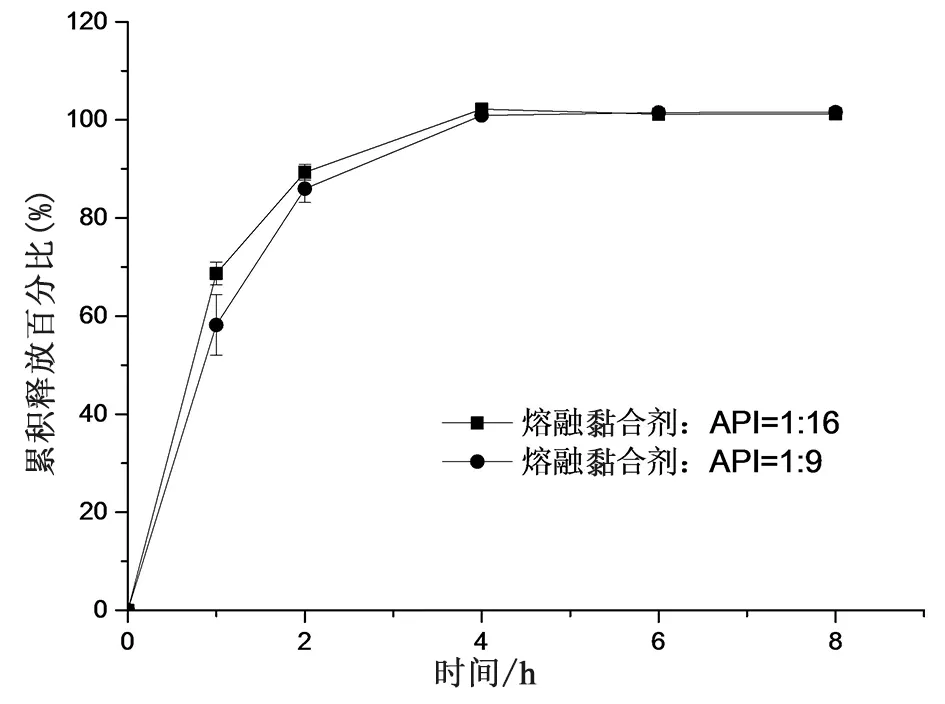
图2 熔融黏合剂与API比例对释放的影响
2.2.1.3 缓释材料型号的考察 缓释材料(羧甲基纤维素钠)作为亲水性基质,暴露于肠液后会溶胀并形成黏性凝胶,将减慢肠液的渗入和药物从片芯的扩散,从而控制释放。根据黏度分类,羧甲基纤维素钠具有不同的型号,可以满足不同释放曲线。美国Ashland 公司的Blanose羧甲基纤维素钠具有多种型号,常用作缓释材料,选择常用的CMC 7HXF PH和CMC 7MF PH进行筛选,固定总用量为50 mg,考察CMC 7HXF PH、CMC 7MF PH和二者合用对释放的影响,按照“2.1.3释放度测定方法”第3阶段测定,释放曲线见图3,结果表明,CMC 7MF PH和CMC 7HXF PH混合比例为1∶3和单独使用CMC 7HXF PH时,均具有较好的缓释效果,药物释放速度无明显差异,选择CMC 7HXF PH作缓释材料。
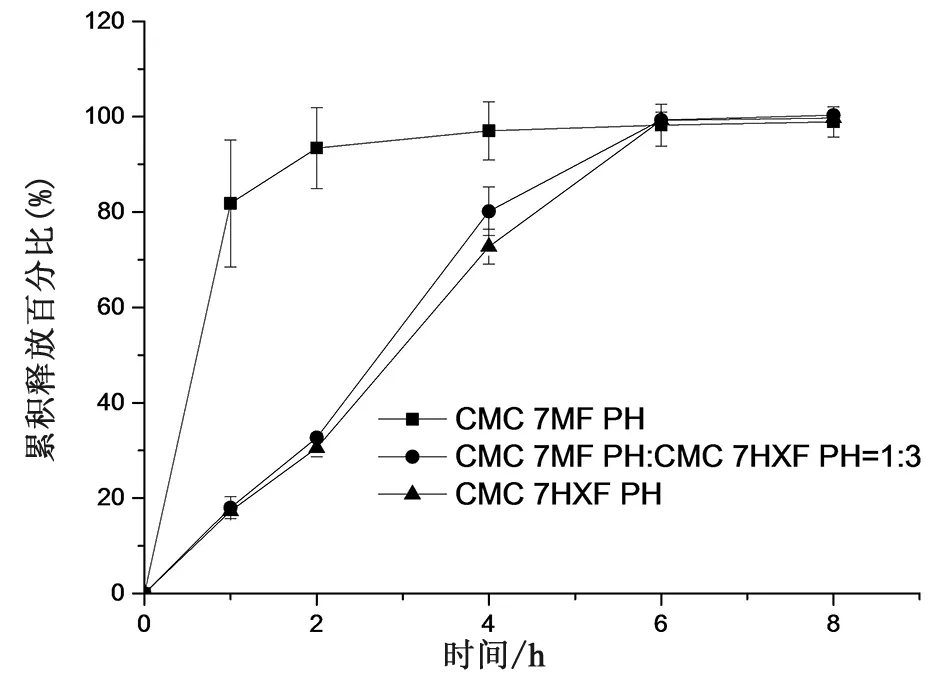
图3 CMC型号对释放的影响
2.2.1.4 缓释材料用量的考察 采用不同用量的CMC 7HXF PH制备片芯,考察缓释材料用量对释放的影响,按照“2.1.3释放度测定方法”第3阶段测定,释放曲线见图4,结果表明,CMC 7HXF PH用量对药物释放有影响,随CMC 7HXF用量增加,药物释放减慢。用量为25 mg时,1 h释放量高于90%,无缓释效果;用量为50 mg和75 mg时,药物缓慢释放,初步选择用量为50 mg,后续进一步优化处方。
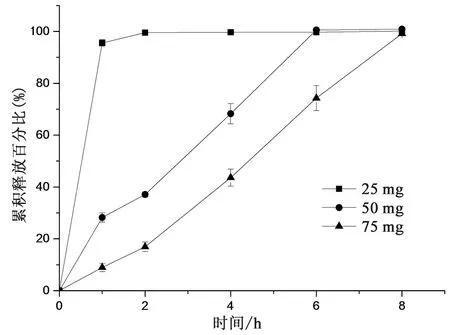
图4 缓释材料用量对释放的影响
2.2.1.5 崩解剂用量的考察 采用不同用量的CMSNa制备片芯,考察崩解剂CMSNa用量对释放的影响,按照“2.1.3释放度测定方法”第3阶段测定,释放曲线见图5,结果表明,用量为15和30 mg时,药物释放无明显差异;用量在30~45 mg范围内,随CMSNa用量增加,药物释放加快,初步选择用量为30 mg,后续进一步优化处方。
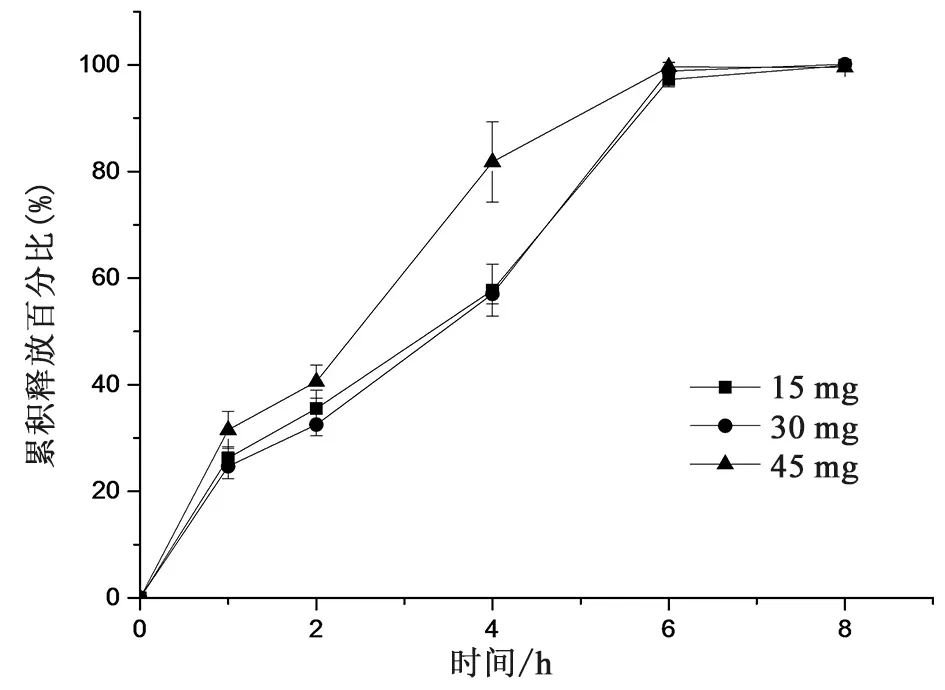
图5 崩解剂用量对释放的影响
2.2.2 肠溶包衣层处方筛选
2.2.2.1 肠溶材料的考察 Eudragit L100和Eudragit S100为常用的肠溶材料,前者在pH>6时溶解,后者在pH>7时溶解。将Eudragit L100和Eudragit S100联用,通过调节比例可控制肠溶包衣膜在不同pH环境中溶解,从而实现肠道靶向功能。固定包衣增重为8%,考察Eudragit L100、Eudragit S100和二者合用包衣时对释放的影响,按照“2.1.3释放度测定方法”测定,释放结果见表1和图6,结果表明,肠溶材料对药物释放有影响,随Eudragit S100比例增加,肠溶缓释片耐酸性增强,药物释放速度减慢。根据参比制剂说明书[12],肠溶包衣层同时含有Eudragit L100和Eudragit S100,二者比例为1∶1时,自制片可有效耐酸,因此,初步选择二者比例为1∶1,后续进一步优化处方。

表1 Eudragit L100和Eudragit S100联用比例对耐酸性(释放度,%)的影响
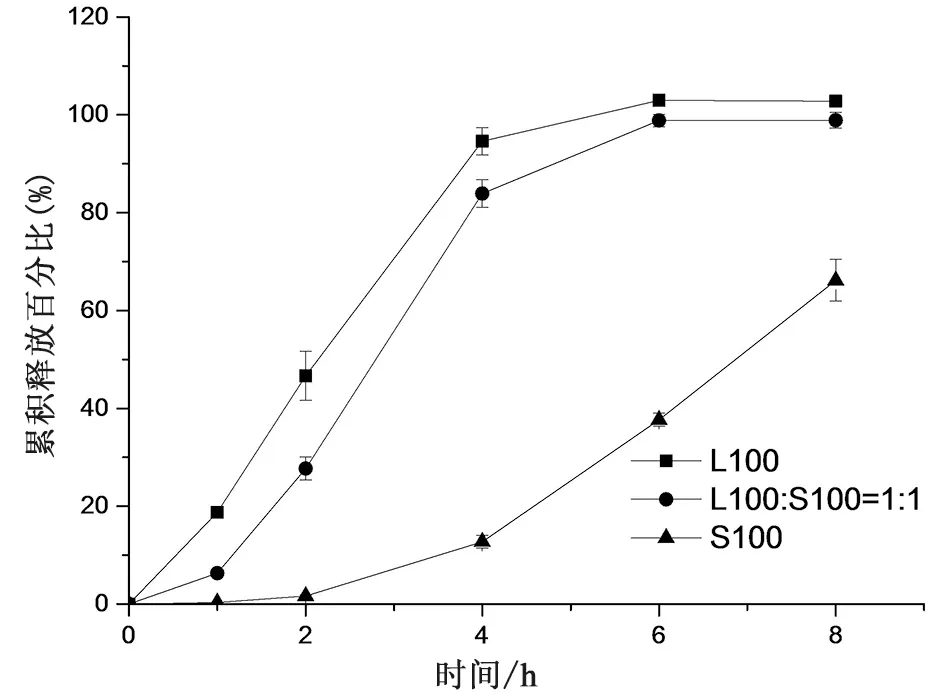
图6 Eudragit L100和Eudragit S100联用比例对释放的影响
2.2.2.2 包衣增重的考察 分别增重6%、8%和10%,考察包衣增重对肠溶缓释片释放的影响,按照“2.1.3释放度测定方法”测定,释放结果见表2和图7,结果表明,包衣增重对药物释放有影响,包衣增重增加,肠溶缓释片的耐酸性增强,药物在pH 7.2磷酸盐缓冲液中的释放减慢。包衣增重为6%时,自制片即可有效耐酸,因此,初步选择包衣增重为6%,后续进一步优化处方。

表2 包衣增重对耐酸性(释放度,%)的影响
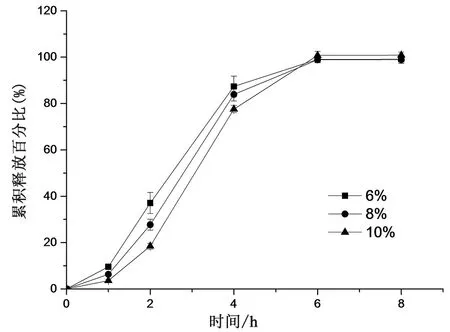
图7 包衣增重对释放的影响
2.3 正交优化 从单因素考察的结果看,片芯中CMC 7HXF PH的用量和CMSNa的用量,肠溶包衣层包衣材料比例和包衣增重对肠溶缓释片的体外释放影响显著,针对上述4个关键因素,每个因素设置3个水平,选取正交设计表L9(34)进行试验,以自制美沙拉嗪肠溶缓释片和参比制剂的相似因子f2为指标,得到最优处方。正交试验设计表及结果见表3~7。
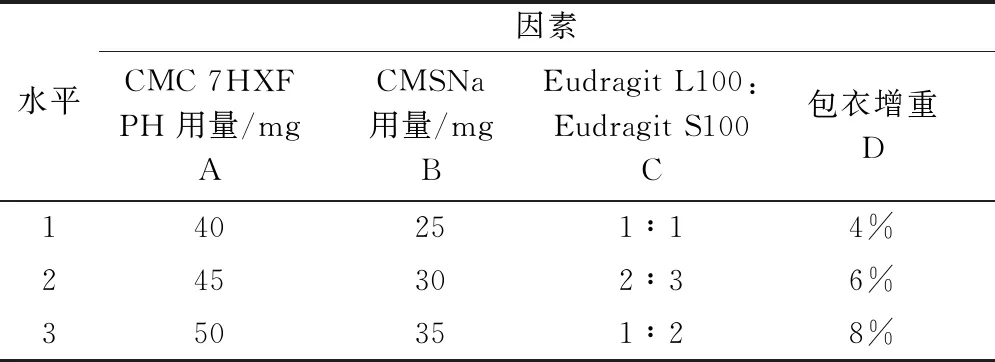
表3 正交试验因素水平表
以自制片与参比制剂的相似因子f2为评价指标,极差R反映了各因素对试验结果的影响程度,极差越大,表明影响越显著,由表5可知,各因素对试验结果的影响程度为:CMSNa用量>包衣增重>CMC 7HXF PH用量>肠溶包衣材料比例,最优组合为A2B3C2D1,即CMC 7HXF PH的用量为45 mg,CMSNa的用量为35 mg,肠溶包衣中包衣材料Eudragit L100∶Eudragit S100=2∶3,包衣增重为4%,即处方4,但该处方在pH 6.4磷酸盐缓冲液中的释放量大于1%,不符合肠溶缓释片的质量标准,因此对该处方进一步优化。
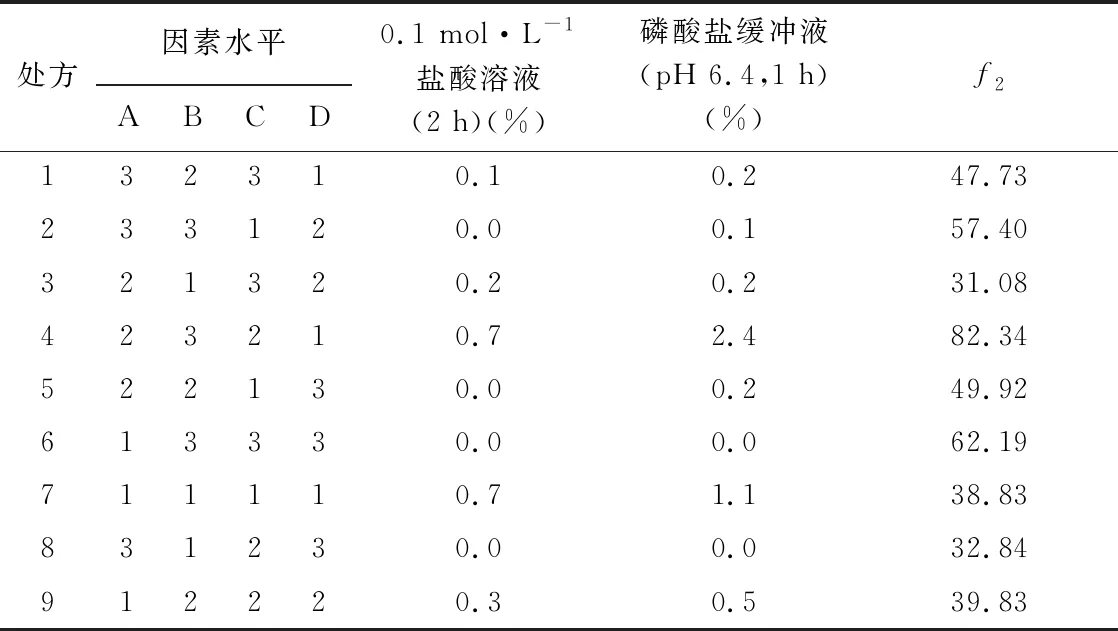
表4 正交试验结果
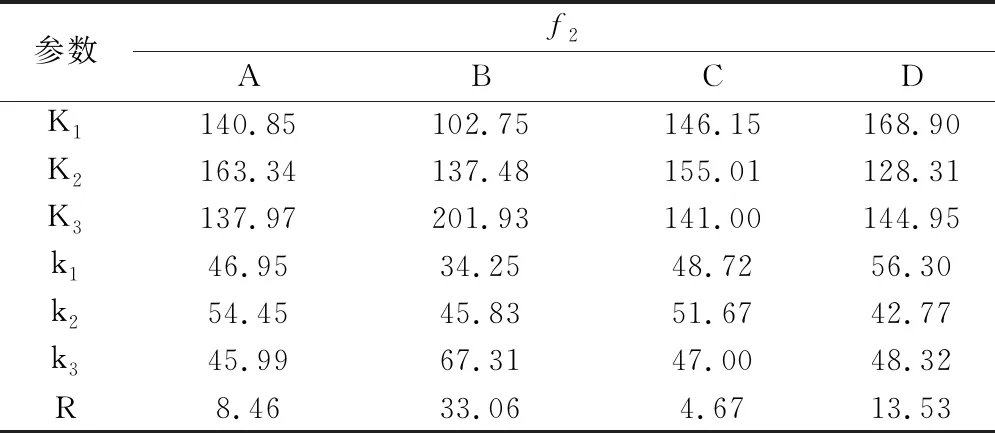
表5 相似因子极差分析
以自制制剂在pH 6.4磷酸盐缓冲液中的释放度为评价指标,由表6可知,各因素对试验结果的影响程度为:包衣增重>CMC 7HXF PH用量、肠溶包衣材料比例>CMSNa用量,故对上述最优处方增加包衣增重,以减少肠溶缓释片在pH 6.4磷酸盐缓冲液中的释放。将上述最优处方包衣增重增加至6%,测定自制片的体外释放,结果见表7,包衣增重为6%时,自制片即可有效耐酸,且f2高于正交试验的各组处方,因此,最优处方为CMC 7HXF PH用量为45 mg,CMSNa用量为35 mg,肠溶包衣材料Eudragit L100∶Eudragit S100=2∶3,包衣增重为6%。
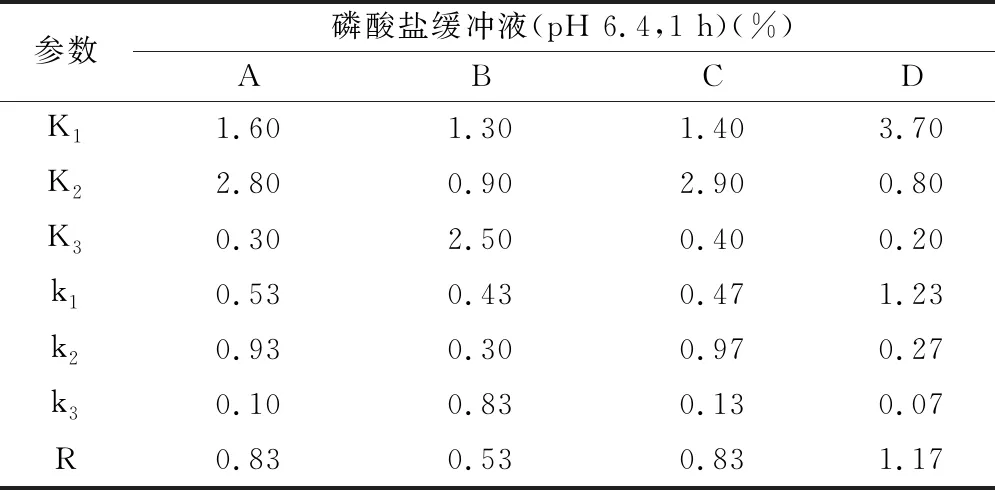
表6 pH 6.4磷酸盐缓冲液中的释放度极差分析

表7 包衣增重对释放的影响
2.4 最优处方工艺重现 按照上述最优处方制备3批美沙拉嗪肠溶缓释片,照“2.1.3”项下进行释放度测定,以验证处方工艺的稳定性,释放结果见表8~9、图8,结果表明,3批自制片均可有效耐酸,体外释放基本一致,且均与参比制剂相似,说明该处方工艺稳定可靠。

表8 美沙拉嗪肠溶缓释片的耐酸性(释放度,%)
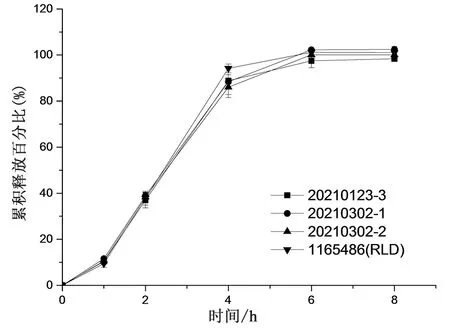
图8 自制制剂、参比制剂的释放曲线
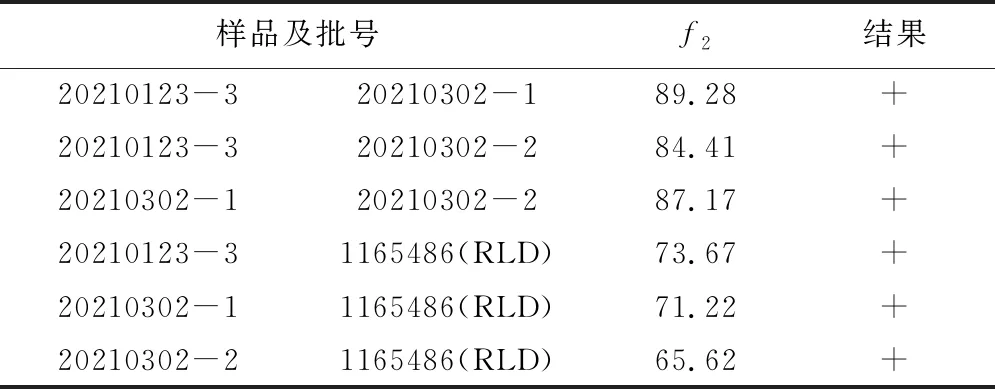
表9 不同批次自制制剂、参比制剂的释放曲线相似性
3 讨论
本研究建立了美沙拉嗪肠溶缓释片释放度测定方法,该方法可用于美沙拉嗪肠溶缓释片体外释放度的测定。
选择美国上市的Lialda为参比制剂,以体外释放为考察指标,通过对片芯和肠溶包衣层进行单因素处方筛选,明确了影响体外释放的关键因素,通过正交优化得到了最优处方,重现3批制剂,批间相似且均与参比制剂体外释放相似,表明处方工艺稳定,具有良好的产业化前景,有望提高溃疡性结肠炎患者用药顺应性问题。
