阿帕替尼用于广泛期小细胞肺癌的疗效和生存分析*
2021-08-17张诗珩熊艳丽李梦侠
罗 皓,戴 楠,杨 博,张诗珩,熊艳丽,李梦侠,王 东
(陆军特色医学中心肿瘤中心,重庆 400042)
小细胞肺癌发生率占肺癌的15.0%~20.0%[1],其生物学特点为细胞分化差、增殖快,具有高度侵袭性。2/3的患者初诊时已属于广泛期,而广泛期患者5年存活率仅为1.0%。半个世纪以来,无论是对局限期还是进展期小细胞肺癌的治疗仍采用的是以化疗药物为主的双药联合或单药方案。虽然患者对初始治疗具有高度的敏感性,但很多患者在一线治疗缓解后很快出现复发进展。既往一线治疗有效的广泛期小细胞肺癌(ES-SCLC)患者的中位无进展生存期(PFS)仅为2~4个月,总生存期(OS)为8个月[2]。因此,如何维持这些有效患者的疗效是突破小细胞肺癌治疗瓶颈的手段之一,值得深入探索。
肿瘤的持续血管生成是影响肿瘤生长的重要因素[3]。几乎80.0%的小细胞肺癌组织中均有血管内皮生长因子(VEGF)的表达[4],有关ES-SCLC的抗血管生成研究已具有一定的成果。VEGF贝伐珠单抗是现阶段应用较多的抗血管生成药物,在小细胞肺癌中早期开展了2项关于单臂的临床研究,即GALGB30306、E3501,此2项研究均证实,VEGF的治疗性与安全性均较为理想[5-6]。而相关研究也表明,贝伐珠单抗可有效延长患者PFS,但其对患者的OS无明显影响[7-8]。近年来,小分子抗血管生成抑制剂已用于多种肿瘤的治疗,2015年READY等[9]研究了舒尼替尼用于ES-SCLC化疗后维持治疗的疗效,结果显示,维持治疗延长了患者PFS,差异有统计学意义(P=0.02),但OS无获益。2项帕唑帕尼用于ES-SCLC二线治疗的临床研究结果显示,PFS较安慰剂延长了近2个月[10]。阿帕替尼是我国自主研发的一种血管内皮生长因子受体-2(VEGFR-2)抑制剂,可高效结合VEGFR-2的ATP位点,阻滞其信号传导效果,抑制肿瘤组织血管生成[11-12]。本研究为单臂单中心临床研究,评估了阿帕替尼联合治疗ES-SCLC患者的疗效和安全性(NCT02875457),旨在为临床治疗ES-SCLC提供参考。
1 资料与方法
1.1资料
1.1.1一般资料 选取2015年9月至2018年2月本院收治的晚期ES-SCLC患者22例作为研究对象,其中男17例,女5例;≤60岁12例,>60岁10例,中位年龄54.9岁;活动状态评分表(ECOG)评分:0~1分14例,2分8例;无转移灶4例,1个转移灶8例,≥2个转移灶10例;转移部位(包括多处转移):骨7例,脑8例,肝7例,肾、肾上腺4例。本研究获得本中心伦理委员会批准,遵循伦理学要求。
1.1.2纳入标准 (1)经病理学检查确诊为小细胞肺癌;(2)经CT或正电子发射断层扫描/CT影像学检查分期为广泛期;(3)年龄18~70岁;(4)ECOG评分0~2分;(5)肝、肾及骨髓功能良好;(6)合并脑转移者需在第1次给药前4周及以上完成全脑放疗且无临床症状。
1.1.3排除标准 (1)ECOG评分大于2分;(2)预计生存期低于1个月;(3)合并其他原发性肿瘤。
1.2方法
1.2.1治疗方法 22例患者均给予阿帕替尼(江苏恒瑞医药股份有限公司,国药准字H20140103)每次250 mg,每天1次,联合化疗和化疗后给予单药阿帕替尼维持治疗,直至患者病情发生进展、患者死亡或无法持续用药。治疗方案:依托泊苷100 mg/m2,第1~3天,顺铂75 mg/m2或卡铂[曲线下面积(AUC)=5],每个周期第1天给药1次,治疗21 d为1个周期;阿帕替尼 250 mg/d,第1~21天,每21天重复1次。全分析集包括所有至少接受1个周期治疗的患者,第1次疗效评估为用药后1个周期(3周),之后每2个周期评估1次疗效(6周)。
1.2.2观察指标 观察患者用药情况、疗效、死亡情况、药品不良反应发生情况等。药品不良反应根据美国国立癌症研究所的常规毒性判定标准进行评价分级。治疗主要终点为客观缓解率(ORR),次要终点为PFS、疾病控制率(DCR)、OS及治疗安全性。
1.2.3疗效判定标准
1.2.3.1近期疗效判定标准 治疗完毕后进行疗效评价:(1)完全缓解(CR)为所有病灶完全消失;(2)部分缓解(PR)为治疗后肿瘤直径明显缩小30%及以上;(3)稳定(SD)为治疗后肿瘤直径有一定缩小但未达到PR或有增加但未达到PD;(4)进展(PD)为治疗后肿瘤直径增加20%及以上或出现新病灶。ORR=(CR例数+PR例数)/总例数×100%。DCR=(CR例数+PR例数+SD例数)/总例数×100%。
1.2.3.2远期疗效判定标准 每个月随访1次,直至患者病情出现进展或死亡,将最长随访期作为中位PFS、OS。PFS指患者自阿帕替尼治疗开始至病情进展或死亡的时间。OS指患者自阿帕替尼治疗开始至死亡、失访或停止随访的时间。
2 结 果
2.1用药情况 22例患者中一线治疗12例均接受一线化疗,依托泊苷(100 mg/m2,第1~3天)联合顺铂(75 mg/m2,第1天)/卡铂(AUC=5)化疗4~6个周期,同时口服阿帕替尼(250 mg/d),4~6个周期后无疾病进展患者采用阿帕替尼单药(250 mg/d)作为维持治疗,直至患者进展、死亡或药物不良反应耐受不良。二线及以上治疗10例,其中二线治疗3例,三线治疗7例,均采用阿帕替尼单药治疗。
2.2单因素分析 截至2019年12月30日随访22例患者死亡,中位OS为11.1个月、中位PFS为5.6个月[95%可信区间(95%CI):6.39~15.81、0.49~9.91]。不同性别、ECOG评分、治疗线数患者OS、PFS比较,差异均有统计学意义(P<0.05);对于区域淋巴结转移数更多、转移脏器数更多患者OS更短,预后更差,但差异均无统计学意义(P>0.05)。见表1、图1~3。
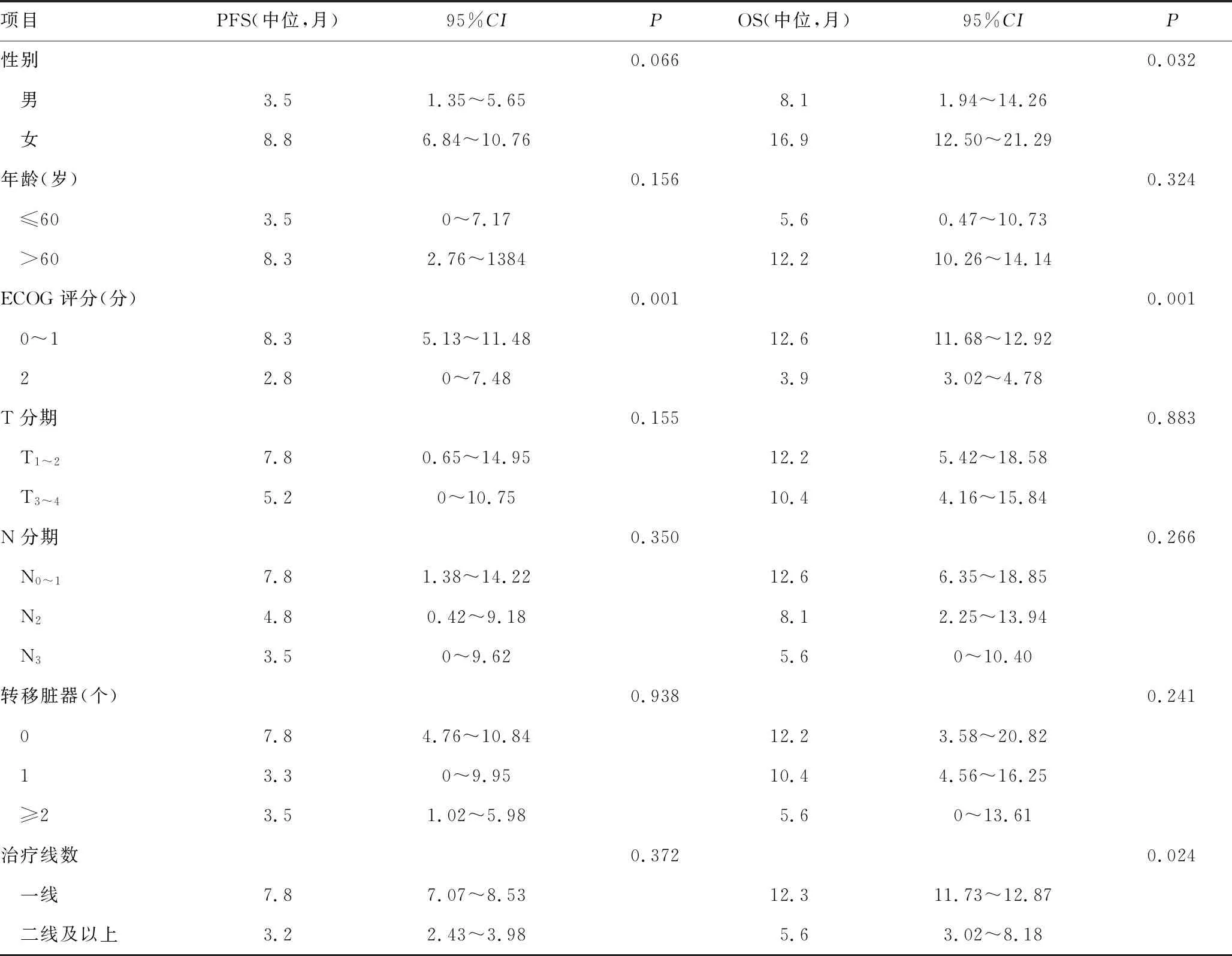
表1 单因素分析
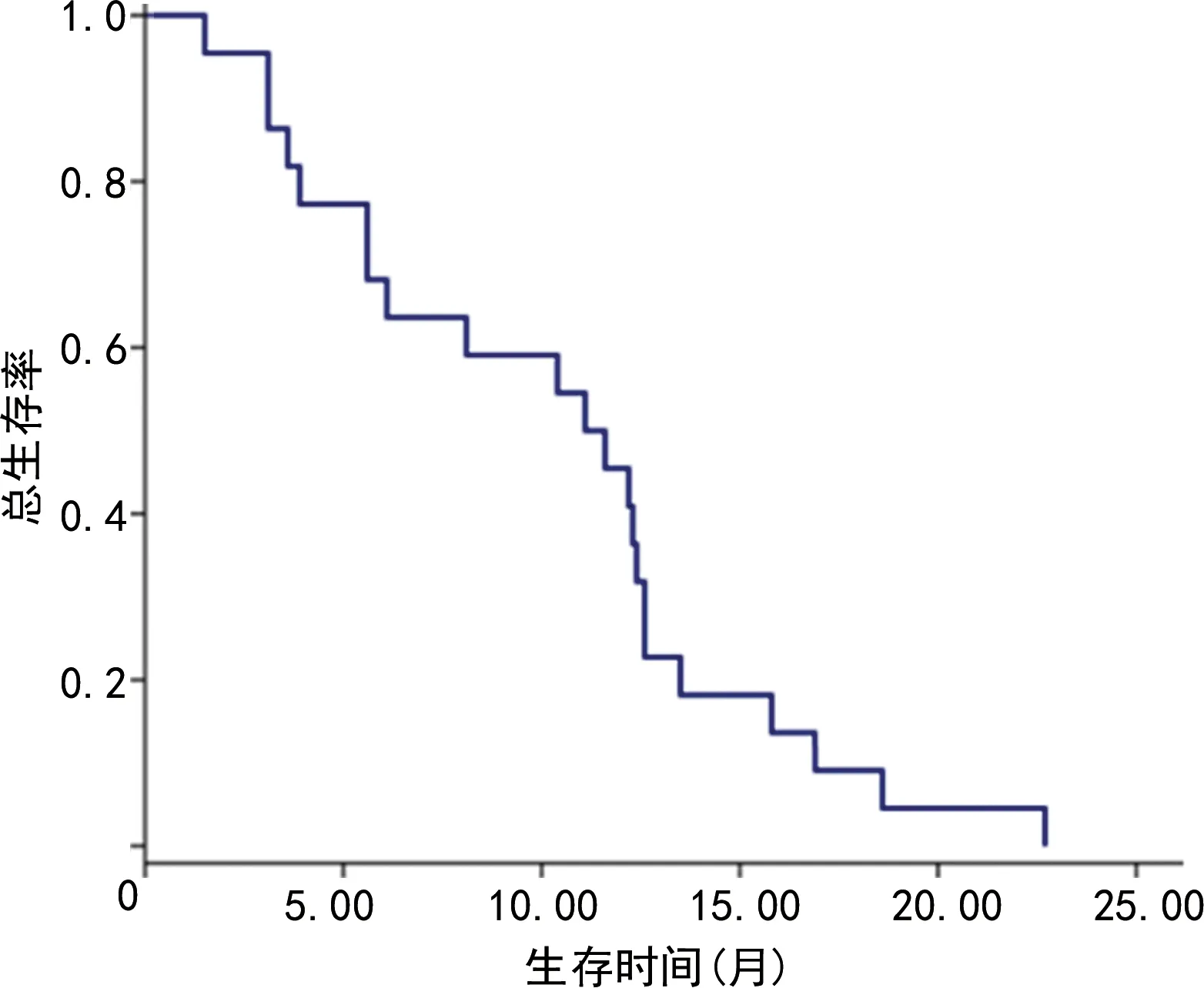
图1 OS曲线

图2 PFS曲线
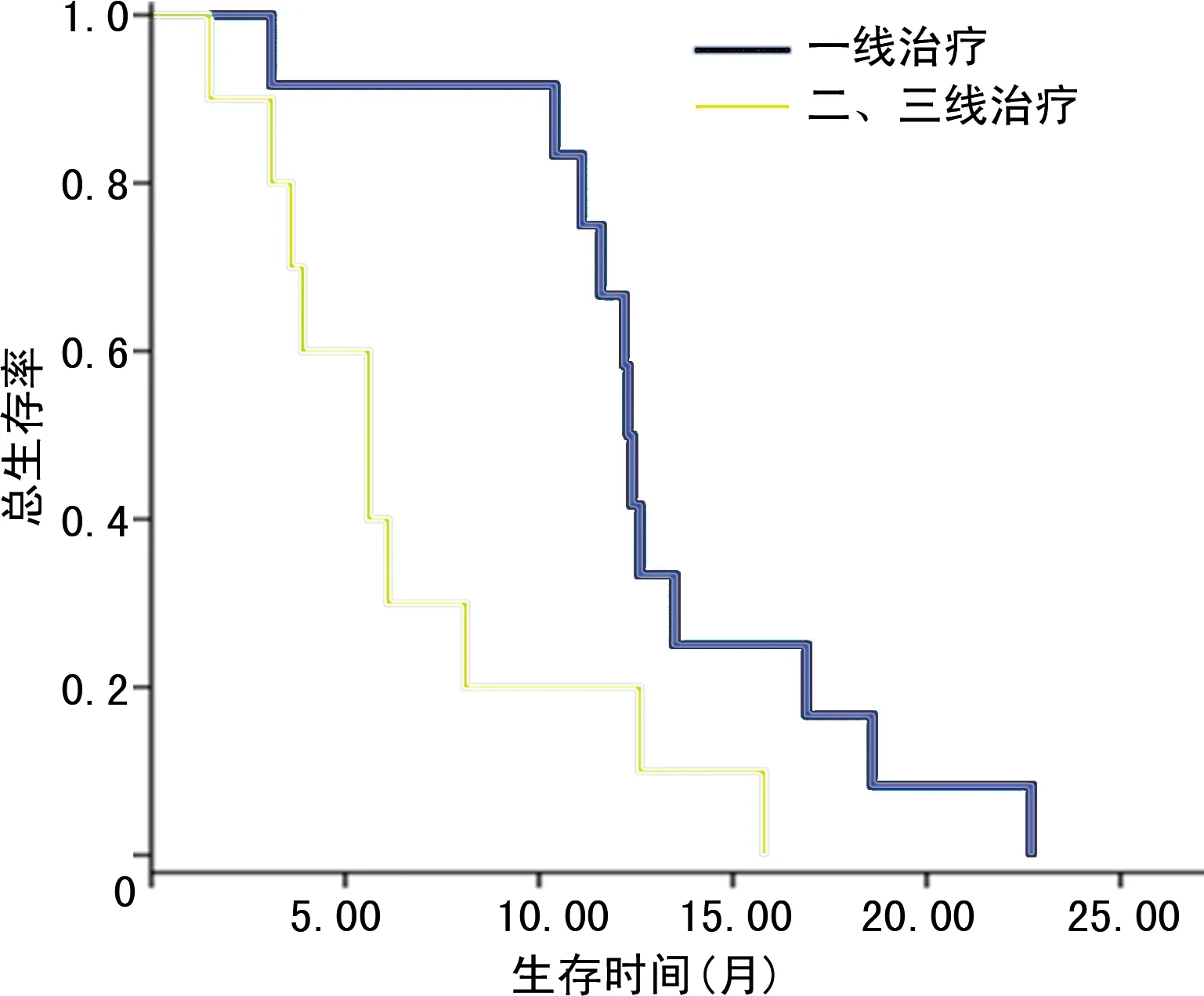
图3 一线或二、三线治疗的OS曲线
2.3近期疗效 22例患者中CR 1例,PR 9例,SD 8例,PD 4例,ORR为45.5%,DCR为81.8%。
2.4疗效瀑布图 22例患者疗效瀑布图显示16例患者病灶缩小,以肿瘤病灶直径减少30%作为治疗有效标准,则有9例患者获得PR,1例为CR。见图4。在阿帕替尼一线治疗中5例患者获得50%以上PR,阿帕替尼一线治疗的肿瘤缓解深度明显优于二线治疗。
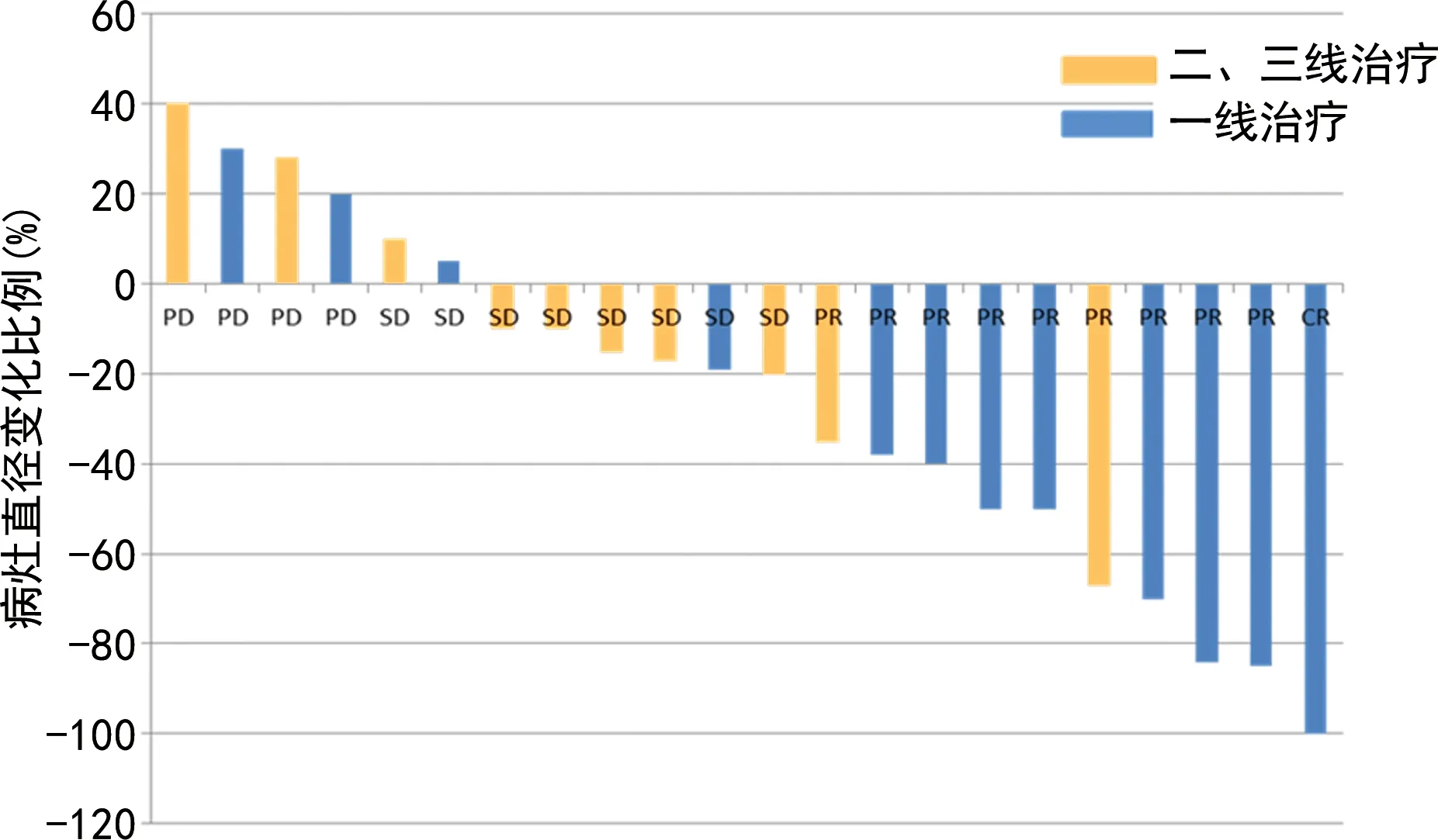
图4 阿帕替尼治疗小细胞肺癌患者后疗效瀑布图
2.5安全性评价 22例患者中14例(63.6%)患者发生各类不良反应,≥Ⅲ级5例(22.7%)。手足皮肤反应、高血压、蛋白尿是最主要的不良反应类型,≥Ⅲ级不良反应常见的为高血压和手足皮肤反应,未发现严重不良反应。见表2。
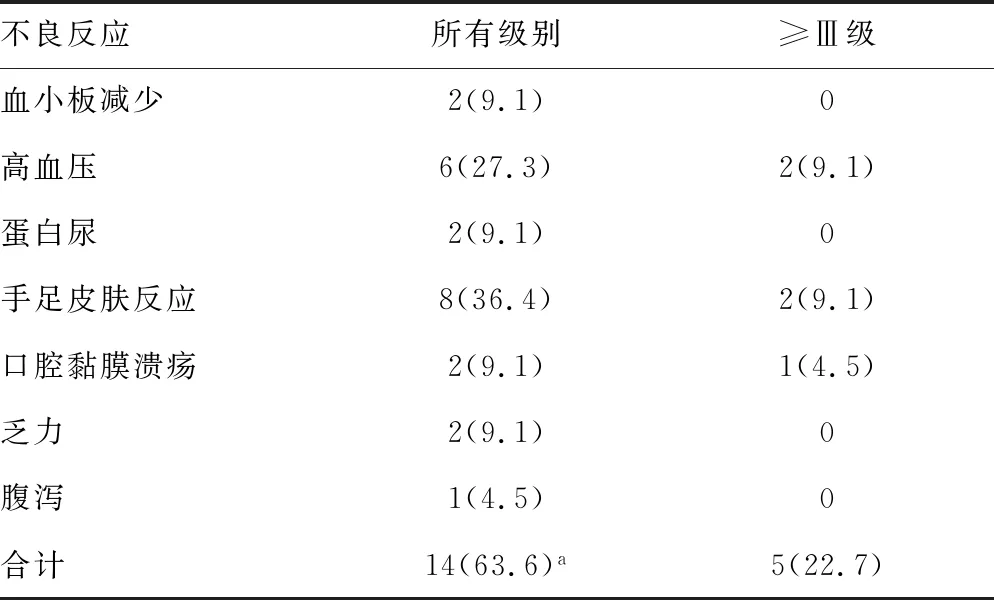
表2 不良反应发生情况[n(%),n=22]
3 讨 论
目前,小细胞肺癌维持治疗并无标准治疗方案。2005年意大利学者公布了一项维持治疗的荟萃分析,其纳入了21例随机对照临床试验,共3 687例患者,治疗药物包括化疗、干扰素和靶向药物。结果显示,化疗和干扰素维持治疗具有一定的生存获益。但该项研究也存在诸多缺陷:纳入患者包括了局限和进展期患者,纳入标准不统一,包括了疾病缓解或SD。干扰素的临床试验是20世纪80年代开展的,试验规范不足等。由于化疗药物的毒性较高,期待靶向药物能在维持治疗中发挥优势。对小细胞肺癌维持治疗初步探索的靶向药物为沙利度胺,其具有免疫调节和抗肿瘤生成作用。PUJOL等[13]发表了一项抗血管沙利度胺维持治疗ES-SCLC的2期临床试验,30例化疗结束3~6周患者使用沙利度胺200 mg/d维持治疗,中位PFS为2.4个月,中位OS 为12.8个月。患者耐受性好,不良反应率较低。随后LEE等[14]在英国开展了一项3期临床试验,化疗同步口服沙利度胺,化疗结束继续使用沙利度胺给予维持治疗。但对比安慰剂沙利度胺联合化疗反而缩短了患者生存期,增加了发生血栓的风险,否定了沙利度胺在小细胞肺癌中的作用。ANDREW等[15]报道了加拿大国立癌症研究所的一项2期临床试验,对诱导化疗有效的局限期小细胞肺癌及ES-SCLC患者应用范德他尼进行维持治疗。范德他尼是一个对EGFR、VEGF等多靶点的药物。很遗憾,是一个阴性结果,范德他尼与安慰剂中位OS分别为10.6、11.9个月,ES-SCLC患者范德他尼较安慰剂组的OS更短[13]。伊马替尼是针对原癌基因酪氨酸蛋白激酶kit(C-kit)靶点的药物,SCHNEIDER等[16]进行的一项2期临床试验将伊马替尼用于维持C-kit阳性的ES-SCLC,共纳入14例患者,伊马替尼未能使患者显著获益,中位PFS为4.8 个月,中位OS为7.8个月[14]。贝伐单抗联合化疗一线治疗ES-SCLC,后续继续给予贝伐单抗维持治疗的几项临床试验结果的PFS也各有差异,并且不能改善患者的生存质量[6-9]。READY等[9]报道了舒尼替尼的一项2期研究,结果显示,患者中位PFS分别为3.7、2.8个月,中位OS分别为9.0、6.9个月,但总生存情况无差异。免疫治疗中PD-1抑制剂纳武单抗(Nivolumab)对照化疗治疗经一线含铂化疗方案治疗复发的小细胞肺癌的开放性、随机、3期临床试验宣告失败[17],PD-L1抑制剂阿特珠单抗(Atezolizumab)+卡铂+依托泊苷治疗ES-SCLC的3期试验的中期研究结果显示,Atezolizumab中位OS分别为12.3、10.3个月,差异有统计学意义(P=0.007),中位PFS分别为5.2、4.3个月[18]。2016世界肺癌大会收录了阿帕替尼治疗二、三线化疗失败后ES-SCLC患者疗效的研究,结果表明,阿帕替尼作为化疗失败后的后线治疗具有有效性和安全性[19]。
血管生成是肿瘤生长的重要因素,也是肿瘤发生进展、转移、浸润的重要环节。VEGF具有促进肿瘤转移与存活的能力,激活肿瘤干细胞,促进肿瘤生长。VEGFR-2是跨膜蛋白,二者相互结合后可激活蛋白激酶C、磷脂酰肌醇3-激酶、丝裂原活化蛋白激酶、黏附斑激酶等,在血管生成中具有较为重要的作用,促进肿瘤增殖、浸润、转移。阿帕替尼结合VEGFR-2,能有效抑制酪氨酸激酶活性,通过抑制血管生成限制肿瘤转移、增殖,提高疗效[20]。
本研究采用阿帕替尼治疗ES-SCLC患者22例,结果显示,中位OS为11.1个月,中位PFS为5.6个月。各类不良反应发生率为63.6%,≥Ⅲ级5例(22.7%)。
石明伟等[21]探讨了采用阿帕替尼治疗晚期非小细胞肺癌的疗效,结果显示,与安慰剂组比较,阿帕替尼组患者不良反应发生率较高,主要为蛋白尿、高血压和手足皮肤反应,与本研究结果一致。阿帕替尼在一线使用并给予维持治疗OS较二线及三线使用阿帕替尼更长。本研究单因素分析提示,女性患者生存时间更长,5例女性患者中一线治疗3例,ECOG评分均为1分,2例患者无其他脏器转移;在ECOG评分0~1分的14例患者中一线治疗10例,二线及以上治疗4例,无其他器官转移病灶4例,说明阿帕替尼作为一线化疗联合治疗及维持治疗药物可有效改善体力状态好、肿瘤负荷较小患者的临床症状,延长患者PFS、OS。虽然大多数小细胞肺癌患者对初始治疗具有高度的敏感性,但在一线治疗缓解后很快出现复发进展。纵观几项大型3期临床研究,既往一线治疗有效的ES-SCLC患者PFS仅为4~6个月,OS为8~10个月,还不到1年,那么采用阿帕替尼维持治疗的一线有效患者,延长一线PFS,为患者后续治疗争取更多机会可能是突破小细胞肺癌治疗瓶颈的手段之一。但由于本研究样本量较少,尚需在后续研究中进一步增大研究样本,提供更为准确、有效的研究结果。
综上所述,阿帕替尼联合依托泊苷+铂类方案化疗在ES-SCLC患者中具有较高的有效性及安全性,延长了患者的PFS、OS;同时,阿帕替尼250 mg联合治疗不良反应相对较高,通过积极对症支持治疗均可控制。因此,阿帕替尼联合依托泊苷+铂类方案可在临床进行更加深入的研究和应用。