外周血HDAC2、IL-17A在重症哮喘患者中的表达及意义研究
2021-07-24涂容芳何振华谭小武杨艳霞
涂容芳,何振华,谭小武,陈 哲,罗 卿,陈 林,陈 伟,谢 莉,杨艳霞
(南华大学附属第二医院呼吸与危重症医学科,湖南 衡阳 421001)
支气管哮喘(以下简称哮喘)是一种全球常见、多发的慢性气道炎性反应性疾病,绝大部分哮喘患者可经吸入性糖皮质激素治疗得到控制,但仍有部分哮喘患者需大剂量吸入甚至口服糖皮质激素才能控制或仍未获控制,称之为重症哮喘(Severe asthma,SA)。最新流行病学调查研究表明全球约有3 亿成年哮喘患者[1-2],重症哮喘发生率高达5%~10%,其产生的医疗负担已超过哮喘总费用的 50%,给人们造成了极大的痛苦及经济负担。因此,探讨一种能早期预测SA 的简便指标,以尽早识别 SA 患者并予以准确干预治疗,对改善患者预后具有重要意义。本研究拟通过研究重症哮喘患者、普通哮喘患者及健康对照人群外周血组蛋白去乙酰化酶2(HDAC2)、白细胞介素-17A(IL-17A)表达水平的差异及重症哮喘患者中两者的相关性,探讨其对重症哮喘早期诊断及激素治疗是否敏感的预测价值。
1 资料与方法
1.1一般资料:选择2018年1月~2019年1月在我院治疗、随访的哮喘患者60例为研究对象,其中重症哮喘患者30例设为重症哮喘组,普通哮喘患者30例设为普通哮喘组。重症哮喘组中男16例,女14例,年龄22~63岁,平均(40.1±8.52)岁;普通哮喘组中男13例,女17例,年龄20~60岁,平均(39.2±7.68)岁。选取同期在本院进行健康体检的30例健康志愿者作为对照组,其中男18例,女12例,年龄18~60岁,平均(40.3±7.56)岁。三组研究对象的性别构成比、年龄比较差异无统计学意义(P>0.05),具有可比性。本研究已获南华大学附属第二医院医学伦理委员会批准实施,全部研究对象均知情同意。病例组纳入标准:①哮喘诊断明确,诊断标准参照中华医学会呼吸病学分会哮喘学组《支气管哮喘防治指南》和 GINA 2015;②年龄 18~65岁,性别不限。对照组纳入标准:①年龄18~65岁,性别不限;②无变态反应性疾病,无吸烟史,无哮喘病史、症状及体征,近2周内无呼吸道感染史。排除标准:①认知能力低影响自评量表填写者;②有严重心、肝、肾功能障碍,或其他感染性疾病;③有严重气胸不能进行肺功能检测者。
1.2方法
1.2.1受试者血清HDAC2、IL-17A水平检测:于清晨空腹时采集肘静脉全血4 ml置于未加抗凝剂的试管中,标本采集后在室温下静置2 h,离心机离心后(3 000 r/min)取上清分装,并将标本放于-20℃冰箱储存待测。采用ELLSA法测定血清HDAC2(试剂盒购自武汉艾美捷科技有限公司)及IL-17A(试剂盒购自欣博盛生物科技有限公司)水平,具体步骤严格按照说明书操作。
1.2.2肺功能检测最大呼气峰流速(PEF)值、1 s用力呼气容积(FEV1)及最大呼气中期流量(MMEF ):患者静息20 min后抬头挺胸,手持仪器,口含咬嘴。嘱患者深吸气,然后用爆发力吹气,吹气时仪器右侧指示灯会快速闪烁,保持稳定吹气6 s至灯灭则吹气完成。采用德国Master Screen肺功能测试系统连续检测3次肺通气功能,所检测到的结果中若用力肺活量(FVC)和FEV1的变异度均<5%则判定为合格,最终结果取3次结果中的最佳值记录。

2 结果
2.1三组受试者血清HDAC2表达对比:重症哮喘组患者外周血血清中HDAC2的水平低于普通哮喘组及对照组,差异有统计学意义(P<0.05),普通哮喘组和对照组外周血血清中HDAC2表达水平差异无统计学意义(P>0.05)。见表1。
2.2三组受试者外周血血清中IL-17A表达对比:重症哮喘患者外周血血清中IL-17A的水平高于普通哮喘组及对照组,差异有统计学意义(P<0.05),普通哮喘组和对照组外周血血清中IL-17A表达水平差异无统计学意义(P>0.05)。见表1。

表1 三组受试者外周血中HDAC2、IL-17A表达水平对比
2.3三组受试者PEF、FEV1及MMEF表达对比:重症哮喘组和普通哮喘组患者PEF、FEV1及MMEF水平均低于对照组,以重症哮喘组最明显,差异有统计学意义(P<0.05)。见表2。

表2 三组受试者PEF、FEV1及MMEF水平对比
2.4重症哮喘组患者肺功能、HDAC 2、IL-17A之间相关性分析:重症哮喘患者肺功能PEF、FEV1及MMEF与其外周血中HDAC2表达呈正相关(r=0.750、0.782、0.708,P<0.05),与IL-17A表达呈负相关(r= -0.719、-0.748、-0.711,P<0.05),HDAC2与IL-17A之间呈负相关(r=-0.892,P<0.05)。见表3。
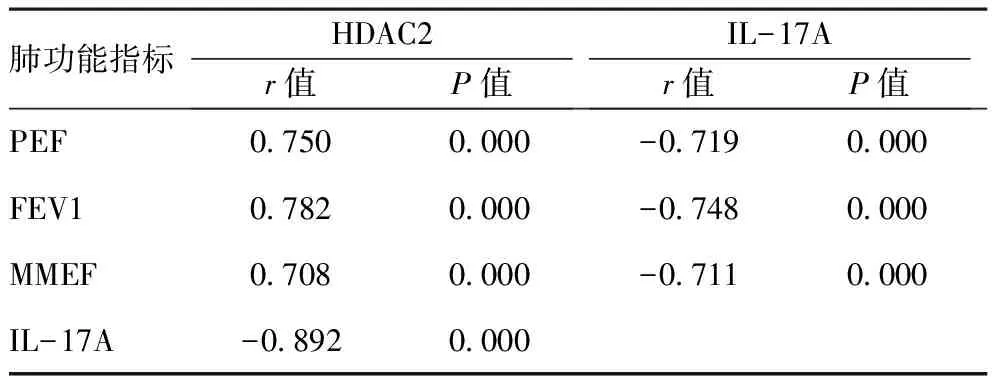
表3 重症哮喘组患者肺功能与HDAC2、IL-17A之间相关性分析
3 讨论
支气管哮喘特别是重症哮喘发病机制复杂,既往研究认为哮喘的主要发病机制是TH1/TH2细胞免疫失衡[3],即抗原经过树突状细胞等呈递后诱导T细胞分化成为TH2细胞,分泌TH2型炎性细胞因子如IL-4、IL-5和IL-13,这些炎性因子导致嗜酸性粒细胞、T淋巴细胞和肥大细胞募集,从而诱导哮喘气道高反应性和黏液高分泌。然而,最近的临床研究发现40%以上的哮喘以中性粒细胞炎性反应浸润为主[4-5],同时约有10%~15%重度哮喘患者对吸入糖皮质激素治疗不敏感,存在激素抵抗(GC 抵抗)[6],激素抵抗机制成为近年来研究的热点和难点。近年来已有研究表明:GR SNPs、GR 修饰(磷酸化、亚硝基化、泛素化、巯基化、氧化还原应激等)、GR-α基因表达减少、GR-β表达增加、GCs 细胞外排增加、促炎转录如JNK/AP-1、JAK3/STAT5、NF-κB、HDAC2、IL-17A等过度激活及促炎转录因子过度表达都可能影响糖皮质激素的生物学效应,引起 SA 对激素抵抗[7-10]。本研究拟通过研究重症哮喘患者、普通哮喘患者及健康对照人群外周血HDAC2、IL-17A表达水平的差异及重症哮喘患者中两者的相关性,探讨它们对重症哮喘早期诊断及激素治疗是否敏感的预测价值。
组蛋白去乙酰化酶(histone deacetylase,HDAC)最初是由 Taunton 等[11]人1996 年发现的一类蛋白酶,其在修饰染色体结构和调控遗传基因转录表达等方面发挥了重要的作用,HDACs 共有四大类,组蛋白去乙酰化酶 2(HDAC2) 是第 I 类组蛋白去乙酰化酶,含有一个保守的、约 400 个氨基酸残基的催化结构域,由 1 个底物结合位点、1 个锌离子结合位点和 2 个金属离子结合位点构成胞核内的一种对染色体的结构修饰和基因表达调控发挥着重要作用的蛋白酶。Trevor 等[12]报告糖皮质激素可通过募集HDAC2使GR去乙酰化,GC 与核因子κB(NF-κB)结合并激活 AP-1形成 GC-NFκB/AP-1 复合体,抑制促炎因子转录,促炎因子合成减少,炎性反应减轻或受抑;此外,HDAC2 可使组蛋白去乙酰化,组蛋白与带负电荷的促炎性反应因子 DNA结合更紧密,促炎性反应转录因子不能与 DNA 特异位点结合,转录受到抑制,表达下调,从而发挥抗炎作用。当 HDAC2 表达下调时,可能引起激素抵抗,抗炎作用减弱。Hao M等在6周龄BALB/c小鼠哮喘模型的研究中发现,暴露于吸烟组(SEA)小鼠肺组织活检标本中 HDAC2 表达较卵清蛋白(OVA)激发哮喘组小鼠低[13]。Ito等在40名受试者的支气管黏膜活检组织中也发现 HDAC2 表达水平与重症哮喘患者的激素疗效有关[14]。白细胞介素-17(IL-17)是 Th17 细胞分泌的一种炎性反应介质[15],Semlali 等发现 IL-17A 可促进GR-β 在外周血单核细胞中表达增多,使 GR-β/GR-α 的比例倒置,最终产生激素抵抗[16]。以中性粒细胞浸润为主的哮喘,对糖皮质激素治疗的反应差,而在募集中性粒细胞的过程中,IL-17 起着至关重要的作用[17-18]。 高水平的 IL-17 与中性粒细胞气道炎性反应的严重程度呈正相关,且这类哮喘患者在糖皮质激素治疗后中性粒细胞的数量并不降低,因此IL-17不仅可诱导杯状细胞增生及黏液分泌造成气道重塑,还在重症哮喘激素抵抗中起了重要作用[19]。SA严重程度常规采用肺功能评估,其中PEF表示最大呼气流速率是判断哮喘严重度最简便可靠的客观手段,当PEF<0.2 L/min提示气道存在严重阻塞;而FEV1、MMEF是反映气道阻力最常用的指标,当FEV1<1.0 L时提示病情严重,当FEV1<0.5 L时则有发生窒息的可能。但肺功能检查操作复杂还对患者要求较高,如遇SA急性发作时不仅会因患者病情重配合不佳而无法准确反映病情,还存在病情加重甚至窒息、死亡风险,因此寻求简单、无创、高特异性检查指标或方法意义重大。本研究表明:重症哮喘患者血清HDAC2水平显著低于普通哮喘患者和对照组人群,差异有统计学意义(P<0.05),且与其PEF、FEV1及MMEF呈正相关,差异有统计学意义(P<0.05)。重症哮喘患者血清IL-17A水平显著高于普通哮喘患者(P<0.05)和对照组人群(P<0.05),且与其PEF、FEV1及MMEF呈负相关(P<0.05)。而普通哮喘与对照组外周血血清中HDAC2、IL-17A水平差异无统计学意义(P>0.05),进一步提示外周血 HDAC2、IL-17A水平作为评估哮喘表型的生物标志是可行的,因其简单、方便和安全,在预测激素治疗效果和识别“真”“假”重症哮喘患者方面有较好的临床运用前景。
综上所述,重症哮喘患者的外周血中存在HDAC2、IL-17A表达增加,并且HDAC2、IL-17A表达水平与患者的肺功能密切相关,但具体机制尚不清楚。最近的一项研究表明,敲除 HDAC2 基因后,能使屋尘螨诱导的气道炎性反应及黏液分泌进一步加重,并能调控 Th17 细胞分化促进 IL-17A的分泌,而敲除 IL-17 基因或使用 IL-17A 中和抗体后能使由 HDAC2 基因缺失诱导的气道炎性反应得到缓解[20],显示 HDAC2 可以通过抑制气道上皮细胞产生IL-17A 的表达来减弱气道炎性反应。另外,有文献报道IL-17A 可在气道上皮中诱导糖皮质激素不敏感,其机制可能与 PI3K 信号通路激活导致 HDAC2 活性降低有关[9]。本研究发现重症哮喘患者中HDAC2、IL-17A表达水平呈负相关,差异有统计学意义(P<0.05),由此推测HDAC2、IL-17A参与重症哮喘的机制可能与下调HDAC2、上调IL-17A参与激素抵抗有关。
