电位滴定法测定过氧化氢溶液中游离酸含量
2021-07-14谭建忠
谭 建 忠
(中石化巴陵石油化工有限公司分析检验中心,湖南 岳阳 414003)
过氧化氢溶液是一种绿色化工产品,其生产和使用过程几乎没有污染,故被称为“清洁”的化工产品,可作为氧化剂、漂白剂、消毒剂、脱氧剂、聚合物引发剂和交联剂,广泛应用于化工、造纸、环境保护、电子、食品、医药、纺织、矿业、农业废料加工等行业[1]。目前,过氧化氢的工业规模化生产方法主要是蒽醌法,其方法是将2-乙基蒽醌溶解在溶剂(C9重芳烃和磷酸三辛酯)中形成工作液,而后依次经历氢化、氧化和萃取、净化等阶段得到过氧化氢溶液。其萃取工艺中萃取剂由脱盐水加微量的磷酸配制,工艺人员将萃取剂俗称为配水,其配水呈弱酸性。过氧化氢溶液为无色透明溶液,遇光、热、氧化物和还原物都会分解;当溶液中有金属离子、碱存在可加速其分解,导致爆炸。过氧化氢溶液中游离酸含量是其在生产、储存、运输和应用中很重要的控制指标,过氧化氢溶液中游离酸含量过低会影响过氧化氢溶液的稳定度,给生产、储存、运输和应用带来安全隐患;由于生产中过氧化氢溶液的游离酸含量是通过增减磷酸来调节的,所以过氧化氢溶液的游离酸含量高会增加生产成本,同时应用过氧化氢溶液后废液中磷含量高,增加了废液的处理成本[2-5]。
目前,测定过氧化氢溶液中游离酸含量的方法有:(1)生产过程中利用测定溶液的pH值来折算游离酸含量的在线分析[6];(2)酸碱中和滴定法测定游离酸含量[7]。其中,第一种方法只能粗略了解工业过氧化氢溶液中游离酸含量;第二种方法可以准确测定游离酸含量,但全过程均为人工操作,对分析人员的操作技能要求较高。为此,作者研究并建立了采用自动电位滴定仪分析过氧化氢溶液中游离酸含量的方法,该方法精密度和准确度较高,且操作简便、快速,可为精准控制过氧化氢溶液中游离酸含量提供可靠的数据支持[8-12]。
1 实验
1.1 仪器
AT-510自动电位滴定仪:带有搅拌台、搅拌子、pH电极,日本京都电子公司制; HF-3000电子天平:日本A&D公司制。
1.2 试剂及试样
氢氧化钠(NaOH):分析纯,天津化学试剂厂产;磷酸:优级纯,质量分数为85%,南京化学试剂有限公产;无水乙醇:分析纯,湖南汇虹试剂有限公司产;甲基红和次甲基蓝指示剂:天津市光复精细化工研究所产;配水试样和过氧化氢溶液试样Ⅰ(简称试样Ⅰ):游离酸质量分数(以H2SO4计)(w)为0.014 6%,中石化巴陵石油化工有限公司煤化工部产。
1.3 实验方法
1.3.1 试样的制备
过氧化氢溶液试样Ⅱ(简称试样Ⅱ):称取优级纯磷酸溶液0.348 0 g,精确至0.000 2 g,加试样Ⅰ至1 000 g;混匀,此试样添加的w为0.014 8%,作为加标回收率实验用。
试样Ⅲ、试样Ⅳ、试样Ⅴ、试样Ⅵ、试样Ⅶ:按试样Ⅱ的制备方法进行配制,即称取一定质量的优级纯磷酸溶液,精确至0.000 2 g,加入一定质量的试样Ⅰ混匀。其中试样Ⅲ添加的w为0.025 0%;试样Ⅳ添加的w为0.030 0%;试样Ⅴ添加的w为0.032 2%;试样Ⅵ添加的w为0.035 1%;试样Ⅶ添加的w为0.039 7%。试样Ⅲ~Ⅶ作为加标回收率实验用。
1.3.2 溶液的配制和标定
(1)NaOH标准滴定溶液:NaOH浓度(c)为0.101 8 mol/L,按HG/T 369.1—2011《无机化工产品化学分析用标准溶液、制剂及制品的制备 第1部分:标准滴定溶液的制备》配制及标定。
(2)甲基红-次甲基蓝混合指示剂:将质量分数为0.2%甲基红乙醇溶液和质量分数为0.1%次甲基兰乙醇溶液按1:1的体积比混合。
1.3.3 酸碱中和滴定法测定w[7]
称取试样约40 g,精确至0.01 g,置于250 mL三角烧瓶中,加入50 mL无二氧化碳的去离子水,加入2~3滴甲基红-次甲基蓝混合指示液,用0.101 8 mol/L氢氧化钠标准滴定溶液滴定至溶液由紫红色变为暗蓝色即为终点,记录消耗的氢氧化钠标准滴定溶液的体积(V)。w按式(1)计算:
w=(VcM×10-3/m)×100%
(1)
式中:m为试样的质量;M为硫酸摩尔质量的1/2,为49.04 g/mol。
1.3.4 电位滴定法测定w
开启AT-510自动电位滴定仪的开关,在自动电位滴定仪工作站中新建w的测定方法:滴定模式: 快速滴定,自动找终点、停止等当点个数1、搅拌速率8 r/s、传感器为pH电极。将pH电极从电极保护液中取出,并置于装有100 mL脱盐水的烧杯中清洗。称取试样约40 g,精确至0.01 g,置于250 mL烧杯中,加入50 mL无二氧化碳的去离子水,将试样置于搅拌台上,将电极、搅拌子和滴定管置于试样中,选定已设定好的分析方法,即可开始滴定分析,分析完成仪器自动出结果。
2 结果与讨论
2.1 电位滴定法测定条件的选择
2.1.1 仪器设定模式的选择
由表1可见,采用自动电位滴定仪测定试样Ⅰ的w,在仪器自动找终点,滴定模式为快速、中速和慢速的条件下,w分析结果的平行性较好,其相对标准偏差(RSD)为1.3%~3.6%。考虑到测试耗时,确定用自动电位滴定仪测试过氧化氢中的w时,其仪器的设置模式选择自动找终点和快速滴定。
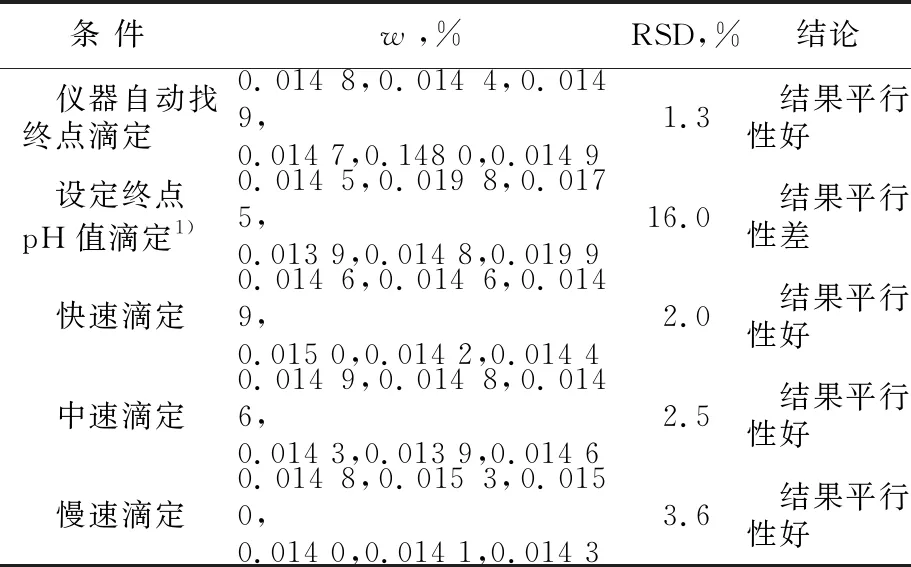
表1 不同仪器条件下试样Ⅰ的w测试结果Tab.1 w test results of sample I under different instrument conditions
2.1.2 搅拌速率的选择
在自动电位滴定仪的设置模式为自动找终点、快速滴定的条件下,采用自动电位滴定仪在不同的搅拌速率下测定试样Ⅰ的w,其结果见表2。

表2 不同搅拌速率下试样Ⅰ的w测试结果Tab.2 w test results of sample I at different stirring rates
从表2可以看出:当搅拌速率为5~10 r/s时,试样Ⅰ的w测定值与用标准方法测得的w值(0.014 6%)的绝对差值最大值为0.000 5%,其值小于国家标准GB/T 1616—2014《工业过氧化氢》两次平行测定结果的绝对差值不大于0.001%的规定。考虑到测试耗时,用自动电位滴定法测试过氧化氢中的w时,确定其仪器的搅拌速率为 8 r/s。
2.2 精密度
从表3可以看出,将自动电位滴定仪设置为自动找终点、快速滴定的模式,在搅拌速率为8 r/s的条件下,采用电位滴定法测试试样Ⅰ 6次,测定的w结果相近,其RSD为0.43%,数据重复性较好,说明使用自动电位滴定仪测定试样的w的精密度高,同时测定1个试样的耗时约3 min,耗时短,满足分析要求。

表3 电位滴定法测定试样Ⅰ的w的精密度结果Tab.3 Precision results of w in sample I determined by potentiometric titration
2.3 加标回收率
过氧化氢溶液生产中,用磷酸来调节过氧化氢溶液的w,因此用磷酸作为回收率实验的标准物质。将仪器设置为自动找终点、快速滴定的模式,在搅拌速率为8 r/s的条件下,采用电位滴定法进行加标回收率实验,结果见表4。

表4 电位滴定法的加标回收率实验结果Tab.4 Experimental results of recovery of standard addition in potentiometric titration
从表4可以看出,加标回收率为97.3%~101.6%,说明采用电位滴定法测定过氧化氢溶液中的w的准确度较高,该方法满足分析要求。
2.4 最小检测限
将仪器设置为自动找终点、快速滴定的模式,在搅拌速率为8 r/s的条件下,平行测定100 mL配水试样的w11次,测定值的标准偏差的3倍即为分析方法的最小检测限,其结果见表5。

表5 电位滴定法的最小检测限的测试结果Tab.5 Test results of minimum detection limit of potentiometric titration
从表5可以看出,采用电位滴定法测定过氧化氢中的w的最小检测限为0.000 09%,最小检测限值满足控制分析的要求。
2.5 可靠性检验
电位滴定法可靠性的检验采用标准分析方法对照法。根据GB/T 1616—2014《工业过氧化氢》的测定方法(酸碱中和滴定法),对过氧化氢溶液试样Ⅰ中的w进行6次平行测试,其结果见表6。
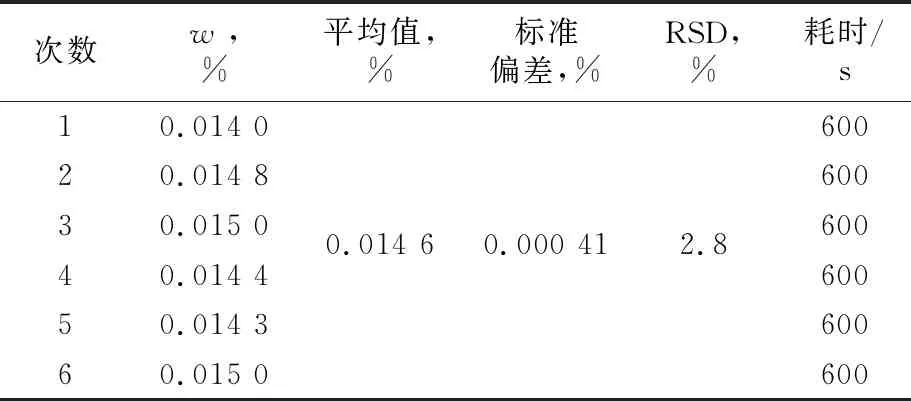
表6 标准分析方法测定试样Ⅰ中的w的结果Tab.6 Results of w in sample I determined by standard analysis method
由表6及表3可知,按t检验法[13]所得的统计量(t)为1.19,当自由度(f)为10时,置信度95%,查t检验临界值表得t(0.05,10)为2.228[13],则所得t值1.19小于t(0.05,10)的值2.228,说明用自动电位滴定仪测定试样Ⅰ和用GB/T 1616—2014《工业过氧化氢》的方法测定试样Ⅰ的结果没有显著差异,该方法可靠,同时自动电位滴定仪测定的耗时更短,精密度更高。
3 结论
a.采用电位滴定法,在自动电位滴定仪自动找终点、快速滴定,以及搅拌速率为8 r/s的条件下测定过氧化氢溶液中的w,其RSD为0.43%,加标回收率为97.3%~101.6%,最小检测限为0.000 09%;测定1个试样耗时为3 min左右。
b.电位滴定法测定试样Ⅰ中的w,其结果与用GB/T 1616—2014《工业过氧化氢》方法测定试样Ⅰ的结果没有显著差异。
c.采用电位滴定法测定过氧化氢溶液中的w,操作简便、快速,可以降低分析人员的劳动强度,改善操作环境。
