低左心耳峰值排空速度对阵发性心房颤动导管消融术后复发的预测价值
2021-07-09王庆亚党成晶
王庆亚,党成晶,惠 杰
(苏州大学附属第一医院心血管内科,江苏苏州 215006)
心房颤动(房颤)是临床上最常见的心律失常类型,截至2010 年,全球房颤患者大约有3 350 万例[1]。房颤诱发心房血液动力学异常并导致血栓形成,血栓可导致心血管相关疾病发病率和病死率增加[2]。在欧洲心脏病协会2020 年房颤管理指南中指出,对于在Ⅰ类或Ⅲ类抗心律失常药物治疗失败或不能耐受的症状性阵发性房颤(parox⁃ysmal atrial fibrillation,PAF)和持续性房颤,导管消融(catheter ablation,CA)为Ⅰ类推荐,但CA 后房颤复发仍然是个问题。因此,研究影响CA 后房颤复发的独立危险因素有利于术前对房颤复发风险进行评估并指导CA 患者的选择,对于提高手术成功率和指导临床工作具有重要意义。房颤诱导心房重构,心房重构可分为结构、电和功能重构,进而促进房颤的持续[3]。过去研究报道了左心房功能降低与CA 后房颤较高的复发率有关[4]。左心耳峰值排空速度(left atrial appendage peak empty⁃ing flow velocity,LAAeV)可作为左心房功能的替代因素[5],其能够反映左心房的功能重构[3]。近年来,经食管超声心动图测量的LAAeV 被认为是导管射频消融术(radiofrequency catheter ablation,RFCA)后房颤复发的有效预测指标[6]。本研究通过对行RFCA 治疗的PAF 患者进行研究,探讨术前LAAeV 与RFCA 后PAF 复发之间的关系。
1 资料和方法
1.1 一般资料
回顾性纳入连续PAF 患者共190 例,所有患者于2017 年6 月至2019 年7 月在苏州大学附属第一医院心内科行RFCA 治疗,根据1 年随访结果分为复发组与未复发组。根据欧洲心脏病协会2020 年指南定义,PAF 是指房颤发作持续时间不超过7 d,7 d 内能自行或经干预终止的房颤。纳入标准:大于18 岁;PAF;首次行RFCA 治疗;术前完善经食道超声心动图并且提示无左心房血栓形成;符合消融指征且自愿行RFCA 治疗;签署知情同意书。排除标准:瓣膜性房颤患者;风湿性心脏病患者;自身免疫性疾病及慢性炎症性疾病患者;严重肝及肾功能不全患者;死亡或失访患者。
1.2 资料收集
通过医院的病历系统收集患者入院时的基线资料,包括(1)一般临床资料:年龄、性别、体质量指数、收缩压、舒张压、房颤病程、抗凝评分、并发症及服用药物史;(2)血清学指标(术前最近一次清晨空腹血结果):肌酐、尿酸、超敏C 反应蛋白(high-sen⁃sitivity C-reactive protein,hs-CRP);(3)超声心动图资料(所有患者在拟定消融手术前24 h内,在窦性心律期间,由2 名心脏专科医师使用飞利浦IE33 超声系统进行经胸超声心动图和经食管超声心动图检查):左心房内径(left atrial diameter,LAD)、左心室射血分数、左心室舒张末期内径、左心室收缩末期内径、右心房内径(right atrial diameter,RAD)、LAAeV。
1.3 围术期处理及导管消融方法
所有PAF 患者术前停用抗心律失常药物(anti⁃arrhythmic drugs,ADDs)(除外胺碘酮)不低于5 个半衰期,术前服用华法林或新型口服抗凝药至少3 周。术前24 h内完善计算机断层扫描左心房三维重建及经食道超声心动图确认无左心房血栓存在。所有房颤患者均完成环肺静脉隔离(circum⁃ferential pulmonary vein isolation,CPVI)。是否添加额外线性消融线(如:二尖瓣峡部线及三尖瓣峡部线等)由术中是否合并心房扑动、房性心动过速发作及手术医生经验决定,是否加行复杂碎裂电位消融视具体情况决定;如果消融后房颤持续存在,则进行直流电复律以恢复窦性心律。消融终点定义:肺静脉内与左心房传导双向阻滞。术后继续使用华法林或新型口服抗凝药抗凝治疗3 个月,3 个月后根据是否房颤复发及CHA2D2-VASc 评分决定是否继续抗凝治疗,视术后具体情况决定是否口服ADDs 治疗,术后口服2~4 周质子泵抑制剂。
1.4 术后随访
随访方式包括门诊随访及电话随访。所有患者于术后第1、3、6、12 个月于本院或当地医院心内科门诊复查普通十二导联心电图或24 h 动态心电图,嘱咐患者出现心悸、胸闷等症状时立即至医院行心电图检查。房颤复发定义:术后3 个月空白期后,普通12 导联心电图记录的任何快速房性心律失常(包括房性心动过速、心房扑动及房颤)或24 h动态心电图记录的持续时间超过30 s的发作。
1.5 统计学分析
数据分析采用SPSS 21.0软件。对于计量资料,均进行正态性检验及方差齐性检验,正态分布资料用()表示,组间资料比较采用两独立样本t检验,偏态分布资料采用M(Q1~Q3)表示,组间资料比较采用Mann-WhitneyU检验。计数资料采用[n(%)]表示,组间资料比较采用χ2检验或Fisher′s精确检验(n<5)。进行单变量和多变量Cox 比例风险回归分析,以确定房颤复发的独立危险因素。选取单因素分析中P<0.05 的相关因素作为自变量进行多元分析。根据受试者工作特性(receiver operating characteristic,ROC)曲线分别计算曲线下面积(area under the curve,AUC)、特异度及灵敏度。生存分析采用Kaplan-Meier 模型,并用检验检验比较组间差异有无统计学意义。双侧P<0.05 表示差异具有统计学意义。
2 结果
2.1 两组患者的基线资料比较
本研究共纳入PAF 患者190 例,随访12 个月期间,有37 例复发(复发组),157 例未复发(未复发组),两组患者的的一般临床资料,血清学指标及超声心动图资料的比较见表1。研究参与者的总体中位年龄为63.00(57.00~68.25)岁,男 性101 例(53.16%),女 性89 例(46.84%)。
表1 复发组与非复发组临床资料比较 [(),M(Q1~Q3),n(%)]
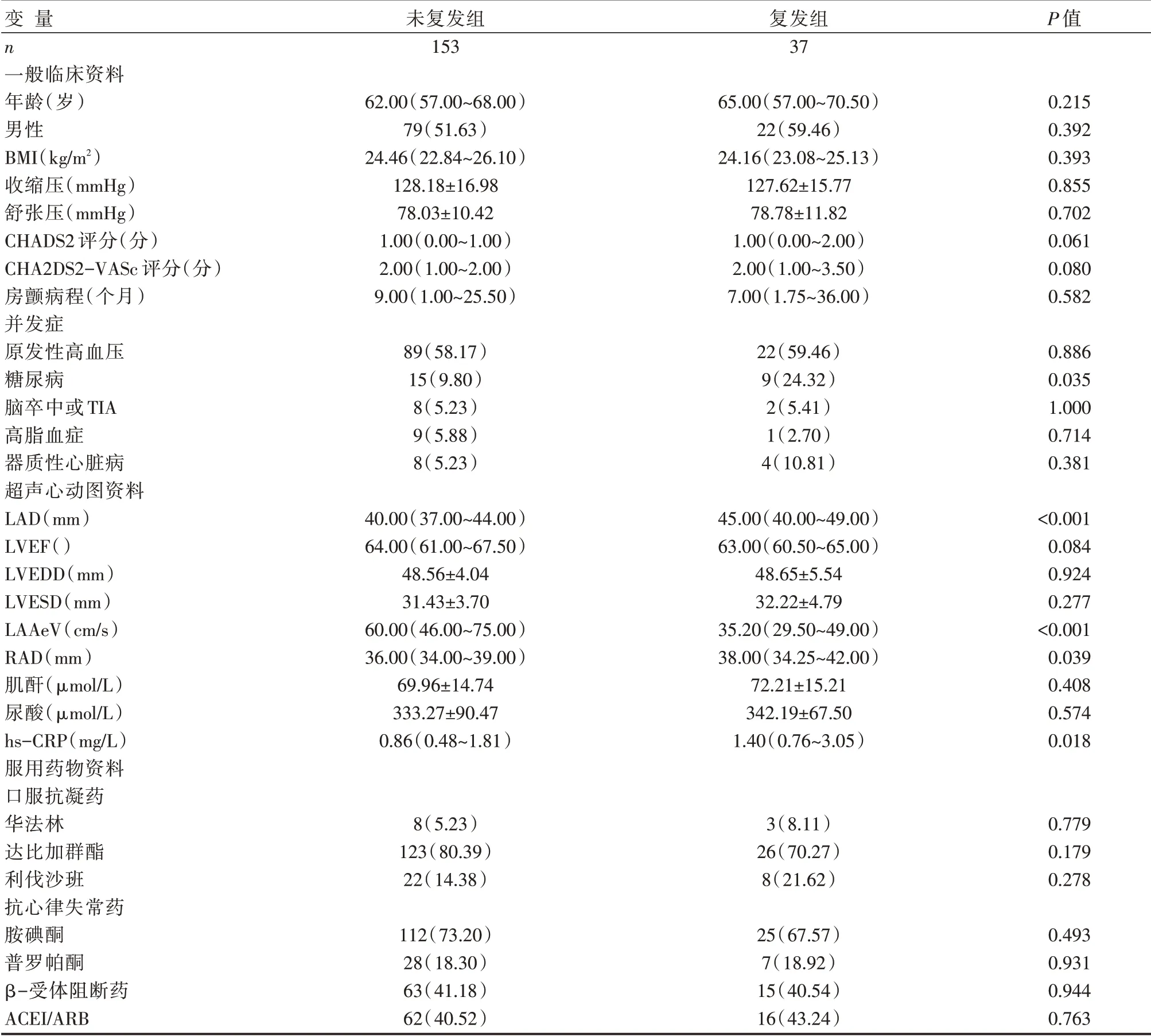
表1 复发组与非复发组临床资料比较 [(),M(Q1~Q3),n(%)]
注:BMI-体质量指数;TIA-短暂性脑缺血发作;LVEF-左心室射血分数;LVEDD-左心室收缩末期内径;LVESD-左心室舒张末期内径;ACEI/ARB-血管紧张素转化酶抑制剂/血管紧张素Ⅱ受体拮抗剂;1 mmHg=0.133 kPa
2.2 术后1 年患者心房颤动复发的危险因素分析
单变量Cox 回归分析结果显示:LAAeV、LAD、RAD 及合并糖尿病与RFCA 后患者PAF 复发显著相关(P<0.05)。多变量Cox 回归分析结果显示:高LAD 是预测术后房颤复发的独立危险因素;高LAAeV 是预防术后房颤复发的独立保护性因素。术后房颤复发患者的单因素及多因素Cox 回归分析结果详见表2。
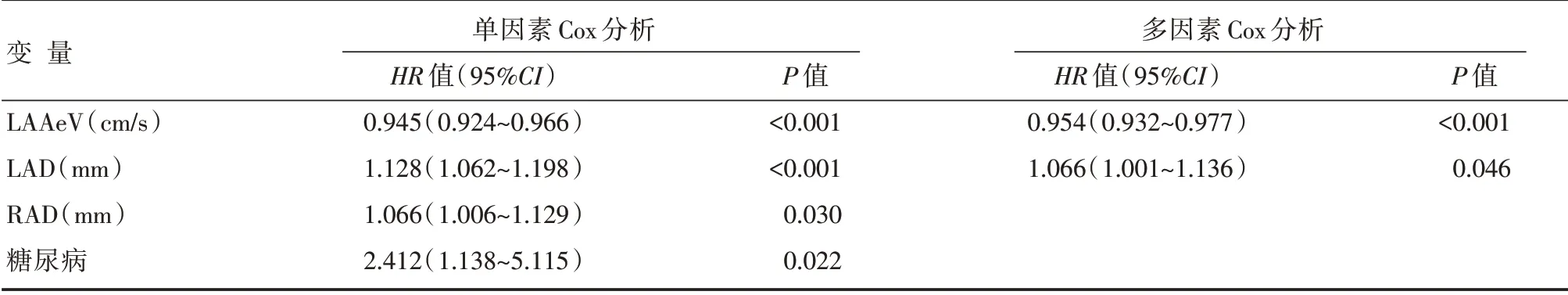
表2 术后1 年患者房颤复发的单因素及多因素Cox 回归分析结果
2.3 左心耳峰值排空速度对术后1 年阵发性心房颤动复发的预测价值
ROC 曲线分析结果显示,LAAeV 预测术后1年PAF复发的最佳截止值为42.05 cm/s、敏感度为67.6%、特异度为85.0%和AUC 为0.802(95% CI:0.716~0.888,P<0.001),见图1。
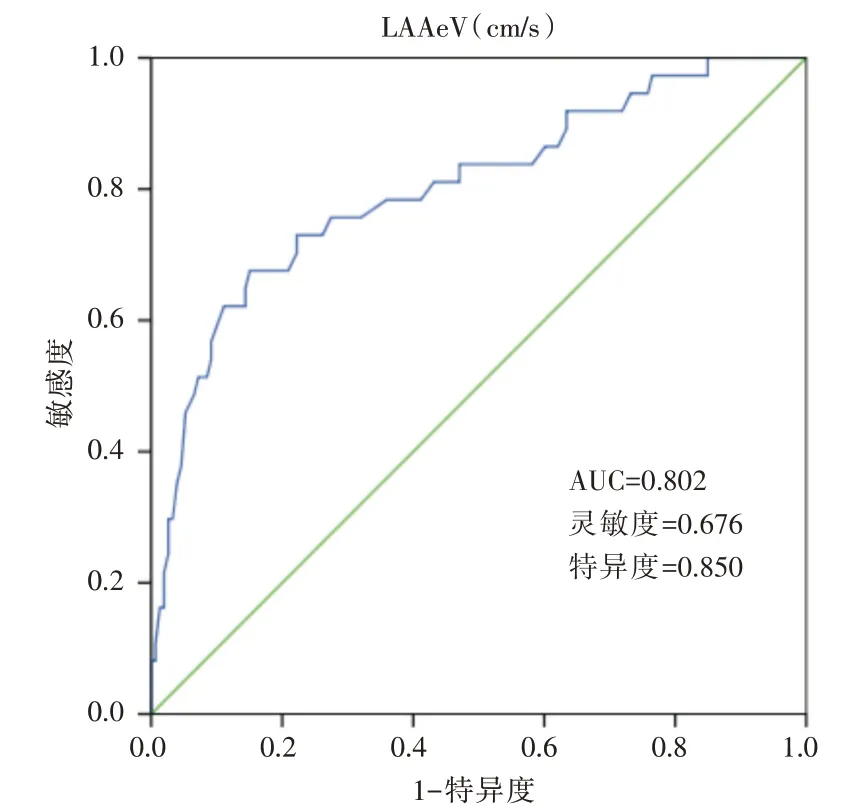
图1 LAAeV 预测术后1 年PAF 复发的ROC 曲线图
2.4 Kaplan-Meier 复发曲线分析结果
基于LAAeV 的最佳截断值(42.05 cm/s)进行分析,结果表明LAAeV<42.05 cm/s 的PAF 患者消融1 年复发率显著高于LAAeV≥42.05 cm/s 的患者(Log-RankP<0.001),见图2。
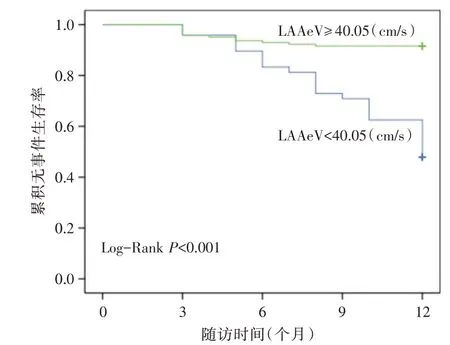
图2 两组患者LAAeV 累积无事件生存曲线比较
3 讨论
房颤是一种常见的心律失常,研究表明,CA在减少房颤复发方面比抗心律失常药物更有效[7],但术后复发仍是RFCA 目前遇到的最大问题。本研究共纳入首次行RFCA 的PAF 患者190 例,在术后12 个月的随访期间,共复发37 例(复发率为19.47%),这一复发率与先前的报告一致,术后较高的复发率仍然困扰着临床医生。
近年来,肺静脉异常电活动触发房颤成为公认的房颤发生机制,CPVI 成为房颤CA 治疗的基石[8],但术后复发率仍高达20%~45%[9]。这与非肺静脉异位病灶发放快速冲动有关[8,10],研究发现左心耳即为触发房颤的非肺静脉异位起搏点之一。在2005 年,Takahashi 等[11]在发表的个案报道中首次发现行CPVI 治疗后无法终止房颤的患者,进行电生理检查表明房颤的触发病灶为左心耳,进一步行左心耳电隔离治疗后转复为窦性心律,术后随访5 个月未复发房颤。Di-biase 等[12]在2010 年对987 例行第二次CA 治疗的房颤患者进行总结分析,其中266 例(27%)患者的房颤触发与局灶放电的起源是左心耳,有86 例(8.7%)的患者左心耳是唯一的触发病灶。Hocini 等[13]在2011 年分析总结了74 例行RFCA 治疗的持续性房颤患者房性心动过速的起源,结果有15 例(19%)的起源为左心耳。在心脏的发育过程中,左心耳在原始肺静脉形成时所形成的,且在左心耳开口处环绕的少部分组织和肺静脉的组织相近,这可能是左心耳能够触发房颤的原因之一[14]。
左心耳是起源于左心房主体的手指状延伸物,可增加左心房的扩张性来调节左心房压力和容积之间的关系,从而提高左心房血流动力学功能。LAAeV 反映了左心耳功能,包括其收缩性、顿抑和纤维化[15],同时LAAeV 与左心房壁收缩速度之间也有很好的相关性[16]。因而,LAAeV 代表了左心房的综合功能和左心房重构的严重程度[5],被认为是房颤复发的可靠预测因子。例如:Antonielli等[17]在一项对193 例非瓣膜性房颤患者的研究中发 现,大 于40 cm/s 的LAAeV(OR=5.2,95% CI:2.7~10.1,P=0.0001)是电复律成功后窦性心律维持的独立预测因子;He 等[15]在一项纳入80 例PAF患者的研究中发现,LAAeV(HR=0.948,95% CI:0.906~0.993,P=0.025)是RFCA 术后PAF 复发的重要预测因子,其预测房颤患者复发的最佳截止值为39.2 cm/s,此时灵敏度达75.0%,特异度达82.1%。Fukushima 等[3]在对105 例PAF 患者的前瞻性研究中也同样发现LAAeV 是RFCA 术后房颤复发的独立预测因子,均与本研究结果相一致。本研究结果显示LAAeV(HR=0.954,95% CI:0.932~0.977,P<0.001)与RFCA 后PAF 患者复发独立相关,且是预防PAF 术后复发的保护性因素,其预测患者复发的准确度、敏感度及特异度分别达80.2%,67.6%和85.0%。术前LAAeV 预测房颤复发的能力对于选择可能受益于RFCA 治疗的PAF 患者方面具有重要的临床意义。然而,据我们所知,还没有数据描述LAAeV 和左心房组织病理学改变之间的关系,仍需要进一步探索。
过去有研究报道了CA 后房颤复发的一些电生理机制,其中肺静脉与左心房电信号的再连接是最常见的机制之一[18]。许多研究报道了房颤的维持与发展伴随着心房结构重构[19-20]。在严重左心房结构重构的患者中,CPVI 线较长,导管操作更加困难。因此这些患者可能有更频繁的肺静脉再连接[15]。另外有研究表明左心房扩大与心房结构重构有关[21]。而左心房内径作为一种无创性的左心房扩大测量方法,广泛用于临床和研究,Berruezo 等[22]证明了较大的LAD 与RFCA 后房颤复发的高风险有关,与本研究结果相一致。本研究结果显示复发组LAD 显著高于未复发组,是房颤复发的独立危险因子(HR=1.066,95%CI:1.001~1.136,P=0.046)。
在本研究中,复发组与未复发组PAF患者之间基线hs-CRP 浓度比较,差异有统计学意义(P<0.05),但多元回归分析显示基线hs-CRP 浓度不能独立预测房颤复发。这与过去研究结果相矛盾,过去研究证实了房颤的发生、发展与心房肌的炎症反应相关[23]。有研究在房颤患者中观察到炎症生物标志物(如hs-CRP 和白细胞介素-6等)的升高[24],并且有研究显示房颤消融前的基线hs-CRP 浓度对预测长期复发有独立的预后价值[25]。考虑导致本研究结果的原因可能是一些入组患者长期服用了血管紧张素转化酶抑制剂/血管紧张素受体Ⅱ拮抗剂和他汀类药物。据报道,这些药物可以通过抗炎作用降低hs-CRP 浓度[26-27]。
首先,本研究为单中心研究,其结论可能不具有代表性,类似的研究尚需要在多中心进一步研究;第二,虽然通过普通12 导联心电图或24 h 动态心电图进行房颤复发的随访监测,但可能没有发现无症状的房颤发作。因此,在这项研究中PAF 的复发率可能被低估。
综上所述,本研究发现较高LAD、较低LAAeV与术后PAF复发独立相关,是预测PAF RFCA后1年复发的独立危险因素。术前基线LAAeV 水平可为临床工作中筛选行RFCA 的房颤患者和制定恰当术后干预措施提供指导。
