慢性阻塞性肺疾病急性加重期患者肺部感染的病原菌及危险因素分析*
2021-07-06高锋马肖龙吕家瑜
高锋,马肖龙,吕家瑜
(1.嘉兴市第一医院呼吸科,浙江嘉兴314001;2.嘉兴常春藤老年医院老年内科,浙江嘉兴314000)
慢性阻塞性肺病急性加重期(acute exacerbation of chronic obstructive pulmonary disease,AECOPD)往往由慢性阻塞性肺病急性加重演变而来,是临床上较为常见的严重呼吸系统疾病,若疾病得不到有效控制,加之患者摄取营养物质能力及免疫力低下、合并症较多,极易引发肺部感染,进一步促进病情进展,严重者可造成呼吸性衰竭等重症疾病,致死、致残率较高,危及患者生活质量及生命安全[1-3]。因此,及早发现AECOPD 肺部感染的相关致病因素,并采取及时有效的干预措施是防止病情恶化的关键。有研究表明,病原菌入侵是导致AECOPD 肺部感染的重要原因[4]。还有研究发现,患者肺部感染风险增加与年龄、基础疾病、长期卧床及激素药物的使用等多种因素有关[5]。随着对AECOPD病理机制研究的深入,发现凝血机制、炎症机制也可能参与该病的发生、发展[6-7]。鉴于此,本研究对AECOPD 肺部感染患者病原菌感染情况、危险因素及相关因子的表达进行分析,以期为AECOPD 肺部感染患者的早期鉴别诊断提供理论基础,现报道如下。
1 资料与方法
1.1 一般资料
回顾性分析2016年8月—2020年5月嘉兴市第一医院收治的AECOPD 患者临床资料102 例。其中,男性65 例,女性37 例;年龄47~81 岁,平均(70.25±11.32)岁。根据患者是否合并肺部感染,分为观察组52 例(合并肺部感染),对照组50 例(未合并肺部感染)。
1.2 纳入与排除标准
1.2.1 纳入标准全部患者符合AECOPD 相关诊断标准[8];患者临床资料齐全;合并肺部感染的患者符合肺部感染诊断标准[9],而未合并肺部感染的患者不符合肺部感染诊断标准[9]。
1.2.2 排除标准并发其他肺部疾病者;恶性肿瘤者。
1.3 诊断标准
1.3.1 AECOPD 诊断标准在吸入支气管舒张剂后明确发生持续的气流受限,并排除其他肺部疾病;呼吸道症状持续恶化,并需调整药物治疗方案;常伴有短期内咳痰、咳嗽、气短、喘息加重,痰液浓稠、量多,可伴发热、炎症加重等表现可诊断为AECOPD[8]。
1.3.2 肺部感染诊断标准在无菌操作条件下,采集患者的痰培养标本,并予以病原菌培养,在排除结核、肺不张、肺癌、肺栓塞等疾病后,符合病原菌培养阳性;胸部计算机断层扫描显示肺部浸润影;体格检查存在肺叩击实音、湿啰音;白细胞计数增加、体温>38℃;呼吸道疾病症状明显。以上超过2 项者可诊断为肺部感染[9]。
1.4 方法
通过自然咳痰、支气管镜、防污染毛刷等采集法收集病原菌标本。采用VITEKMALDI-TOF MF全自动快速微生物质谱检测系统(法国梅里埃公司)鉴定标本中病原菌的菌种。收集全部研究对象入院时静脉血,采用全自动血凝分析仪(法国斯塔高公司)检测血浆中D-二聚体(D-dimer,DD)及纤维蛋白原(Fibrinogen,FIB)水平,采用免疫比浊法(Cobas 8000 全自动生化分析仪,德国罗氏公司) 检测C 反应蛋白(C-reactive protein,CRP)水平,采用化学发光法(CARIS200 全自动化学发光免疫分析仪,北京万泰公司) 测定降钙素原(Procalcitonin,PCT)水平。
1.5 统计学方法
数据分析采用SPSS 24.0 统计软件。计量资料以均数±标准(±s)表示,比较用t检验;计数资料以构成比或率(%)表示,比较用χ2检验;影响因素的分析用多因素Logistic 回归模型。P<0.05为差异有统计学意义。
2 结果
2.1 AECOPD肺部感染者病原菌分布情况
52 例AECOPD 肺部感染者中检出病原菌69 株。其中革兰阴性菌44 株(63.77%),以肺炎克雷伯菌(21.74%)及铜绿假单胞菌(18.84%)为主;革兰阳性菌23 株(33.33%),以金黄色葡萄球菌(17.39%)及屎粪肠球菌(8.70%)为主;真菌2 株(2.90%)。见表1。

表1 AECOPD肺部感染者病原菌的分布
2.2 AECOPD并发肺部感染的单因素分析
单因素分析显示,观察组与对照组的年龄≥60岁、吸烟、糖皮质激素使用时间≥7 d、住院时间≥14 d、有机械通气史、慢性阻塞性肺病ABCD 分组为C 组和D 组、合并糖尿病比较,经χ2检验,差异均有统计学意义(P<0.05),观察组高于对照组。观察组与对照组的性别构成、意识功能障碍、心力衰竭、合并冠状动脉粥样硬化性心脏病(以下简称冠心病)、合并高血压及贫血比较,经χ2检验,差异均无统计学意义(P>0.05)。见表2。
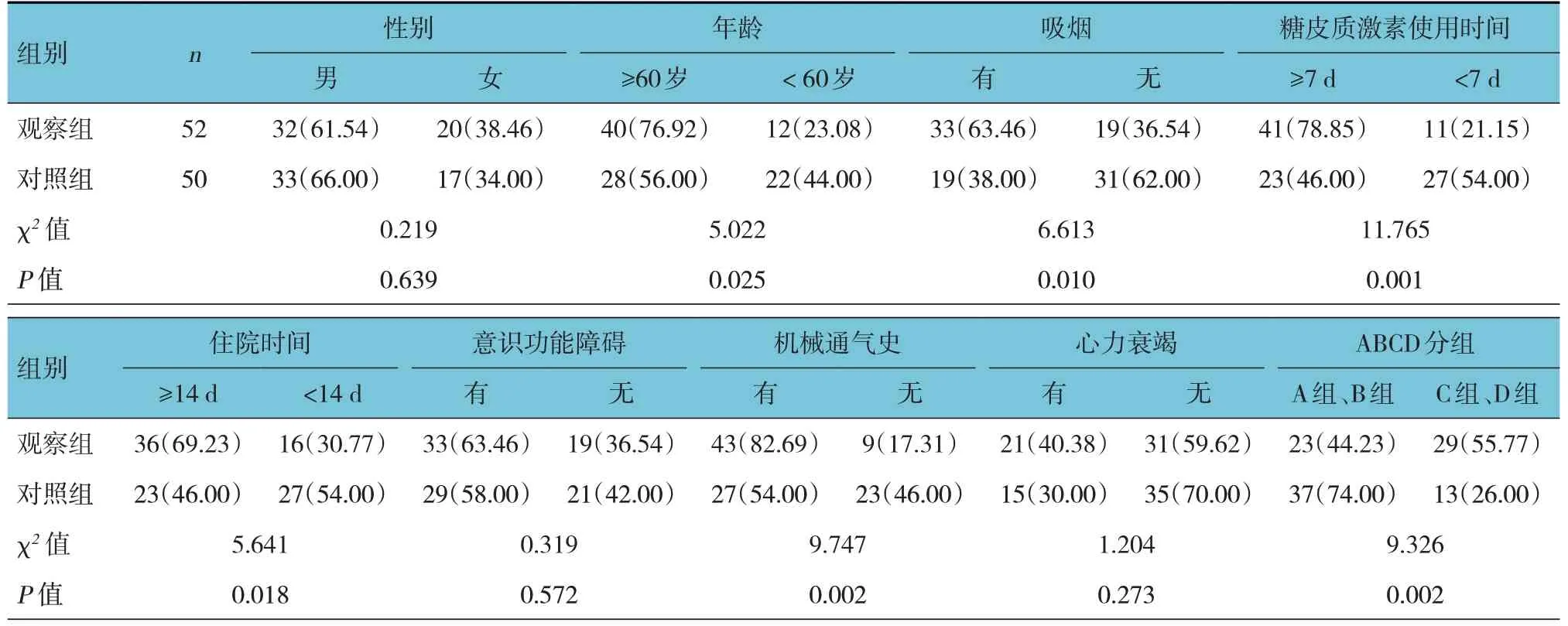
表2 AECOPD并发肺部感染的单因素分析 例(%)

续表2
2.3 AECOPD 并发肺部感染的多因素Logistic分析
以AECOPD 患者是否并发肺部感染作为因变量,以表2 中差异有统计学意义的7 个因素作为自变量,采用逐步后退法行多因素Logistic 回归分析(α入=0.05,α出=0.10)。各自变量赋值见表3。结果显示,年龄、糖皮质激素使用时间、住院时间机械通气史及ABCD 分组3.347(95%CI:1.091,10.271)]为AECOPD 并发肺部感染的独立危险因素(P<0.05)。见表4。

表3 赋值表

表4 AECOPD并发肺部感染的多因素Logistic分析参数
2.4 两组患者凝血指标、炎症指标比较
观察组与对照组DD、FIB、CRP、PCT 水平比较,采用t检验,差异有统计学意义(P<0.05),观察组高于对照组。见表5。
表5 两组患者凝血指标、炎症指标比较 (±s)

表5 两组患者凝血指标、炎症指标比较 (±s)
组别观察组对照组t 值P 值n 52 50 DD/(mg/L)2.67±0.35 0.93±0.24 26.169 0.000 FIB/(g/L)5.94±1.26 4.05±0.87 8.782 0.000 CRP/(mg/L)42.14±17.52 17.46±5.05 9.584 0.000 PCT/(μg/L)2.47±0.42 1.08±0.14 22.240 0.000
3 讨论
AECOPD 通常是由病毒或细菌经呼吸道感染引起的,但也可能是暴露在污染环境中造成的,AECOPD 可进一步加剧肺功能衰退,破坏肺部正常菌群平衡,促进肺部感染的发生,增加患者的死亡风险[10]。
因此,为有效发现、诊治及降低AECOPD 肺部感染率,本研究对AECOPD 肺部感染者病原菌分布情况进行鉴定,并分析引发AECOPD 肺部感染的相关危险因素及相关生物指标的变化。本研究结果显示,52 例AECOPD 肺部感染者检出病原菌69 株。其中革兰阴性菌较为常见,革兰阳性菌次之。有研究认为,AECOPD 病原菌感染原因可能与年龄、抗生素滥用、低蛋白血症、吸烟、接触粉尘及化学物质等危险因素密切相关[11-12]。
为进一步明确AECOPD 发生肺部感染的相关危险因素,多因素Logistic 回归分析结果显示,年龄、糖皮质激素使用时间、住院时间、机械通气史及ABCD 分组为AECOPD 并发肺部感染的独立危险因素。分析其原因:①年龄≥60 岁患者自身免疫功能较为低下,加之常合并多种基础疾病,患者多器官功能严重衰退,更易发生肺部感染;②长期使用糖皮质激素药物及机械通气时间过长可一定程度增强肺部多次感染与多重耐药菌感染的风险;③住院时间过久可进一步削弱患者各项生理机能,弱化呼吸系统功能,还会影响患者肺部痰液的排出,进一步增加肺部感染风险;④ABCD分组中C 组及D 组患者临床病理症状更为明显,肺功能更为低下,意味着患者病情更为严重,故该类患者病原菌感染风险更高,且并发肺部感染可能性更高。因此,应针对患者危险因素进行早期临床干预,尽量缩短患者住院时间,合理使用抗菌药物、做好营养支持等防治措施,以避免肺部感染。
有研究表明,长期炎症反应可诱发血栓前状态,导致弥散性血管内凝血,认为气道炎症及凝血机制紊乱是AECOPD 病情进展的主要病理生理基础[7,13]。DD 作为纤维蛋白溶解的终产物,其水平越高,提示血管内凝血状态越明显,FIB 属于机体凝血系统的重要因子,常作为动脉粥样硬化及血栓形成等不良事件的危险因素[14-15]。PCT、CRP 属于炎症因子,其水平变化可一定程度反映患者肺部病原菌感染的严重程度[16]。本研究结果显示,观察组DD、FIB、CRP、PCT 水平均显著高于对照组,提示AECOPD 肺部感染患者凝血机制及炎症反应异常。分析其原因主要与革兰阴性菌等病原菌的感染入侵有关,激活患者气道炎症反应,致使凝血功能紊乱。因此,通过检测患者凝血及炎症指标的变化对评估患者是否发生肺部感染具有指导意义。
综上所述,AECOPD 患者发生肺部感染的致病菌以革兰阴性菌为主,而年龄、糖皮质激素使用时间、住院时间及机械通气史是患者肺部感染的独立危险因素,且该类患者凝血机制及炎症反应异常,可为预测患者的预后提供一定的参考依据。
