重组人干扰素α-2b溶液型鼻腔给药制剂稳定性初探研究
2021-07-06胡乐非董明明
胡乐非,董明明,林 霞
0 引言
干扰素 α-2b 属于I型干扰素,临床应用于抗病毒、抗肿瘤及治疗急慢性病毒性肝炎,在新冠肺炎治疗中得到了广泛应用,它由165~166个氨基酸组成,其分子量约为19kD[1]。干扰素可与靶细胞表面受体相结合,刺激细胞内多种效应蛋白质分子合成,包括阻止细胞核糖体翻译的病毒蛋白;弱化转录酶活性的蛋白,从而抑制mRNA的形成,同时还可以形成病毒核酸对应的核酸酶,从而降解病毒核酸[2-3]。
目前雾化吸入注射用干扰素 α-2b已被新冠肺炎诊疗方案推荐用于一般治疗。但雾化吸入疗法需要特殊装置,不利于疾病的预防及早期治疗。干扰素 α-2b鼻腔给药制剂,经鼻黏膜给药,可在局部直接发挥抗病毒作用。此外,鼻腔部位存在丰富的毛细血管和淋巴管,鼻腔上皮与血管壁紧密相连,上皮细胞间间隙较大,具有较高的渗透性,且鼻腔部位蛋白酶含量较低,也可吸收入血,通过其他途径发挥抗病毒作用[4]。给药无需医院的雾化吸入给药装置,有效避免特殊时期交叉感染,患者顺应性好。
由于干扰素α-2b为蛋白类药物,其水溶液稳定性较差。因此,本文系统考察了缓冲体系pH、缓冲体系磷酸盐的浓度、稳定剂的种类及浓度、组合稳定剂对干扰素α-2b稳定性的影响,旨在开发一种稳定的干扰素α-2b溶液型鼻腔给药制剂。
1 仪器与试药
重组人干扰素α-2b干扰素原液(上海华新生物高技术有限公司,批号:B202005025,纯度99.9%,生物学活性2.1×108IU/ml,蛋白浓度1.1 mg/ml);磷酸二氢钠(二水)、无水磷酸氢二钠、氯化钠、赖氨酸、组氨酸、乙二胺四乙酸二钠(EDTA二钠,分析纯,国药集团化学试剂有限公司);吐温80(南京威尔有限公司),娃哈哈纯净水(杭州娃哈哈集团有限公司),蒸馏水。
分析天平 BSA124S(赛多利斯科学仪器有限公司);SHK-Ⅲ循环水式多用真空泵(郑州科泰实验设备有限公司);离心机(上海卢湘仪离心机仪器有限公司);Agilent 1260 高效液相色谱仪(美国安捷伦公司);DF-101S集热式恒温加热磁力搅拌器(郑州科泰实验设备有限公司);pH计(梅特勒-托利多仪器有限公司);冰箱(青岛海尔科技有限公司);SHZ-B水浴恒温振荡器(上海博迅医疗生物仪器股份有限公司);移液器(大龙兴创实验仪器股份公司)。
2 方法与结果
2.1 体外分析方法
2.1.1 色谱条件 参照《中国药典》2020版测定蛋白含量,色谱柱以适合分离分子质量为5~60 kD蛋白质的色谱用凝胶为填充剂。色谱柱:TSK gel G200SWXL(7.8 mm×30 cm,5 μm);流动相为:0.1 mol/L磷酸盐-0.1 mol/L氯化钠缓冲液,pH 7.0;流速:1 ml/min;进样体积:50 μl;检测波长:280 nm;柱温:25 ℃。
2.1.2 线性关系考察 分别精密量取1 ml干扰素原液置于容量瓶中,流动相稀释定容至 5、10、25、50、100 ml,分别得到蛋白浓度为220、110、44、22、11 μg/ml的干扰素标准溶液。离心(12 000 r/min,10 min,10 ℃),进样,于“2.1.1”项下测定峰面积。浓度为横坐标,峰面积为纵坐标进行线性回归,R2=0.999 5满足测试要求。
2.1.3 精密度试验 取 “2.1.2”项下浓度为11 μg/ml的干扰素标准溶液适量,离心(12 000 r/min,10 min,10 ℃),取上清液,于“2.1.1”项下连续进样6次,记录峰面积,结果峰面积RSD=0.44%,小于2.0%,表明仪器精密度良好。
2.1.4 稳定性考察 取“2.1.2”项下浓度为44 μg/ml的干扰素标准溶液适量,室温下放置,在 0、4、8、12、24 h,取样离心(12 000 r/min,10 min,10 ℃),于“2.1.1”项下进样,考察主峰面积的变化。结果显示,室温放置样品的峰面积RSD值为 0.92%,小于2.0%,稳定性较好。
2.1.5 滤膜吸附性考察 取“2.1.2”项下浓度为44 μg/ml的干扰素标准溶液适量,用 0.22 μm聚醚砜微孔滤膜过滤,每次过滤1 ml,取滤液作为供试品,直至过滤样品峰面积不再发生变化,同时以离心(12 000 r/min,10 min,10 ℃)的溶液作为对照,按“2.1.1”项下色谱条件进样,记录色谱图,考察主峰峰面积的变化情况。结果显示,分别过滤弃去1、2、3 ml初滤液后,峰面积并无明显变化,RSD值为0.31%,说明滤膜对样品溶液的吸附作用可忽略不计,无需弃去初滤液。
2.2 磷酸盐缓冲体系pH的筛选 由于鼻腔给药制剂pH过高或过低,可能引起鼻黏膜刺激,因此,需将干扰素α-2b溶液pH值调节至与生理环境接近的pH范围。而pH值亦可显著影响干扰素α-2b的稳定性。因此,本文考察了pH值5.0~7.5范围内干扰素α-2b溶液的稳定性。
采用不同比例的磷酸二氢钠与磷酸氢二钠的溶液,配制pH值分别为5.0、5.5、6.0、6.5、7.0、7.5且浓度为10 mmol/L的磷酸盐缓冲体系。以干扰素α-2b蛋白总浓度的变化筛选磷酸盐缓冲液的pH值。精密量取1 ml干扰素原液与9 ml不同pH值磷酸盐缓冲液置于10 ml的EP管中,在37 ℃的水浴条件下考察稳定性,以0 h干扰素α-2b蛋白浓度作为对比,分别于0、2、4、6、8、12、24 h取样,离心(12 000 r/min,10 min,10 ℃)进样分析,结果见图1。
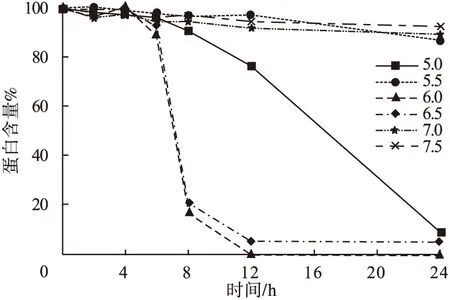
图1 不同pH缓冲液下干扰素α-2b蛋白相对百分含量结果
图1显示,当pH值为5.5、7.0、7.5时,干扰素稳定性较高,24 h后干扰素α-2b的相对百分含量分别为0 h的87.1%、89.9%、92.1%。其中pH为7.0和7.5时优于pH 5.5。而当pH为5.0、6.0和6.5时,干扰素的稳定性较差。α-2b干扰素在近中性(pH 7.0)环境中稳定性较高,酸性和碱性条件活性易降低,此外,本研究显示,与pH为5.0、6.0和6.5时相比,pH 5.5环境下,蛋白浓度下降较为缓慢。可能是由于干扰素等电点为4.0~6.7,在此pH范围内,干扰素净电荷为0,易聚集沉淀,导致蛋白浓度下降。在此pH范围内,由于离子环境微小差异,其聚集程度也有所区别。pH 5.5时,干扰素聚集速率略低于其他相近pH,从而导致蛋白浓度下降较为缓慢。
基于上述结果,当pH为7.0时为中性,对鼻腔的刺激性较弱,初步选择pH为7.0的磷酸盐缓冲液作为缓冲体系。
2.3 磷酸盐缓冲液浓度的考察 分别配制浓度为5、10、20、50 mmol/L的磷酸盐缓冲液,精密量取1 ml干扰素α-2b原液与9 ml不同浓度的磷酸盐缓冲液于10 ml的EP管中,以0 h干扰素α-2b蛋白浓度作为对比,考察37 ℃的稳定性。分别于0、4、6、8、12、24、48、72、144 h取样,离心(12 000 r/min,10 min,10 ℃)进样,HPLC分析,结果见图2。

图2 不同浓度磷酸盐缓冲液中干扰素α-2b蛋白含量结果
图2显示,当磷酸盐缓冲液的浓度为10 mmol/L时,24 h内稳定性较好,因此,确定磷酸盐缓冲液的浓度为10 mmol/L。
2.4 不同稳定剂的考察 蛋白制剂中多含有一定浓度稳定剂,以提高稳定性[5-7]。氨基酸对蛋白质的空间结构有一定的支撑作用,同时氨基酸可以作为抗氧化增效剂,如:组氨酸、赖氨酸等均具有较强的抗氧化作用。EDTA二钠是一种重要的螯合剂,可以螯合溶液中的金属离子,防止金属离子引起制剂变色、变质、变浊等氧化降解。聚山梨酯80为亲水型非离子表面活性剂,常用做助溶剂、乳化剂和稳定剂,也具有一定的稳定作用。
本文分别考察浓度为1 mg/ml的聚山梨酯80、EDTA二钠、赖氨酸、组氨酸,以及赖氨酸与EDTA二钠的组合作为稳定剂,同时以不含稳定剂的磷酸盐缓冲液(10 mmol/L,pH 7.0)药物溶液为对照(即空白组),优化稳定剂种类。
精密量取1 ml干扰素原液与9 ml含有不同稳定剂的磷酸盐缓冲液(10 mmol/L,pH 7.0)于10 ml的EP管中,以0 h干扰素α-2b蛋白浓度为对比,考察不同溶液在37 ℃条件下的稳定性。分别于0、4、8、12、24、48、72、144 h取样,离心(12 000 r/min,10 min,10 ℃),HPLC分析,结果见图3。

图3 不同稳定剂溶液体系中干扰素α-2b蛋白含量结果
图3显示,与不含稳定剂的干扰素α-2b溶液相比,分别以1.0 mg/ml EDTA二钠、赖氨酸和组氨酸为稳定剂时,干扰素α-2b溶液稳定性显著提高。1.0 mg/ml EDTA二钠稳定作用显著优于其他稳定剂,37 ℃水浴孵育6 d时,干扰素α-2b蛋白相对百分含量仍高达89.6%。
进一步考察组合稳定剂对干扰素稳定性的影响,结果显示,与单独加入EDTA二钠或赖氨酸相比,加入组合稳定剂(赖氨酸+EDTA二钠),干扰素α-2b稳定性降低,这可能是由于赖氨酸降低了EDTA二钠的络合作用。
基于上述研究结果,确定稳定剂为EDTA二钠。
2.5 稳定剂浓度的考察 以EDTA二钠为稳定剂,pH值为7.0的10 mmol/L磷酸盐缓冲液为溶剂,优化稳定剂浓度。分别考察浓度为0.2、0.4、0.6、0.8、1.0 mg/ml的EDTA二钠对干扰素α-2b稳定性的影响。
精密量取1 ml干扰素原液与9 ml含有不同浓度EDTA二钠的磷酸盐缓冲液(10 mmol/L,pH 7.0)于10 ml的EP管中,以0 h干扰素α-2b蛋白浓度为对比,考察不同溶液在37 ℃条件下的稳定性。分别于0、4、8、12、24、48、72、144 h取样,离心(12 000 r/min,10 min,10 ℃),HPLC分析,结果见图4。

图4 不同浓度EDTA二钠溶液中干扰素α-2b蛋白含量结果
结果显示,随着EDTA二钠浓度的降低,干扰素α-2b稳定性逐渐降低,EDTA二钠浓度为1.0 mg/ml时,稳定性显著优于其他浓度。因此,确定EDTA二钠浓度为1 mg/ml。
基于上述研究结果,确定干扰素α-2b溶液的组成为:10%(w/w)干扰素原液,1 mg/ml EDTA二钠、10 mmol/L磷酸盐缓冲液(pH值为7.0)。溶液中干扰素α-2b蛋白浓度为0.11 mg/ml,生物学活性为2.1×107IU/ml。该溶液可在37 ℃稳定6 d。
3 讨论
当前新冠肺炎疫情在全球范围肆虐,干扰素α-2b不仅作为此次新冠病毒感染的治疗方案推荐,也是作为儿童抗病毒治疗推荐药物。但是干扰素作为蛋白类药物,其稳定性较差且贮存条件较为苛刻,在此背景下开发一种处方简单、稳定性较好、使用方便、适用于新冠疫情期间普通人群和隔离人群的预防以及早期感染者治疗的干扰素制剂十分必要。
本研究系统考察了磷酸盐缓冲体系pH值、缓冲体系磷酸盐的浓度、稳定剂种类、稳定剂浓度对干扰素α-2b蛋白稳定性的影响,对干扰素α-2b干扰素溶液型鼻用制剂的处方进行了初步探索,确定磷酸盐缓冲体系的浓度为10 mmol/L,且pH为7.0;筛选了4种常用稳定剂,EDTA二钠稳定作用明显优于其他3种稳定剂;EDTA二钠浓度为1 mg/ml。后续将继续考察干扰素α-2b在该溶液体系中的长期稳定性,为α-2b干扰溶液型鼻用制剂的开发提供基础。
