颈管内膜刮取术在宫颈病变诊断中的应用发展现状与展望*
2021-07-05李元幸雒海瑕综述审校
李元幸,雒海瑕,李 晶 综述,王 伟,郝 敏 审校
(山西医科大学第二医院妇产科,太原 030001)
预防和发现早期宫颈病变是阻断宫颈癌发生的先决条件。预防性疫苗短期内覆盖面有限,发现早期宫颈病变并及时干预仍是临床工作重点。近年来宫颈病变筛查和评估的流程愈发精准化和规范化。对于宫颈初筛阳性的女性,予阴道镜检查,必要时多点活检,已形成标准的宫颈筛查三阶梯程序并在临床广泛应用。颈管内膜刮取术(endocervical curettage,ECC)又称宫颈管诊刮术、宫颈管刮术、颈管搔刮术等,是一种使用特殊纤维刷或刮匙留取宫颈管内膜组织送检病理标本进而明确是否存在宫颈病变的术式,属于阴道镜检查取样中的一个重要组成部分。ECC具有识别可能隐匿的宫颈上皮内瘤变(cervical intraepithelial neoplasia,CIN)的优势,尤其是对腺上皮病变(adenocarcinoma in situ,AIS)和宫颈病变治疗后的“跳跃性病变”有着独特的补充诊断和预后价值;ECC与最终病理一致率高,特异性强[1-2]。近期还发现ECC可能对宫颈病变有一定的治疗作用。ECC不仅可提高宫颈病变检出率,还可指导临床决策及管理,其应用对减少宫颈癌的发病率和死亡率有着重要意义。然而ECC还存在一些争议,目前尚无明确规范可遵循,还有较大改进空间。因此,本文就ECC的发展历程、存在的问题与挑战做一总结,并提出ECC可改善的空间与进步的方向。
1 ECC的由来与发展
1921年德国医师Hans Hinselmann发明了世界上第一台阴道镜[3],而后阴道镜逐渐应用于宫颈初筛阳性女性的转诊检查。阴道镜是一种附有光源的放大仪器,用于观察宫颈、阴道以及肛门生殖器区域的被覆上皮和血管。获得一个满意的阴道镜检查的必备条件是:转化区(原始鳞柱交界与新鳞柱交界之间的区域)以及病变的内外边界必须完全可视化。识别年老妇女、有宫颈多次活检史和宫颈治疗史女性的转化区通常十分困难,因为年老女性的转化区经常移行到宫颈管内,成为阴道镜医师的盲区;有多次宫颈活检或治疗史女性的转化区已遭到破坏,阴道镜图像易令人迷惑。ECC正是在这一背景下出现的。最早在1950年Pund等[4]报道了ECC在宫颈病变中的检出价值。ECC的出现与应用可将这一盲区暴露于病理医师的视野,有助于发现藏匿于宫颈管内的病变,使组织学评价更加全面。1989年在Philip John DiSaia的带领推广下,正式将ECC列为阴道镜检查中的补充程序[5]。
随着宫颈癌最重要的诱发因子——高危型人乳头瘤病毒(human papilomavirus,HPV)的发现,以及HPV检测的临床应用,使得宫颈癌筛查技术的重心从细胞学的症状学筛查部分转移到分子生物学的病因学筛查,弥补了细胞学对AIS识别的局限性,大幅提高了AIS检出率,也直接导致阴道镜转诊指征的变化。尤其是自2009年美国阴道镜检查与子宫颈病理学会(the American Society for Colposcopy and Cervical Pathology,ASCCP)新增HPV16/18型阳性作为阴道镜转诊指征以来,使得阴道镜下出现了不少还未病变的正常宫颈以及较难识别的AIS,无疑为阴道镜医师带来了新的巨大挑战。ECC在发现AIS或某些因宫颈治疗后产生的“跳跃性病变”有着独到优势,这有助于解决阴道镜转诊指征变化带来的困难局面。
ECC已在诊断领域发挥重要作用,近期有研究报道了ECC可能存在治疗作用,可使病变更易转归。一项对555例因CIN2+行宫颈切除术患者进行的回顾性研究分析了CIN转归的影响因素,结果发现阴道镜同时行ECC与CIN转归有关(P=0.002)[6]。尤其是当阴道镜检查不满意时,ECC理论上可清除宫颈管内部分孤立表浅的病灶,或ECC可能引起局部的炎症反应从而增强免疫识别和清除。
筛查策略的进步同时促成了宫颈病变治疗的广泛发展。ECC在宫颈病变治疗后的随访管理中也担任着重要角色。对于高级别宫颈鳞状上皮内病变(high-grade squamous intraepithelial lesion,HSIL),现有干预手段主要为子宫颈环形电切术(loop electrosurgical excisional procedure,LEEP)与子宫颈锥切术。ASCCP推荐HSIL治疗后6个月随访时行阴道镜检查和ECC[7]。已有大量研究证明ECC阳性是LEEP、锥切术后残留或复发的独立危险因素,可作为简单可靠的预测指标[8-11],与切缘病理相结合进行预测效果更佳[12]。此外,ECC对AIS患者的预后也有一定的价值[13],建议对有生育要求而保守治疗后的ECC阳性AIS患者,推荐重复诊断性切除,间隔6月重新评估,进行密切随访。
ECC在宫颈病变中的应用已有半个多世纪,随着筛查策略的进步与发展,ECC更能发挥独有优势,更加契合筛查现状,在宫颈病变的筛查中扮演着越来越重要的角色。如若出现更多有力证据支撑ECC兼顾诊断、治疗与预后的多重作用,无疑将为临床宫颈病变患者带来更多福音。
2 ECC目前面临的挑战
2.1 患者选择 关于ECC患者的选择,国内外均无明确细化的专家共识或指南可参考。推进ECC患者选择原则的建立,需要了解ECC补充检出率影响因素,并由此划分风险人群。已有一些研究对此进行了初步探索,见表1。
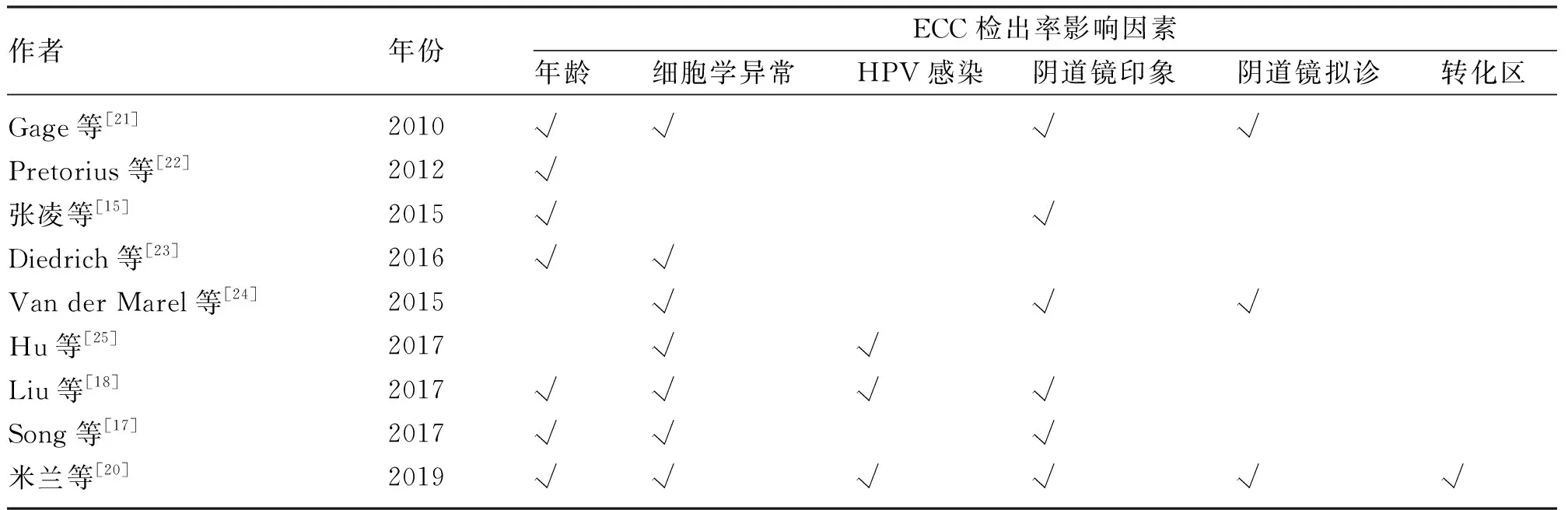
表1 近十年内文献报道的ECC检出率影响因素统计
年龄是影响ECC检出率的主要因素之一。这是因为随着年龄增长,宫颈鳞柱交界逐渐内移,一旦出现病变极有可能隐藏于宫颈管内。如Schneider等[14]以50岁为分界,将人群划分为年老组与年轻组,研究结果显示年老组从ECC中受益更多。张凌等[15]以40岁为分界,≥40岁与<40岁者ECC阳性率分别为40.7%(44/108)和19.2%(24/125),差异有统计学意义。Shepherd等[16]分别对50岁以下和50岁以上女性进行了阴道镜检查中ECC的成本效益分析,结果显示50岁以上女性行ECC能有效降低宫颈癌发病率和死亡率,且花费显著少于50岁以下女性。这项研究从社会经济水平佐证了对ECC患者的选择应将年龄因素考量在内。然而如何定义应行ECC患者的年龄分界线,仍无统一观点。不同文献划分的年龄节点有所不同,哪些人群受益更多?这还需今后具有更细化分层的大样本研究。
除年龄外,多项研究结果显示,HPV感染、细胞学结果异常、阴道镜拟诊也与ECC检出率相关。与年龄因素研究结果相似,HPV型别、细胞学异常等级节点的界定也各有不同。如Song等[17]建议对35岁以上、细胞学HSIL+的患者应行ECC。Liu等[18]认为下述人群应行ECC:45岁以上、HPV16感染女性;30岁以上、细胞学HSIL+/不能除外高度病变的非典型鳞状细胞(atypical squamous cells,cannot exclude HSIL,ASC-H)或阴道镜拟诊HSIL+;细胞学意义不明确的非典型鳞状细胞(atypical squamouscells of undetermined significance,ASC-US)或低度鳞状细胞病变(low-grade squamous intraepithelial lesion,LSIL)、阴道镜检查不满意的患者。Poomtavorn等[19]则认为,细胞学ASC-US和LSIL的女性最终诊断为HSIL+的几率很低,对这些女性是否应行ECC值得商榷。但总体而言,各项研究的理念均是为识别有高风险宫颈病变的人群并行ECC以进一步辅助诊断,这也与2019年ASCCP最新推出的基于风险的阴道镜检查策略相契合。
多项研究表明,阴道镜印象、转化区类别也是ECC检出率的影响因素。但目前并无明确证据推荐阴道镜满意患者是否应行ECC。理论而言,当阴道镜检查满意时,宫颈未观察到病变,则宫颈管亦应不存在病灶,即ECC应为阴性。研究数据显示,即使阴道镜检查转化区完全可见时,也有5%患者ECC阳性[20]。ECC报告结果可能将是诊断CIN或宫颈癌的唯一证据,即使ECC敏感性不强,也可能促使临床医师进行ECC。ASCCP现行指南写道,ECC更适用于阴道镜检查不充分、有一定发病风险但阴道镜下未见病变区的非妊娠女性,但当病变区可见时进行ECC也可接受[7]。换言之,现无针对ECC的可量化的、多方面考量的风险评估准则;对于阴道镜下满意的女性,指南认为执行与不执行ECC均可。阴道镜医师通常根据个人经验有选择地进行ECC,无明确规章可循,这明显不符疾病治疗的精准化、规范化原则。
对于ECC患者的选择是探索过程中不可忽略的研究重点。如何在提高宫颈病变检出率的同时,减少过度检查及治疗率并尽可能降低筛查成本,筛选风险人群并有针对性ECC即是解决此问题的关键之处,亟需更多研究进一步探讨。
2.2 对阴道镜及活检的补充价值 阴道镜的固有局限是宫颈管内病变无法被观测,而ECC具有发现藏匿于宫颈管内病变的显著优势。阴道镜和多点活检均阴性而ECC阳性的情况被定义为ECC对宫颈病变的补充诊断。然多年来ECC的补充诊断价值一直是争论的焦点所在,研究对象不同,ECC补充检出率也有较大差异,1.1%~18.5%不等(表2)。ECC属有创性操作,实行过程对于患者来说较痛苦,降低了患者随访依从性;且ECC获得的标本常常呈小的碎片状且间质较少,常伴有宫颈分泌物或凝血块,为病理观察带来了一定困难。ECC是否具有足够高的补充价值,能抵过上述缺陷带来的代价?尚无定论。
ECC补充价值高低与病理类型与分级有强相关性,对于鳞状病变和腺上皮病变,有截然不同的补充诊断价值。因而应首先着眼于病理类型与分级进行分层分析。对于宫颈鳞状上皮病变,ECC的性能尚有待商榷。阴道镜多点活检阴性但ECC为CIN1者较为少见,ECC对CIN1的补充价值有限。多数研究将重点放在CIN2+与CIN3+,即可从LEEP或宫颈锥切标本得到更进一步的病理金标准。如表2所示,以CIN2+为研究对象的研究结果差异较大,可能是由于CIN2病灶常较小且局限,可重复性较差。ECC可能对CIN3+患者有更大意义。
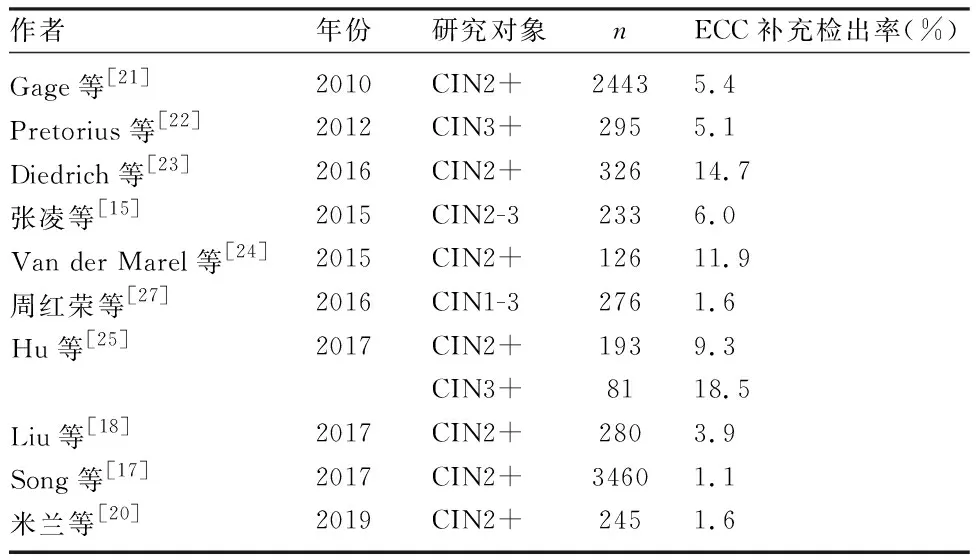
表2 近十年内文献报道的ECC对宫颈鳞状上皮病变的补充检出率统计
ECC在AIS中的应用更被大多临床医师所认可。因AIS常延伸至宫颈管,部分病变呈多中心性或跳跃性,ECC在AIS中可发挥重要作用。ASCCP建议对于初检不典型腺上皮(atypical glandular cells,AGC)行阴道镜及ECC并同时进行子宫内膜取样[7]。Jung等[26]在2019年就报道了1例仅通过ECC诊断为极早期宫颈腺癌并伴有盆腔淋巴结转移的患者。但英国国家子宫颈筛查卫生服务项目(the National Health Service Cervical Screening Program,NHSCSP)则认为ECC诊断宫颈AIS的敏感性较低,且假阴性率达59%~78%,因此并不常规推荐利用ECC排查AIS。ASCCP与NHSCSP的观点显然是矛盾的,现无有力证据充分说明ECC在AIS中的诊断价值。
ECC患者选择与补充价值是ECC未能良好应用于临床的两大根本障碍。ECC对不同人群的补充价值是ECC患者选择的理论基础依据,而ECC患者选择也同时决定了ECC在宫颈病变中的补充应用价值。期待今后更多高质量的临床研究出现,为ECC患者选择提供细化指南与准则,也能对ECC补充价值有一公正评价。
3 ECC临床应用的关键点
ECC在患者选择与补充诊断价值仍存争议,但ECC已在临床应用多年且将发挥越来越重要的角色,增加ECC可靠性对提高患者依从性与病变检出率至关重要,尤其ECC在取材器械、病理技术等方面仍有较大提升空间。
目前临床常使用刮匙来搔刮宫颈管以获得标本,此过程需将刮匙多次反复伸入再拉出宫颈管,标本质量一般,且给患者带来巨大痛苦;刮匙为重复使用的不锈钢材质,消毒灭菌和维护都增加了人力成本。现有一种新的纤维刷采样器械,此纤维刷有圆锥形的尖端,可通过旋转来收集标本,无需反复在宫颈管抽拉。数据显示纤维刷ECC比常规ECC有显著更高的标本满意率(91.1% vs 84.6%)[28]。纤维刷为一次性器械,无需设备灭菌与维护,还可显著减轻患者ECC过程的痛苦程度[29-30],有利于提高患者依从性。
ECC的病理技术也有一定改善空间。在病理医师对ECC标本的解释中,病理诊断的一致性只达中等(κ=0.52)[31],ECC诊断的可重复性较差。鉴于ECC研究结果同质性不强,病理医师对如何有效提高ECC病理标本的准确性进行了探讨。Shah等[32]将p16免疫组化技术应用于58例ECC标本中,补充诊断出18例HSIL。免疫组化技术已在宫颈病变的分级诊断中被广泛应用,将此技术同样应用于ECC的病理标本,有助于提高ECC的准确率。
此外,宫颈病变的检出率依赖于经验丰富的阴道镜医师和病理医师。在临床实践中,阴道镜医师和病理医师双方经常处于“素未谋面”的状态。阴道镜医师操作评估完毕后,应追踪病理结果,将阴道镜图像、活检定位与病理结果全面对比,回顾总结;病理医师也应保持与阴道镜医师之间的沟通交流,获取临床相关信息,共同提高ECC的准确度和可靠性。
4 总 结
宫颈癌的防治是一个受益与伤害共存的过程,这是临床医师和患者都需明确的一个理念。盲目追求零漏诊,必定导致增加过度治疗率;而选择患者伤害最小化,无疑会导致漏诊。这为阴道镜医师带来了辨证观念、逻辑推理上的极高挑战。ECC可有效弥补阴道镜宫颈管盲区的缺陷,尤其对AIS与“跳跃性病变”的诊断价值优越,这对目前阴道镜转诊指征变化、宫颈腺癌比例逐年升高的现状有着深远意义。ECC可进一步提高宫颈病变的诊断准确率,可作为宫颈病变治疗后残留和复发的预测指标,还可能在一定程度上促进宫颈病变的转归。然而ECC在宫颈病变的应用中存有争议,尤其是ECC患者选择无明确指南遵循,诊断价值高低争执不下。现今ECC临床应用还不能完全令人满意,无论是操作器械、病理技术,还是阴道镜医师与病理医师的经验水平,都有较大提升空间。阴道镜医师应多方面多角度衡量ECC的患者选择,尽可能识别可能有高风险的宫颈病变患者,精进ECC技术,与病理医师精诚合作,在提高宫颈病变检出率的同时,最大化减少患者痛苦。如何权衡ECC患者身心负担、社会经济效益与宫颈病变检出率的问题,值得今后更多医师与研究者的进一步深入探讨,以尽早推出针对ECC的临床实践指南,推进宫颈病变的精准化、规范化诊疗。
