芍药苷对幼鼠癫痫持续状态后海马神经元的保护作用
2021-06-30郑婷婷赵聪选张莉
郑婷婷 赵聪选 张莉
(1.大连市儿童医院神经内科,辽宁 大连116000;2.辽宁中医药大学附属医院超声心电中心,辽宁 沈阳110032)
癫痫是以大脑神经元突发异常放电导致大脑功能出现短暂障碍的一种神经系统疾病,可导致大脑皮质、海马体等区域神经元损伤,也是儿童最常见的神经系统疾病之一[1-2]。研究表明,约75%的癫痫患者于儿童时期起病,口服抗癫痫药物是主要治疗方法[3]。尽管癫痫的诊断和治疗研究不断进步,但抗癫痫药物的长期使用可导致诸多不良反应,且仍有30%左右的儿童患者疗效不佳,严重者发展为难治性癫痫,对患者的身心健康造成严重影响[4]。因此,探究癫痫的发病机制,寻找新的癫痫治疗药物及靶点具有重要的临床意义。芍药苷是是白芍、赤芍和牡丹的主要有效成分,属于水溶性单萜类糖苷,据报道,芍药苷具有镇痛、抗炎、抗肿瘤、保护神经和调节免疫的作用,已广泛用于神经系统疾病的研究和治疗中,能够通过多种作用机制减轻神经元细胞损伤,抑制神经细胞凋亡[5-7]。癫痫发病后往往造成神经元的损伤,我们猜想是否芍药苷对癫痫发病造成的神经元损伤具有保护作用。本研究采用腹腔注射氯化锂-匹鲁卡品诱发癫痫持续状态(status epilepticus,SE),观察芍药苷对幼鼠癫痫持续状态后海马神经元的保护作用,探究其作用机制。
1 材料和方法
1.1 实验动物 SPF级雄性Wistar幼年鼠72只,3周龄,体重(100±10)g,购自北京维通利华实验动物技术有限公司,许可证号:SCXK(京)2017-0011。饲养条件:室温(22±2)℃,湿度(50±10)%,每天定时换气,保持12 h:12 h光暗照明,食水不限。研究方案获本院伦理委员会批准。
1.2 主要试剂与仪器 芍药苷(纯度≥98%,美国Sigma-Aldrich);氯化锂、匹罗卡品(美国Sigma-Aldrich);地西泮注射液(天津金耀药业有限公司);HE染色试剂盒、TUNEL细胞凋亡检测试剂盒(北京索莱宝科技有限公司);Nissl染色液(上海碧云天生物技术有限公司);兔IgG-免疫组化试剂盒SABC即用型(博士德生物工程有限公司);引物(日本Takara);RevertAidTMfirst Strand cDNA Synthesis Kit,SYBR Green Real-Time PCR Master Mixes(美国Thermo Scientific);超氧化物歧化酶(superoxide dismutase,SOD)活力、丙二醛(malondialdehyde,MDA)ELISA试剂盒(武汉伊莱瑞特生物科技有限公司);B淋巴细胞瘤-2基因(B-cell lymphoma-2,Bcl-2)、Bcl-2相关X蛋白(Bcl-2-associated X protein gene,Bax)、线粒体动力学相关蛋白(dynamin-related protein 1,DRP1)、甘油醛-3-磷酸脱氢酶(glyceraldehyde-3-phosphate dehydrogenase,GAPDH)兔源单克隆抗体,羊抗兔二抗(美国CST公司);平衡型核苷转运载体-1(equilibrative nucleoside transporter-1,ENT1)蛋白兔源单克隆抗体(美国abcam公司);双板垂直电泳仪(北京六一仪器厂,型号:DYCZ-24KS);显微镜(日本奥林巴斯,型号:IX53);多功能凝胶成像系统(Syngene,型号:G:BOX);酶标仪(Thermo Fisher Scientific,型号:Multiskan MK3);高速冷冻离心机(长沙湘智离心机仪器有限公司,型号:TGL16MB)。
1.3 方法
1.3.1 分组、造模与给药 3周龄SPF级Wistar大鼠72只,随机分为对照组、模型组、芍药苷组(50 mg/kg,i.p.)。除对照组外,其余各组幼鼠腹腔注射氯化锂-匹鲁卡品诱发SE,造模方法参考文献[8]:大鼠称重后腹腔注射127 mg/kg氯化锂,20 h后腹腔注射1 mg/kg硫酸阿托品以降低匹罗卡品的外周胆碱能反应,30 min后腹腔注射50 mg/kg匹罗卡品。对照组大鼠仅腹腔注射等量生理盐水。造模后2 h,芍药苷组大鼠腹腔注射芍药苷(50 mg/kg/d),对照组和模型组同时腹腔注射等量生理盐水。造模后密切观察大鼠行为学变化,按照Racine评分标准[9]分为6级:0级为造模后无任何反应;Ⅰ级为大鼠面部抽搐、口角咀嚼、胡须抖动;Ⅱ级为大鼠面部抽动阵挛,不自主点头;Ⅲ级为大鼠单侧肢体阵发性抽搐;Ⅳ级为大鼠双侧前肢抽搐,并出现站立现象;Ⅴ级为在Ⅳ级的基础上大鼠出现站立不稳和跌倒。达到 4级或以上的大鼠视为造模成功,癫痫发作30 min后腹腔注射10 mg/kg地西泮终止SE。
1.3.2 组织处理 造模1 d、3 d、7 d后,各组大鼠腹腔注射5%水合氯醛溶液进行麻醉。每组取4只大鼠快速断头取脑,将脑组织存放于-80 ℃超低温冰箱保存,用于ELISA试剂盒、Western blot和qRT-PCR检测。剩余大鼠固定于手术台,开胸,暴露心脏,剪开右心耳,灌注150 mL生理盐水冲去血液,然后灌注150 mL 4%多聚甲醛固定,先慢后快,内固定完毕后断头取脑,置于4%多聚甲醛溶液中继续固定48 h,用于Nissl染色。
1.3.3 Nissl染色观察海马组织病理学改变 脑组织4%多聚甲醛固定,冠状切取含海马的视交叉前后3 mm 脑组织,常规脱水、透明,石蜡包埋,预冷切片(厚度为4 μm),二甲苯脱蜡,梯度乙醇复水,Nissl染色液染色3~10 min,蒸馏水洗涤2次,每次15 s,95%乙醇脱水5 min,二甲苯透明5 min,滴加中性树胶封片,置于显微镜高倍镜下观察,计数每个高倍镜视野下Nissl阳性染色细胞数量,取平均值。
1.3.4 ELISA法检测海马组织SOD活力和MDA含量 取造模第7天获取的大鼠海马组织,加入预冷PBS缓冲液,冰上研磨成匀浆,10 000 r·min-1离心10 min取上清,离心半径为12.5 cm,分装在EP管中,-80 ℃保存。①SOD活性检测:取待测样品20 μL,依次加入SOD检测缓冲液、WST-8工作液和反应启动工作液,37 ℃孵育30 min,450 nm波长测定吸光度(A)值,计算抑制百分率,抑制百分率=(ΔA空白-ΔA测定) /ΔA空白×100%,按照标准曲线计算待测样品的SOD酶活力(U/mg)。②MDA含量检测:取待测样品100 μL,依次加入工作液、蒸馏水和待测样品,置于100 ℃水浴中孵育60 min,冰浴冷却,10 000 g常温离心10 min,吸取200 μL上清液加入玻璃比色皿中,测定各样品在450 nm、532 nm和600 nm处的吸光度A值,计算ΔA450=A450测定-A450空白,ΔA532=A532测定-A532空白,ΔA600=A600测定-A600空白,MDA含量(nmol/g)=5×[12.9×(ΔA532-ΔA600)-2.58×ΔA450]。
1.3.5 Western Blot检测海马组织Bcl-2、Bax、DRP1和ENT1蛋白表达 取造模第7天获取的大鼠海马组织,冰上研磨,离心取沉淀,加入裂解液提取组织蛋白,BCA蛋白定量试剂盒测定蛋白浓度,配置15%的分离胶和5%的浓缩胶进行SDS-PAGE电泳,上样后80 V电泳2 h,60 V转膜2 h,5%脱脂奶粉封闭2 h,随后将条带放入10 mL Bcl-2、Bax、DRP1、ENT1兔源一抗稀释液中,稀释比例均为1∶1000,4℃过夜,第2天用TBST清洗后加入羊抗兔二抗(1∶2000)37℃孵育2 h,洗膜,滴加发光液,置凝胶成像系统显影。免疫印迹实验的内参蛋白为GAPDH,Image J软件分析各个蛋白对应的灰度值,计算蛋白的相对表达量,蛋白相对表达量=目的蛋白灰度值/内参蛋白灰度值。
1.3.6 qRT-PCR法检测海马Bcl-2、Bax、DRP1和ENT1 mRNA表达 取造模第7天获取的大鼠海马组织,冰上研磨,加1 mL Trizol裂解液提取组织总RNA,使用RevertAidTMfirst Strand cDNA Synthesis Kit逆转录试剂盒合成cDNA,作为荧光定量模版。引物由日本Takara 公司设计合成,所有样品均以GAPDH为内参。反应体系:dNTPs 0.5 μL+5×Buffer 5 μL+Taq 酶0.3 μL+MgCl21.5 μL+cDNA 模板2 μL+上下游引物分别1 μL,加去离子水至总体积25 μL。反应条件为:95 ℃预变性5 min,95 ℃变性30 s、62 ℃退火30 s、72 ℃延伸30 s,重复40个循环,最后72 ℃延伸10 min,4 ℃ 5 min终止反应,实验重复3次。采用2-△△CT的方法计算目的基因mRNA相对表达水平的变化。引物序列,见表1。

表1 基因引物序列Table 1 Primer sequences
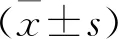
2 结果
2.1 造模后大鼠行为学变化 造模后5 min,大鼠出现面部抽搐、口角咀嚼、流涎、腹泻等外周反应。造模后10 min,大鼠面部抽动阵挛,不自主眨眼、点头、胡须抖动。造模后30 min以上,大鼠呈双侧前肢抽搐和站立现象,甚至出现站立不稳和跌倒,表明造模成功。
2.2 芍药苷对海马组织病理变化的影响 Nissl染色显示,对照组大鼠海马CA3区神经元呈多层分布,锥体细胞及颗粒细胞形态正常,染色均匀,排列紧密,胞体呈圆形或椭圆形,核仁明显,胞浆内尼氏小体丰富,偶见细胞核固缩。与正常组比较,模型组大鼠海马CA3区神经元数量减少、变形,排列紊乱,胞体缩小或破裂,细胞核固缩,胞浆内尼氏小体显著减少。与模型组比较,芍药苷组大鼠海马CA3区神经元受损程度减轻。见图1。对照组、模型组、芍药苷组Nissl阳性染色细胞数量分别进行组间比较,差异有统计学意义(F1d=89.36,P1d<0.01;F3d=68.65,P3d<0.01;F7d=72.38,P7d<0.01)。进一步两两比较结果显示,第1天、第3天和第7天时模型组(t1d=44.25,P1d<0.01;t3d=38.91,P3d<0.01;t7d=52.17,P7d<0.01)和芍药苷组(t1d=25.73,P1d<0.05;t3d=36.84,P3d<0.01;t7d=42.28,P7d<0.05)Nissl阳性染色细胞数量均显著高于对照组,芍药苷组Nissl阳性染色细胞数量均低于模型组(t1d=47.69,P1d<0.01;t3d=37.19,P3d<0.01;t7d=26.58,P7d<0.05),差异有统计学意义。其中,对照组在第1天、第3天、第7天时Nissl阳性染色细胞数量进行组间比较,差异无统计学意义(F=1.02,P>0.05),模型组和芍药苷组在第1天、第3天、第7天时Nissl阳性染色细胞数量分别进行组间比较,差异有统计学意义(F模型组=18.36,P<0.05;F芍药苷组=11.14,P<0.05)。进一步两两比较显示,模型组在第3天和第7天时Nissl阳性染色细胞数量均高于第1天(t3d=24.21,P3d<0.05;t7d=21.54,P7d<0.05),第7天时Nissl阳性染色细胞数量高于第3天(t7d=34.06,P7d<0.01)。芍药苷组第3天和第7天时Nissl阳性染色细胞数量低于第1天(t3d=19.36,P3d<0.05;t7d=33.27,P7d<0.01),第3天和第7天时Nissl阳性染色细胞数量比较差异无统计学意义(t3d=1.33,P3d>0.05;t7d=0.94,P7d>0.05)。见表2。
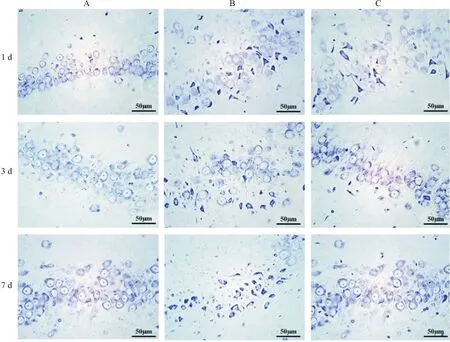
图1 Nissl染色观察大鼠海马组织病理变化(400×)Figure 1 Nissl staining was used to observe the pathological changes of rat hippocampus注:A.对照组;B.模型组;C.芍药苷组

表2 各组大鼠在不同时间点时Nissl染色阳性细胞数量比较Table 2 Comparison of Nissl staining positive cells in each group at different time
2.3 ELISA法检测芍药苷对海马组织氧化应激的影响 对照组、模型组、芍药苷组大鼠海马组织SOD活力、MDA含量分别进行组间比较,差异均有统计学意义(F=36.25、41.28、31.20,均P<0.01),进一步两两比较显示,模型组和芍药苷组SOD活力低于对照组(t模型组=25.66,P<0.05;t芍药苷组=39.24,P<0.01),MDA含量高于对照组(t模型组=31.32,P<0.01;t芍药苷组=48.96,P<0.01)。与模型组比较,芍药苷组SOD活力升高(t芍药苷组=26.47,P<0.05),MDA含量降低(t芍药苷组=42.58,P<0.01)。见表3。

表3 各组大鼠海马组织SOD活力和MDA含量比较Table 3 Comparison of SOD activity and MDA content in hippocampus of rats in each group
2.4 Western Blot检测芍药苷对海马组织Bcl-2、Bax、DRP1、ENT1蛋白表达的影响 结果显示,对照组、模型组、芍药苷组Bcl-2、Bax、DRP1、ENT1蛋白表达水平分别进行组间比较,差异有统计学意义(F=25.98、33.87、63.21、49.82,均P<0.01)。进一步两两比较显示,模型组(tbax=20.51,P<0.05;tDRP1=33.19,P<0.01;tENT1=26.32,P<0.05)和芍药苷组(tbax=19.34,tDRP1=27.63,tENT1=19.77,均P<0.05)海马组织Bax、DRP1和ENT1表达显著高于对照组,模型组(tbcl-2=37.36,P<0.01)和芍药苷组(tbcl-2=29.57,P<0.05)Bcl-2表达显著低于对照组。与模型组比较,芍药苷组Bax、DRP1和ENT1表达降低(tbax=61.25,tDRP1=58.17,tENT1=36.49,均P<0.01),Bcl-2表达增加(tbcl-2=59.01,P<0.01)。见图2,表4。

表4 各组大鼠海马组织Bcl-2、Bax、DRP1、ENT1蛋白表达比较Table 4 Comparison of protein expression of Bcl-2,Bax,drp1 and ENT1 in hippocampus of rats in each group

图2 Western Blot检测大鼠海马组织Bcl-2、Bax、DRP1、ENT1蛋白表达Figure 2 Western blot was used to detect the protein expression of Bcl-2,Bax,DRP1 and ENT1 in hippocampus of rats
2.5 qRT-PCR检测芍药苷对海马组织Bcl-2、Bax、DRP1、ENT1 mRNA的影响 结果显示,对照组、模型组、芍药苷组3组间Bcl-2、Bax、DRP1、ENT1 mRNA表达水平比较,差异有统计学意义(FBcl-2=26.14,P<0.05;FBax=49.78,P<0.01;FDRP1=24.76,P<0.05;FENT1=32.33,P<0.01)。进一步两两比较显示,模型组(tbax=44.36,P<0.01;tDRP1=46.37,P<0.01;tENT1=25.03,P<0.05)和芍药苷组(tbax=43.45,tDRP1=52.24,tENT1=31.55,均P<0.01)海马组织Bax、DRP1和ENT1 mRNA表达显著高于对照组,模型组(tbcl-2=29.31,P<0.05)和芍药苷组(tbcl-2=48.05,P<0.01)Bcl-2 mRNA表达显著低于对照组。与模型组比较,芍药苷组Bax、DRP1和ENT1 mRNA表达降低(tbax=24.54,tDRP1=26.83,tENT1=19.06,均P<0.05),Bcl-2 mRNA表达增加(tbcl-2=28.65,P<0.05)。见表5。

表5 各组大鼠海马组织Bcl-2、Bax、DRP1、ENT1 mRNA表达比较Table 5 Comparison of Bcl-2,Bax,DRP1 and ENT1 mRNA expression in hippocampus of rats in each group
3 讨论
癫痫是神经系统的常见发作性疾病,具有重复性、短暂性和发作性等特点,也是幼儿神经系统疾病中致死率和致残率极高的急重症,严重影响患者的生活质量[10-11]。癫痫发作时神经元异常放电和兴奋,这种活动与能量代谢密切相关,而线粒体在能量代谢和转换过程中起关键作用[12-13]。研究表明,长期反复的癫痫发作可导致线粒体功能受损,使参与调控线粒体分裂过程的关键蛋白——DRP1异常高表达,引发细胞凋亡和神经元损伤[14]。ENT1是一种转运核苷及其类似物的膜整合蛋白,该蛋白在哺乳动物组织中广泛存在,在控制神经系统细胞外腺苷的水平中发挥主导作用,参与调节神经元的活动[15]。研究表明,癫痫发作时,ENT1可通过抑制腺苷受体提高胞外谷氨酸水平,谷氨酸是人体内主要的兴奋性氨基酸,而兴奋性氨基酸的水平过高可导致癫痫的发作[16]。Luo等[17]的研究表明,DRP1的表达异常可影响线粒体动力学失衡,影响ENT1功能变化,增加谷氨酸等兴奋性氨基酸的释放增加,是导致癫痫的机制之一。在本研究中,我们以DRP1-ENT1轴为切入点,观察芍药苷对癫痫幼鼠神经元的保护作用,初步探究其作用机制。
在本研究中,我们通过腹腔注射氯化锂-匹鲁卡品诱发SE,模型组、芍药苷组大鼠均出现癫痫发作,Racine评分为4级以上,表明造模成功。研究表明,癫痫发作可造成脑神经细胞数量减少、神经元损伤和细胞凋亡,可直接影响患儿的病情发展和预后情况[18]。本研究通过Nissl染色观察芍药苷对癫痫大鼠海马损伤的保护作用。病理切片染色显示,模型组癫痫大鼠海马区神经元受损明显,排列紊乱,胞体缩小或破裂,细胞核固缩,胞浆内尼氏小体减少,随着时间的推移,损伤细胞数量增加。与模型组比较,芍药苷组大鼠海马CA3区受损神经元数量减少,受损程度减轻,损伤细胞数量随着时间的推移未增加,表明芍药苷对癫痫造成的大鼠海马神经元损伤具有抑制作用。研究表明,癫痫等神经系统疾病可诱发大脑细胞氧化应激损伤,同时削弱其抗氧化能力,是癫痫发生及持续发作的重要机制之一,其中,SOD是一种重要的抗氧化酶,SOD的水平可反映机体清除自由基的能力;MDA则与组织细胞受损程度相关,是氧自由基损伤组织细胞后产生的脂质过氧化物[19-20]。夏顺刚等[21]研究表明,调节患者机体氧化应激状态可有效减少癫痫发作。本研究结果显示,癫痫可增加海马组织MDA含量,降低SOD活力,而芍药苷可抑制癫痫诱发的氧化应激损伤,增加SOD活力,减少MDA产生。Bcl-2和Bax是调控细胞凋亡的关键基因,Bax过表达可促进细胞凋亡,而Bcl-2可与Bax形成二聚体,抑制Bax基因的表达,从而抑制细胞凋亡[22-23]。研究表明,增加Bcl-2和降低Bax的表达水平可减少海马神经元的凋亡,产生对海马神经元的保护作用和抑制癫痫的作用[24]。在本研究中,我们检测了第7天时各组大鼠海马组织中Bcl-2和Bax的表达情况,以此检验芍药苷对癫痫发作诱导的细胞凋亡的影响。结果显示,模型组大鼠海马组织Bcl-2蛋白和mRNA表达水平显著低于对照组,Bax蛋白和mRNA表达水平显著高于对照组,使用芍药苷对大鼠进行干预后可显著减少Bax的表达水平,增加Bcl-2的表达水平,表明芍药苷可显著改善癫痫发作导致的细胞凋亡。研究表明,癫痫发作与线粒体功能密切相关,DRP1是调控线粒体活动的关键蛋白,可通过影响ENT1的表达参与癫痫的发生,而抑制EMT1的功能可降低海马神经元的动作电位频率,对癫痫发作后神经元损伤产生保护作用[25-26]。本研究检测了癫痫发作后第7天时各组大鼠海马组织DRP1和ENT1的蛋白和mRNA的表达水平,结果显示,对照组大鼠海马组织存在DRP1和ENT1基础表达,而模型组海马组织DRP1和ENT1蛋白和mRNA的表达显著增加。与模型组比较,使用芍药苷对大鼠进行干预可显著减少DRP1和ENT1蛋白和mRNA的表达水平,表明芍药苷能够抑制癫痫诱发的DRP1和ENT1异常高表达。
4 结论
芍药苷可减轻癫痫诱发的海马组织损伤和细胞凋亡,其作用机制可能与抑制DRP1和ENT1的活化有关。
