Rho激酶抑制剂对脑梗死模型大鼠抗炎作用及TLR4/TRIF通路的影响
2021-06-30郭春保张毅周文芳王兴
郭春保 张毅 周文芳 王兴
(三峡大学第三临床医学院·国药葛洲坝中心医院 1.神经内科;2.重症医学科;3.心血管内科,湖北 宜昌 443002)
脑梗死主要因脑组织区域出现供血不足、在缺血和缺氧条件下造成脑组织病变或坏死而形成的,其发病机制有很多种,主要的发病原因是动脉粥样硬化[1-2]。脑梗死中最常见的类型为血栓形成性脑梗死,脑动脉主干和皮质支动脉粥样硬化导致血管腔狭窄或闭塞是血栓形成性梗死的主要表现。脑梗死致残率和病死率高,容易复发,是危害人类健康常见的疾病[3-4]。目前临床对于脑梗死的治疗可在一定程度上改善患者临床症状,但多数患者预后不良,较易出现神经功能障碍等不良事件的发生。Rho激酶抑制剂可改善脑部供血状态、降低血脑屏障和血脊髓屏障的通透性。还可以抑制细胞的死亡和减轻体外谷氨酸的神经兴奋毒性。基于此背景,为改善脑梗死患者预后,促进神经功能恢复,将Rho激酶抑制剂应用于脑梗死模型大鼠的干预治疗中,以并观察大鼠神经功能和抗炎因子,明确Rho激酶抑制剂改善大鼠神经功能和抗炎作用,为临床上脑梗死的治疗提供新方向。
1 材料与方法
1.1 材料 实验动物:SPF级SD健康大鼠45只,由北京维通利华实验动物技术有限公司提供,鼠龄(3.6±0.5)个月,体重(222.8±10.6)g。所有大鼠均养殖在干净笼子里,室温(22.1±2.0)℃,相对湿度38%~42%,每天光照12h,喂饮纯净水,饲养时间一周。本文研究所做实验均获得我院伦理委员会批准。主要试剂:Rho激酶抑制剂(上海源叶生物科技有限公司,货号:155558-32-0);水合氯醛(上海士锋生物科技有限公司,货号:302-17-0);大鼠抗小鼠TLR4抗体(上海恒斐生物科技有限公司,货号:K003881P);兔抗大鼠TRIF抗体(深圳市豪地华拓生物科技有限公司,货号:253451);兔抗大鼠TRAM抗体(武汉菲恩生物科技有限公司,货号:FNab10225)。
1.2 方法
1.2.1 分组及建模 随机选取45只大鼠中15只作为空白组,另外30只大鼠参照卞鑫等[5]研究实验中采用线栓法建立脑梗死模型。用10%水合氯醛腹腔注射麻醉,然后将它以仰卧位的姿势摆放,做颈正中切口后将右侧颈总动脉、颈内动脉和颈外动脉进行分离。颈外动脉结扎离断后,用缝线将颈总动脉近端结扎,用动脉夹将远端夹闭,在颈动脉分叉处做一个小切口,将尼龙线栓经切口插入并松开动脉夹,慢慢向前推进约18~20mm,遇到阻力后停止,把血管外的线栓剪断,缝合切口建模成功。最终30只大鼠中27只模型建立成功,建模成功率为90%,将建模成功的27只大鼠随机分为模型组14只、给药组13只。
1.2.2 给药 在建模成功后给药组大鼠腹腔注射Rho激酶抑制剂(法舒地尔)15mg/kg,空白组和模型组腹腔注射等容量生理盐水。
1.2.3 切片及染色 采用断头法处死大鼠,立即取大鼠脑组织,将提取的组织制作标本,使用40mL/L的多聚甲醛进行固定,常温下使用15%的EDTA脱钙,脱水后进行石蜡包埋,制作3μm的组织切片,之后行HE染色处理,使用光学显微镜观察大鼠脑组织变化。
1.2.4 BDNF、NSE、GFAP、TNF-α、ICAM-1、IL-1β水平检测 抽取3组大鼠尾部静脉血3mL,以离心半径5cm、转速3000r/min离心处理10min,分离上层血清,-80℃保存待检。BDNF、NSE、GFAP、TNF-α、ICAM-1、IL-1β水平采用酶联免疫吸附试验法检测,将血清样本置于室温后,取出试剂盒,标记酶标板,制作标准品,以1∶2的稀释液稀释样品;在反应孔上依次加入稀释好的待测血清及标准品100μL/孔,放置37℃恒温孵育箱中湿育2h;用专用洗涤液将反应板清洗3次后,加入抗体工作液(1∶100倍稀释后)100μL/孔,置于37℃恒温孵育箱中湿育45min;继续清洗反应板4次后,在反应孔内加入TMB溶液100μL/孔,置于37℃恒温孵育箱中湿育45min后在反应孔内加入终止液100μL/孔以终止反应,在450nm波长(参考波长570-630nm)测定吸光度,颜色反应深浅与BDNF、NSE、GFAP、TNF-α、ICAM-1、IL-1β水平成正比,经绘制标准曲线计算BDNF、NSE、GFAP、TNF-α、ICAM-1、IL-1β水平。
1.2.5 TLR4/TRIF通路蛋白检测 采用实时荧光定量PCR法进行检测,取100mg样品加100μL Trizol,研磨后加900μLTrizol,手动摇晃15秒,在温室中静置5分钟;再加入200μL氯仿,手动摇晃15秒,在温室中静置3分钟;在4℃的环境下,将它12000转离心15分钟;取上清500μL,加入500μL异丙醇,手动摇晃15秒,在温室中静置15分钟;再将它12000转离心10分钟,弃上清,加入200-300μL75%冰酒精;然后再7500转离心5分钟,5-10分钟的通风橱干燥,最后加入双无水20μL,85℃水浴5分钟。采用2-△△Ct方法计算出TLR4/TRIF通路蛋白中TLR4、TRIF、TRAM表达量,内参β-actin:上游引物5′-CACGATGGAGGGGCCGGACTCATC-3′,下游引物5′-TAAGACCTCTATGCCAACACAGT-3′;TLR4:上游引物5′-TCCTCTCCTGCCTGAGACC-3′,下游引物5′-CATGCATTGGTAAGTAGTGTTGGA-3′;TRIF:上游引物5′-TGAGGAGGGTTTCTGGTAGC-3′,下游引物5′-GGATGCCCAGAAGAACTTGT-3′;TRAM:上游引物:5′-CTCGCCTGCTTTTGTGGT-3′,下游引物:5′-TCGTTGGTGTCATCTTCTGC-3′。
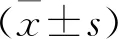
2 结果
2.1 病理组织学观察 空白组大鼠纹状体和皮层有清晰的层。模型组大鼠炎性细胞浸润到病变部位,一些空洞的病变被界定的胶质瘢痕包围,并在大脑同侧(受伤)侧变成囊性。给药组大鼠在同侧(损伤)脑皮质和纹状体未见空洞和排列不规则的细胞,见图1。

图1 三组大鼠病理组织学观察图(HE×400)Figure 1 Histopathological observation of rats in three groups
2.2 Rho激酶抑制剂对大鼠神经功能的影响 模型组、给药组大鼠NSE、GFAP水平高于空白组,BDNF水平低于空白组,具有统计学差异(P<0.05);给药组大鼠NSE、GFAP水平低于模型组,BDNF水平高于模型组,差异有统计学差异(P<0.05),见表1。
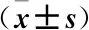
表1 Rho激酶抑制剂对大鼠神经功能的影响Table 1 Effects of Rho kinase inhibitor on nerve function in rats
2.3 Rho激酶抑制剂对大鼠抗炎作用的影响 模型组、给药组大鼠TNF-α、ICAM-1、IL-1β水平高于空白组,差异有统计学差异(P<0.05);给药组大鼠TNF-α、ICAM-1、IL-1β水平低于模型组,差异有统计学差异(P<0.05),见表2。
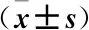
表2 Rho激酶抑制剂对大鼠抗炎作用的影响Table 2 Effects of Rho kinase inhibitor on anti-inflammatory effect in rats
2.4 Rho激酶抑制剂对大鼠脑组织中TLR4/TRIF通路蛋白的影响 模型组、给药组大鼠脑组织中TLR4、TRIF、TRAM蛋白表达量高于空白组,差异有统计学差异(P<0.05);给药组大鼠脑组织中TLR4、TRIF、TRAM蛋白表达量低于模型组,差异有统计学差异(P<0.05),见表3。
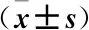
表3 Rho激酶抑制剂对大鼠脑组织中TLR4/TRIF通路蛋白的影响Table 3 Effect of Rho kinase inhibitor on TLR4 / TRIF pathway protein in rat brain
3 讨论
脑梗死属于神经系统疾病之一,大多数都是由于脑部血液供应障碍造成的。脑组织中出现了缺血缺氧坏死和神经功能缺损,会引起一系列临床症状和体征,比如偏瘫、肢体麻木和失语等[5-6]。随着生活水平的提升,脑梗死发病率逐年升高,严重影响了人们的生活质量和身心健康。受影响的大脑部位决定脑梗死的症状,当梗死位于原发性运动皮层时会引起对侧偏瘫[7-8],还会引起身体对侧虚弱和失去知觉,头部体检表现为对侧眼球运动不足和瞳孔扩张异常等现象。
Rho激酶抑制剂对脑血管痉挛选择性扩张,可以增加脑血流量、降低血管阻力和改善脑灌注,还能通过增加肌球蛋白轻链磷酸酶的活性促使血管平滑肌舒张,改善脑组织的供血和供养。Rho激酶抑制剂可抑制炎性细胞、脑神经元细胞凋亡和炎性因子分泌及释放,减少脑组织出现炎症反应和组织损伤[9-10];可促进Ca2+浓度的恢复,保证脑组织中线粒体功能正常,促进乳酸氧化,从而保护脑组织;可促进还原型烟酰胺腺嘌呤二核苷酸形成,对细胞骨架蛋白的消失具有抑制作用;可抑制血浆中ET-1的表达,增加脑循环血量,促进脑组织恢复[11-12]。本研究结果显示,与模型组和空白组大鼠相比,Rho激酶抑制剂可显著改善脑梗死大鼠神经功能,清除机体炎症反应。
BDNF主要分布于大脑的所有皮层区以及部分皮层下和脊髓区,是中枢神经系统中的神经生长因子,与神经细胞死亡、神经元修复相关[13]。NSE存在于神经元细胞浆内,是一种特殊蛋白酶,由神经细胞分泌形成的,可作为鉴别诊断脑梗死的主要指标[14]。中枢神经系统重要的组成成分是星形胶质细胞,星形胶质细胞骨架组成重要成分是GFAP,其水平高低与神经系统损伤程度相关[15]。TNF-α、ICAM-1、IL-1β等因子与大脑缺血有关,可以作用于血脑屏障破坏、髓鞘脱失、胶质细胞凋亡和白细胞浸润[16]。大脑在接受缺血性损伤刺激时会产炎性因子,它会诱导脑微血管内皮细胞表达多种粘附分子,比如单核细胞黏附蛋白、血管细胞黏附分子和细胞间黏附分子等[17]。临床研究显示[18-19],TLR4/TRIF信号通路与多种脑血管疾病相关,其中TLR4组织分布十分广泛,在许多组织细胞中进行表达,在脑组织中主要表达于小胶质细胞,主要分布在大脑血管内皮细胞、侧脑室和软脑膜。在中枢系统坏死凋亡的细胞会释放出HSP60,TLR4的神经毒性化合物会诱导小胶质细胞合成。TLR4还可以识别表面活性剂A、纤维蛋白原肽、硫酸肝素片段、透明质烷低聚糖和防御素[20]。TRIF是TLR下游信号通路中的重要因子,可以抵抗炎症和抑制细胞的凋亡,为机体提供内源性的保护作用。TRIF途径主要通过接受内毒素等刺激因子的刺激激活IRF-3,其信号转导通路为:TLR4→TRIF相关的接头分子→TRIF→TRAF结合蛋白-1→IRF-3,之后经过作用于神经递质,最终导致神经病变[21]。本研究结果显示,Rho激酶抑制剂经作用于TLR4/TRIF信号通路,抑制脑梗死患者炎症反应,改善神经递质表达,最终起到改善脑梗死症状的目的。
4 结论
Rho激酶抑制剂可显著改善脑梗死大鼠神经功能和抑制炎症反应,其机制可能与TLR4/TRIF信号通路相关。
