采用[bmi m]Zn 2Cl 5/NH 3和NaSCN/NH 3为工质的两级复叠吸收式制冷稳态特性
2021-06-09李邹路马连湘
白 杨,李邹路,陈 伟,张 斌,马连湘
(青岛科技大学 机电工程学院,山东 青岛266061)
吸收式制冷是一种由中低品味热源来驱动的制冷技术,可以高效利用工业余热[1]、太阳能[2]、生物质能[3]和地热能[4]等可再生能源。氨具有较大的汽化潜热,较高的临界温度和较低的蒸发温度,这使其适合作为吸收式制冷系统中的制冷剂。
由于H2O和NH3的沸点之差很小,精馏器是H2O/NH3系统中必不可少的组成部分,精馏器中的液氨回流会导致性能系数(COP)下降[5]。为了克服这一缺陷,新型氨吸收式工质的筛选受到广泛关注。最受瞩目的是以无机盐[6]和离子液体[7]作为吸收剂的氨吸收式工质。
科研工作者首次提出将NaSCN/NH3和Li NO3/NH3作为吸收式制冷系统的工质对[8-9],并对Na-SCN/NH[10-12]3和Li NO3/NH3[13-15]的密度、黏度、热容量和气液平衡(VLE)做了详细的研究。SUN等和ZHU等[16-18]对NaSCN/NH3和Li NO3/NH3作为工质对的吸收式制冷系统的热力学性能进行了数值研究,并将其与H2O/NH3系统进行了比较。结果表明,NaSCN/NH3吸收式制冷的热力学性能显著。
2005年,AKI MICHI和MARK[19-20]提出将IL/NH3作为新型制冷工质对用于吸收制冷。YOKOZEKI等[19]测量了NH3在4种咪唑基离子液体中的溶解度。LI等[21]研究了[Cnmi m][BF4]/NH3(n=2、4、6、8)溶液的饱和蒸气压。PALOMAR等[22]使用了[Et OHmi m][BF4]和[choline]·[NTf2]的2种特殊的离子液体作为NH3的吸收剂。然而上述IL/NH3吸收式制冷系统的COP均低于H2O/NH3,主要原因是NH3在离子液体中的溶解度较小。WEI等[23]合成了一种具有金属离子的新型离子液体[b mi m]Zn2Cl5,由于Zn2+和NH3的络合反应,使NH3的溶解度大大提高。相关文献[24-25]报道了[bmi m]Zn2Cl5/NH3溶液的气液平衡特性和吸收系统的理论循环性能,证明了该工质的应用潜质。
在两级吸收式制冷(TAR)系统中,高温循环的制冷剂蒸汽在低温吸收器中被冷却吸收,而低温循环的制冷剂由高温热源发生。如果可以适当地提高高温循环的吸收温度,则可以将来自高温循环吸收器的热流量作为低温循环的热源。在此基础上,提出了一种以[b mi m]Zn2Cl5/NH3和NaSCN/NH3为工质对的新型两级复式吸收式制冷系统(TCAR)。基于各部件质量守恒,能量守恒和方程,建立了TCAR系统的稳定数学模型。运用MATLAB在可变工况条件下进行数值模拟,详细计算和分析TCAR系统的热力性能和各部件的损失。
1 [b mi m]Zn 2 Cl 5/NH 3和NaSCN/NH 3的热力学性质
[b mi m]Zn2Cl5/NH3和NaSCN/NH3的气液平衡是TCAR系统最重要的特性。[b mi m]Zn2Cl5/NH3的饱和蒸气压根据UNIFAC模型计算[24]。NaSCN/NH3的饱和蒸气压根据文献[12]中的多项式模型计算。纯NH3的饱和蒸气压根据Antoine公式计算得出[26]。
[b mi m]Zn2Cl5/NH3和NaSCN/NH3的比焓和比熵是TCAR系统数值模拟必不可少的特性。[b mi m]Zn2Cl5/NH3溶液比焓的计算公式[25]:
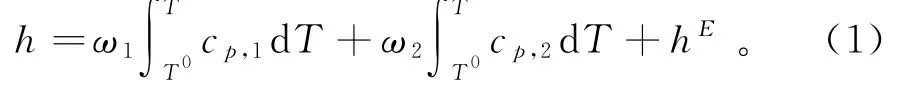
[b mi m]Zn2Cl5/NH3比熵的计算公式:
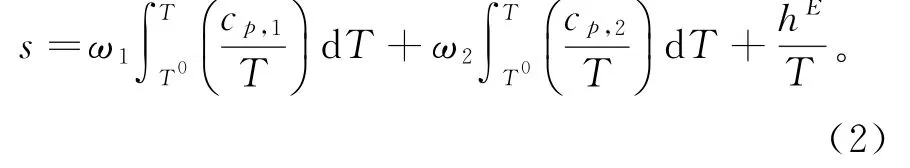
其中:T0是计算比焓和比熵的参考温度;ω代表质量分数;c p表示比热容;下标1和2分别代表NH3和[b mi m]Zn2Cl5的组分;hE表示[b mi m]Zn2Cl5/NH3的过量焓,可以通过UNIFAC模型预测[25]。
NaSCN/NH3溶液比焓的计算公式[17]:
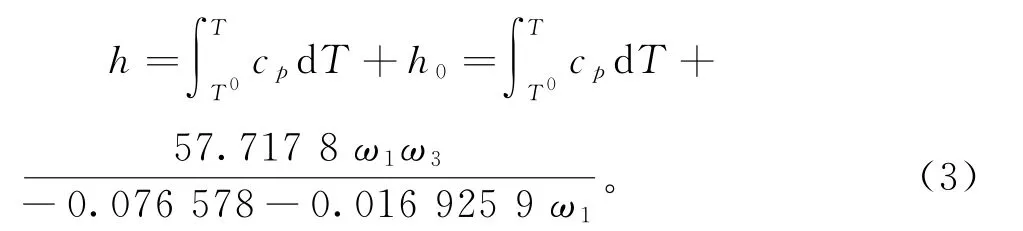
NaSCN/NH3比熵的计算公式:
其中,c p是NaSCN/NH3溶液的比热容,可以通过文献[12]中的多项式方程计算。对于[b mi m]Zn2Cl5/NH3和NaSCN/NH3系统,参考温度设置为273.15 K。
2 TCAR系统循环
图1是TCAR系统的原理图。TCAR系统主要包括以下部件:发生器(GEN),冷凝器(CD),吸收发生器(CAG),蒸发冷凝器(CEC),蒸发吸收器(CEA),蒸发器(EV),2个溶液热交换器(HX1和HX2),2个溶液泵(SP1和SP2)和4个节流阀(V1,V2,V3和V4)。高温循环的工质对为[b mi m]Zn2Cl5/NH3,低温循环的工质对为NaSCN/NH3。
图2显示的是TCAR系统的p-T-x图。图中实线和点线分别代表[b mi m]Zn2Cl5/NH3和Na-SCN/NH3溶液的气液平衡特性。方形点和圆形点分别代表高温循环和低温循环的状态点。图2中状态点的标记数字与图1一致。由于Zn2+与NH3强烈的化学作用,[b mi m]Zn2Cl5在较高温度下仍然对NH3有很强的吸收作用,因此可以将吸收温度提高到相对较高的水平(343.15 K左右)。同时由于低温循环的吸收温度低于273.15 K,因此,低温级的发生温度和吸收温度将达到353.15 K左右,完全可以构建吸收式制冷循环。图2中T4与T14的温差即为高温循环吸收器释放热量驱动低温循环发生过程的传热温差。故而,高温循环吸收过程的热流量可以用作低温循环的热源。与传统的TAR相比,低温循环的热源是高温循环吸收过程中释放的吸收热,因此TCAR系统应该具有更好的热力循环性能。
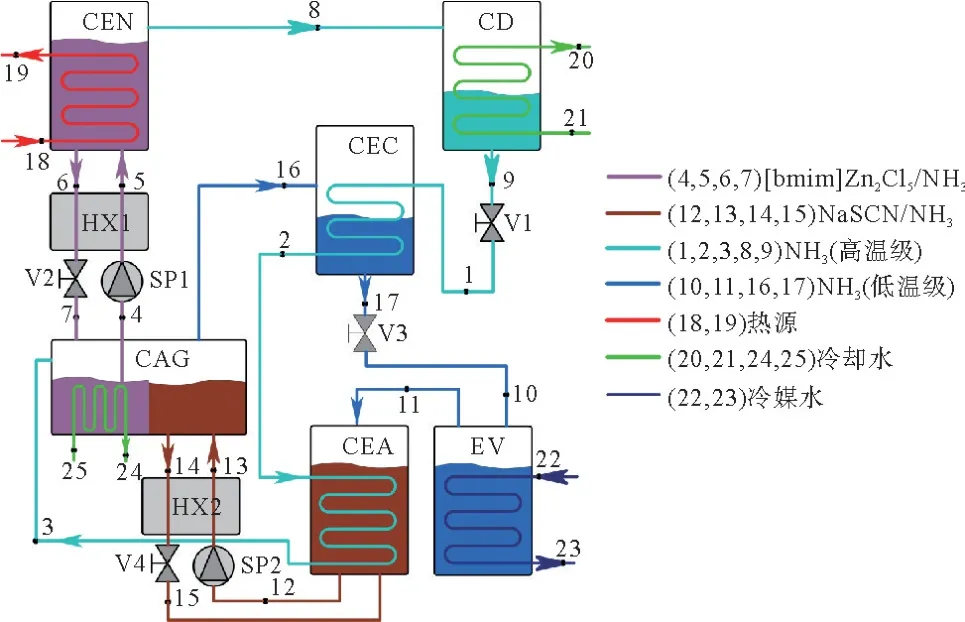
图1 TCAR系统原理图Fig.1 Schematic of the proposed TCAR system
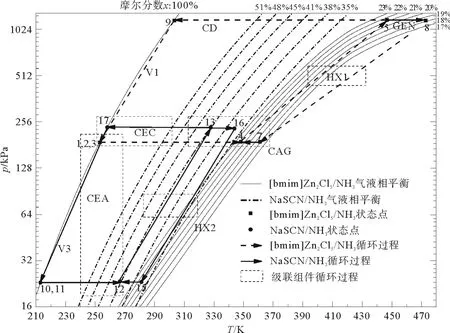
图2 TCAR系统在工况下的p-T-x图Fig.2 p-T-x diagra m of the TCAR syste m under the operating condition
3 建模与仿真
基于系统各部件的质量守恒,能量守恒和熵方程,构造了TCAR系统的稳定数学模型。发生器的液质量守恒、IL质量守恒、能量守恒方程和熵方程:
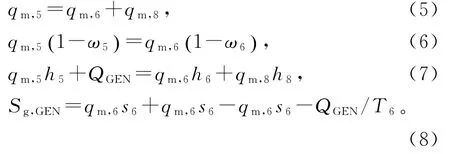
冷凝器的质量守恒、能量守恒方程和熵方程:
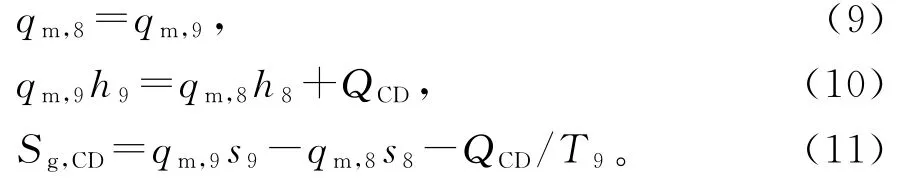
对于吸收发生器,溶液质量守恒、IL质量守恒、能量守恒方程和熵方程:

蒸发冷凝器的质量守恒、能量守恒和熵方程:
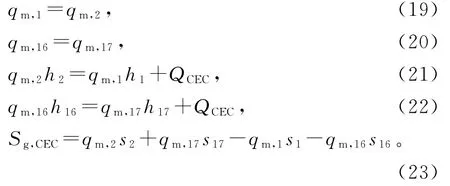
蒸发吸收器的质量守恒、能量守恒和熵方程:
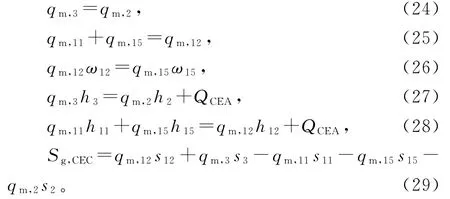
蒸发器的质量守恒、能量守恒和熵方程:
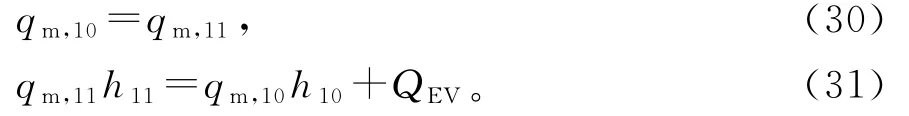
蒸发冷凝器的熵产公式:
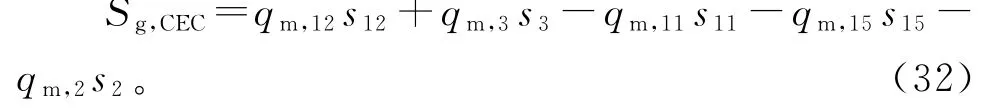
对于HX1和HX2,能量守恒和熵方程如下:
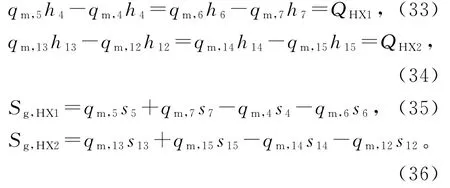
高温循环和低温循环的循环倍率f1和f2分别定义为
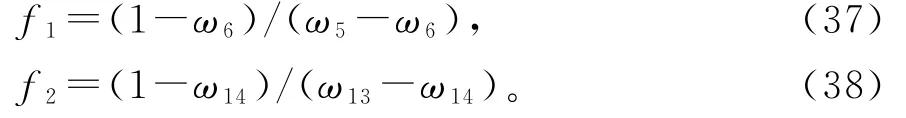
TCAR系统的γCOP(COP)和效率ηex定义为
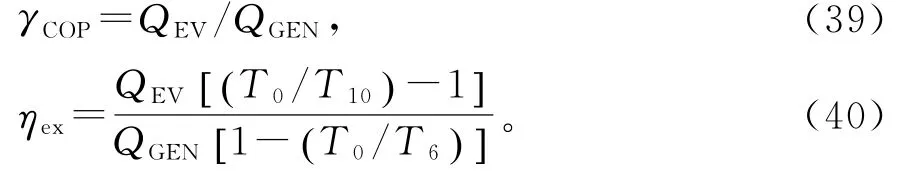
4 结果与讨论
表1给出TCAR系统的基本工况。在TCAR系统中发生器的温度和压力最高,分别为443.15 K和1 166.80 k Pa。高温循环的放气范围为0.218~0.305,低温循环的放气范围为0.380~0.411。可见,在提升了高温循环的吸收温度后,高温循环的放气范围仍然高于低温循环的放气范围,也客观上说明了提升高温循环吸收温度驱动低温循环的可行性,且高温循环的循环流量均高于低温循环。
图3表示了热源温度T18对TCAR系统的工作温度的影响。如图3(a)所示,T6和T9随着T18线性升高。T18的升高导致发生器中热源与溶液之间的温差变大,溶液的热流量随温差增大而增大,最终导致T6的升高。冷凝器中的制冷剂蒸气气压随着T6的升高而增大,从而增大冷凝器的热流量,使得T9升高。如图3(b)所示,T2和T12随着T18的升高而下降。[b mi m]Zn2Cl5/NH3的气液相平衡性质表明ω7随着T6的升高而减小。吸收发生器中[b mi m]Zn2Cl5/NH3溶液的饱和蒸气压随ω7的减小而降低,这使液态NH3在低温下蒸发。因此,T2随着T18的升高而下降,从而导致T12的下降。如图3(c)所示,T6和T9随着T18升高而升高;T11随着T18升高而下降。T18的升高导致qm,3变大,从而导致吸收发生器的总热流量增大。在相同的冷凝水条件下,吸收发生器的热流量增大导致[bmi m]Zn2Cl5/NH3溶液与冷凝水之间的温差增加。因此,T4和T14随着T18升高而升高。
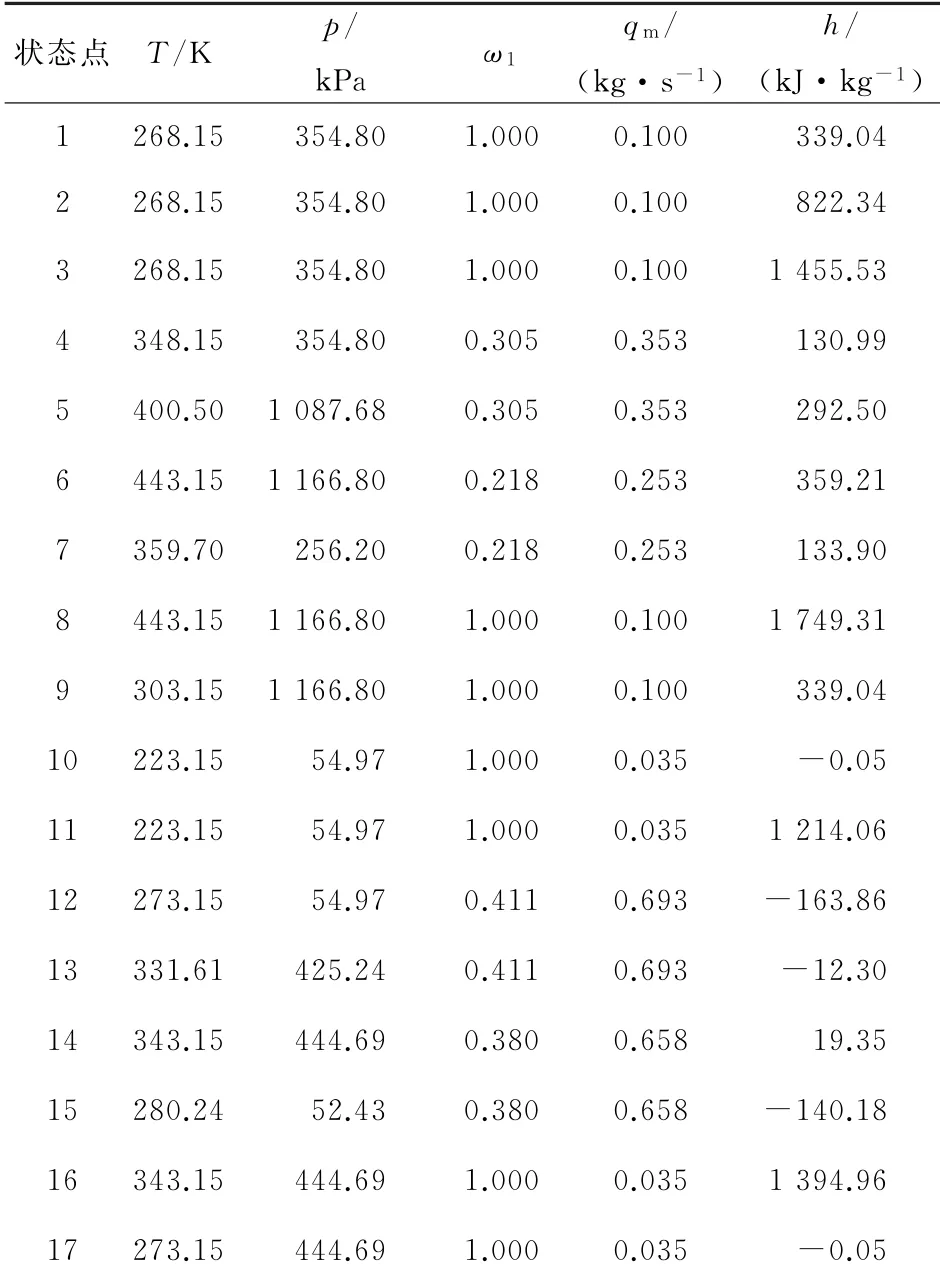
表1 TCAR系统的基本工况Table 1 The basic condition for the TCAR system

图3 T 18对系统工作温度的影响Fig.3 Effect of T 18 on the operating temperatures of the TCAR system
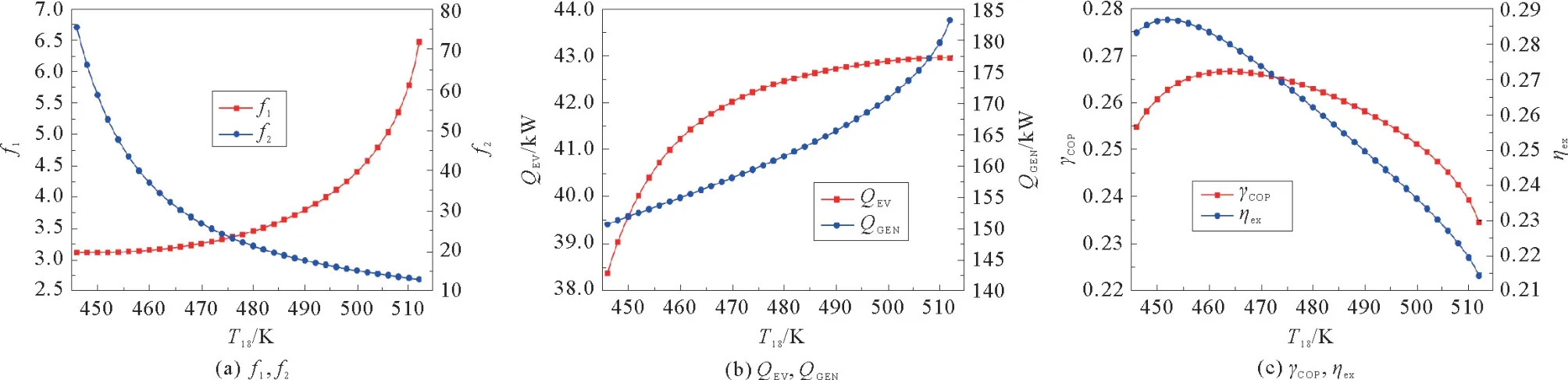
图4 T 18对系统参数的影响Fig.4 Effect of T 18 on para meters of the TCAR syste m
图4表示T18对TCAR系统参数的影响。如图4(a)所示,随着T18的升高,高温循环的循环倍率f1增大,而低温循环的循环倍率f2减小。这是由于对于高温循环,T8和T4随着T18升高而升高,ω6增加、ω4减少,从而使稀溶液和浓溶液之间的浓度差减小,f1随着浓度差的减小而增加。对于低温循环,T2随着T18的升高而下降,这使得T17和T12下降,从而导致ω14减少,ω12增加,增大了稀释溶液与浓缩溶液之间的浓度差,最终导致f2的减小。如图4(b)所示,随着T18的增加,蒸发器和发生器的热流量(QEV,QGEN)增大,同时,当T18温度低时,QEV的增加速度快于QGEN。当T18温度高时,QEV的增加速率变慢。T18的升高使得发生器中热源和溶液之间的温差增大,从而导致QGEN增大。T18的升高还引起T14的升高,T16的下降,使得吸收发生器中NH3蒸气质量流量的增大,最终导致QEV的增加。由于T11随着T18的升高而下降,从而导致ω12的减小,不利于吸收发生器中NH3的气化,因此QEV的增长率呈现出减缓的趋势。图4(c)表明COP和ηex随着T18的升高先增大后减小。当T18分别为464.11和455.89 K时,系统COP和ηex的峰值分别为0.267和0.287。
图5表示了T21对TCAR系统工作温度的影响。如图5(a)所示,随着T21升高,T9升高而T6下降。这是因为,T21的升高导致冷凝器中的液氨和冷凝水之间的温差减小,从而减少了冷凝水带走的热量。因此,T21的升高最终导致T9升高从而使发生器的蒸气压增大,这不利于发生器中NH3的气化。为了获得相同的制冷量,扩大了发生器中溶液的质量流量,最终导致[b mi m]Zn2Cl5/NH3溶液与热源之间的温差增大。在T18温度恒定时,T6随着T21升高而升高。如图5(b)所示,T2、T12随着T21的升高而升高。T12的升高导致h9增大从而使蒸发冷凝器和蒸发吸收器中液氨的冷却能力下降,从而导致T2升高。T2对QCEC的影响并不明显,因此,T2和T12之间的温差基本保持不变,T12随T2升高而升高。图5(c)表明T11,T4和T14随着T21的升高而升高。T21的升高导致发生器中溶液的质量流量增加从而使得吸收发生器中吸收热流(QCAG)增大。在相同的冷凝水条件下,T4随着QCAG的增大而升高。
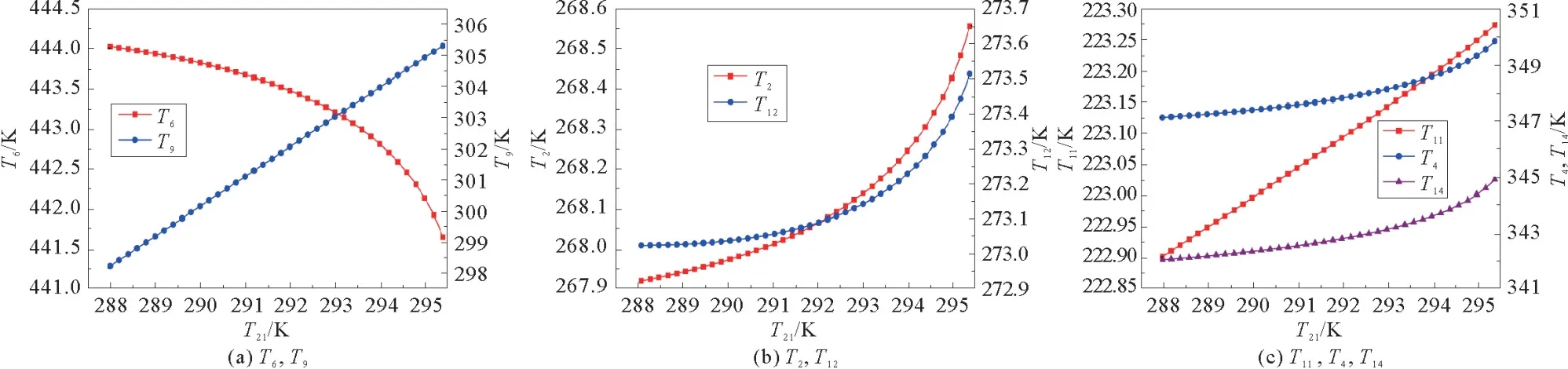
图5 T 21对系统工作温度的影响Fig.5 Effect of T 21 on the operating te mperatures of the TCAR syste m
图6表示T21对系统参数的影响,如图6(a)所示,随着T21的升高,f1增大,f2减小。主要原因是,T21的升高导致T6下降,T9和T2升高。T9升高和T6下降导致ω6增大,T2升高导致ω4减小。ω6增大和ω4减小意味着高温循环的放气范围减小。因此,f1随着T21的升高而增大,这导致T14和T11升高,从而使ω14减小,ω12增大,增大了稀溶液和浓溶液之间的浓度差,导致f2下降。如图6(b)所示,随着T21的升高,QEV减小,QGEN增大。这是因为T12和T16随T21的升高,导致qm,16减少,从而使得QEV减小。T21升高也导致T9升高。T9升高意味着发生器中蒸汽压的升高,这不利于发生器中NH3的气化。为了获得相同制冷量,增加了发生器中溶液的质量流量,最终导致了QGEN的增大。由于T21的升高导致f1的快速增大,因此QGEN的增长速率呈加速趋势。如图6(c)所示,随着T21的升高,COP和ηex呈现下降趋势。原因主要是T21的升高导致QEV的减少和QGEN的增大。随着T21的升高,QGEN的增长速率加快,因此COP和ηex的下降速率也越快。
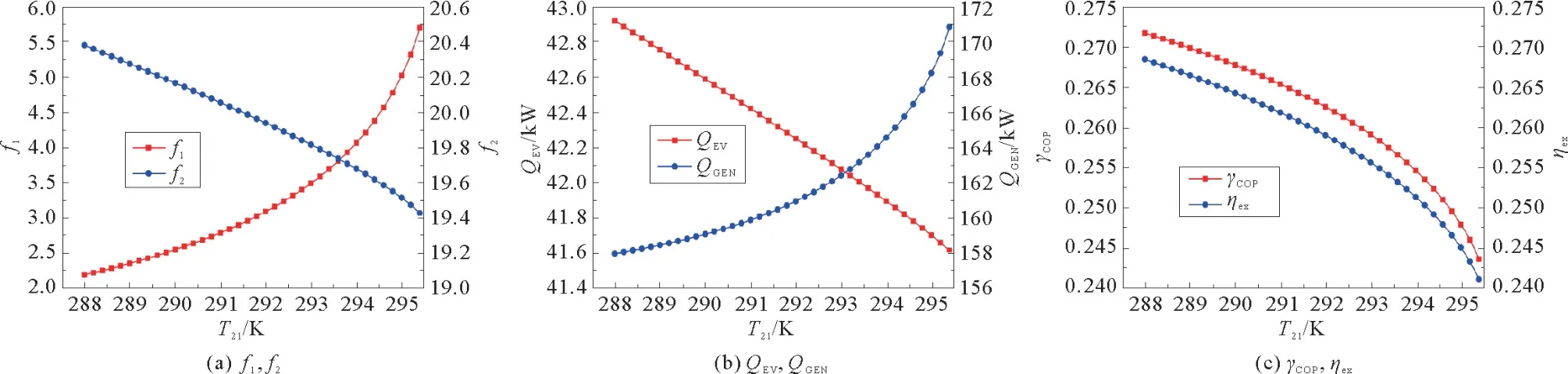
图6 T 18对系统参数的影响Fig.6 Effect of T 18 on parameters of the TCARsystem
图7表示T22对系统工作温度的影响。如图7(a)所示,T11,T4,T14随T22呈线性升高。主要原因是T22升高扩大了液氨和冷凝水之间的温差,从而增大了从冷凝水到液氨的热流量。热流量的增大最终导致T11升高从而引起蒸发吸收器中蒸气压的增加,导致ω12减小,这不利于吸收发生器中NH3的蒸发。因此,ω12的减少导致qm,16的减少,这意味着NH3蒸气从吸收发生器中带走的热流量减少。所以T14随着T22升高。而T14对QCAG的作用不明显,T4和T14之间的温差基本保持不变,因此,T14随T4增加。如图7(b)所示,T2和T12随着T22的升高呈线性递减。这是因为T22升高导致qm,16减小,从而使蒸发冷凝器的热负荷减小,最终导致T2的减少。T22的增加还导致蒸发吸收器的蒸气压增加,不利于吸收过程。因此,蒸发吸收器中蒸气压的增加导致qm,11减小。使得蒸发吸收器的热负荷降低,最终导致T12降低。如图7(c)所示,T6和T9随T22增加呈线性升高。主要原因是T22升高导致T4升高,ω4减小,ω4的减小导致qm,5减小。在热源固定的情况下,qm,5的减小最终导致T6升高。T8与T6温度相等,因此,T22的升高导致T8升高,h8变大。h8的增加导致冷凝器中的热负荷增加,最终导致T9升高。
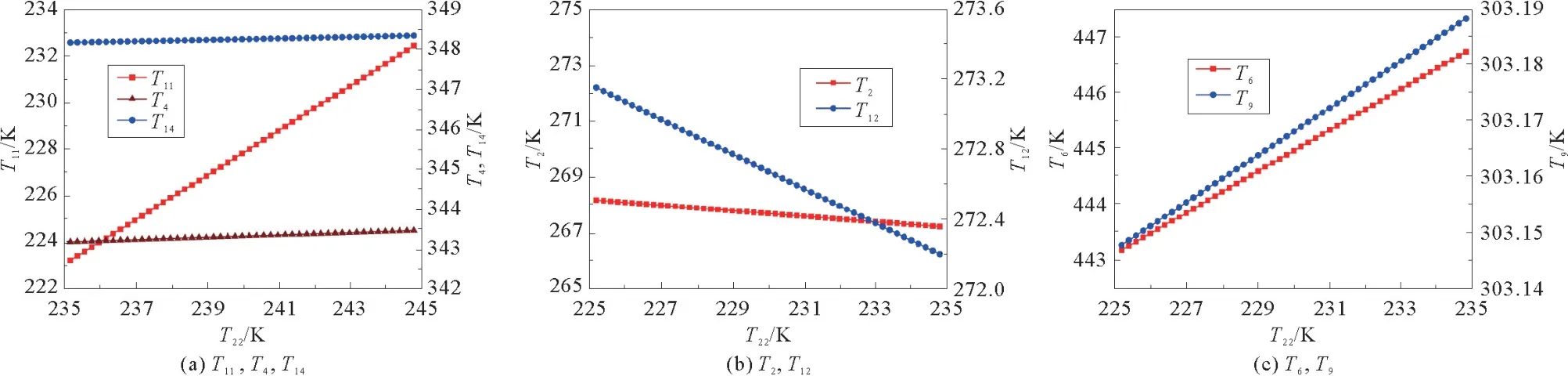
图7 T 22对TCAR系统工作温度的影响Fig.7 Effect of T 22 on the operating te mperatures of the TCAR system
图8表示了T22对系统参数的影响。如图8(a)所示,随着T22的升高,f1增大,f2减小。主要原因是T4和T9随着T22升高而升高。T4和T9升高分别导致ω4的减小和ω6的增大从而减小了浓溶液和稀溶液之间的浓度差,因此,f1随着T22的升高而增加。T22升高还导致T11和T14的升高以及T12的降低。T11的升高和T12的降低导致ω12增大;T14的升高导致ω14的减小,从而扩大了稀溶液和浓溶液的浓度差,因此,f2随着T22的升高而减小。如图8(b)所示,QEV和QGEN随着T22的升高呈线性增加。因为ω4的减小不利于发生器中NH3的气化。为了获得相同数量的NH3蒸气,增加了发生器的热负荷(QGEN)。T22的升高导致蒸发吸收器中蒸气压变大,导致ω12的增大。ω12的增大有助于从吸收发生器中NH3的气化,并导致qm,10增大,最终使QEV变大。如图8(c)所示,COP随T22升高而增大,ηex随T22升高而减小,这也导致了QEV和QGEN的增大。QEV的增长率高于QGEN,因此COP随T22增大,同时使T11和T4升高。T11的升高会降低QEV的比,而T4的升高会增大QGEN的比。QGEN比的增大和QEV的比的减小导致QGEN输入的增长速率快于QEV。因此,ηex随着T22的升高而减小。
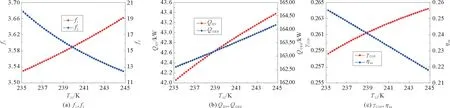
图8 T 22对系统其他参数的影响Fig.8 Effect of T 22 on other para meters of the TCAR syste m
如图9所示,将TCAR系统的热性能与TAR和HACR系统进行了比较[27]。TAR和HACR系统的工质对均为NH3/H2O,蒸发和冷凝温度分别固定为218.15和308.15 K。在低热源温度条件下,TCAR系统具有比TAR系统更高的COP。这一发现表明,本研究所提出的TCAR系统的热性能优于以NH3/H2O作工质对的TAR系统。TCAR系统的COP略低于HACR系统,但TCAR系统的热源温度远低于HACR系统。另外,由于在HACR系统中使用了压缩机和涡轮机,因此TCAR系统的结构比HACR系统更简单。

图9 TCAR与其他系统的热性能比较Fig.9 Co mparison of the ther mal perfor mance of TCAR with other syste ms
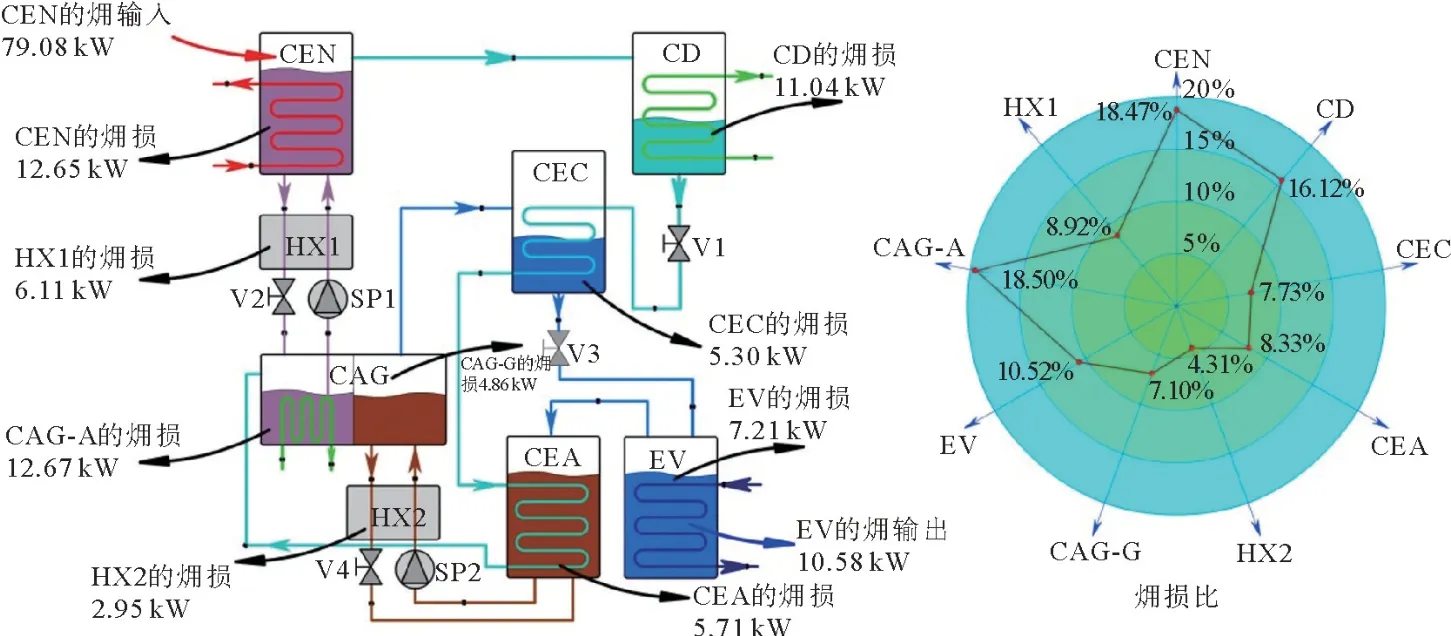
图10 系统的流示意图Fig.10 Schematic of the exergy flow f or the proposed TCAR system
5 结 论
模拟并分析了使用[b mi m]Zn2Cl5/NH3和Na-SCN/NH3为工质对的TCAR系统的热性能和损,还将TCAR系统的热性能与HACR和TAR系统能进行了比较,主要结论如下:
1)随着T18的升高,T6,T9,T4,T14,f1,QEV和QGEN呈上升趋势;T2,T12,T11和f2呈下降趋势;COP和ηex先增大后减小。
2)随着T22的升高,T6,T9,T4,T14,T11,f1,QEV,QGEN和COP呈上升趋势;T2,T12,f2和ηex呈下降趋势。
3)TCAR系统的COP高于TAR系统,略低于HACR系统。但TCAR系统有更低的热源温度和更简单的系统结构。
