心肌T1、T2 mapping技术和细胞外容积分数对急性心肌梗死的诊断价值
2021-06-05赵细辉刘新峰马海彦刘远成王荣品
赵细辉 刘新峰 马海彦 刘远成 王荣品
1贵州省人民医院放射科(贵阳550002);2贵州省智能医学影像分析与精准诊断重点实验室(贵阳550002)
缺血性心肌病的发病率和病死率逐年递增,严重危害我国人民健康。通过心脏磁共振(cardi⁃ac magnetic resonance,CRM)的多种序列尤其是T2⁃加权(T2WI)成像及晚期增强(late gadolinium enhancement,LGE)检测可以检测心肌梗死情况[1]。磁共振延迟增强成像是目前最常用的、成熟的影像技术,LGE 能反映心脏形态改变、局部运动情况和心脏功能参数的信息,并能对心肌疾病进行定性诊断,但目前尚不能定量评估急性心肌梗死的程度。T1 mapping 和T2 mapping 序列等CMR的新技术,有助于对早期定量地评价心肌缺血、水肿及纤维化等心肌疾病,有效、全面地评估心肌损伤区域的心肌活性,为临床提供诊断依据,可作为常规LGE 检查的重要补充[2]。细胞外容积分数(extracellularvolume fraction,ECV)是评估心肌纤维化最有效的指标,与病理学结果有较高的一致性[3]。近年来鲜有对探讨T1、T2 mapping 技术对急性心肌梗死的诊断价值差异的相关研究报道,因此本文通过直接测量T1、T2 值,计算ECV 值,以LGE 为金标准,定量评估急性心肌梗死的范围以及梗死后心肌重塑情况,分析对比T1 mapping 和T2 mapping 及ECV 对急性心肌梗死的诊断价值。
1 资料与方法
1.1 一般资料收集本院2018年1月至2020年2月临床诊断为急性心肌梗死的患者共24例,男12例,女12 例,年龄15 ~80 岁,平均(57.8±12.8)岁。纳入标准:符合2012年美国心脏病学会基金会/美国心脏协会(ACCF/AHA)《不稳定心绞痛⁃非ST 段抬高心肌梗死患者管理指南》[4]及我国2015年《急性ST 段抬高型心肌梗死诊断和治疗指南》[5]的诊断标准。本院伦理委员会批准后,所有受检者均知情同意。实验前1 d 所有患者均进行实验室检查,记录其血细胞比容。
1.2 设备与方法采用西门子1.5TAera 磁共振扫描仪,18 通道体线圈,扫描各序列均使用心电门控,在检查前对患者进行呼吸训练。采行两腔心、四腔心和一系列短轴位电影完成心脏形态学检查。短轴层面均为6 层;采用改良Look⁃Locker MOLLI 序 列(Modified Look⁃Locker inversion recov⁃ery,MOLLI)[6]进行心脏T1 mapping 的测量,扫描参数:TR 324.96 ms,TE1.12 ms,FOV360 mm×306 mm,矩阵2.1 mm × 1.4 mm × 10.0 mm,层厚8 mm,翻转角35°,加速因子2;注入对比剂(Gd⁃DTPA,剂量为0.2 mmol/kg,流量以1~1.5 mL/s 采用双ms)。心脏延迟成像参数:TR 395.96 ms,TE 1.12 ms;FOV 350 mm2,矩阵2.1 mm×1.4 mm×5.0 mm,层厚8 mm,翻转角35°,加速因子2。T2 mapping 序列扫描采用多回波的快速自旋回波(multi⁃echo fast spin⁃echo,MEFSE)序列,参数如下:TR 239.69 ms,TE 1.12 ms,矩阵1.9 mm × 1.9 mm × 8.0 mm,层厚8.0 mm,翻转角12°,FOV 360 mm×288 mm,层间距1.6 mm。
1.3 图像分析将扫描图像输入到syng MR D13后处理工作站,采用双盲法,由2 名高年资主治医师在SIEMENS Argus 分析软件上进行图像分析和测量,取两者平均值。扫描左心室心底段、心中段、心尖段短轴位各1 层,手动勾画,不包含心腔和心外膜外脂肪组织[7],采用后处理软件,在T1 、T2 mapping 伪彩图上相同位置上手动画取延迟强化节段兴趣区上进行数据测量(图1),感兴趣区范围约50 mm2,测量各兴趣区初始T1 值和强化后T1值、T2 值,每人测量3 次取平均值。根据ECV 值计算公式计算ECV 值:ECV=(1⁃血细胞比容)(心肌强化后T1 值⁃心肌初始T1 值)/(血池强化后T1 值⁃血池初始T1 值)。以LGE 远隔未强化区域为对照组,同样方法测量各节段初始T1 值和强化后T1值、T2 值,并计算ECV 值。
1.4 统计学方法采用SPSS 21.0 统计分析软件。计量资料表示为均数±标准差。同一患者,在急性心肌梗死区域与远隔未强化区域分别测得并计算初始T1 值、强化后T1 值、T2 值和ECV 值,分别行两独立样本t检验。以LGE 为参照,采用ROC 曲线分析初始T1 值、强化后T1 值、T2 值及ECV 值评价急性心肌梗死的差异,计算曲线下面积(area under the curve,AUC),计算其诊断心肌梗死的灵敏度、特异度、准确度。P<0.05 为差异有统计学意义。
2 结果
2.1 图像获取所有符合纳入标准的受试对象均完成检查并获得较为满意的图像。24 例患者,LGE 检查共获得144 层短轴位图像,排除12 个层面受伪影干扰,30 个层面无LGE 阳性区域,不能进行测量,共获得可测量分析的LGE 阳性显示心肌梗死层面和对应的T1、T2 mapping 短轴图像各102层,测得延迟强化区域和远隔未强化区域ROI 各102 个。
2.2 急性心肌梗死区域测量数值比较急性心肌梗死区域初始T1值(1 320.0±28.4)ms大于远隔未强化区域初始T1值(1 196.8±27.0)ms(P<0.001),急性心肌梗死区域T1 值下降较远隔未强化区域更明显,两者ECV 分别为(38.7 ± 2.1)%、(24.8 ±2.5)%(P<0.001);急性心肌梗死区域T2 值为(93.3 ± 6.6)ms 大于远隔未强化区域T2 值(80.7 ±6.7)ms(P<0.001)。见表1。
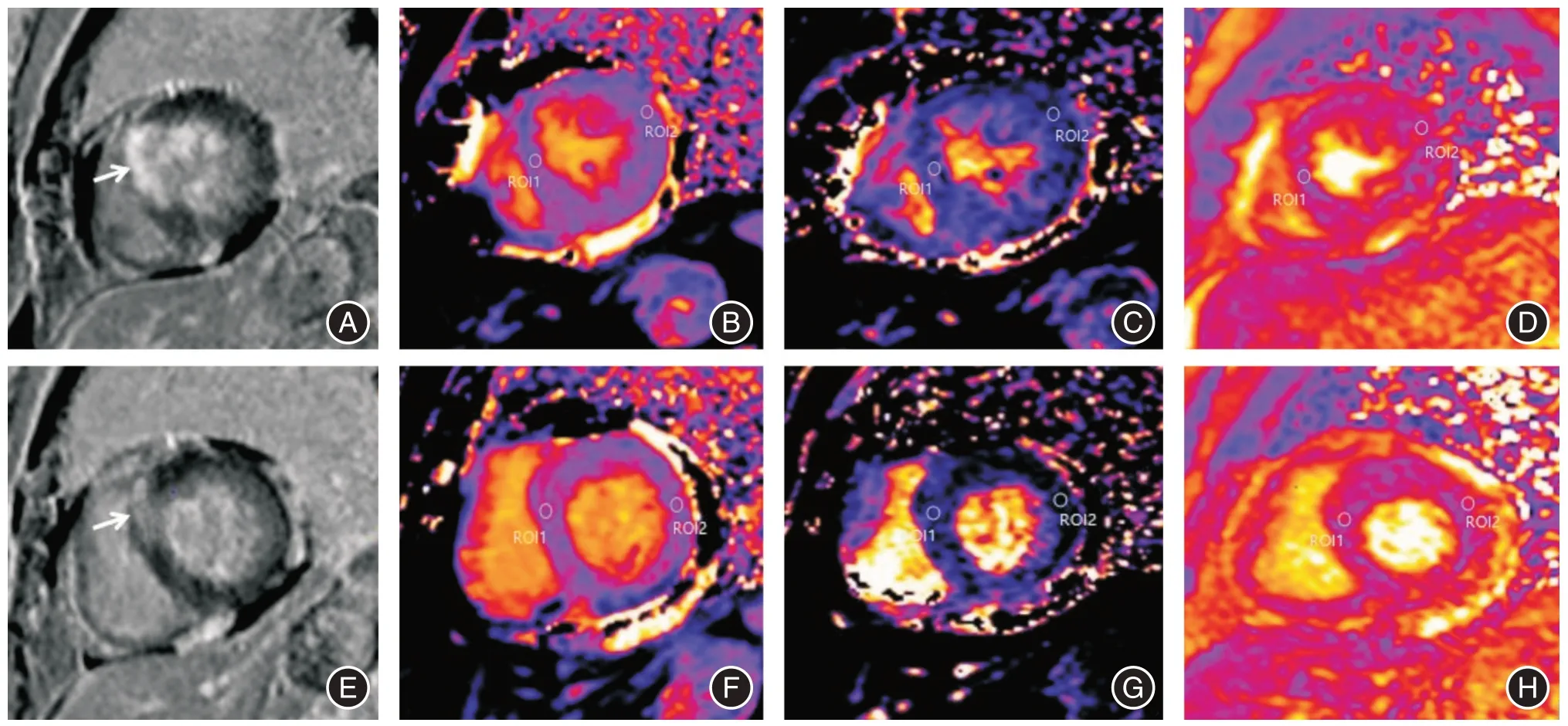
图1 CMR 图像Fig.1 CMR Images
表1 急性心肌梗死区域与远隔未强化区域增强前、后T1 值、ECV 及T2 值比较Tab.1 Comparison of T1 values,ECV and T2 value before and after enhancement in acute myocardial infarction area and remote unenhanced area±s
项目 初始T1 值(ms) 强化后T1 值(ms)ECV(%)T2(ms)急性心肌梗死区域1 320.0±28.4443.4±17.338.7±2.193.3±6.6远隔未强化区域t 值P 值1 196.8±27.0 11.06<0.001 502.9±14.1 27.35<0.001 24.8±2.5 5.33<0.001 80.7±6.7 17.87<0.001
2.3 ROC 曲线以LGE 结果为参照,得到心肌梗死区域初始T1 值、强化后T1 值、ECV 值和T2 值的ROC 曲线下面积(AUC)分别为0.812、0.840、0.875、0.819,均具备较好的灵敏度、特异度和准确度。从ROC 曲线图中可看出,各参数中ECV 值对于急性心肌梗死在的诊断效能最高。见表2、图2。
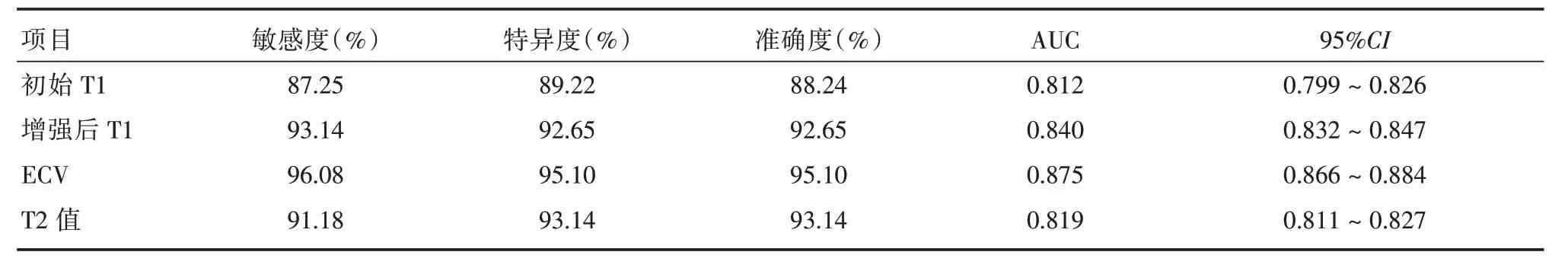
表2 初始T1 值、增强后T1 值、ECV 和T2 值诊断心肌梗死的效能Tab.2 The value of native T1,post⁃contrast T1,ECV and T2 in the diagnosis of myocardial infarction
3 讨论
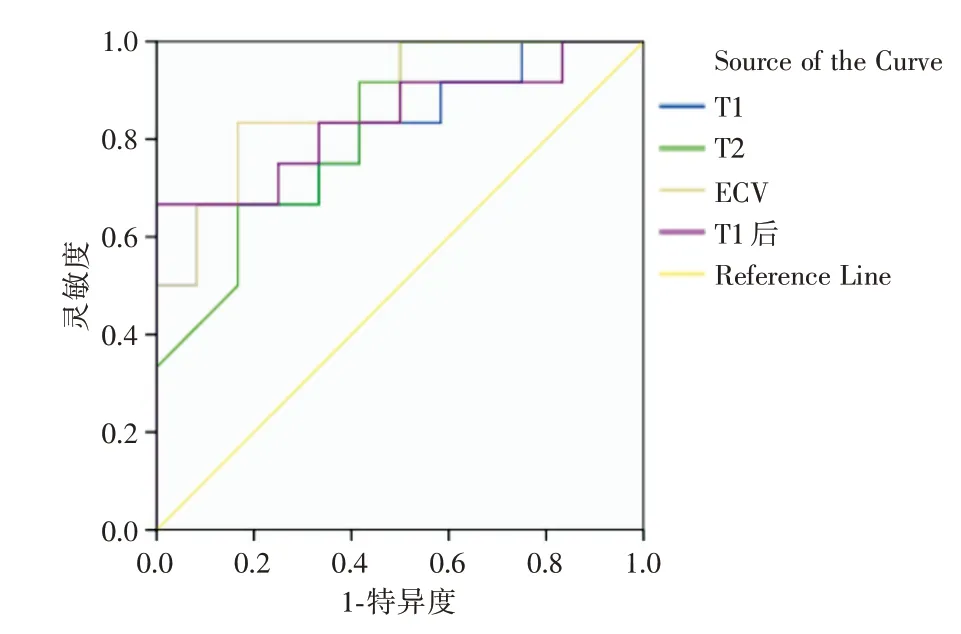
图2 常规LGE 与初始T1 值、增强后T1 值、ECV 值和T2 值评价心肌梗死的ROC 曲线图Fig.2 The ROC curves of routine LGE and initial T1,enhanced T1,ECV and T2 in evaluation of myocardial infarction
3.1 T1 mapping与ECV技术联合应用的优势本实验采用改良的Look⁃Locker 反转恢复技术(modi⁃fied look⁃locker inversion recovery,MOLLI),配合呼吸门控,只需较短的屏气采集时间,可容纳较广的心率范围,显著减小了呼吸及心脏搏动伪影的影响,缩短采集时间,重复性更高[8]。T1 值的变化受心肌细胞的组织学特性影响,在急性心肌梗死后,心肌细胞膜破坏,造影剂向细胞内流入,心肌间质水肿,会引起初始T1 值和ECV 值的增加,强化后T1 值降低。T1 mapping 序列能定量每个心肌体素的T1 值,在伪彩图上可直观显示T1 值差异,识别出病变心肌,无论是对局限性还是弥漫性心肌疾病,均有重要的临床诊断价值。ECV 反映的是增强后对比剂在心肌间质内的容积分布,是评估心肌纤维化程度最有效的指标,ECV 的升高代表心肌细胞间的自由空间增大[9]。因此,能够引起细胞外间隙增大的任何病灶(如心肌水肿、弥散性纤维化、瘢痕、淀粉样变性等)均可导致ECV 值的增大,与组织病理学结果高度一致[10]。本实验测得的急性心肌梗死区域初始T1 值为(1 320.0±28.4)ms 高于远隔未强化区域(1 196.8 ± 27.0)ms,急性心肌梗死区域增强后T1 值(443.4 ± 17.3)ms 低于远隔未强化区域(502.9 ± 14.1)ms,增强扫描急性心肌梗死区域与远隔未强化区域T1 值明显缩短,且急性心肌梗死区域T1值缩短更明显;急性心肌梗死区域ECV 值(38.7 ± 2.1)%,远隔未强化区域ECV 值(24.8 ± 2.5)%,急性心肌梗死区域的ECV值比远隔未强化区域高,这与在GARG 等[11]对急性心肌梗死的研究中得出的结果一致,梗死区域T1 值减小,且延迟强化区域与T1 值减小的区域较为一致。本实验得出ECV 对诊断急性心肌梗死有较高的敏感度、特异度,诊断效能在各参数中也最高,表明ECV 是急性心肌梗死后评估左室心肌损伤程度和预测功能恢复指标,可以增加LGE 的预测价值。ECV 提供了梗死区心肌损伤严重程度的定量信息,特别是对于跨壁程度较高的梗死,ECV有更全面、更有效的诊断价值。说明其为较为稳定的参数,可应用于临床诊断急性心肌梗死。
3.2 T2 mapping 的技术优势及临床应用急性心肌梗死或梗死后缺血心肌的再灌注,Na+/K+泵平衡被打破,水分子内流,引起细胞内水分的增加,导致心肌T2 时间的延长,因此T2 值高信号能反映组织中水含量,识别心肌水肿,更加有利于识别缺血心肌。T2 mapping 技术可定量测定T2 值,评估水肿程度,不易受到局部慢速血流引起的高信号伪影、呼吸伪影及心搏伪影影响,诊断更加准确[12]。与常规T2WI 序列比较,T2 mapping 对T2值的细微变化特别敏感,可以更稳健、精确和可重复地估计与梗死相关的水肿[13]。在本研究中,急性心肌梗死区域的T2 值明显超过远隔未强化区域,对水肿的显示具有很高的灵敏度和特异度,与FERNÁNDEZ⁃JIMÉNEZ 等[14]有研究结果一致。在急性缺血性心肌损伤的CMR 检测中,缺血区域心肌T2 值增高可发生于LGE 出现高信号及实验室检查肌钙蛋白升高前,证明T2 mapping 技术有助于临床在急性心肌梗死早期不可逆损伤发生前做出诊断和干预[15]。MARKOUSIS⁃MAVROGENIS 等[16]报道1 例既往体健的马拉松运动员在比赛中突发心脏骤停,在心肺复苏后行CMR 检查,T2 mapping测得的T2 值明显增加(>60 ms)的区域与可疑责任血管的供血范围一致,这也说明了T2 mapping在心脏复苏后节段性心肌损伤的检测价值,体现了T2 mapping 技术在急性期的关键作用。
3.3 定量T1、T2 mapping 技术联合应用的优势本研究结果表明,T1 mapping 技术利用T1 值和ECV 值的定量变化来评估急性心肌梗死的损伤情况,较LGE 更加灵敏、准确和直观,测得的T1 值的差异反应心肌损伤可能,预计未来能通过T1值的改变对心肌梗死程度进行分级。ECV 通过比值分数有效地校正了各种客观因素(如扫描参数、场强、延迟扫描时间等)的影响,克服了T1 mapping 对弥漫性病变测量时的受制,是更加稳定的指标[17]。T2 mapping 技术通过定量反应心肌梗死后心肌炎性和水肿情况,可以鉴别急慢性心肌梗死,并早期定量评估心肌梗死程度及预后情况。定量的T1、T2 mapping 技术联合应用,可以全面地评价心肌损伤程度和范围。TAHIR 等[18]对首次急性心肌梗死患者8 d、7 周、3、6 个月后行T1 mapping、T2 mapping 及LGE 检查,发现T1、T2 值逐渐下降,T1、T2 值对鉴别急慢性心肌梗死的ROC 曲线下面积为0.975 和0.979,而LGET2 序列凭视觉分析水肿的ROC 曲线下面积为为0.863。TESSA 等[19]对急慢性心肌梗死的患者心肌水肿评估的对比,得出T1、T2 mapping 对评价急慢性心肌梗死的心肌损伤程度有较高的价值。有研究[20]表明将ECV 和T2 mapping 的定量CMR 方法联合应用于心脏移植后的患者中,可以准确地诊断急性排斥反应的情况。相关研究[21]表明,T1和T2 mapping在监测癌症治疗中的心脏是否受累可能非常有价值,主要表现为在癌症治疗暴露的早期,心肌受累炎症水肿,T1 值和T2 值升高;暴露的晚期,心脏间质纤维化改变、心肌细胞重塑,T1 值升高,而T2 值正常。T1、T2 mapping 技术联合应用具有非常高的临床应用价值和可行性,可以用于探讨心肌损伤后组织重构的病理学机制,但若要应用于临床,仍需进行深入的技术改进。展望未来,CMR 影像诊断需联合各新技术,改善单独使用某一种技术的缺点,提高诊断的准确度、特异度和灵敏度。
3.4 本研究的局限性(1)本研究纳入的样本量较少,属于初期的研究,后期需扩大样本量,进一步研究。(2)本研究未对心肌梗死区域进行进一步细化,如梗死核心区、边缘区、周围水肿区。(3)在评估急性心肌梗死时,因心肌出血、水肿、钙盐沉积等改变均可引起T1、T2 值的变化,还需探讨与其他技术结合进行进一步研究,以明确能引起T1、T2 值变化具体的原因。(4)未联合心脏功能参数进行研究,未对预后进行评价。
随着未来研究的深入及CMR 衍生技术的不断改进,对新技术进一步探索研究,有望将T1、T2 mapping 及ECV 技术从科研手段转化为临床常规应用技术,为心肌疾病的诊断、治疗及预后评估提供更多的影像诊断支持。
