检测β⁃CTX和N⁃MID水平的双标记时间分辨免疫荧光分析方法的建立和评价
2021-06-04陈翠翠梁焕坤刘鹏娥钟树海李来庆
毛 骞,陈翠翠,梁焕坤,刘鹏娥,钟树海,李来庆
(1.北华大学附属医院内分泌科,吉林 吉林132001;2.广州优迪生物科技股份有限公司,广东 广州510663)
近年来,骨质疏松症发病率不断升高,严重威胁人们的健康和生命安全[1]。骨质疏松症早期常不能引起人们的注意和重视,就诊时病情严重甚至已发生骨折。目前主要采用双能X线吸收仪(dual energy X-ray absorptiometry,DXA)测定骨密度来诊断骨质疏松症,但存在价格昂贵、操作繁琐和普及率低等不足,在基层难以推广应用[2-3]。因此,早期快速、准确、敏感和定量诊断对预防和监测骨质疏松症具有重要意义。β胶联降解产物又称Ⅰ型胶原羧基端肽β特殊序列(β-cross-linked C-terminal telopeptide of typeⅠcollagen,β-CTX),是骨重建过程中胶原被降解后释放入血的片段,β-CTX水平的升高反映了骨吸收程度、骨质流失增加,以致骨质疏松症和变形性骨病的发生。β-CTX与骨转换或骨矿物质密度(bone mineral density,BMD)等标志物之间存在相关性,是诊断骨转移的潜在标志物[4-5]。骨钙素可直接反映骨形成的状况,但血液标本放在室温下1 h后,骨钙素即会大量降解,其降解产物骨钙素N端中分子片段 (N-terminal middle molecular fragment of osteocalein,N-MID)因其具有良好的稳定性和重复性,可代替骨钙素反映骨形成状态[6]。因此,N-MID常应用于骨质疏松症的临床疗效观察和预后判断[7-8]。本研究在国内首次建立了β-CTX和N-MID水平双标记的时间分辨免疫荧光分析(double-labeled time-resolved immunofluorescence analysis,TRFIA)法,以ELISA检测结果作为金标准进行对比,为快速、精准筛查或监测骨质疏松症提供了新的技术手段。
1 材料与方法
1.1 抗体、试剂和仪器
抗β-CTX和N-MID单克隆抗体(MAb)4E5和2B7(包被抗体)、2G6和5A 3(检测抗体)和β-CTX和N-MID标准抗原均由广州优迪生物科技股份有限公司制备,铕离子(Eu3+)和钐离子(Sm3+)标记试剂盒(美国PerkinElmer公司),牛血清白蛋白(美国Fitzgerald公司),Sephades-G50填料(美国GE公司),96孔培养板(美国Costar公司),包被缓冲液、洗涤液、封闭液和增强液均为自制。Victor 1420全自动时间分辨荧光免疫分析检测仪(美国PerkinElmer公司)。
1.2 固相包被抗体的制备和检测抗体的标记
将构建好的包被抗体采用缓冲液稀释至10 mg·L-1,按每孔100μL加入96孔微孔板中包被,4℃过夜,弃去包被液,加入封闭液,每孔250μL,37℃封闭2 h,弃掉封闭液,洗涤液洗涤2次,真空冷冻抽干,于-20℃保存备用。按照试剂盒说明书,采用Eu3+和Sm3+标记试剂盒进行抗体标记。
1.3 标准品的制备
采用Tris-HCl缓冲液(pH 7.8),将β-CTX抗原配制成浓度为0、0.1、0.2、0.5、1.0、2.5和5.0μg·L-1的系列标准品溶液,将N-MID抗原配制成浓度为0、10、20、80、160和200μg·L-1的系列标准品溶液。
1.4 TRFIA方法检测性能评估
1.4.1 灵敏度和特异度检测 采用“1.3”步骤中制备的β-CTX系列标准品绘制标准曲线,以0μg·L-1β-CTX标准品为样本,将其测定的20次荧光值均值(mean)加上2倍的标准差(2SD)代入标准曲线方程,计算TRFIA方法的灵敏度。采用“1.3”步骤中制备的N-MID系列标准品绘制标准曲线,绘制方法同β-CTX标准品。
特异度检测:同时检测β-CTX标准品、N-MID标准品、Ⅰ型胶原蛋白氨基末端肽(N-terminal peptide of collagen typeⅠ,NTX)、抗酒石酸酸性磷 酸 酶 (tartrate resisitant acid phosphatase,TRACP)、生长激素(growth hormone,GH)、骨特异性碱性磷酸酶(bonespecific alkalinephosphatase,BACP)、骨保护蛋白(osteoprotegerin,OPG)和甲状旁腺素(parathyroid hormone,PTH)水平。
1.4.2 准确度和精密度实验 对浓度已知的3个β-CTX和N-MID标准品分别按1∶2、1∶4和1∶8浓度倍比稀释,每个样本重复检测3次,比较样本的测定值、真值并计算其比值(稀释回收率)。
将β-CTX和N-MID标准品分别稀释至高、中和低3个浓度,每个浓度各设3个复孔,重复检测10次,对测定结果进行分析。
1.4.3 稳定性实验 采用本研究制备的TRFIA试剂盒置于4℃冰箱6个月和37℃、7 d,对试剂盒的物理外观,剂量-反应曲线的线性、灵敏度、准确度和特异度等指标进行测定,具体检测方法同“1.4.1”和“1.4.2”步骤。
1.5 临床样本对比检测
收集2018年3月—2019年3月北华大学附属医院X射线骨密度仪确诊的骨质疏松症患者晨起空腹血清和对应健康成人的晨起空腹血清。骨质疏松症患者分为青少年组(15例)、妊娠期妇女组(22例)、绝经期妇女组(26例)和老年人组(31例),阴性样本为对应年龄段的非骨质疏松的健康者。β-CTX和N-MID分别采用TRFIA法、化学发光法和ELISA法进行比对试验,分析评价其对骨质疏松症的检测效果。
1.6 统计学分析
采用SPSS 17.0统计软件进行统计学分析。平行测定10次0μg·L-1参考标准品的荧光值,计算其标准差,并代入标准曲线计算灵敏度,采用Graph Pad Prism 5统计软件计算标准曲线方程,采用Origin 8软件绘图。
2 结 果
2.1 TRFIA的最佳反应条件
经过优化,最终确定TRFIA最佳的反应条件:β-CTX和N-MID包被抗体的浓度为10 mg·L-1,每孔100μL和8 mg·L-1,每孔100μL;Eu3+标记试剂:标记抗体最佳比例为70μL∶30μL;Sm3+标记试剂:标记抗体最佳比例为75μL∶25μL;反应体系为25μL标准品或待测样品+200μL分析缓冲液+每孔200μL Eu3+(或Sm3+)-检测抗体+每孔200μL增强液。
2.2 灵敏度和特异度实验结果
β-CTX方程:Y=0.998 8X+0.857 6,R2=0.999 4,线性范围 为0.025~5.000μg·L-1;N-MID方程:Y=0.033 0X+0.621 1,R2=0.999 4,线性范围为0.5~200.0μg·L-1。平行测定10次0μg·L-1参考标准品的荧光值,并计算其均值(mean)及标准差(SD),采用mean+2SD代入标准曲线方程,计算出TRFIA法对β-CTX的检测灵敏度为0.025μg·L-1,TRFIA法对N-MID的 检 测 灵 敏 度 为0.5μg·L-1。同 步 检 测NTX、TRACP、GH、BALP、OPG和PTH均为阴性,无明显交叉反应表明该试剂盒特异性良好。绘制的标准曲线见图1。
2.3 准确度和精密度实验结果
β-CTX的3个样品3个水平稀释度的稀释回收率为98.6%~104.6%,N-MID的3个样品3个水平稀释度的稀释回收率为98.9%~105.6%(表1),稀释倍数与浓度呈线性关系。批内变异系数(CV)为5.81%~7.82%,β-CTX批间CV为5.97%~8.02%;N-MID批内CV为6.05%~8.32%,批间CV为6.14%~8.56%(表2)。批内和批间CV均小于10%,符合临床检测试剂盒要求。
2.4 稳定性实验结果
试剂盒置于4℃冰箱能稳定保存6个月以上,37℃热破坏性试验能稳定保存7 d以上,说明该TRFIA方法制备的试剂盒稳定性较好。见表3。
2.5 临床样本的对比检测结果
将制备的双标记检测试剂盒与CLIA和ELISA法同时检测94例骨质疏松症患者和94例非骨质疏松症健康者的血清,TRFIA法与CLIA和ELISA法检测结果一致,3种检测方法的符合率为100%(表4),表明本研究建立的TRFIA方法可快速、准确和定量地检测β-CTX和N-MID临床样本。

图1 TRFIA试剂盒的标准曲线Fig.1 Standard curves of TRFIA Kit
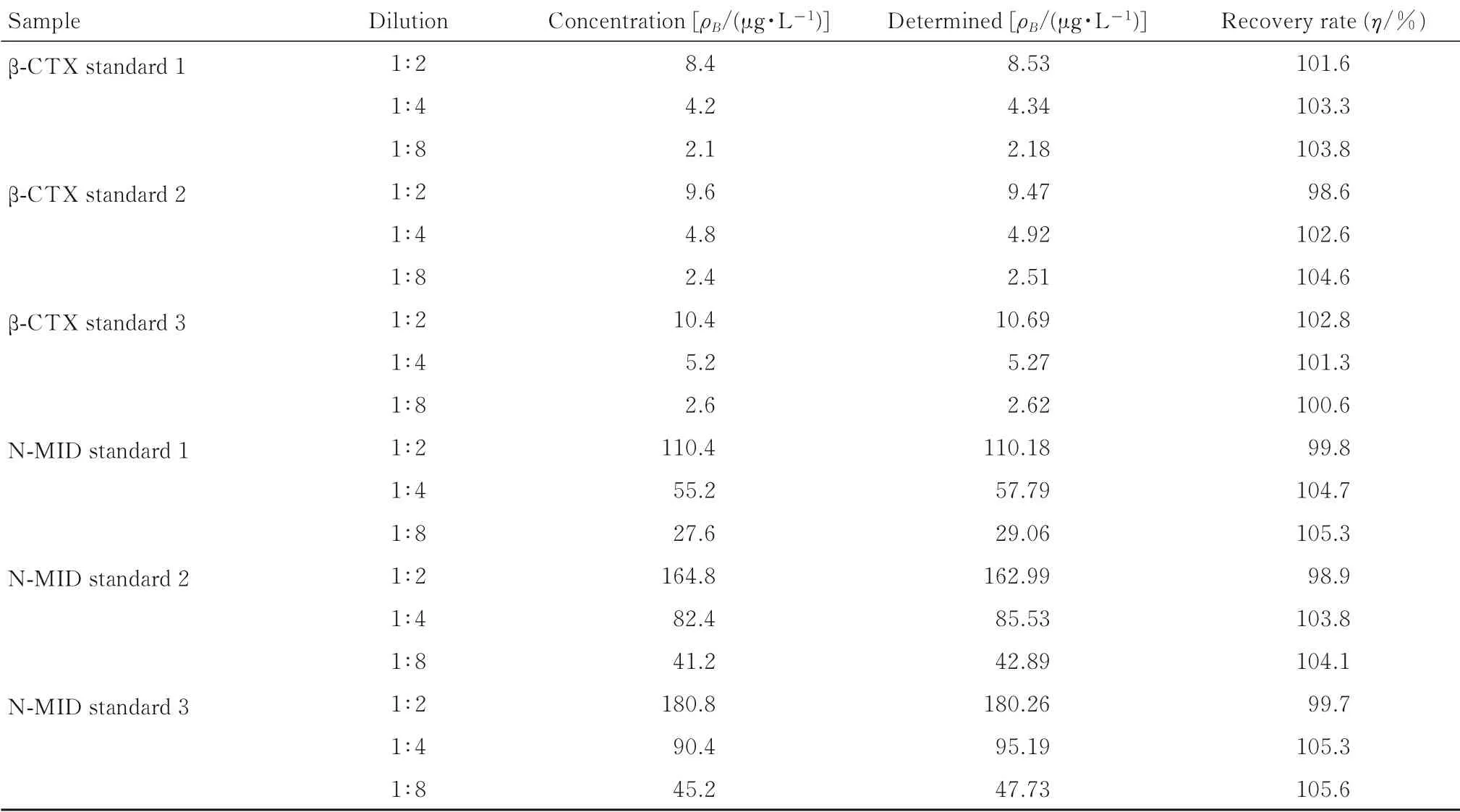
表1 TRFIA试剂盒的稀释回收率Tab.1 Dilution recovery rates of TRFIA Kit
3 讨 论
TRFIA是一种理想的免疫测定方法,已广泛应用于各个领域,如临床研究、分子生物学、药物分析和病毒的检测[9-12]。采用镧系元素螯合物时,由于发射波长和动力学不同,非特异性背景和特异性信号的时间分辨荧光有区别,因而能够采用Eu3+和Sm3+螯合物开发双标签TRFIA,从而可以同时检测2种分子[13-15]。
骨质疏松相关的骨折风险通常通过BMD评估,但是由于骨强度也由其他因素决定,如骨几何形状、微结构和大小,因此BMD本身并不是骨折风险的良好预测指标[16-17]。目前,骨转换的生化标志物正被用于预测骨质流失的速度和评估老年人骨折的风险。可以通过确定代表骨重塑过程的某些蛋白质的血清或尿液浓度来估计骨转换率[18]。这些蛋白质可以分为骨形成标记和骨吸收标记,最具特异性和最敏感的骨形成标记物包括β-CTX和N-MID[19-21]。
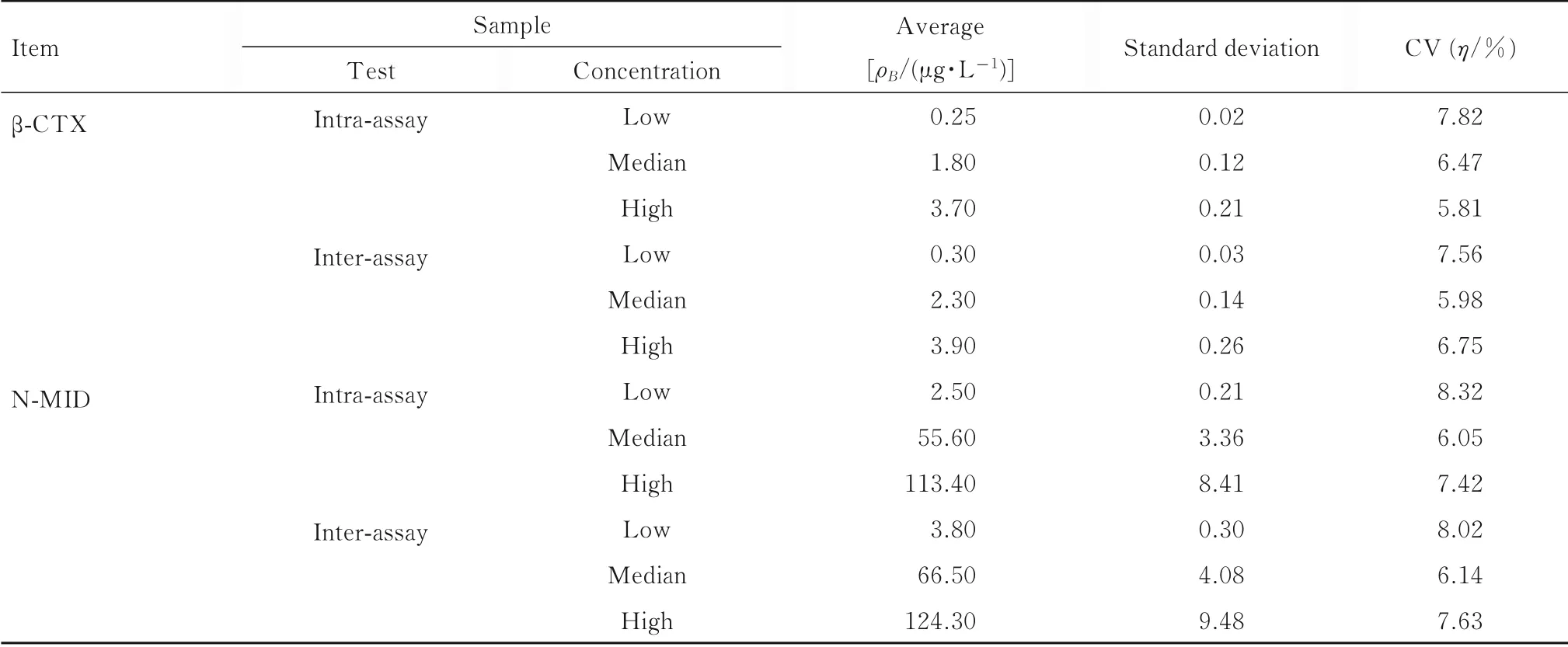
表2 TRFIA试剂盒检测的精密度T ab.2 Precision of T RFIA Kit detection
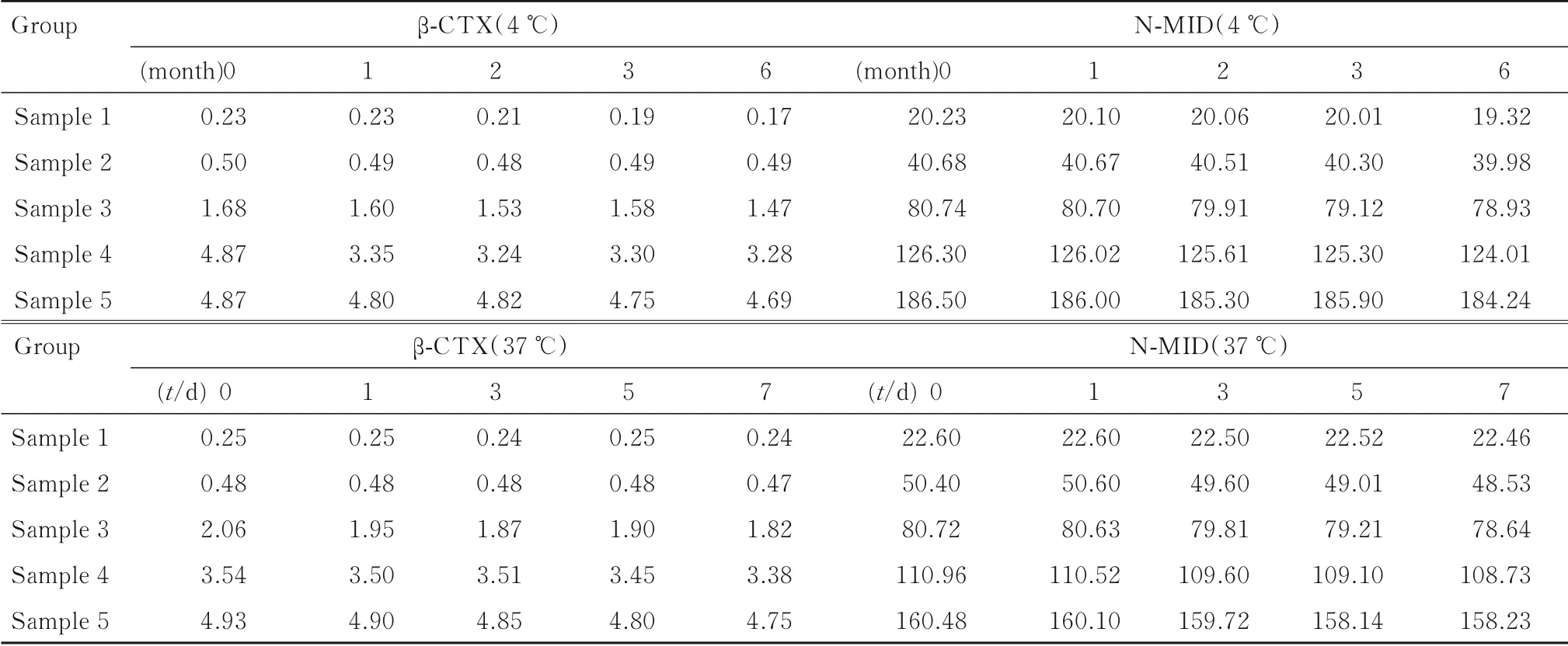
表3 TRFIA试剂盒检测的稳定性Tab.3 Stabilities of TRFIA Kit detection
本研究拟采用Eu3+标记抗β-CTX单克隆抗体和Sm3+标记抗N-MID单克隆抗体,采用双抗体夹心法建立β-CTX/N-MID双标记TRFIA试剂,自行研制能同时检测人血液β-CTX和N-MID的TRFIA试剂盒,本研究所研制的试剂盒检测结果显示:β-CTX的检测灵敏度为0.025μg·L-1、N-MID的检测灵敏度为0.5μg·L-1,定量线性范围β-CTX在0.05~5.00μg·L-1、N-MID的线性范围为0.5~200.0μg·L-1,检测范围宽。β-CTX平均稀释回收率为102.13%,N-MID平均稀释回收率为103.02%,与其他常见骨检测指标无明显交叉反应,特异性较强;β-CTX批内CV为5.81%~7.82%,批间CV为5.97%~8.02%;N-MID批内CV为6.05%~8.32%,批间CV为6.14%~8.56%,达到临床测试要求(批内CV<10%,批间CV<15%)。此外,双标记试剂盒可在4℃稳定保存6个月,37℃稳定保存7 d,这使该双标记TRFIA成为本方法的良好替代品。

表4 TRFIA试剂盒、CLIA和ELISA法对临床样本的对比检测结果Tab.4 Comparison test results of clinical samples detected by TRFIA Kit,CLIA,and ELISA methods
本项目研发的检测试剂盒可同时检测单个样本中的β-CTX和N-MID水平,集中了TRFIA敏感、定量、简便和快速的优势,更适于广泛推广,特别适合于基层无法开展仪器检测的实验室。本试剂盒的应用将有利于推动检测基层和城镇血清样品中β-CTX和N-MID水平的检测,使该检测项目成为一个常规的普查项目或者家庭式的自检项目,从而更有效地预防骨质疏松症的发生发展。
