特发性肠系膜静脉硬化性结肠炎多层螺旋CT表现
2021-05-31姬丽娟万书友
姬丽娟,万书友,李 琮,程 瑾,陈 雷,洪 楠
(1.焦作市人民医院CT室,河南 焦作 454150;2.北京大学人民医院放射科,北京 100044)
特发性肠系膜静脉硬化性结肠炎(idiopathic mesenteric phlebosclerotic colitis, IMP)又称静脉硬化性结肠炎或肠系膜静脉硬化病,是罕见的缺血性结肠炎[1],主要特征为肠系膜静脉及其属支和结肠壁内静脉管壁增厚钙化、管腔狭窄闭塞,并继发结肠肠管(以右半结肠为著)缺血表现。本病临床症状及实验室检查无明显特异性,易漏、误诊。本研究回顾性分析3例IMP,结合相关文献分析其多层螺旋CT表现,以期提高临床医师对本病的认识。
1 资料与方法
1.1 一般资料 回顾性分析2013年7月—2019年10月3例临床诊断IMP患者,均为女性,年龄分别为60、64、65岁,均以黑便及腹泻等消化道症状就诊;2例有高血压史,1例有高血脂病史,1例有血小板减少症及丙型肝炎史,2例有服用中草药史;均于CT检查后接受结肠镜检查及活检组织病理学检查。
1.2 仪器与方法 检查前30 min嘱患者饮水800~1 000 ml。采用Philips 64排CT机及GE Revolution CT机行全腹部平扫+双期增强扫描,扫描范围自膈顶至盆底,管电压100 kV,管电流100 mA,层厚和层间距为5 mm;以流率3~4 ml/s经肘静脉注射对比剂碘海醇(350 mgI/ml)1.2~1.5 ml/kg体质量,分别于注射对比剂后35、70 s行动脉期、门静脉期扫描。扫描结束后行最大密度投影(maximum intensity projection, MIP)、CT血管成像(CT angiography, CTA)及曲面重建(curved planar reformation, CPR)。
2 结果
2.1 CT表现 2例见肠系膜上静脉及受累增厚的右半结肠静脉管壁多发钙化;1例肠系膜上、下静脉及属支管壁弥漫钙化(图1A),以右侧为著,全结肠管壁增厚,右半结肠肠壁内多发点、条状血管钙化影(图1B),伴远端回肠管腔轻度扩张、积液。增强后增厚肠壁均轻度均匀强化(图1C),程度低于正常肠壁,其中2例病变肠壁水肿呈分层状。3例病变肠段管壁略僵硬,周围腹膜密度略增高,相应系膜血管增多、紊乱;CTA、MIP图像示钙化处肠系膜静脉走行紊乱、僵硬(图1D、1E);CTA示肠系膜动脉及其属支显影良好,管腔未见狭窄。
2.2 结肠镜及病理结果 结肠镜检查中,1例结肠肝曲见糜烂病变,充血、糜烂明显;另2例病变肠壁散在糜烂及多发溃疡形成,局部黏膜水肿、充血,横结肠黏膜色素沉着(图2)。病理:光镜下见固有膜及小血管管壁增厚伴广泛玻璃样变,黏膜慢性炎细胞浸润,未见明确肿瘤细胞,局灶呈缺血/毒性损伤性改变。
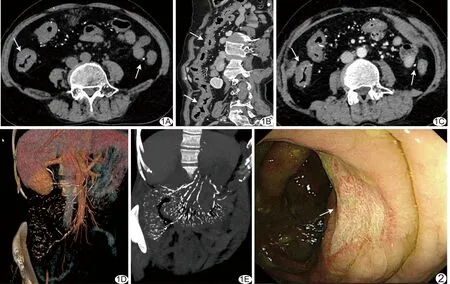
图1 患者女,60岁,IMP A.平扫CT; B.平扫CPR图像; C.增强CT; D.CTA; E.MIP图像 (箭示钙化灶) 图2 患者女,64岁,IMP 结肠镜于横结肠见2.0 cm×1.5 cm溃疡,附着清洁白苔,周边见褐色再生上皮
3 讨论
3.1 临床及病理表现 IMP多见于中老年人,既往有研究[1-2]报道女性发生率略高于男性,也有相反的结果[3-4]显示男性明显多于女性;本组3例均为女性。IMP的发病机制尚不明确,有学者[2-6]认为与服用中草药酒导致静脉损伤、硬化及闭塞有关,或因化学制品、毒性物质等致静脉损伤[5];肝炎、门静脉高压亦可能是其发病原因[7]。本组2例有长期服用中草药史,1例有丙肝病史。IMP临床常表现为消化道症状,如腹痛、腹泻及黑便等,可伴肠梗阻[2]表现,与结肠缺血程度及病程长短有关。结肠镜及病理检查对诊断IMP有较大提示作用。结肠镜检查可见继发于结肠缺血的肠黏膜水肿,呈暗紫色,可伴散在糜烂及溃疡形成;光镜下肠黏膜下层纤维变性,静脉血管纡曲、管壁增厚,静脉壁纤维化、钙化并伴管腔狭窄。
3.2 CT表现 多层螺旋CT分辨率较高,对细小钙化敏感,能清晰显示IMP中静脉管壁钙化,且扫描速度快,是诊断IMP的主要影像学方法。多层螺旋CT扫描范围大,有利于追踪观察钙化血管壁;增强扫描后应用MIP、CTA技术可显示肠系膜动脉及静脉的整体走行;MIP图像可较好显示血管壁钙化范围、分布;CTA则有利于评估钙化血管腔的狭窄程度。
IMP的特征性钙化表现为病变区肠系膜静脉及其属支血管管壁多发钙化,伴或不伴肠壁内小静脉钙化,多见于肠系膜上静脉引流的右半结肠,可同时累及肠系膜上、下静脉分支甚或门静脉主干[5]。IMP以右半结肠壁受累为主,可能与该段肠管收缩蠕动较明显及肠管蠕动方向有关;静脉回流障碍导致病变局部肠系膜长期慢性淤血、硬化,肠壁厚度一般为6~15 mm,随着病情进展,病变可累及全结肠,增厚的肠管壁稍僵硬,部分结肠袋消失。增强CT扫描可见肠壁多呈轻度均匀强化,水肿明显时可呈分层状;病变区系膜脂肪密度可增高、紊乱,炎症反应可使肠系膜淋巴结增生,可伴小肠、结肠管腔扩张、积液或合并肠梗阻。CPR图像显示本组3例病变肠管全程,可见增厚的肠壁和无狭窄的肠腔形似道路,而肠壁内的点钙化形似路灯。
3.3 鉴别诊断 ①动脉粥样硬化所致缺血性结肠炎,多见于老年人,钙化较粗大,常累及肠系膜动脉近端或较大分支,增强CT有助于区分肠系膜动、静脉;②血吸虫病后遗改变,多累及乙状结肠和直肠,受累肠壁增厚不明显,结肠壁血管钙化多呈线状或轨道状,一般不伴肠系膜静脉钙化。此外,炎性肠病、结肠癌等CT亦可见肠壁增厚、管壁僵硬,但均无肠系膜静脉管壁钙化形成。
综上所述,IMP的CT表现具有一定特征性,结合结肠镜及病理所见有助于确诊。
