腹腔热灌注化疗联合全身系统化疗及阿帕替尼转化治疗对胃癌腹膜转移的疗效*
2021-05-24丁平安杨沛刚田园庞悦郭洪海刘洋张志栋王冬檀碧波李勇赵群
丁平安 杨沛刚 田园 庞悦 郭洪海 刘洋 张志栋 王冬 檀碧波 李勇 赵群
腹膜转移是胃癌常见的也是最严重的转移方式,近20%胃癌患者术前或术中诊断存在腹膜转移,尤其T3、T4 期胃癌患者在行根治性切除术后腹膜转移发生率更高,同时此类患者生存期较短,是影响预后的主要原因之一[1]。目前关于胃癌腹膜转移(P1CY1)的治疗尚缺乏疗效显著且国际公认的标准治疗方案,全身系统化疗(neoadjuvant intraperitoneal and systemic chemotherapy,NIPS)仍是美国国家综合癌症网络(NCCN)指南中的推荐方案,但由于血浆-腹膜屏障的存在,分子较大的化疗药物难以透过该屏障作用于腹腔内的微小转移病灶,因此全身性化疗对于腹膜转移疗效甚微[2]。日本开展的PHOENIXGC[3]研究结果为P1CY1胃癌患者腹腔化疗提供一种新的治疗思路,也有研究[4]证实阿帕替尼在晚期胃癌转化治疗中取得较好的疗效,但针对HIPEC 化疗同时联合NIPS及阿帕替尼转化治疗P1CY1胃癌患者的研究较少。据此,本研究纳入的P1CY1胃癌患者,经HIPEC 化疗联合NIPS 及阿帕替尼转化治疗后,多数患者耐受性良好,显示出初步疗效,现总结并分析该治疗方案的临床安全性和有效性。
1 材料与方法
1.1 病例资料
收集2017 年10 月至2018 年10 月河北医科大学第四医院收治的32 例P1CY1 胃癌患者的病例资料。纳入标准:1)胃镜活检经组织病理学证实为胃癌,HER-2 检测结果为阴性;同时腹腔镜探查活检腹膜转移组织,经病理学证实为消化道来源以及腹腔灌洗液检测为阳性;2)术前影像学提示无远处脏器转移和第3站以上远处淋巴结转移;3)年龄≤75岁;4)美国东部肿瘤协作组(ECOG)活动状态评分≤2分;5)骨髓功能、肝功能、心功能及肾功能良好,能够耐受化疗;6)无其他严重免疫抑制疾病或同时性恶性肿瘤;7)必须有可测量的病灶,符合实体瘤疗效评价标准(RECIST 1.1)。排除标准:1)存在影响口服药物的因素(如无法吞咽、慢性腹泻和消化道梗阻等);2)伴高血压且经单一降压药物治疗无法良好控制;3)尿常规提示尿蛋白≥++且证实24 h 尿蛋白定量>1.0 g;4)根据研究者判断,有严重危害患者安全或影响完成研究的其他伴随疾病;5)未能完成6 个周期转化治疗;6)未能获取完整临床病理资料及随访信息。本研究所有患者及家属均签署知情同意书。
1.2 方法
1.2.1 腹腔镜探查术[5]患者体位为平卧位,以开放法在脐下建立观察孔,并直视下分别于左、右两侧脐锁骨中线处置入5 mm Trocar,置入操作钳进行探查和灌洗。腹腔探查顺序:左右膈下→肝脏、脾脏→腹腔壁层腹膜→盆腔→大网膜、小肠及系膜→横结肠系膜→胃。探查内容:有无腹水,腹盆腔腹膜、肠系膜、大网膜和Douglas腔有无转移病灶,肝表面有无转移,胃周淋巴结是否肿大,胃浆膜面有无浸润,胃壁是否僵硬。腹腔冲洗脱落细胞学检查:以500 mL灭菌生理盐水分别冲洗左右膈下、腹盆腔腹膜及肠系膜。取头高脚低位于Douglas腔、肝下及脾窝收集腹腔冲洗液,离心沉渣,细胞学检查有无脱落的肿瘤细胞。对于胃体后壁肿瘤,需要切开胃结肠韧带,探查小网膜囊,包括横结肠系膜和胰腺被膜。对腹腔内可疑病灶均应行活检,同时记录病灶位置、大小、是否融合及腹膜癌指数(peritoneal cancer index,PCI)等。PCI评分评估标准[6]:腹部分为13个区,分别行各区域内的病灶体积(lesion size,LS)评分,LS-0 为未发现种植病灶,LS-1 为种植病灶<0.5 cm,LS-2为0.5~5.0 cm,LS-3为>5.0 cm;PCI值为各区域LS分值累计所得,范围为0~39分。
1.2.2 腹腔脱落细胞学结果判定[7]由2位病理科专业医师阅片,胃癌腹腔脱落细胞染色的阳性结果主要包括:核大深染,核浆比例失调;核染色质致密、粗糙,分布不均,排列紊乱;核膜增厚,出现中断或皱折;核仁增多等。若出现腹腔脱落细胞学阳性则定义为CY1。
1.2.3 腹膜转移组织结果判定 完整切除可疑腹膜转移组织,病理诊断均由2位病理科医师阅片后予以证实。若活检组织经H&E染色及免疫组织化学法提示来源于消化道,则定义为P1。
1.2.4 腹壁化疗港留置术 化疗港选取口径较大的腹腔专用港,包含1枚基座、连接套环、穿刺装置及化疗管(15F-420 mm)。港座放置区通常选取髂前上棘与脐连线中外1/3位置,保证底座下方能够起到支撑作用。手术切口(长度通常取3~4 cm)选取在港座放置区的外侧行斜行切口,切开皮肤及皮下脂肪,分离脂肪层至筋膜层,充分止血,使化疗港距离表皮1.0~1.5 cm,另在切口内侧充分游离周围组织形成港腔,至能够完整放置腹壁化疗港。然后将穿刺杆沿盆腔方向穿刺形成隧道,沿隧道置入腹壁化疗管(一般取12~15 cm),后将港座与化疗管通过连接套环相连,在腹腔镜辅助下钳住化疗管的管头置入盆腔,同时在保证导管无折曲的前提下,使用不可吸收丝线将港座四周固定于筋膜层,依次关闭皮下脂肪、皮肤,最后试验港座及导管通畅性。
1.2.5 转化治疗方案 HIPEC 化疗第1 个疗程在腹腔镜探查术后次日开始,每间隔24 h 进行1 次,连续行3次HIPEC化疗,腹腔注药选择紫杉醇(75 mg/m2);HIPEC治疗结束后休息2周进行NIPS化疗,每3周为1 个疗程,共进行6 个疗程的转化治疗。在每次化疗的第1天和第8天,经腹腔化疗港输注紫杉醇(20 mg/m2,溶于1 000 mL生理盐水,输注1 h以上),同时静脉输注紫杉醇(50 mg/m2,溶于500 mL生理盐水,输注1 h以上),在给予紫杉醇治疗前需给予地塞米松及西咪替丁预处理;连续14 d在早、晚餐30 min后口服替吉奥80 mg/(m2·d),停药7 d,同时连续21 d 口服阿帕替尼500 mg/d。
1.2.6 疗效和不良反应评估 所有患者每转化治疗2 个周期后进行CT 影像学检查,疗效评估采用RECIST 1.1 标准,分为完全缓解(complete response,CR)、部分缓解(partial response,PR)、疾病稳定(stable disease,SD)和疾病进展(progressive disease,PD)。客观缓解率(objective response rate,ORR)为CR+PR 病例占可评价病例的百分数,CR 或PR 患者需经4 周后再证实;疾病控制率(disease control rate,DCR)为CR+PR+SD病例占可评价病例的百分数。新辅助化疗后组织病理学反应参照AICC/CAP 标准即肿瘤退缩分级(tumor regression grading,TRG):TRG 0级为无残余肿瘤细胞;TRG 1 级为稀少残余肿瘤细胞;TRG 2 级为纤维化多于残余肿瘤细胞;TRG 3 级为残余肿瘤细胞多于纤维化或无退缩改变。无进展生存期(progression-free survival,PFS)定义为本方案转化治疗开始至疾病进展时间。6 个周期转化治疗结束后再次进行腹腔镜探查联合腹腔脱落细胞学检测评估腹膜转移情况。本研究采用美国国立卫生研究院发布的常见不良反应术语评定标准(CTCAE)评估不良反应和并发症发生率,评价安全性。
1.2.7 随访 所有患者经门诊、住院和电话等方式收集随访资料。随访时间自转化治疗开始,截至死亡终点或2020年10月。1年内每月电话随访1次,每2个月门诊复查1次。1年后每3个月电话随访1次,每3个月门诊随访1次。
1.3 统计学分析
采用SPSS 21.0软件进行统计学分析。计数资料采用χ2检验,计量资料使用t检验。Kaplan-Meier法绘制生存曲线,单因素生存分析采用Log-rank检验,多因素生存分析采用Cox回归模型。以P<0.05为差异具有统计学意义。
2 结果
2.1 临床病理特征
按照入组标准共纳入32例P1CY1患者,其中男性16例(50.00%),女性16例(50.00%);中位年龄54(34~62)岁;病灶部位位于贲门9 例(28.12%),胃体5 例(15.63%),胃窦11例(34.38%),全胃7例(21.87%);肿瘤病灶直径≥5 cm 者23 例(71.87%),<5 cm 者9 例(28.13%);Borrmann分型为Ⅰ~Ⅱ型12例(37.50%),Ⅲ~Ⅳ型20 例(62.50%);肿瘤浸润深度:cT3 期7 例(21.88%),cT4a期16例(50.00%),cT4b期9例(28.12%);淋巴结转移:cN1~cN2期6例(18.75%),cN3a~cN3b期26例(81.25%);高-中分化腺癌10例(31.25%),低-未分化腺癌22例(68.75%);腹膜转移指数PCI评分>10分13例(40.62%),PCI评分≤10分19例(59.38%)。
2.2 治疗情况
32例P1CY1胃癌患者经6个周期转化治疗后均行全腹增强CT扫描,经RECIST 1.1评估局部病灶变化为CR 2例(6.25%),PR 18例(56.25%),SD 9例(28.13%),PD 3例(9.38%),其中ORR为62.50%(20/32),DCR为90.63%(29/32)。32例P1CY1胃癌患者均再次进行腹腔镜探查联合腹腔脱落细胞学检测,探查发现PCI评分较之前下降者24例(75.00%),上升者8例(25.00%)。其中6例(18.75%)患者PCI评分(起始PCI评分分别为39、15、12、10、6、6分)降为0分,进行R0切除;3例(9.38%)患者PCI评分(起始PCI评分分别为30、24、15分)降为5分;4例(12.50%)患者(起始PCI评分分别为27、15、9分)降为3分,均因合并肿瘤相关并发症而进行R2切除。其余19例患者继续原方案转化治疗(图1)。
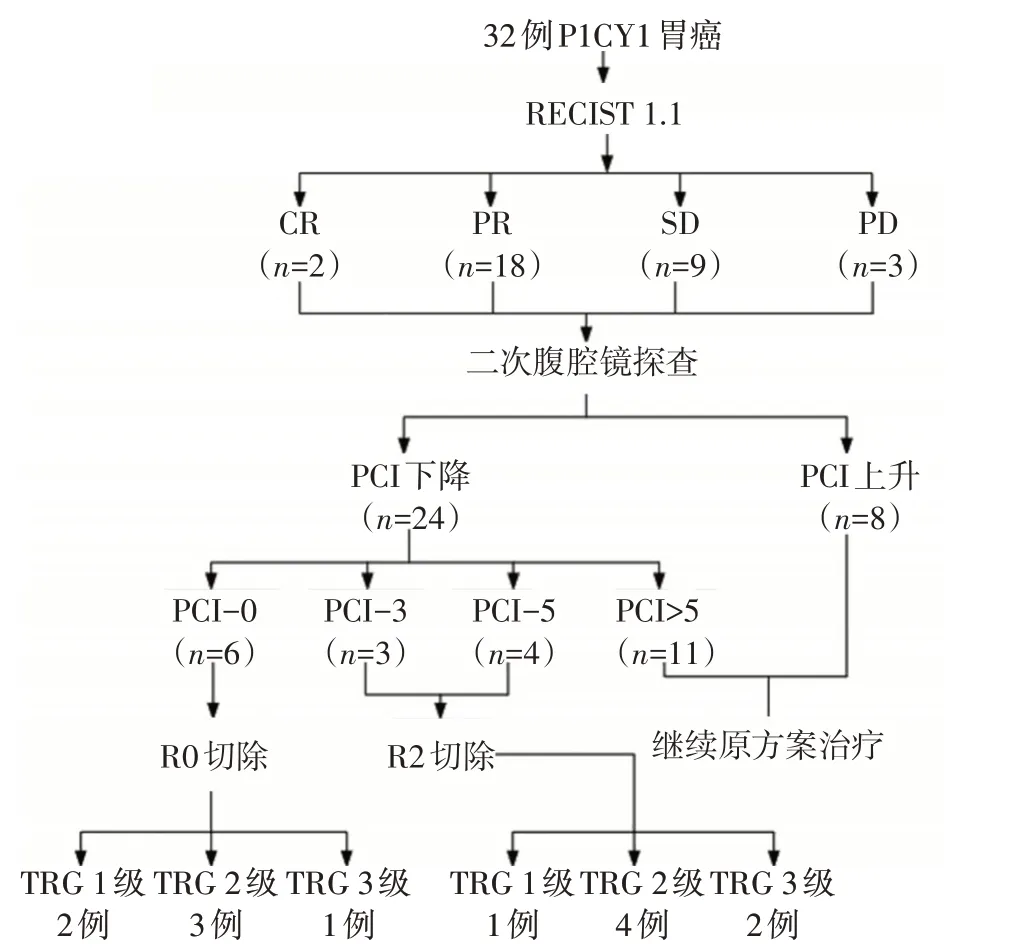
图1 32例P1CY1胃癌患者诊治流程图
2.3 预后情况
32 例P1CY1 胃癌患者均获得随访,随访时间为5.7~38.9个月,中位随访时间为25.2个月,随访率为100%。全组2 年总生存率(overall survivall,OS)为34.38%,中位OS(median,mOS)为16.2(13.5~22.5)个月;2 年PFS 为25.00%,中位PFS(median PFS,mPFS)为14.9(11.4~20.3)个月(图2A,2B)。其中行R0、R2手术切除患者2年OS分别为83.33%、42.86%,2 年PFS 分别为66.67%、28.57%,而未行手术切除患者2年OS、PFS分别为15.79%、10.53%,三组之间2年OS、PFS 差异有统计学意义(P<0.05,图2C,2D)。单因素分析结果显示,浸润深度cT 分期、组织学类型、转化治疗后是否行R0 手术切除、腹膜转移PCI 评分是影响患者预后的危险因素(P<0.05,表1)。Cox 回归多因素分析显示,转化治疗后未能行R0 手术切除(P=0.039)以及腹膜转移PCI评分>10分(P=0.026)是影响P1CY1胃癌患者预后的独立危险因素(表2)。
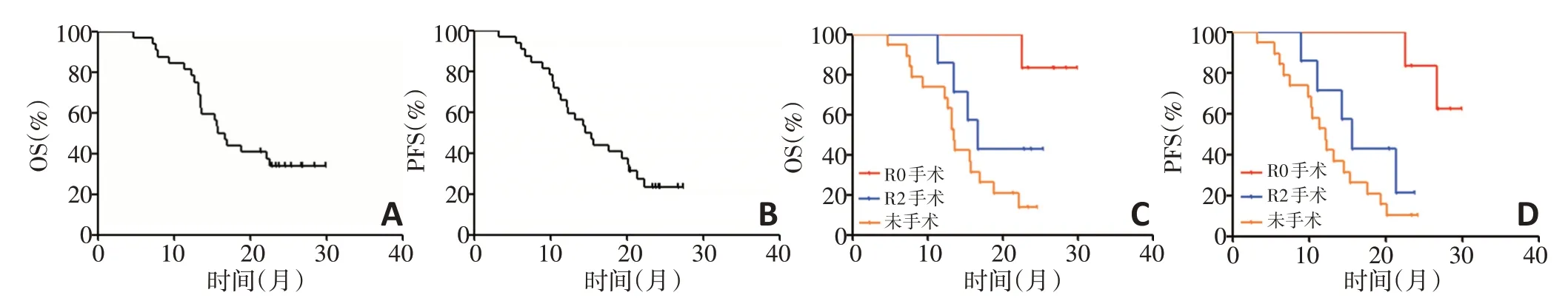
图2 32例P1CY1胃癌患者生存曲线
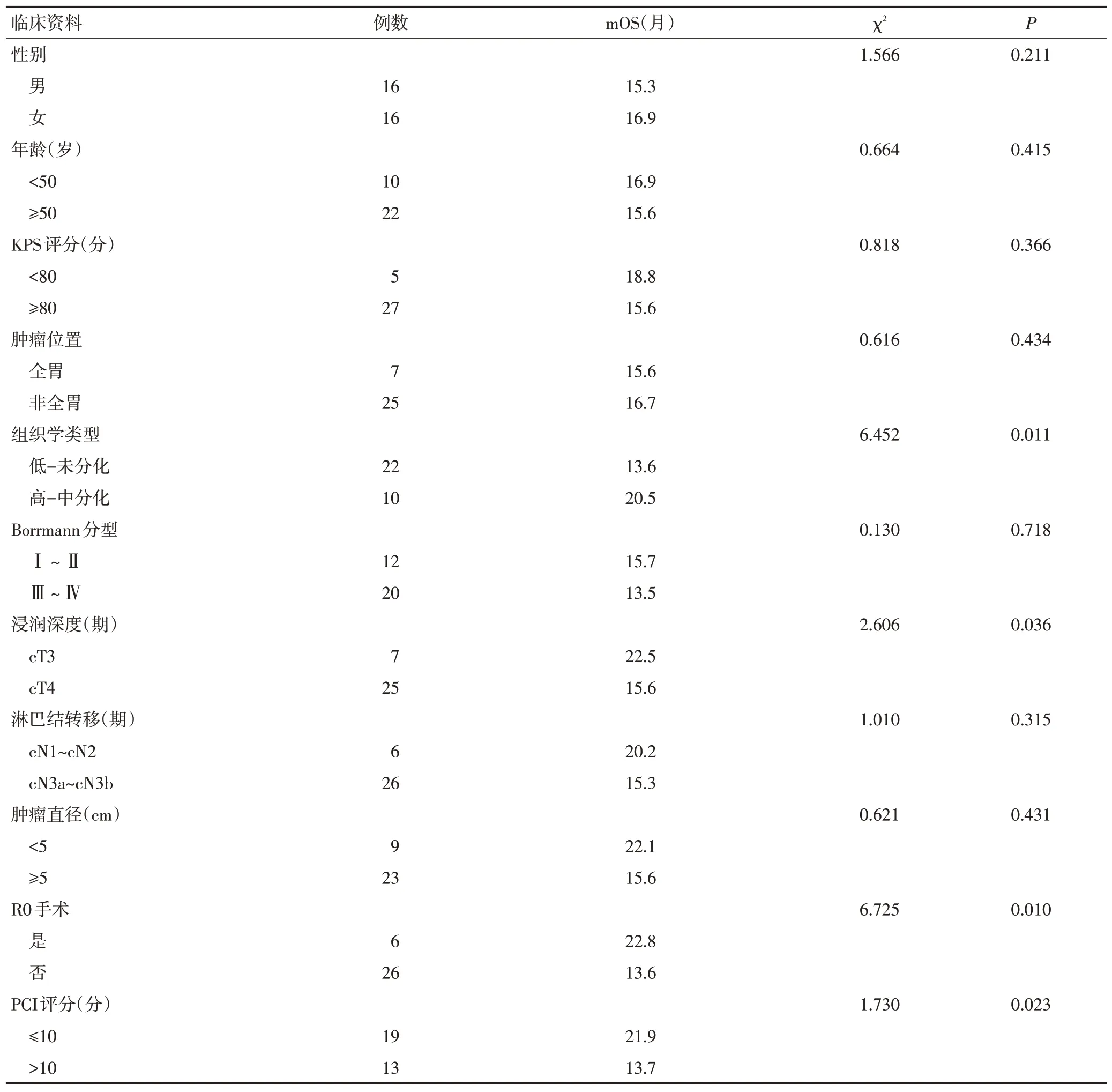
表1 影响32例P1CY1胃癌患者预后的单因素分析
2.4 治疗期间不良反应
全组患者均未出现因HIPEC、NIPS 以及口服阿帕替尼、S-1 治疗而死亡,也未出现手术相关并发症。在接受转化治疗的32 例患者中,Ⅲ度及以上血液学不良反应发生率为9.38%,主要为白细胞减少、中性粒细胞减少以及血小板减少;非血液学不良反应主要为恶心、呕吐和食欲下降,发生率分别为28.13%(9/32)、21.88%(7/32)(表3)。全组患者治疗期间腹腔化疗港相关并发症为2例切口感染,但均未因腹腔化疗泵不良反应而终止治疗。
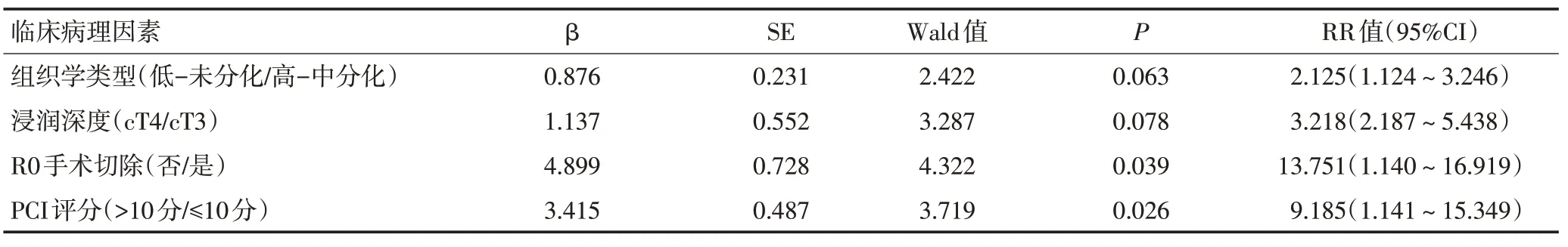
表2 影响32例P1CY1胃癌患者预后的Cox回归多因素分析
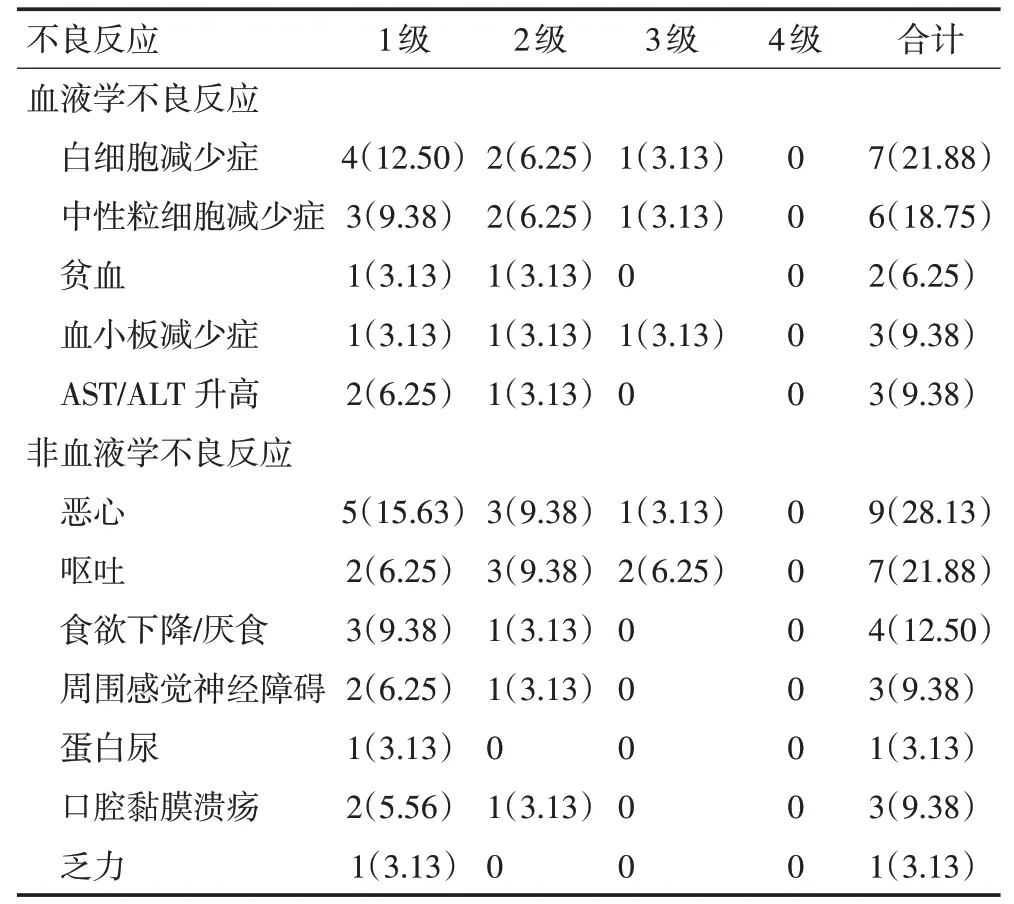
表3 32例P1CY1胃癌患者转化治疗期间的不良反应 例(%)
3 讨论
胃癌是一种发病率较高的恶性肿瘤,死亡率亦较高,腹膜转移是治疗失败以及最终导致死亡的主要原因之一[1]。相关报道有14%胃癌患者在首诊时出现了腹膜转移,而在晚期患者中达到39%~43%,同时发现在行D2根治术后复发的患者中发生腹膜转移的比例达45%[8]。既往曾有学者采用肿瘤细胞减灭术联合术后辅助化疗治疗此类患者,降低肿瘤负荷,然而日本的一项前瞻性REGATTA 研究[9]结果发现,具有单一不可切除因素的转移性胃癌患者接受单纯化疗组中位生存时间为16.6 个月,而接受减量胃切除手术联合化疗组中位生存时间仅为14.3 个月。因此对于合并腹膜转移的晚期胃癌患者,先进行原发病灶切除并术后辅以化疗不能带来任何生存获益,对这类患者进行全身性化疗可能将会延长生存期。但由于体内存在“血浆-腹膜屏障”,经全身性化疗时化疗药物难以透过该屏障而无法作用于腹膜转移病灶,因此寻找一种合适的转化治疗手段尤为重要。
HIPEC是近年来提出的一种通过高温、化疗药物作用、机械冲刷腹腔从而杀灭腹膜转移的新型治疗方法,能够有效地防治腹腔内转移,提高患者生存率以及降低腹膜复发转移率[10]。相比于全身性化疗,运用HIPEC治疗腹膜转移有如下优势[11-12]:1)药物可以在腹腔内与转移病灶或游离癌细胞直接作用;2)由于“血浆-腹膜屏障”的存在,药物在腹腔内存留时间长,尤其是大分子药物;3)药物主要经过腹膜与门静脉先进入肝脏再进入全身循环,减轻了不良反应。但由于HIPEC 治疗难以在后续治疗中重复进行,而NIPS化疗却可以根据患者治疗情况进行多次、持续腹腔给药,能弥补这一不足之处。日本PHOENIX系列研究证实了NIPS化疗对伴有腹膜转移的胃癌具有较好的疗效,能够改善患者预后[3,13]。基于此,本研究针对合并腹膜转移的胃癌患者进行HIPEC治疗同时联合NIPS 化疗腹腔给药模式,腹腔注药及静脉途径均选择紫杉醇,同时全身性化疗药物选择口服S-1。其理论依据为,Soma等[14]针对紫杉醇在腹腔内给药的药代动力学研究显示,紫杉醇在腹腔组织与血浆中的曲线下面积(AUC)比值较高,腹腔内用药后其腹腔内药物最高浓度较血浆高6 896.2 倍,由于其为大分子药物,腹腔吸收缓慢,可以在腹腔内长时间作用且不良反应发生率较低,而替吉奥在一些研究中被认为针对腹膜转移有一定疗效[15]。阿帕替尼是VEGFR-2 的小分子酪氨酸激酶抑制剂,能高效地抑制肿瘤血管的生成,从而发挥抗肿瘤作用。国内研究[16]回顾性分析了33 例晚期不可切除胃癌患者,口服阿帕替尼联合转化治疗后ORR为75.7%,R0切除率高达63.6%,该研究表明在晚期胃癌转化治疗中联合口服阿帕替尼可提高R0 切除率,且安全可行。本研究中在HIPEC及NIPS转化的基础上同时采用了阿帕替尼应用于胃癌腹膜转移患者,多种途径联合给药进行转化治疗,并评价该治疗方案的安全性和有效性。
Yonemura 等[17]于2017 年首次报道了HIPEC 联合腹腔及NIPS 治疗方案,53 例胃癌腹膜转移患者单纯行HIPEC,52 例行HIPEC+NIPS,再次腹腔镜探查发现后者的PCI值降低更多,提示该方案也被认为较单纯HIPEC 降低PCI 的作用更明显;同时随访发现,HIPEC+NIPS 组患者中位生存时间为19.2个月,而单纯行HIPEC 组仅为14.4个月。本研究针对此类患者也采用相同的治疗模式,但同时亦联合口服阿帕替尼治疗,通过CT 检查评估后发现,ORR 为62.50%(20/32),DCR 为90.63%(29/32);所有患者均再次行腹腔镜探查,发现有6例腹膜转移病灶达CR,达到R0切除标准;同时还有4例患者因治疗后出现肿瘤出血及3 例出现幽门梗阻等相关并发症,但此7 例患者PCI 评分均较起始明显下降,故行R2 手术切除。通过多因素分析发现,转化治疗后能否达到R0 切除是影响患者预后的独立预后影响因素之一,这表明对于胃癌腹膜转移患者若能通过积极转化治疗后进行R0 切除将会明显提高患者预后,而如何选择合适的转化治疗方案将显得尤为重要。有研究[18]发现,接受NIPS 转化治疗的79 例胃癌腹膜转移患者中,2 例(2.5%)出现3~4级骨髓毒性,3例(3.8%)出现3级肾毒性,3 例(3.8%)出现化疗管周皮下感染,经相应处理后均康复。本研究中32例胃癌腹膜转移患者经转化治疗后,主要不良反应是骨髓抑制及消化道反应,其中出现1~2级不良反应16例(50.00%),3级和4级不良反应6例(18.75%),余均未出现不良反应。所有患者未发生因化疗和手术治疗相关的死亡。全组患者治疗期间腹腔化疗泵相关并发症发生率为6.25%(2/32),均为港座切口感染,但均未因腹腔化疗泵不良反应而终止治疗。
综上所述,HIPEC 化疗联合NIPS 化疗应用紫杉醇及口服阿帕替尼及替吉奥是治疗胃癌腹膜转移患者的一种安全、有效转化治疗方案。此治疗方法可显著提高R0 手术切除率,延长患者的生存时间和改善患者生存质量,因此是具有潜在的临床应用前景的转化治疗方法。
