山西小杂粮露酒制备工艺研究
2021-05-14闫文瑾张颖昭袁然然张湘晨任晓莉
闫文瑾, 张颖昭, 袁然然, 张湘晨, 李 昕, 任晓莉
(太原工业学院环境与安全工程系,山西 太原 030008)
引 言
山西省以其独特的自然地理区位,悠久的杂粮种植历史获得了“杂粮小王国”的称号,是中国重要的杂粮基地,拥有中国最大数量的杂粮种质资源样本[1]。山西省地处黄土高原地带,土地集中为旱地,当地光照充足、气候温和,热量与资源十分丰富,十分适宜小杂粮的种植与生长。小杂粮含有丰富的蛋白质、不饱和脂肪酸、膳食 纤维、矿物质、常量及微量元素等,其营养丰富全面、药食同源,是我国传统的保健食品原料作物。小杂粮因此越来越受到消费者的青睐[2]。
近年来,随着人们生活水平的提高和保健意识的加强,保健酒被越来越多的消费者所接受。露酒作为目前较受欢迎的一种保健酒,有极大发展空间。本文研究具有养生功能的山西小杂粮风味露酒的制备工艺条件,既可以提供出一种功能性保健食品,也符合山西省政策导向,利用山西小杂粮开发高品质的功能性食品,具有较强的实践意义。
1 材料与方法
1.1 实验材料、试剂及仪器
清香型汾酒,山西杏花村42°红盖汾酒;小米,晋亿园牌沁州黄;燕麦米,晋西口牌;荞麦米,晋西口牌。
蒽酮,分析纯;硫脲;葡萄糖,分析纯;牛血清白蛋白(BSA),纯度大于99.0%;考马斯亮蓝G-250;无水乙醇,分析纯;98%硫酸,分析纯;85%磷酸,分析纯。
无油隔膜真空泵,JOANLAB VP-10L;超声波清洗机,新芝牌SB 3200DT;大容量全温恒温振荡培养摇床,ZHWY-211D;分光光度计,752型紫外分光光度计。
1.2 实验方法
1.2.1 制备工艺流程
山西小杂粮露酒的制备工艺流程见图1。

图1 山西小杂粮露酒的制备工艺流程
将选取的山西小杂粮粉碎混合,以汾酒为酒基,进行声能处理后,在恒温培养箱内进行振荡浸泡,室温下进行静置浸泡,最后进行真空抽滤,即可得到露酒样品。
(3)南疆地区1950年代中叶之前呈增加趋势,1950年代中叶~1970年代呈减少趋势,后呈显著增加趋势。
1.2.2 研究方法
采用正交实验的方法,在振荡时间(A)、投入量(B)、声能处理时间(C)及振荡温度(D)4个因素的影响下进行三水平的实验,以确定最佳条件。正交实验因素与水平见第5页表1。

表1 小杂粮露酒正交实验因素与水平
1.3 分析方法
1.3.1 总糖含量测定
配制葡萄糖标准溶液,吸取系列标准溶液和蒸馏水各2 mL,分别沿管壁各加入0.1%蒽酮试剂10 mL,立即摇匀,放入沸水浴准确加热10 min,取出后迅速冷却至室温,在暗处放置10 min,以零管调零点后于620 nm波长处测定吸光度。以空白试剂作为参比,根据标准溶液吸光度,以葡萄糖质量浓度为横坐标,吸光度为纵坐标,绘制标准曲线,得到标准曲线回归曲线方程为式(1)。
Y=0.005 7X-0.006 5,R2=0.998 6
(1)
式中:X为葡萄糖质量浓度,μg/mL;Y为吸光度。
将各样液稀释10倍,吸取各稀释样液和蒸馏水各2 mL,放入10只比色管中,沿管壁各加入0.1%蒽酮试剂10 mL,立即摇匀,放入沸水浴准确加热10 min,取出后迅速冷却至室温,在暗处放置10 min,以蒸馏水为零管调零点后于620 nm波长处测定吸光度,根据标准曲线计算总糖浓度。
1.3.2 可溶性蛋白测定
配制1 mg/mL的标准蛋白溶液,吸取标准溶液和蒸馏水配制总量为1 mL的浓度梯度,分别加入考马斯亮蓝溶液5 mL,振荡混匀,静置2 min后,在595 nm波长处测定吸光度。以试剂空白为参比溶液,根据标准溶液吸光度,以标准蛋白溶液质量浓度为横坐标,吸光度为纵坐标,绘制标准曲线,得到标准曲线回归曲线方程,见式(2)。
Y=8.715X+0.021,R2=0.995 1
(2)
吸取0.5 mL试样待测液,置于比色管中,加入0.5 mL蒸馏水,再加入5 mL考马斯亮蓝G-250溶液,振荡混匀,静置2 min。用1 cm比色皿以试剂空白为参比溶液或调零点,用分光光度计于595 nm波长处测定吸光度,根据标准曲线方程计算样液中的可溶性蛋白质含量[3]。
2 结果及讨论
2.1 小米露酒制备工艺
以总糖为评价指标,小米露酒制备工艺的正交实验结果见表2。
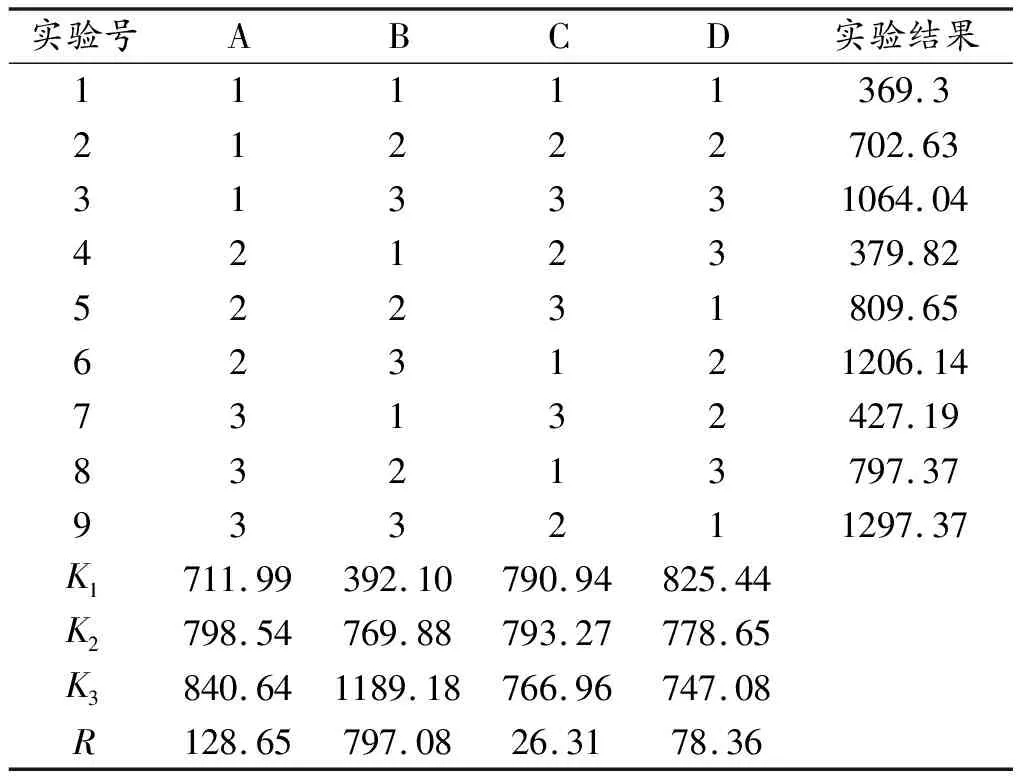
表2 小米浸泡酒液总糖正交实验结果
由表2可知,对总糖含量结果的影响因素顺序为:投入量>振荡时间>温度>声能处理时间。由极差R的大小分析可知,最佳条件为A3B3C2D1,投入量和振荡浸泡时间的影响占比很大,更多的投入量和更长时间的振荡浸泡使小杂粮更充分地与酒基混合[4],能够得到更高的总糖含量。
以可溶性蛋白为评价指标,小米露酒制备工艺的正交实验结果见表3。

表3 小米浸泡酒液蛋白质正交实验结果
由表3可知,对可溶性蛋白含量结果的影响因素顺序为:投入量>温度>声能处理时间>振荡时间。由极差R的大小分析可知,最佳条件为A3B3C1D3,不同振荡时间和声能处理时间对应的结果相差很小,而越多的投入量和更高的温度有利于可溶性蛋白质的浸出。
综合小米浸泡酒液的总糖含量和可溶性蛋白含量两个指标来看,声能处理时间对可溶性蛋白含量的影响比总糖含量大,于是选C1为最佳声能处理时间,温度对可溶性蛋白含量的影响比总糖含量大,于是选D3为最佳温度。因此,本文认为小米露酒最佳制备条件为A3B3C1D3,即,振荡时间3 d,投入量90 g/L,声能处理时间10 min,温度40 ℃。
2.2 燕麦米露酒制备工艺
以总糖为评价指标,燕麦米露酒制备工艺的正交实验结果见表4。

表4 燕麦浸泡酒液总糖正交实验结果
由表4可知,最佳条件为A3B3C3D1,极差R的大小分析可知,对总糖含量结果的影响因素顺序为:投入量>振荡时间>声能处理时间>温度。由数据可知,投入量是主要的影响因素,越高的投入量能够得到更高的总糖含量。与小米浸泡酒液相同,越高的温度反而会降低总糖含量,最适宜的温度为20 ℃。
以可溶性蛋白为评价指标,燕麦米露酒制备工艺的正价实验结果见表5。

表5 燕麦浸泡酒液蛋白质正交实验结果
由表5可知,最佳条件为A1B3C3D3,由极差R的大小分析可知,对可溶性蛋白含量结果的影响因素顺序为:投入量>温度>振荡时间>声能处理时间。不同振荡时间和声能处理时间对应的数值相差很小,且影响程度很小,而越多的投入量和更高的温度有利于可溶性蛋白质的浸出。
综合燕麦米浸泡酒液的总糖含量和可溶性蛋白含量两个指标来看,振荡时间对总糖含量的影响比可溶性蛋白含量大,于是选A3为最佳振荡时间,温度对可溶性蛋白含量的影响比总糖含量大,于是选D3为最佳温度。因此,本文认为燕麦米露酒最佳制备条件为A3B3C3D3,即,振荡时间3 d,投入量90 g/L,声能处理时间30 min,温度40 ℃。
2.3 荞麦米露酒制备工艺
以总糖为评价指标,荞麦米露酒制备工艺的正交实验结果见表6。
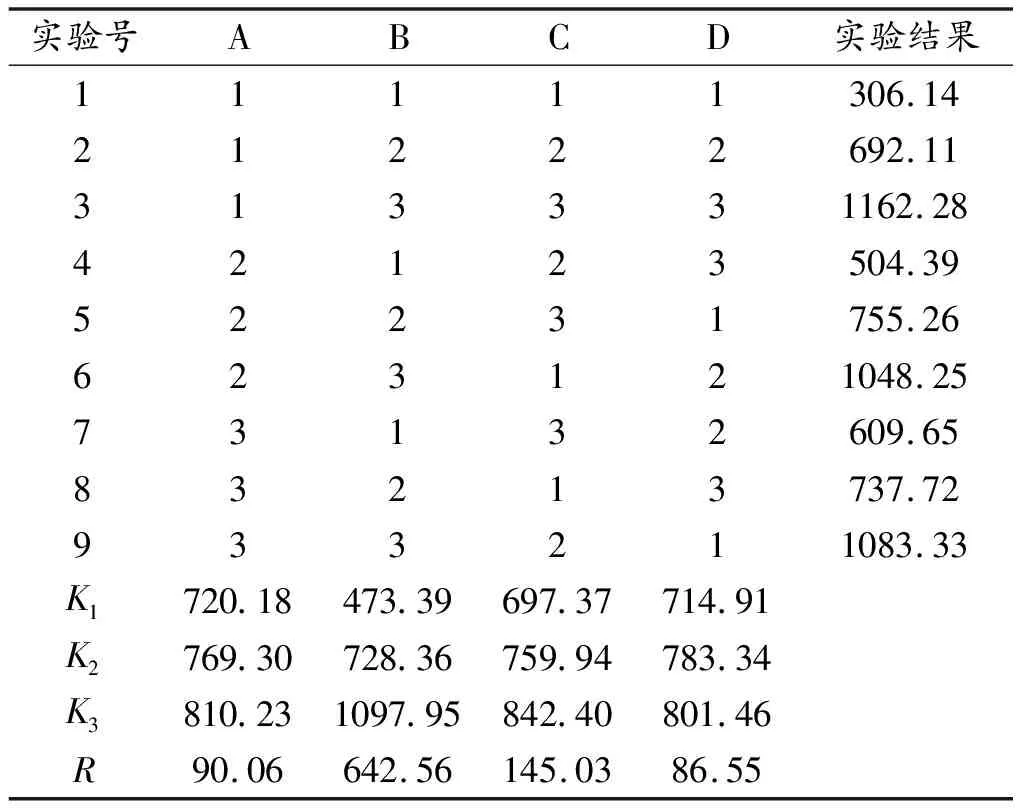
表6 荞麦浸泡酒液总糖正交实验结果
由表6可知,最佳条件A3B3C3D3,由极差R的大小分析可知,对总糖含量结果的影响因素顺序为:投入量>声能处理时间>振荡时间>温度。由数据可知,与小米、燕麦米露浸泡酒液不同,荞麦米露浸泡酒液总糖含量随温度升高而增加,因此,荞麦米露最适温度为40 ℃。
以可溶性蛋白为评价指标,荞麦米露酒制备工艺的正交实验结果见第7页表7。
由表7可知,最佳条件为A3B3C1D3,由极差R的大小分析可知,对可溶性蛋白含量结果的影响因素顺序为:投入量>温度>振荡时间>声能处理时间。由数据可知,投入量和温度对可溶性蛋白质含量影响因素较大,荞麦米浸泡酒液的最适声能处理时间为10 min,与小米、燕麦米露浸泡酒液不同。
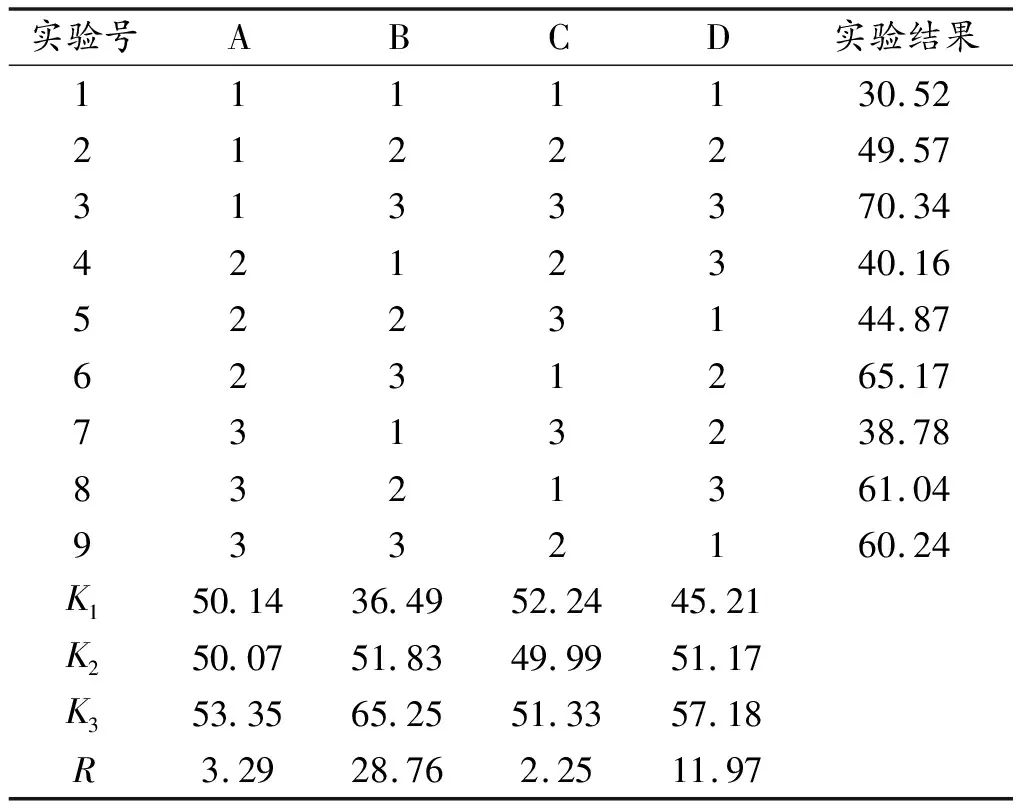
表7 荞麦浸泡酒液蛋白质正交实验结果
综合荞麦米浸泡酒液的总糖含量和可溶性蛋白含量两个指标来看,声能处理时间对总糖含量的影响比可溶性蛋白含量大,于是选C3为最佳振荡时间,因此,本文认为荞麦米露酒最佳制备条件为A3B3C3D3,即,振荡时间3 d,投入量90 g/L,声能处理时间30 min,温度40 ℃。
3 结论
本实验以总糖和可溶性蛋白为评价指标,研究了三种小杂粮浸泡酒的最佳工艺条件。小米浸泡酒的最佳工艺条件为:振荡时间3 d,投入量90 g/L,声能处理时间10 min,温度40 ℃;燕麦米泡酒的最佳工艺条件为:振荡时间3 d,投入量90 g/L,声能处理时间30 min,温度40 ℃;荞麦米浸泡酒的最佳工艺条件为:振荡时间3 d,投入量90 g/L,声能处理时间30 min,温度40 ℃。
