探究浓硫酸性质实验的改进与创新
2021-05-14福建省晋江市第一中学庄亚婷
福建省晋江市第一中学 庄亚婷
一、硫及其化合物在教材中的地位
2020 级高一学生使用的是新教材,化学1 教材在元素化合物这块知识点上做了适当的删减和调整,删掉了硅、铜及其化合物的相关章节,氢氧化铝的性质在学习元素周期律部分知识点时进行穿插分析,将氮、铁及其化合物的知识点挪到了化学2,保留了钠、镁、氯、溴、碘(卤素)、硫及其化合物的知识点。其中,用了专题四整整一个专题、三个单元来分析硫与环境保护,足见硫及其化合物的重要性。掌握好硫及其化合物的知识点对于化学2 氮及其化合物的学习有着承上启下的作用。对于变价元素的性质探究,难免要讨论到氧化还原反应。学生在初中对浓硫酸的吸水性、脱水性有一定的了解,但是强氧化性没有系统学习,这个是高中教学的重点和难点。化学是以实验为基础的学科,问题的分析离不开实验的探究。特别是在元素及其化合物的教学中,实验演示能帮助学生更好地理解物质的反应变化与规律。苏教版教材设计了三个实验,依次要证明浓硫酸吸水性、脱水性和强氧化性。笔者旨在对苏教版教材中的实验进行探究、适当改进和创新。
二、苏教版教材中的实验设计
实验1:向表面皿中加入少量胆矾(CuSO4·5H2O),再加入约3mL 浓硫酸,搅拌,观察实验现象。
实验2:取2g 蔗糖(C12H22O11)放入大试管中,加2—3滴水,再加入约3mL 浓硫酸,迅速搅拌,然后塞进带玻璃导管的橡皮塞,将玻璃导管的另一端插入盛有品红溶液的试管中,观察实验现象。
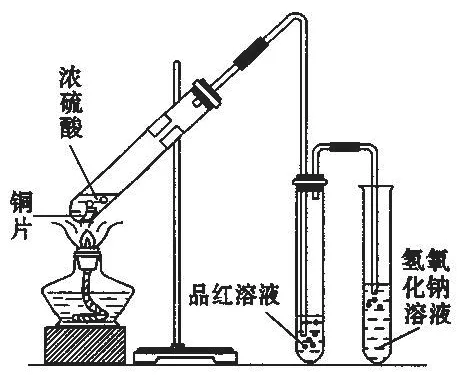
实验3:将一小片铜片放入大试管中,然后加入2mL 浓硫酸,用如左图装置进行实验,观察实验现象。
三、问题的提出与解决
(一)浓硫酸吸水性实验
实验1 关于浓硫酸吸水性的实验设计,比较简单易操作,学生对浓硫酸吸水性的性质掌握已经有了一定的基础。但是,学生容易把胆矾(CuSO4·5H2O)和无水硫酸铜的颜色混淆。如何更好地设计实验,让学生对二者的颜色更好地辨别,达到更好的教学效果?
改进措施:实验1 的实验如果能在原设计的基础上加入空白对比实验,那么效果会更好,也符合现在高考命题的趋势。通过空白实验对比,教师现场拍照投屏,学生能直观对比观察胆矾(CuSO4·5H2O)和无水硫酸铜的颜色。而本操作也不会影响实验所需的操作时间。课堂实验时间的控制,主要取决于胆矾的用量,取2 到3 勺使加入的浓硫酸没过胆矾能看到现象即可。
(二)浓硫酸脱水性及强氧化性实验
实验2 的实验设计是要验证浓硫酸的脱水性以及强氧化性。本实验的设计对比于人教版的设计已经有了更新。人教版的做法是取20g 蔗糖和几滴水于200mL 烧杯中,加入15mL 浓硫酸,迅速搅拌。该设计操作简单、现象明显、趣味性强,但药品量大,且是在敞口烧杯中进行,产生的大量有毒气体会直接逸散到空气中,不仅会危害师生身体健康,还会污染环境。苏教版设计减小了药品的用量,并能检验产生的二氧化硫气体。但笔者在实践中发现,在试管中搅拌不容易操作,且有时搅拌较长时间才会出现混合物体积迅速膨胀的现象。这导致实验耗时较长,课堂松散,甚至可能达不到预期效果。
改进措施:可先将蔗糖研磨以利于后续反应顺利进行,从而控制反应时间。浓硫酸与碳反应要在较高温度下进行,而蔗糖的脱水是一个放热反应,一般能提供后续反应所需的热量。但是如果冬天天气寒冷,温度有可能达不到反应所需温度。这时可用酒精灯微热试管底部,促发后续反应的进行。但要注意的是,微热的操作应该是在碳化后进行,且微热只要看到有混合物体积膨胀的倾向,就可以停止。由于反应产生的二氧化硫气体有毒,是大气主要污染物之一,我们可以在装有品红溶液的试管口处放一团蘸有氢氧化钠溶液的脱脂棉进行尾气处理。
(三)浓硫酸强氧化性实验
实验3 的设计意图是用浓硫酸与不活泼金属铜反应来验证浓硫酸的强氧化性。笔者在实际操作中发现了几个问题。第一,大试管中有酸雾产生,而产生的酸雾量大会堵住试管口,气体不容易跑出去。第二,在验证反应生成气体是二氧化硫时,需将导气管深入盛有品红溶液的试管中,但由于二氧化硫易溶于水,易引起倒吸的现象,存在安全隐患。在实际操作中为了防止倒吸,停止加热前要先打开双孔橡皮塞,而大试管中的反应仍在进行,会导致产生的二氧化硫气体逸出影响师生健康。
改进措施:酸雾的产生是由于酒精灯加热可达到400°C以上,而硫酸的沸点是338°C,所以产生了硫酸酸雾。书本中设计导管长,产生的酸雾不能及时排出,反应又不断在进行,会造成酸雾不能及时排出而堵在试管口的现象。可以考虑缩短导管,或加快反应速率等方法来防止酸雾堵住试管口。而防倒吸,可以通过增加一个防倒吸装置或者改用蘸有品红溶液的滤纸来代替品红溶液进行物质的检验。
综上,笔者对浓硫酸与铜的性质探究实验做了一定的改进创新,最后得到了较好的实验效果,具体设计如下。
四、浓硫酸与铜反应改进实验
(一)实验用品
实验器材:酒精灯、火柴、铁架台(带铁夹)、单孔橡皮塞(2 个)、大试管(1 个)、燃烧管(双通管)、橡皮管、滤纸、棉花。
实验药品:铜片、98%浓硫酸、品红溶液、酸性高锰酸钾溶液、氢氧化钠溶液。
(二)实验装置(其中铁架台等夹持仪器省略)

(三)实验操作、现象、结论
操作:将一小片铜片剪成细条状,放入大试管,再加入2mL浓硫酸,迅速与事先放好药瓶的燃烧管(双通管)连接。如图组装好仪器。先用酒精灯外焰预热试管底部,然后集中加热。
现象:加热一会儿后可以看见铜片逐渐溶解,有气泡生成,吸有高锰酸钾溶液和品红溶液的滤纸褪色。待试管冷却后取下,将大试管中的液体倒入盛有少量水的烧杯中,可以看到溶液呈现蓝色。
结论:有二氧化硫气体生成,铜与浓硫酸反应生成了二价铜离子。浓硫酸可以和不活泼金属铜反应,体现了浓硫酸的强氧化性和酸性。
(四)实验疑问解释
1.为什么不用湿润紫色石蕊试纸检验二氧化硫气体?由于反应有硫酸酸雾,不能准确解释试纸变红的原因。
2.铜片剪成细条状可以增大浓硫酸与铜反应的接触面积,加快反应速率。
3.实验室如果没有滤纸条可以用滤纸加工,剪成细短条(类似于pH 试纸大小)。滤纸条只要能看到现象变化就行,没有必要剪很大。过大,送入试管后试纸容易卷缩到一起而有一部分会接触不到二氧化硫气体,直观视觉上就是滤纸一部分褪色,一部分不褪色,或者需要较长时间才能看到实验现象,耽误教学进程。
4.实验室提供的品红溶液和酸性高锰酸钾溶液如果浓度较大,可以适当稀释以后再用滤纸吸收,这样更容易观察到实验现象,缩短反应时间。
5.该实验的成功关键还在于药品的选择和使用。由于浓硫酸的吸水性强,在药品选择上要尽量挑选近期开封的药品。药品取用完,马上盖好瓶盖,防止浓硫酸吸收空气中的水蒸气浓度下降而拉长实验演示时间或实验演示不明显。
(五)改进实验的优点
一是实验仪器简单,操作简易,用蘸有药品的滤纸或脱脂棉来代替溶液,节约药品,减少器材。二是实验装置避开了倒吸现象的产生,消除了安全隐患,有利于各校开展。三是缩短了导管的长度,不会出现酸雾堵住试管口的现象。且二氧化硫气体能快速转移到燃烧管中,使吸有品红溶液的滤纸和吸有酸性高锰酸钾溶液的滤纸快速褪色,实验现象明显。四是实验所需时间短,课堂教学环节紧凑,能保证实验课堂的有序进行,教学效果好。
综上所述,根据《普通高中化学课程标准(2017 年版)》,普通高中化学课程是与义务教育化学或科学课程相衔接的基础教育课程,是落实立德树人根本任务、发展素质教育、弘扬科学精神、提升学生核心素养的重要载体;化学学科核心素养是学生必备的科学素养,是学生终身学习和发展的重要基础;化学学科核心素养包括“宏观辨识与微观探析”“变化观念与平衡思想”“证据推理与模型认知”“科学探究与创新意识”“科学态度与社会责任”五个方面。在浓硫酸的性质探究实验中,笔者采用人人通移动讲台同步直播实验教学过程,投屏现象明显。创设真实化学实验情境,是基于真实情境的教学。实验探究物质的性质,并对实验进行创新,体现核心素养中强调的科学探究与创新意识。同时,对宏观现象进行微观探析,解释现象发生的本质,总结浓硫酸的性质,这体现了宏观辨识与微观探析在课堂上的呈现。通过实验原理与方法的分析,渗透化学学科必备知识,有利于培养学生学科素养。
