落叶松基氮掺杂泡沫炭的制备及其CO2吸附性能研究
2021-05-11张宇航马春慧刘守新
张宇航, 应 浩, 李 伟, 马春慧, 罗 沙, 刘守新*
(1.东北林业大学,生物质材料科学与技术教育部重点实验室,黑龙江 哈尔滨 150040;2.中国林业科学研究院 林产化学工业研究所,江苏 南京 210042)
由温室气体大量排放所带来的全球变暖问题是目前最严峻的环境问题之一。CO2作为主要的温室气体,其大气中的浓度已由未工业化时的503 mg/m3升至历史最高值726 mg/m3,并预计在2050年达到987.8 mg/m3[1]。因此,CO2吸附技术得到了广泛的关注,其中固体吸附法由于吸附稳定性和再生性能高、对设备腐蚀性低以及价格便宜等优点,应用最为广泛[2]。固体吸附法常用的吸附剂包括沸石[3]、金属有机骨架[4]、介孔氧化硅[5]、多孔聚合物材料[6]和多孔炭材料[7]等,其中多孔炭材料具有原料来源广泛、化学稳定性和热稳定性高、吸附性能好和价格便宜等优点,是最常用的固体吸附剂。生物质原料作为一种绿色资源,其制备出的多孔炭材料具有孔结构易于调控和表面含氧官能团丰富等优点而成为研究的热点[7]。生物质多孔炭材料的CO2吸附性能一方面由其表面化学性质决定[8],主要通过氮掺杂来提高其CO2吸附性能。如Han等[9]采用甘蔗渣为碳源、尿素为氮源制备氮掺杂生物质多孔炭,较未掺杂炭材料相比,CO2吸附容量由1.66 mmol/g提高到了4.80 mmol/g(25 ℃和100 kPa)。另一方面,孔结构也影响多孔炭材料的CO2吸附性能[10]。由于生物质多孔炭材料宏观结构多为粉末状,用于吸附CO2时需要用黏合剂制成整体式材料,不仅操作复杂而且会因为孔结构的阻塞而降低炭材料的吸附容量,所以制备整体式多孔炭材料是CO2吸附研究的重点之一。泡沫炭作为一种整体式炭材料,因具有高比表面积、低体积密度、良好的导电和导热性而被用作催化剂载体、隔热材料和电容器材料等[11];并且泡沫炭大多具有分级孔结构,有利于气体分子的扩散,也是良好的气体吸附剂[12]。关于制备生物质泡沫炭并用于CO2吸附的研究鲜有报道。因此,本研究基于课题组前期研究成果[13-14],以落叶松作为生物质原料、尿素作为氮源,利用苯酚液化-物理发泡-活化工艺制备落叶松基氮掺杂泡沫炭材料,并讨论了尿素添加量和活化温度对材料结构和吸附性能的影响,以期为制备用于CO2吸附的生物质炭材料提供理论指导。
1 实 验
1.1 原料与试剂
落叶松木屑(黑龙江省加格达奇林场),粒径≤0.178 mm,105 ℃烘干8 h,备用。苯酚、浓硫酸、磷酸、盐酸、尿素、正戊烷、吐温80、甲醇、Na2CO3、NaOH等化学试剂均为市售分析纯。
1.2 落叶松基氮掺杂泡沫炭的制备
采用苯酚液化-物理发泡-活化工艺制备落叶松基氮掺杂泡沫炭。首先,取20 g落叶松木屑、60 g苯酚、1 mL浓硫酸(98%)、1.70 mL磷酸(85%)加入四口烧瓶中,安装搅拌器和冷凝器后加热。在回流温度124~136 ℃下反应1 h,停止加热。冷却至室温后,加入130 mL甲醇并充分搅拌,混合液过滤后用Na2CO3中和至中性并再次过滤去除盐等不溶物,收集滤液,在50 ℃下减压蒸馏去除甲醇,得到落叶松液化物。向液化物中加入100 mL甲醛溶液(37%)、1 g NaOH及20 mL蒸馏水,搅拌均匀并升温至55~60 ℃,保温反应2 h后分别添加4、 6和8 g的尿素,加热至95~98 ℃反应1 h。将产品冷却至60 ℃,用盐酸调节pH值至中性,在0.08~0.085 MPa下减压蒸馏脱去部分水,得到适宜黏度的热固性酚醛树脂产物。随后快速将5 mL吐温80和35 mL正戊烷加入热固性酚醛树脂产物中,强力搅拌使物料混合均匀,然后滴加4 mL浓硫酸(98%),强力搅拌均匀,将混合物快速取出放入模具中,在60 ℃ 下发泡并固化24 h,得到落叶松基氮掺杂泡沫,记为NF-x,其中x表示尿素的掺杂量(g),下同。将制得的氮掺杂泡沫在N2气氛下以5 ℃/min的速率分别升温至700、800和900 ℃,然后转换为CO2气氛活化2 h得到氮掺杂泡沫炭,记为NCF-x-y,其中y表示活化温度(℃),下同。为设置对照,又制备出不添加尿素的落叶松基泡沫,记为LF;将LF按照上述方法活化制备落叶松基泡沫炭,样品记为CF-y。
1.3 分析与表征
采用FEI Apreo S型场发射扫描电子显微镜(SEM)观测样品的微观形貌,测试前对样品进行喷金处理,样品的孔泡尺寸和韧带平均厚度利用Nano measurer软件测量得到。采用德国布鲁克公司生产的BRUCKER D8 ADVANCE型X射线衍射(XRD)仪测定泡沫炭材料的晶型结构,测试条件为室温,Cu Kα射线,管电压40 kV,电流40 mA,扫描范围2θ为25~80°,步速4(°)/min,X射线波长(λ)为0.154 nm,样品的晶面间距利用MDI jade 6.0软件计算得到。采用德国耐驰公司生产的NETZSCH STA 449 F5/F3 Jupiter型热重(TG)分析仪在N2气氛下测试材料的热稳定性,升温速率10 ℃/min,温度测试范围为 30~900 ℃。采用美国赛默飞公司生产的Thermo escalab 250Xi型X射线光电子能谱(XPS)仪测试氮掺杂泡沫炭的表面元素组成及化学价态。采用美国麦克公司生产的Micromeritics ASAP 2020物理吸附仪测试样品的比表面积、微孔面积、总孔容积、微孔容积和孔径分布等微观孔参数,所有样品在300 ℃下真空干燥脱气4 h,比表面积通过BET方法计算,微孔容积通过t-plot法得到,介孔孔径分布通过BJH法计算,微孔孔径分布通过HK法计算。
1.4 CO2吸附性能测试
单组分CO2和N2的吸附等温线是利用物理吸附仪测定,所有样品在300 ℃下真空干燥脱气6 h,并测定25 ℃下CO2和N2在0~100 kPa的吸附等温线数据。分别使用单点Langmuir(SSL)和双点Langmuir(DSL)模型来拟合N2和CO2的吸附等温线,公式见式(1)~(2)。
(1)
(2)
式中:p—气体平衡压力,MPa;q—单位吸附剂的吸附量,mmol/g;qm—吸附剂的饱和吸附量,1和2分别代表点1和点2,mmol/g;b—亲和系数。
材料的吸附选择性由下述2种方法计算:1) 初始斜率比(亨利定律常数):选取CO2/N2的单组分吸附等温线上在0~20 kPa的数据,通过Origin线性拟合得到每条等温线的初始斜率,根据式(3)计算吸附选择性。2) 理想吸附溶液理论(IAST)吸附选择性(式(4))。
(3)
(4)
其中S表示吸附选择性;下标1和2代表混合气体的组分,这里代表CO2和N2;k表示线性拟合等温线的初始斜率;x和y分别表示吸附相和本体相中组分的摩尔分数。
IAST模型假定在一定的扩散压力和温度条件下,吸附体系中的混合组分是一个理想混合物,所有组分遵循一个规则,吸附相的化学势能与达到平衡时气相的吸附势能相等。根据上述原理,通过式(1)和(2)计算出两种气体在吸附相中的摩尔分数,并代入式(4)便可计算得到吸附剂对二元混合气体的吸附选择性。
2 结果与讨论
2.1 泡沫炭表征结果分析
2.1.1SEM分析 未掺杂泡沫炭CF-700、CF-900和氮掺杂泡沫炭NCF- 4-900、NCF-6-900的SEM图片如图1所示。由图可知,多种泡沫炭具有不规则的蜂窝状孔泡,并且孔泡由韧带和节点组成。通过观察CF-700和CF-900发现,随着活化温度的升高部分孔泡壁在活化过程中破裂。CF-900、NCF- 4-900和NCF- 6-900的孔泡尺寸分别在200~450、 150~370和150~320 μm之间,进一步观察放大图像,发现3种材料韧带平均厚度分别为1.00、 0.60和0.50 μm,说明随着氮掺杂量的提高,材料的孔泡和韧带尺寸减小。这可能是因为尿素与游离甲醛和苯酚反应,使尿素单元嵌入到树脂大分子中,增大了树脂的交联程度并提高了黏度使其在发泡时阻力变大导致的。

a.CF-700; b.CF-900; c.NCF- 4-900; d.NCF- 6-900
2.1.2XRD分析 不同条件下制备的多种泡沫炭的XRD图见图2,泡沫炭的(002)晶面间距(d)见表1。
由图2可以看出,所有样品在2θ为23°和43°左右各有一个宽的衍射峰,分别对应于(002)晶面和(100)晶面的衍射角,说明泡沫炭材料都具有石墨层无序堆积的晶型结构特点[15]。表1显示,这几种泡沫炭材料的晶面间距都在0.38~0.41 nm之间,该结果要高于石墨相应的参数(0.34 nm)[16],也说明了材料非石墨化的碳质结构。

表1 泡沫炭材料的晶面间距
如图2(a)所示,相同活化温度下,不同氮掺杂量的材料与未掺杂材料具有类似的谱图,说明氮掺杂不会影响泡沫炭的晶面结构。根据图2(b)可见,随着活化温度的升高,材料的衍射峰变弱变宽,这可能是因为活化温度的升高使得材料的骨架受到了破坏,所以整体变得无序,这与SEM图像结果一致。
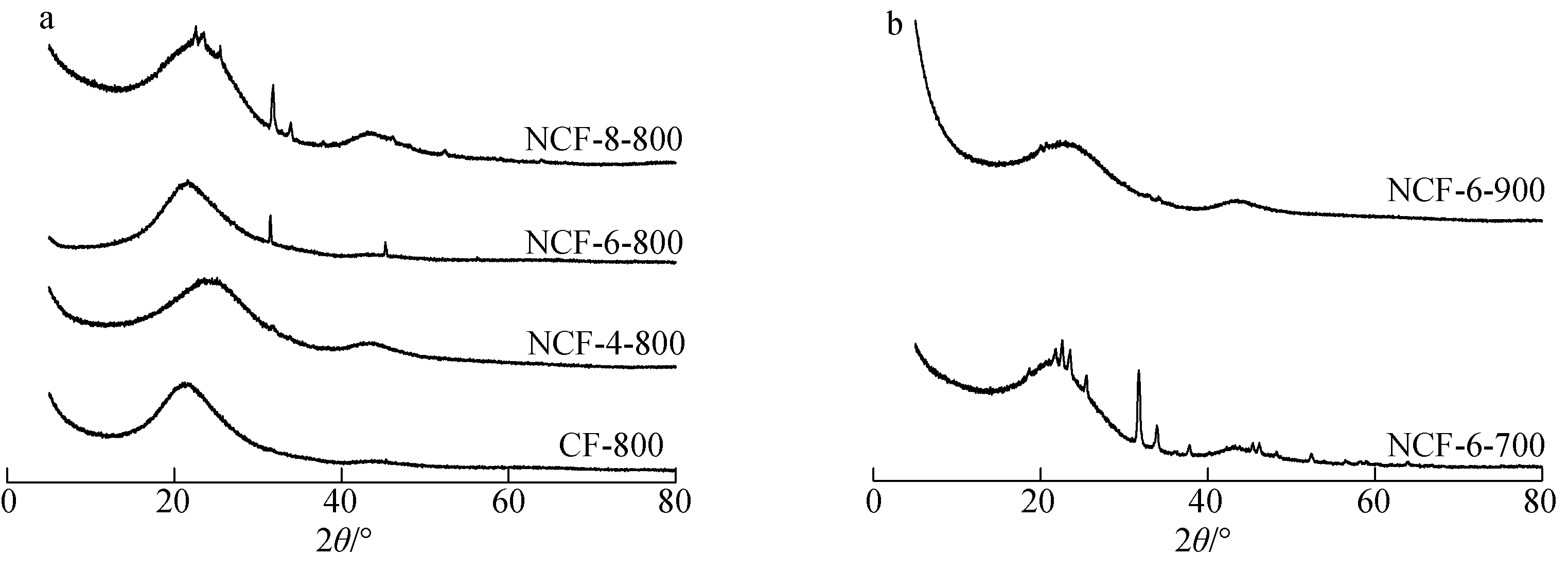
图2 不同氮掺杂(a)和活化温度(b)下制备的泡沫炭材料的XRD图
2.1.3热重分析 未掺杂的落叶松基泡沫(LF)与氮掺杂泡沫NF-8的TG和DTG曲线见图3。图中的DTG曲线表明LF和NF-8在30~900 ℃之间主要经历了2个热分解阶段,第一阶段的温度范围分别为30~360.80和30~402.80 ℃,该阶段主要是材料吸附的水分和游离苯酚等挥发性物质逸出的过程[17]。该阶段氮掺杂泡沫NF-8的最大热分解速率(-1.61%/min)高于LF(-1.11%/min),NF-8的残炭率(73.81%)低于LF(79.64%),主要是因为未反应的尿素分子会在300~400 ℃时与H2O反应生成氨基甲酸铵(H2NCOONH4),再经过热处理生成CO2和NH3逸出材料表面[18]。随后进入热分解的第二阶段,首先树脂分子内的醚键和末端羟甲基开始断裂,随着温度的升高,酚醛树脂分子主链的不同部位发生断裂,生成了多种挥发性小分子脱离炭材料。此阶段LF和NF-8的最大热分解速率及其对应温度相差不大,分别为464.40 ℃、-1.45%/min和457.50 ℃、-1.42%/min。900 ℃时未掺杂泡沫炭LF和氮掺杂泡沫炭NF-8的残炭率分别为45.77%和40.98%,通过残炭率判断氮掺杂会降低材料的热稳定性。
2.1.4XPS分析 氮掺杂泡沫炭的XPS图如图4所示。图4(a)通过对材料的表面化学元素组成进行分析,发现氮掺杂材料的XPS谱图主要包含位于285.10、 399.10和532 eV的3个峰,分别对应于C1s、N1s和O1s。图4(b)~(d)通过对NCF-8-700、NCF-8-800和NCF-8-900样品的N1s峰进行分峰处理,研究发现当活化温度低于900 ℃时,NCF-8-700和NCF-8-800主要含有结合能为398.40和400.80 eV的2种N,分别对应于吡啶型氮(N- 6)和吡咯型氮(N-5)[19]。当活化温度升高到900 ℃时,除了上述2种N,NCF-8-900又出现了结合能为401.40 eV的四元型氮(N-Q)。这是可能是因为随着活化温度的升高,部分N-5和N- 6与活化剂发生反应,转化为热稳定性更好的N-Q。

a.CF-900,NCF-8-900; b.NCF-8-700(N1s); c.NCF-8-800(N1s); d.NCF-8-900(N1s)
表2是通过XPS结果计算得到的材料表面各元素含量。由表2可知,随着活化温度的升高,材料的氮含量降低。进一步通过对氮元素分峰结果计算出所有类型氮元素的含量,发现其含量由高到低顺序为N-5>N- 6>N-Q。由于在多种类型的氮元素中,N-5与CO2分子的相互作用最强,所以该结果有利于CO2的吸附[20-22]。

表2 氮掺杂泡沫炭表面元素含量和各类型氮元素含量1)
2.1.5孔结构分析 泡沫炭材料的孔结构参数见表3。由表3可知所有炭材料的微孔孔容占比都在60%以上,最高的NCF-8-800可以达到95.83%,NCF- 6-900具有最高的比表面积(778.22 m2/g)、总孔容(0.43 cm3/g)和微孔孔容(0.38 cm3/g)。研究发现,随着活化温度的升高,材料的孔结构参数都随之增加。
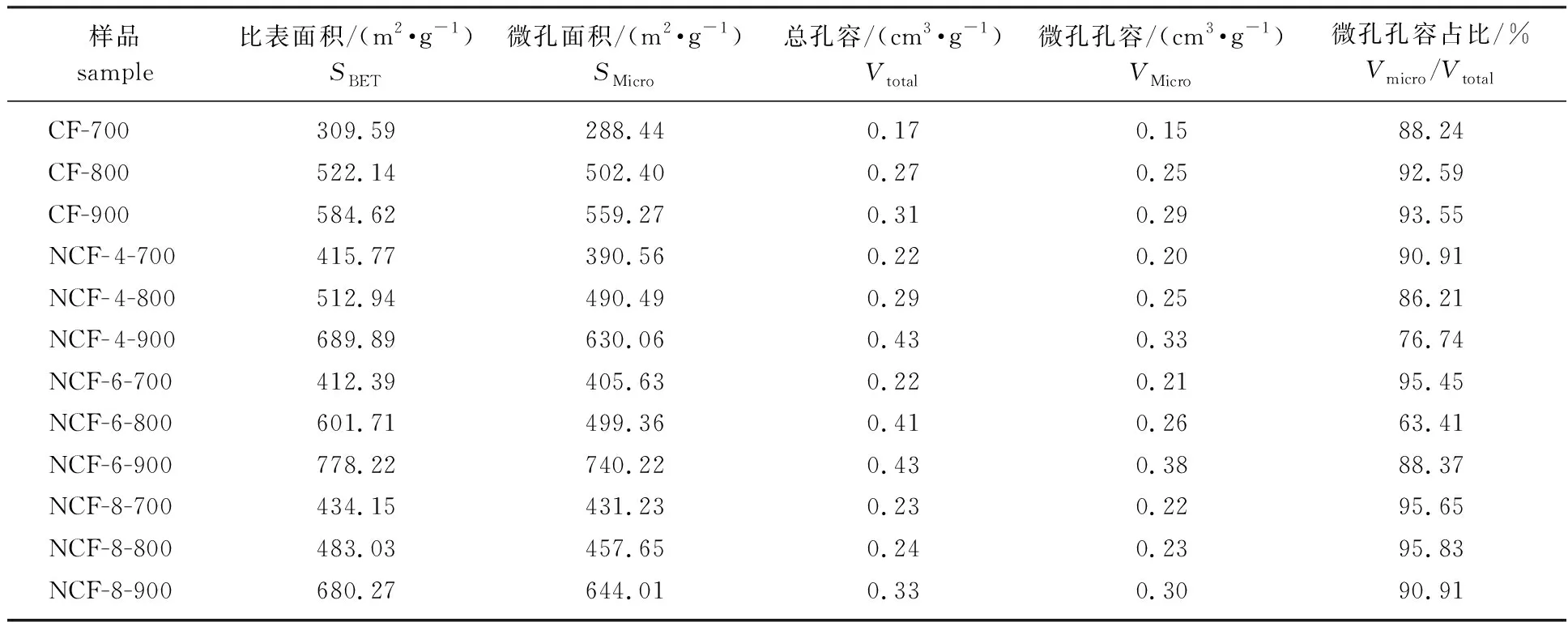
表3 泡沫炭材料的孔结构参数
活化温度为900 ℃时炭材料的氮气吸附-脱附等温曲线及孔径分布图见图5。

图5 泡沫炭材料的氮气吸附-脱附等温曲线(a)、微孔孔径分布图(b)和介孔孔径分布图(c)
从图5(a)可以观察到,4个样品的N2吸附等温线都是典型的Ⅳ型吸附等温线,在相对压力(P/P0)为0.40~0.90处都有典型的H1型滞后环,说明样品还存在比较少的介孔。图5(b)和5(c)的孔径分布图也印证了图5(a)的结论,其中CF-900微孔区域集中在0.50和1.26 nm左右;NCF- 4-900、NCF-6-900和NCF-8-900微孔区域集中在0.50、 0.81 和1.26 nm左右,介孔区域集中在3.85 nm左右。氮掺杂泡沫炭出现更多超微孔(<1 nm)的原因可能是由于尿素在高温下更容易与活化剂发生反应,在炭骨架上生成更多的微孔[23]。
2.2 泡沫炭的CO2吸附性能
2.2.1CO2吸附容量分析 在25 ℃和0~100 kPa条件下测得了CO2和N2在多种泡沫炭材料上的单组分吸附等温线如图6所示。

a.700 ℃; b.800 ℃; c.900 ℃
材料的2种气体吸附等温线均表现出良好的可逆性,没有迟滞现象,表明吸附的气体分子在解吸过程中都可以被很好地脱除。因此,制备的氮掺杂泡沫炭很容易在真空状态下再生而无需任何加热处理,可以有效减少能耗。同时,材料的CO2吸附容量随着压力的升高持续增大且未达到饱和,说明在高压下材料可以吸附更多的CO2。

表4 25 ℃,100 kPa时泡沫炭材料的CO2和N2吸附容量
100 kPa时泡沫炭材料的CO2、N2吸附容量见表4。结合图表可以看出,所有材料的CO2吸附容量远高于N2吸附容量,并且在100 kPa时CO2吸附容量随着活化温度的升高而增大。与未掺杂泡沫炭相比,氮掺杂泡沫炭的CO2吸附容量都有所提高,如CF-900的CO2吸附容量为2.62 mmol/g,而NCF-8-900具有最高的CO2吸附容量3.19 mmol/g。值得注意的是,NCF-6-900具有比NCF- 4-900更高的比表面积、微孔容积和氮含量,但是其CO2吸附容量低于NCF- 4-900,根据孔径分布图分析这可能是因为NCF- 4-900超微孔孔容高于NCF-6-900,所以这说明材料在100 kPa时的CO2吸附容量可能由超微孔孔容决定[24-25]。
2.2.2CO2/N2吸附选择性分析 通过单组分吸附等温线的初始斜率比预测二元混合气体的选择性是常用的评价材料吸附性能的方法之一。本实验选取900 ℃活化的样品CF-900、NCF- 4-900、NCF-6-900和NCF-8-900的CO2和N2单组分吸附等温线在0~20 kPa之间的数据,通过Origin软件进行线性拟合并利用1.4节中公式(1)计算CO2/N2选择性,相关拟合方程和选择性见表5。由表5可知,NCF-8-900具有最理想的CO2/N2吸附选择性,其值为11.98。

表5 CO2和N2在泡沫炭上的线性拟合方程与IAST拟合参数
由于没有考虑气体分子之间的竞争等因素,初始斜率比只能对材料的二元混合气体选择性提供大概参考,并不代表实际的性能。因此,为了准确分析材料的CO2/N2气体吸附选择性,又采用理想吸附溶液理论(IAST)分析上述4个样品对CO2/N2的选择性。首先分别用DSL模型和SSL模型拟合25 ℃ 下CO2和N2在泡沫炭上的吸附等温线,随后选择CO2和N2体积比15 ∶85的常见煤层气二元混合气体比例并利用1.4节中公式(2)和(4)来计算选择性,详细拟合数据及IAST吸附选择性亦见表5。通过数据可以发现,随着氮掺杂量的提高,材料的吸附选择性增加,NCF-8-900具有最高的吸附选择性118.63,与初始斜率比结果一致。这说明材料的吸附选择性可能由其氮含量决定。
3 结 论
3.1以落叶松木屑为原料,尿素为氮源,制备了落叶松基氮掺杂泡沫炭,采用SEM、XRD、XPS、TG和N2吸附-脱附等温线对其进行表征,结果表明:氮掺杂会使泡沫炭的孔泡尺寸变小并降低其热稳定性;泡沫炭材料具有石墨层无序堆积的晶型结构,随着活化温度的提高,其晶面间距变大且无序性提高。
3.2氮掺杂泡沫炭主要为微孔结构,其中NCF-8-800微孔孔容占比达到95.83%,NCF- 6-900具有最高的比表面积(778.22 m2/g)、总孔容(0.43 cm3/g)和微孔孔容(0.38 cm3/g),并且NCF- 4-900、NCF- 6-900 和NCF-8-900的微孔孔径主要集中在0.50、 0.81和1.26 nm。
3.3随着活化温度的提高,泡沫炭的氮含量降低。活化温度为700和800 ℃的材料主要含有2种类型氮元素,即吡啶型氮(N-6)和吡咯型氮(N-5);当活化温度达到900 ℃时,部分N-5和N-6转化为热稳定性更好的四元型氮(N-Q),并且其含量顺序为N-5>N- 6>N-Q。
3.4泡沫炭的CO2吸附容量随着活化温度的升高而提高,在25 ℃和100 kPa下NCF-8-900具有最高的吸附容量,达到了3.19 mmol/g;并且NCF-8-900也具有良好的CO2/N2吸附选择性,其值为118.63。
