左侧前额叶背外侧区高频重复经颅磁刺激对帕金森病患者的效果观察
2021-05-06雍雨暄杨新玲
白 睿 张 敏 雍雨暄 杨新玲
新疆医科大学第二附属医院,新疆 乌鲁木齐830028
帕金森病(Parkinson’s disease,PD)是第二大神经系统变性疾病,其中60 岁以上人群患病率高达1%,且这一数据随着年龄的增长呈上升趋势[1],尤其是在疾病晚期,约80%的患者可能出现静息震颤、运动迟缓、强直、步态障碍和姿势不稳定等严重影响患者生活的运动症状[2]。研究发现,随着α-突触核蛋白(α-syn)的广泛沉积,患者还会出现各种非运动症状,如抑郁、认知障碍和睡眠障碍等[3],从而加重了PD 患者的日常管理难度和照料者的负担[3-4]。目前对于PD 的治疗手段仍以经典的左旋多巴药物替代治疗为主,但长期使用药物后也会出现运动症状和非运动症状并发症,甚至还会加速神经退行性变[5]。PD 药物相关并发症及药效持续时间缩短的问题引起了人们对新型且更有效治疗方法的探索。
重复经颅磁刺激(rTMS)是一种通过一系列电磁脉冲对大脑皮质进行重复刺激的无创诊疗技术。研究发现rTMS 是一种安全、无创伤且对PD 有显著疗效的治疗方法[6],其原理是依据法拉第电磁感应原理而发明的一项体外神经调控电生理技术,利用脉冲电流产生的磁场改变大脑皮质细胞的动作电位,继而发挥神经功能的干预及治疗作用[7]。目前许多研究者将rTMS 用于多种神经和精神疾病的潜在治疗。早期rTMS 主要用于抑郁症的治疗,且有十分显著的疗效[8]。后来一些研究者开始把rTMS运用于各种运动障碍性疾病的治疗,特别是帕金森病、肌张力障碍。1994 年PASCUAL-LEONE等[9]首次将TMS技术应用于PD患者,并通过观察发现治疗后患者的运动症状得以改善,为PD 治疗提供了方向。后续的研究也发现,rTMS 是一种能够改善PD 患者运动和非运动症状的无创性神经调制技术[10-11]。近年来大量研究及临床试验发现,高频rTMS(HF-rTMS)(>1.0 Hz)可增强皮质的兴奋性[12-13],但在左侧DLPFC 上使用高频rTMS 以观察运动症状改善的研究结果参差不齐,这些研究在rTMS 频率、刺激位点、PD 严重程度和治疗目的等方面存在差异,同时这种刺激方式可否用于改善PD 患者睡眠障碍仍未可知。本研究旨在分析左侧DLPFC 给予高频rTMS对PD患者运动症状及睡眠障碍的疗效。
1 资料与方法
1.1 研究对象 选择2019-07—2020-07就诊于新疆医科大学第二附属医院的PD患者,严格按照入纳入与排除标准,最终纳入试验组34例(rTMS+药物组),药物组45例。2组基本情况方面比较差异均无统计学意义(P>0.05),具有可比性。见表1。本研究已获新疆医科大学第二附属医院伦理委员会批准,批准号:GDREC2017082H。研究干预前获得每位参与者的知情同意。
表1 2组一般情况比较 (±s)Table 1 Comparison of general conditions between the two groups (±s)
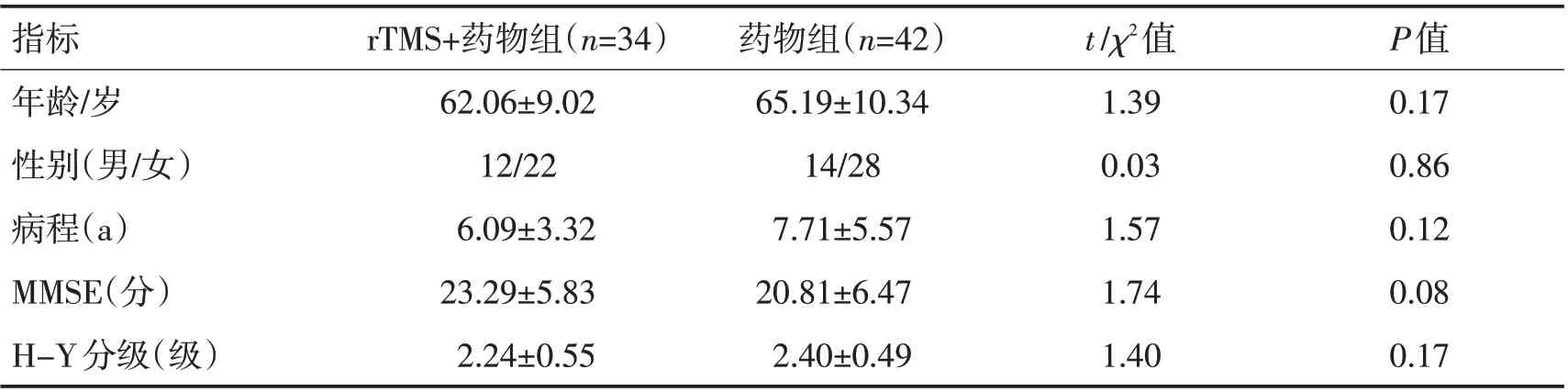
表1 2组一般情况比较 (±s)Table 1 Comparison of general conditions between the two groups (±s)
指标年龄/岁性别(男/女)病程(a)MMSE(分)H-Y分级(级)rTMS+药物组(n=34)62.06±9.02 12/22 6.09±3.32 23.29±5.83 2.24±0.55药物组(n=42)65.19±10.34 14/28 7.71±5.57 20.81±6.47 2.40±0.49 t/χ2值1.39 0.03 1.57 1.74 1.40 P值0.17 0.86 0.12 0.08 0.17
1.2 入选标准
1.2.1 纳入标准:①年龄18~80 岁;②依据英国帕金森病协会制订的PD 诊断标准,诊断为原发性PD的患者;③研究期间可维持稳定剂量抗帕金森病药物治疗者;④患者及其家属能够遵守研究方案、访视计划;⑤患者及家属对本研究知情同意并签署相关文件。
1.2.2 排除标准:①继发性帕金森综合征或帕金森叠加综合征患者;②严重心、肺、肝、肾、血液系统疾病患者;③有严重精神异常症状或严重认知障碍者;④既往接受DBS 或毁损术者;⑤有重复经颅磁刺激使用禁忌者。
1.3 治疗方法 rTMS+药物组及药物组均给予稳定剂量抗帕金森病药物治疗,药物组不给予rTMS 治疗。经颅磁刺激仪(型号YRD CCY-Ⅰ型)由武汉依瑞德医疗设备新技术有限公司提供,治疗时刺激线圈置于左侧DLPFC。采用10 Hz rTMS,刺激时间2 s,间歇时间18 s,1 200 次/d,20 min/次,输出刺激强度为100%静息运动阈值,连续治疗10 d。
1.4 评定方法 研究开始前采用简易智能量表(MMSE)评估所有患者的认知功能。采用统一帕金森病评定量表第三部分(UPDRS-Ⅲ)及起立-行走测试(TUG)进行运动症状评估。采用匹兹堡睡眠质量指数(PSQI)进行睡眠障碍的评估。每个参与者必须在基线、治疗结束时和治疗结束后1 个月完成评估。评估由专业的神经内科医生或运动障碍专家完成。
1.5 统计学分析 使用统计软件包SPSS 23.0 对结果进行统计分析。计量资料以均数±标准差(±s)表示,2 组间均数的比较采用独立样本t 检验,组内治疗前后比较采用配对t检验,计数资料比较采用χ2检验或Fisher 精确概率法,以P<0.05 为差异有统计学意义。
2 结果
2.1 rTMS+药物组基线、治疗结束时和治疗结束后1 个月各项评分比较 rTMS+药物组治疗结束时、治疗结束后1个月的UPDRS-Ⅲ总分、TUG时间及PSQI总分明显低于基线(P<0.05);治疗结束后1 个月的UPDRS-Ⅲ总分、TUG 时间及PSQI 总分较治疗结束时无明显变化(P>0.05)。见表2。
2.2 药物组基线、治疗结束时、治疗结束后1个月各项评分比较 药物组治疗结束时、治疗结束后1个月的UPDRS-Ⅲ总分、TUG 时间及PSQI 总分较基线无明显变化(P>0.05)。见表2。
2.3 2组治疗结束时、治疗结束后1个月各项评分比较 rTMS+药物组治疗结束时、治疗结束后1个月的UPDRS-Ⅲ总分、TUG 时间及PSQI 总分均显著低于药物组(P<0.05)。见表2。
表2 2组患者不同治疗阶段各量表评分比较 (±s)Table 2 Comparison of scores of various scales at different treatment stages between the two groups (±s)

表2 2组患者不同治疗阶段各量表评分比较 (±s)Table 2 Comparison of scores of various scales at different treatment stages between the two groups (±s)
注:与rTMS+药物组基线比较,aP>0.05;同组内与基线比较,bP<0.05,cP>0.05;同组内随访末与治疗后立即比较,dP>0.05;与rTMS+药物组治疗后立即及随访末比较,eP<0.05
rTMS+药物组(n=34)药物组(n=42)指标治疗结束后1个月23.07±6.87cde 17.08±5.14cde 21.52±6.36cde UPDRSⅢ(分)TUG(s)PSQI(分)基线24.85±6.78 15.32±5.99 22.56±8.16治疗结束时19.35±5.91b 12.37±4.44b 18.62±7.64b治疗结束后1个月19.88±5.94bd 12.59±4.61bd 17.41±6.86bd基线22.45±6.76a 16.35±5.12a 21.21±6.17a治疗结束时22.38±6.73ce 16.94±5.16ce 21.31±6.26ce
3 讨论
帕金森病是一种进行性神经退行性疾病,主要临床特征为静息性震颤、运动迟缓、强直、步态障碍和姿势不稳等。目前PD 的治疗仍以左旋多巴替代治疗为主,药物治疗能在一定程度上控制症状,但随着疾病的进展,这些药物作用降低且长期服药会增加相关不良反应。因此,寻找能有效改善PD症状及延缓疾病进展的治疗手段,是目前急需解决的临床问题。rTMS具有广阔临床应用前景,大量研究表明,PD 患者在rTMS治疗后运动症状及非运动症状均能较前明显改善[10-11]。PD 是TMS 研究中最多的运动障碍性疾病,尤其是在治疗运动症状方面[14]。目前,虽然已经证实不同的大脑皮质区域与改善PD 症状有关[15],但有关于rTMS 治疗PD 的高质量证据有限。在PD 早期rTMS 研究中,DLPFC 是研究者最为感兴趣的刺激靶点之一。神经影像学研究表明,PD患者情绪变化主要与左侧DLPFC失活有关[16]。研究证实在左侧DLPFC使用高频rTMS治疗对PD 患者情绪改变的改善与抗抑郁药的疗效相当[17]。同时也有部分研究发现,在左侧DLPFC使用高频rTMS 刺激对治疗PD 相关抑郁症有效[18-19]。研究发现右侧DLPFC 在执行功能中起至关重要的作用[20],主要与工作记忆、决策和应对新任务等执行功能有关[21],且这些功能一般在PD 早期已经受损[22]。相关研究证明rTMS可以调节运动皮质的兴奋性,可以刺激或抑制大脑皮质的兴奋性,并取决于刺激参数,这些参数主要包括刺激的强度、频率、次数、持续时间等。在以往涉及TMS 和PD 运动障碍的研究中显示大脑皮质兴奋性的变化。各种研究表明,高频刺激会增加皮质兴奋性[23-24],低频刺激抑制皮质兴奋性[25]。目前,在rTMS治疗靶点中主要是基于右侧DLPFC过活跃和左侧DLPFC欠活跃的原理[26]。本研究选择左侧DLPFC给予高频rTMS刺激而不是右侧有几个原因:首先,左侧DLPFC 运动障碍的研究结果仍缺乏高质量证据。其次,很少有人研究左侧DLPFC 给予高频rTMS 治疗对PD 患者睡眠障碍的影响。睡眠障碍也是PD 的一种常见的非运动症状,研究发现右侧DLPFC上的低频rTMS可以改善睡眠障碍[27],但目前对左侧DLPFC使用高频rTMS刺激是否助于改善PD睡眠障碍并不清楚,而且在左侧DLPFC 使用高频rTMS 以观察运动症状改善的研究结果参差不齐,值得临床进一步研究。
本研究观察到连续10 d 对左侧DLPFC 高频rTMS治疗可以改善PD患者的运动症状和睡眠障碍,而且对改善帕金森病患者的运动症状和睡眠障碍有一定的持续效果。目前对于PD 运动症状改善的指南中仅将双侧M1区高频刺激评定为C级证据[28],但多项荟萃分析表明其他刺激部位如DLPFC、辅助运动区(SAM)同样可以改善PD患者运动症状。CHOU等[11]一项荟萃分析显示,与假刺激相比,积极进行rTMS 治疗有利于改善PD 患者的运动症状,DLPFC、SMA 的低频(≤1 Hz)rTMS 均可产生疗效。WAGLE等[29]Meta 分析同样显示低频及高频rTMS 均可改善PD 患者的运动症状。ZHUANG 等[30]随机对照研究发现,右侧DLPFC 上的低频rTMS 可以改善PD 患者运动症状、抑郁和认知表现。在一项随机、双盲、假对照研究中,2周内8次使用50 Hz rTMS的刺激运动皮质,患者运动症状有所改善,且无任何不良事件[31]。采用高频rTMS治疗PD运动症状的几个随机对照试验的Meta分析发现是有益的,而低频不能改善PD患者的运动症状[32]。然而,这些研究在刺激靶点、使用的刺激方案、样本量、rTMS前UPDRS评分、疾病持续时间、各种治疗药物剂量等方面存在差异。所有的这些因素使得制定一个理想的刺激方案非常困难。结合上述研究结果可以发现,rTMS在一定程度上可以改善PD 患者的运动症状,但影响rTMS 作用效果的外在因素很多,包括刺激部位、刺激频率、刺激强度、治疗持续时间、样本量及患者疾病严重程度等。目前研究中使用的rTMS 方案差异很大,缺乏一致性,结果往往不一致。由于没有统一的标准,容易导致治疗误差,因此对于上述因素的选择及控制尤为重要。本研究发现,在运动症状及睡眠障碍方面,2组治疗结束时、治疗结束后1 个月比较,药物组UPDRS-Ⅲ总分、TUG 时间及PSQI 总分均明显高于rTMS+药物组(P<0.05);rTMS+药物组治疗结束时、治疗结束后1 个月的UPDRS-Ⅲ总分、TUG 时间及PSQI 总分较基线有所降低(P<0.05),提示rTMS 辅助治疗PD 可改善运动症状及睡眠障碍。本研究还发现rTMS+药物组治疗结束后1 个月的UPDRS-Ⅲ总分、TUG 时间及PSQI总分较治疗结束时无明显变化(P>0.05),考虑可能与随访时间过短有关。本研究还发现1 个月后患者运动症状及睡眠障碍较治疗结束后未进一步恶化,表明该治疗方案对改善帕金森病患者的运动症状和睡眠障碍有一定的持续效果,但需要进一步的长期随访研究进一步证实。
左侧DLPFC上的高频rTMS可能是改善PD患者运动症状、睡眠障碍的潜在治疗方案。但由于本研究样本量较小,随访时间短,存在一定的局限性,其临床疗效特别是长期疗效仍然需要,随访时间更长的大样本研究证实。总之,rTMS在PD患者中的疗效还存在争议,关于最有效的rTMS 治疗方案尚未出现,需要更多中心试验解决。未来在rTMS的研究中可把rTMS 与不同的神经成像技术或神经电生理技术相结合,以便更好地理解rTMS是如何通过干预调节大脑活动的机制,从而寻找出与症状改善一对一的刺激部位,制定更精准的rTMS治疗方案。
